文档内容
第二十八讲 难溶电解质溶解平衡
及反应过程中溶液粒子浓度变化的图像分析
【基础巩固】
1.医院中常用硫酸钡(俗称钡餐)作为内服造影剂,其不溶于水和脂质,所以不会被胃肠道黏膜吸收,因此对
人基本无毒性。已知:K (BaCO)=5.1×10-9;K (BaSO)=1.1×10-10。下列推断正确的是( )
sp 3 sp 4
A.BaCO 的溶度积常数表达式为K (BaCO)=n(Ba2+)·n(CO)
3 sp 3
B.可用2%~5%的NaSO 溶液给钡离子中毒患者洗胃
2 4
C.若误服含c(Ba2+)=1.0×10-5 mol·L-1的溶液时,会引起钡离子中毒
D.不用碳酸钡作为内服造影剂,是因为K (BaCO)>K (BaSO)
sp 3 sp 4
2.(2023·浙江·高考真题)碳酸钙是常见难溶物,将过量碳酸钙粉末置于水中达到溶解平衡:
[已知 , , 的电离常
数 ],下列有关说法正确的是
A.上层清液中存在
B.上层清液中含碳微粒最主要以 形式存在
C.向体系中通入 气体,溶液中 保持不变
D.通过加 溶液可实现 向 的有效转化
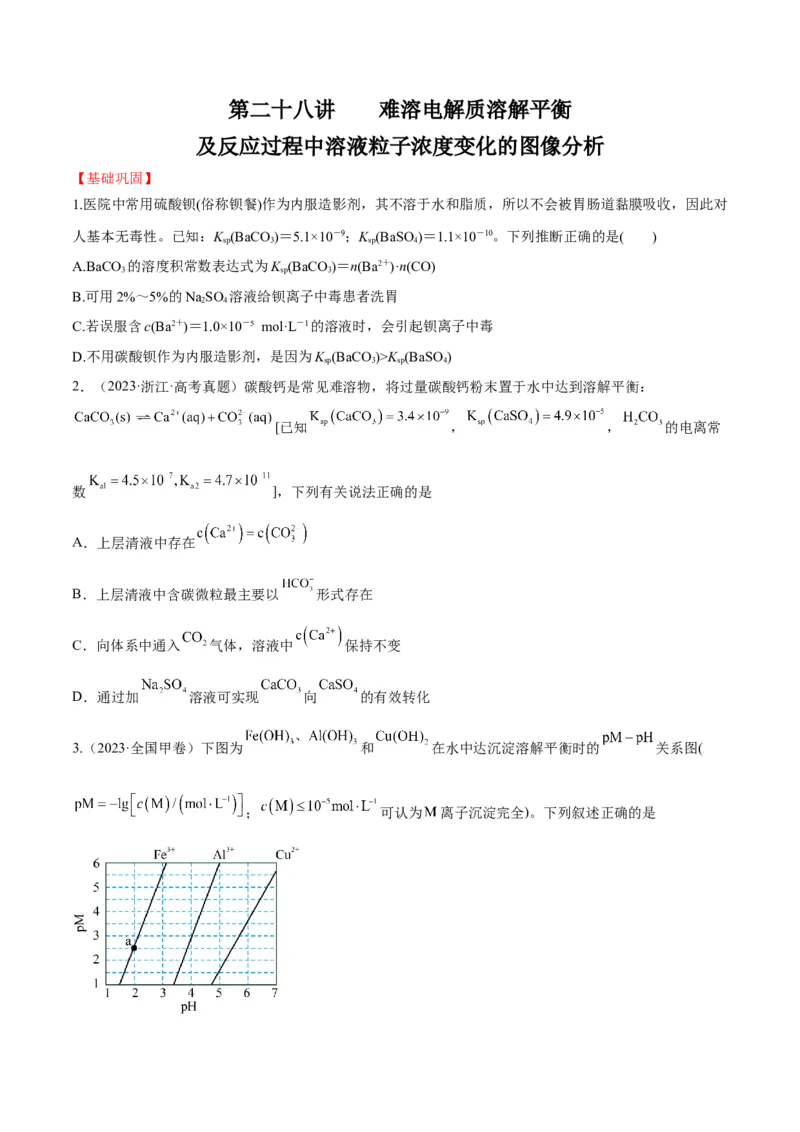
3.(2023·全国甲卷)下图为 和 在水中达沉淀溶解平衡时的 关系图(
; 可认为 离子沉淀完全)。下列叙述正确的是A.由 点可求得
B. 时 的溶解度为
C.浓度均为 的 和 可通过分步沉淀进行分离
D. 混合溶液中 时二者不会同时沉淀
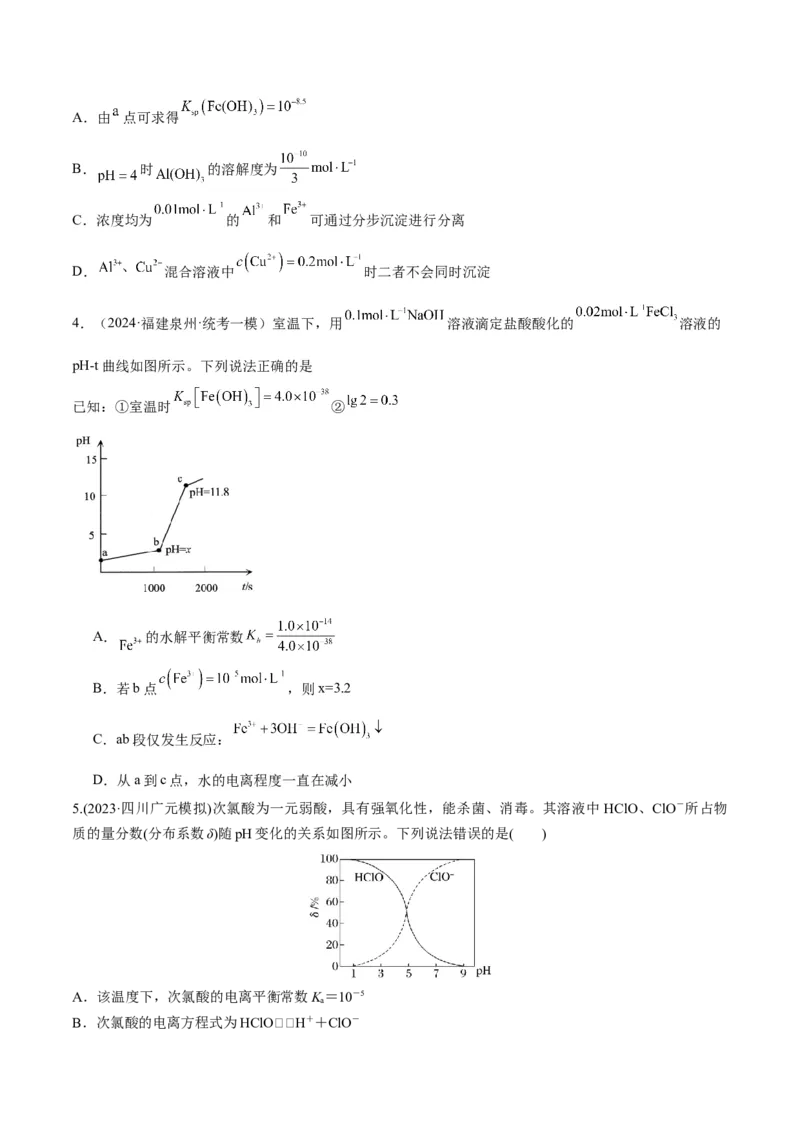
4.(2024·福建泉州·统考一模)室温下,用 溶液滴定盐酸酸化的 溶液的
pH-t曲线如图所示。下列说法正确的是
已知:①室温时 ②
A. 的水解平衡常数
B.若b点 ,则x=3.2
C.ab段仅发生反应:
D.从a到c点,水的电离程度一直在减小
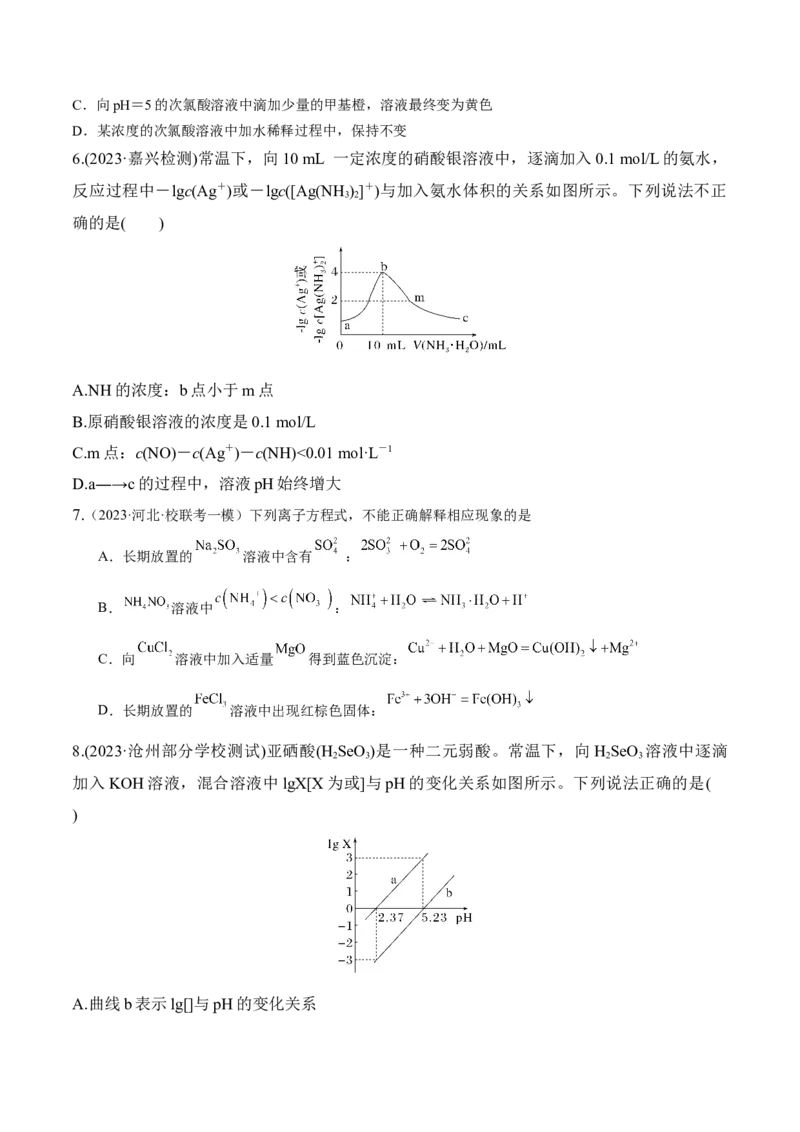
5.(2023·四川广元模拟)次氯酸为一元弱酸,具有强氧化性,能杀菌、消毒。其溶液中 HClO、ClO-所占物
质的量分数(分布系数δ)随pH变化的关系如图所示。下列说法错误的是( )
A.该温度下,次氯酸的电离平衡常数K=10-5
a
B.次氯酸的电离方程式为HClOH++ClO-C.向pH=5的次氯酸溶液中滴加少量的甲基橙,溶液最终变为黄色
D.某浓度的次氯酸溶液中加水稀释过程中,保持不变
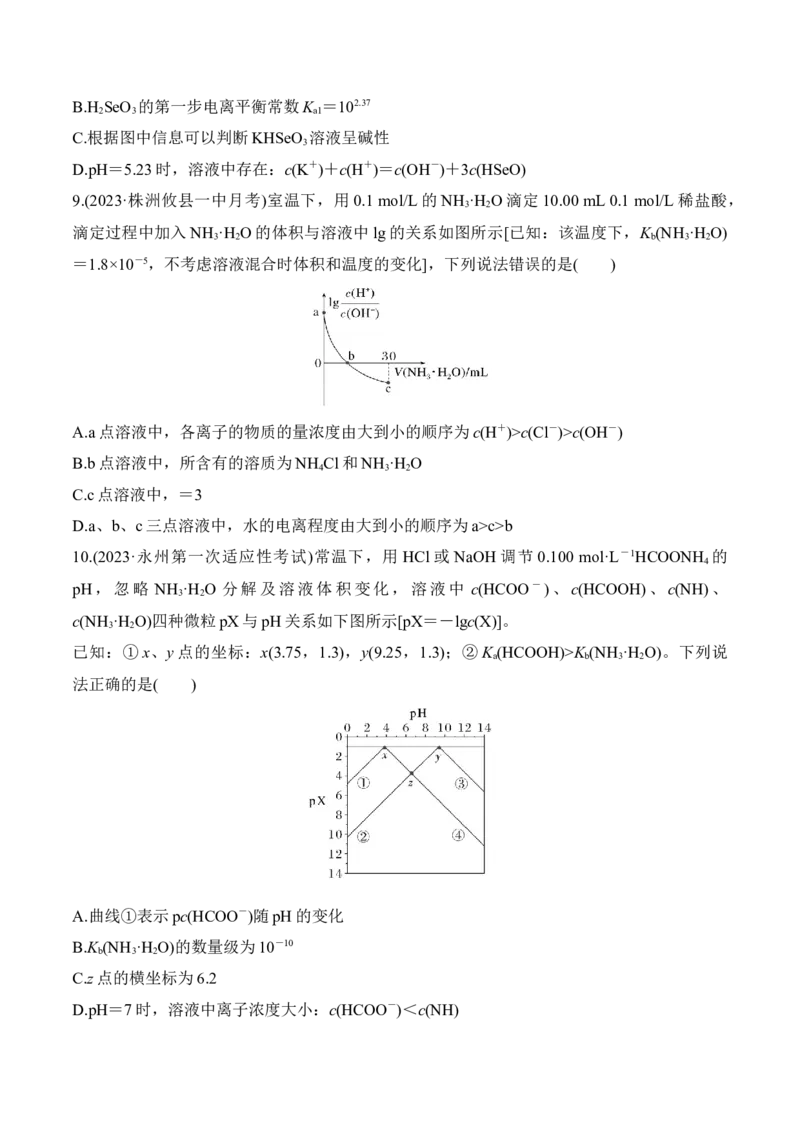
6.(2023·嘉兴检测)常温下,向10 mL 一定浓度的硝酸银溶液中,逐滴加入 0.1 mol/L的氨水,
反应过程中-lgc(Ag+)或-lgc([Ag(NH ) ]+)与加入氨水体积的关系如图所示。下列说法不正
3 2
确的是( )
A.NH的浓度:b点小于m点
B.原硝酸银溶液的浓度是0.1 mol/L
C.m点:c(NO)-c(Ag+)-c(NH)<0.01 mol·L-1
D.a―→c的过程中,溶液pH始终增大
7.(2023·河北·校联考一模)下列离子方程式,不能正确解释相应现象的是
A.长期放置的 溶液中含有 :
B. 溶液中 :
C.向 溶液中加入适量 得到蓝色沉淀:
D.长期放置的 溶液中出现红棕色固体:
8.(2023·沧州部分学校测试)亚硒酸(H SeO )是一种二元弱酸。常温下,向 H SeO 溶液中逐滴
2 3 2 3
加入KOH溶液,混合溶液中lgX[X为或]与pH的变化关系如图所示。下列说法正确的是(
)
A.曲线b表示lg[]与pH的变化关系B.H SeO 的第一步电离平衡常数K =102.37
2 3 a1
C.根据图中信息可以判断KHSeO 溶液呈碱性
3
D.pH=5.23时,溶液中存在:c(K+)+c(H+)=c(OH-)+3c(HSeO)
9.(2023·株洲攸县一中月考)室温下,用 0.1 mol/L的NH ·H O滴定10.00 mL 0.1 mol/L 稀盐酸,
3 2
滴定过程中加入NH ·H O的体积与溶液中lg的关系如图所示[已知:该温度下,K (NH ·H O)
3 2 b 3 2
=1.8×10-5,不考虑溶液混合时体积和温度的变化],下列说法错误的是( )
A.a点溶液中,各离子的物质的量浓度由大到小的顺序为c(H+)>c(Cl-)>c(OH-)
B.b点溶液中,所含有的溶质为NH Cl和NH ·H O
4 3 2
C.c点溶液中,=3
D.a、b、c三点溶液中,水的电离程度由大到小的顺序为a>c>b
10.(2023·永州第一次适应性考试)常温下,用 HCl 或 NaOH 调节 0.100 mol·L-1HCOONH 的
4
pH,忽略 NH ·H O 分解及溶液体积变化,溶液中 c(HCOO-)、c(HCOOH)、c(NH)、
3 2
c(NH ·H O)四种微粒pX与pH关系如下图所示[pX=-lgc(X)]。
3 2
已知:①x、y点的坐标:x(3.75,1.3),y(9.25,1.3);②K (HCOOH)>K (NH ·H O)。下列说
a b 3 2
法正确的是( )
A.曲线①表示pc(HCOO-)随pH的变化
B.K (NH ·H O)的数量级为10-10
b 3 2
C.z点的横坐标为6.2
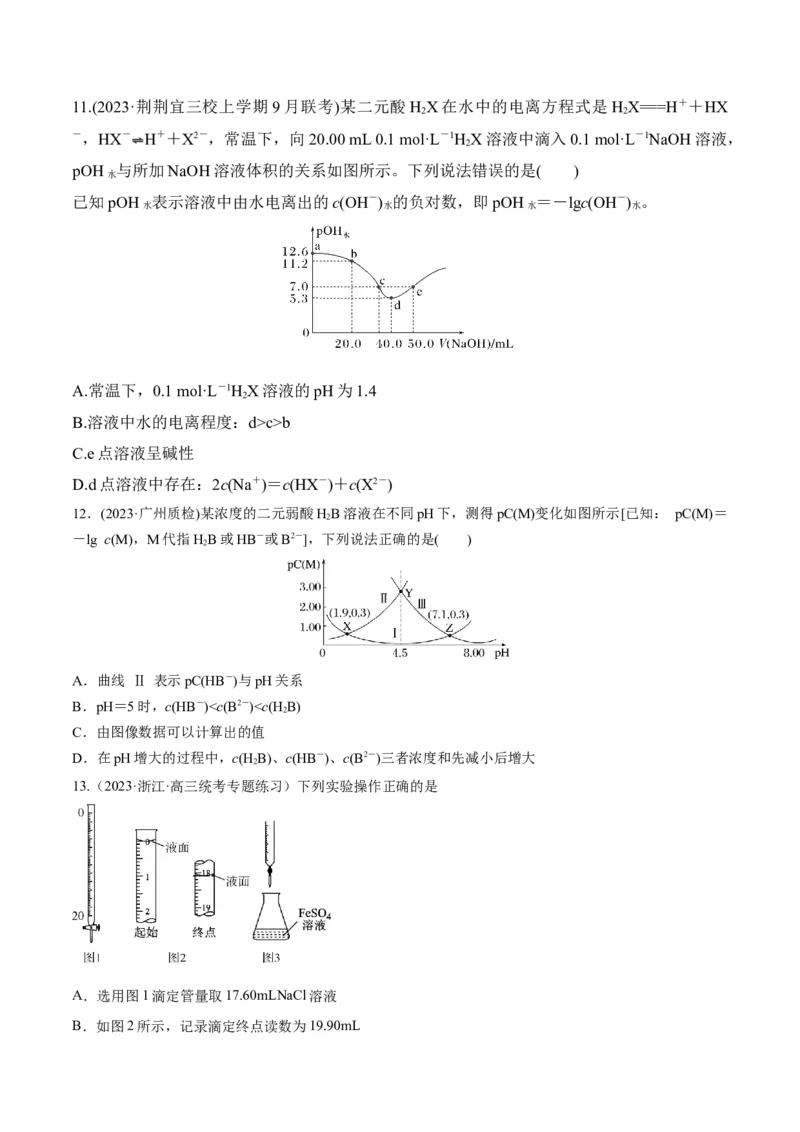
D.pH=7时,溶液中离子浓度大小:c(HCOO-)<c(NH)11.(2023·荆荆宜三校上学期9月联考)某二元酸H X在水中的电离方程式是 H X===H++HX
2 2
-,HX- H++X2-,常温下,向20.00 mL 0.1 mol·L-1H X溶液中滴入0.1 mol·L-1NaOH溶液,
⇌ 2
pOH 与所加NaOH溶液体积的关系如图所示。下列说法错误的是( )
水
已知pOH 表示溶液中由水电离出的c(OH-) 的负对数,即pOH =-lgc(OH-) 。
水 水 水 水
A.常温下,0.1 mol·L-1H X溶液的pH为1.4
2
B.溶液中水的电离程度:d>c>b
C.e点溶液呈碱性
D.d点溶液中存在:2c(Na+)=c(HX-)+c(X2-)
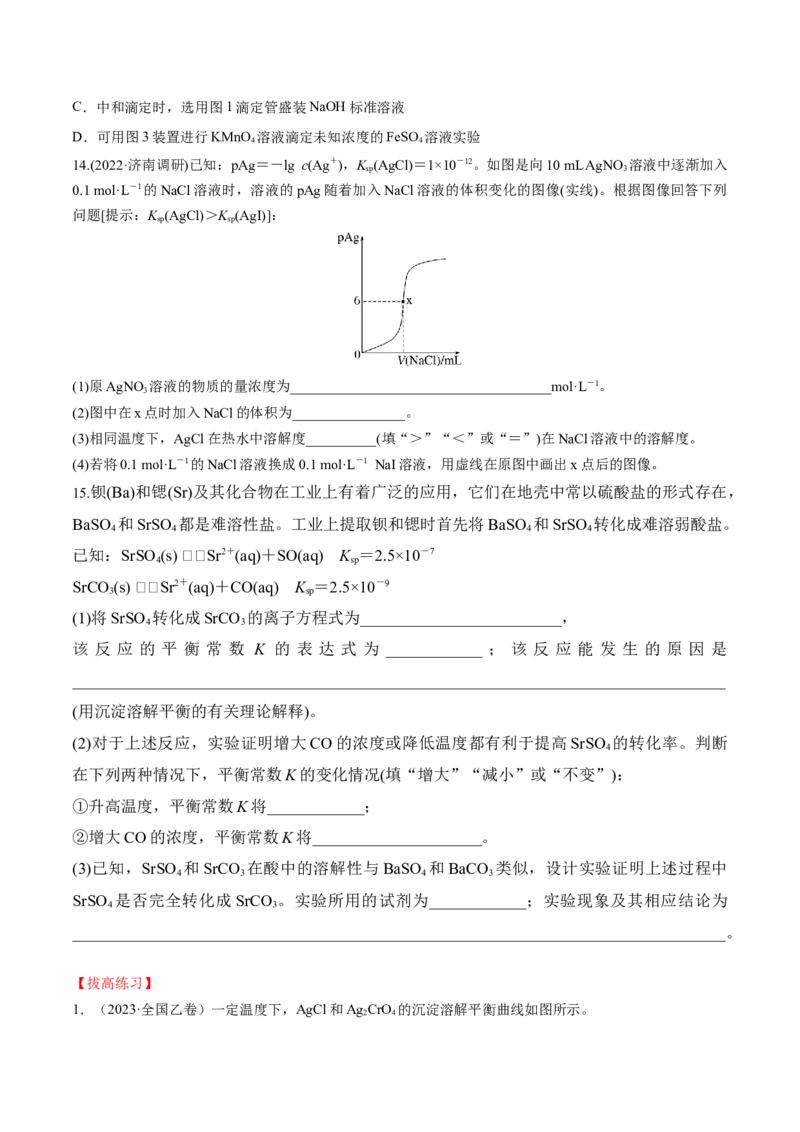
12.(2023·广州质检)某浓度的二元弱酸HB溶液在不同pH下,测得pC(M)变化如图所示[已知: pC(M)=
2
-lg c(M),M代指HB或HB-或B2-],下列说法正确的是( )
2
A.曲线 Ⅱ 表示pC(HB-)与pH关系
B.pH=5时,c(HB-)c
C.当 被完全中和时,
D.滴定至c点时,c(Na+)<2c(A2-)+c(HA-)
5..(2023·河南·校联考模拟预测)用强碱滴定某一元弱酸时,弱酸被强碱部分中和后得到“弱pH酸盐和
弱酸”组成的缓冲溶液,其中存在pH=pK 一lg 。25°C时0.1mol·L-1的NaOH溶液滴定16.00mL某未
a
知浓度的HA溶液,滴定过程中消耗NaOH溶液的体积与混合溶液pH之间的关系如图所示(已知:pK=-
a
lgK,100.48=3,酸性HA>HCN)。下列说法错误的是
a
A.25℃时,HA电离常数的数量级为10-5
B.b点溶液中存在c(HA)+c(H+)>c(A-)+c(OH-)
C.c点溶液中离子浓度的大小关系为c(HA)>c(A-)>c(H+)>c(OH-)
D.若将HA改为等体积、等浓度的HCN,则pH随NaOH溶液体积的变化曲线竖直上移
6..(2023·河南·校联考模拟预测)食用级NaHSO 产品用作防腐剂、抗氧化剂等。根据常温时下列实验得
3
到的粒子浓度关系正确的是
实验操作和现象 粒子浓度的关系
向蓝色石蕊试纸上滴入2滴0.1 mol ·L-1NaHSO 溶液,试纸
① 3 c(Na+) >c( ) >c( ) >c(HSO )
变红 2 3
向10 mL0.1 mol ·L-1NaHSO 溶液中加入等体积等浓度的 c(Na+)-c( ) -c( ) -c(H SO ) =0.05
② 3 2 3
NaOH溶液 mol ·L-1向0.1 mol ·L-1NaHSO 溶液中加入等浓度的NaOH溶液至
③ 3 c( ) +c( )=c(Na+)
pH=7
A.①③ B.②③ C.①② D.①②③
7.(2023·江苏·统考高考真题)室温下,用含少量 的 溶液制备 的过程如题图所示。已
知 , 。下列说法正确的是
A. 溶液中:
B.“除镁”得到的上层清液中:
C. 溶液中:
D.“沉锰”后的滤液中:
8..(2023·河北衡水·河北衡水中学校考模拟预测)25℃时,用 调节 二元弱酸 溶
液的 ,假设不同 下均有 。使用数字传感器测得溶液中含R微
粒的物质的量浓度随 的变化如图所示。下列分析不正确的是A.25℃时, 溶液的
B. 溶液和 溶液中 :前者大于后者
C. 的溶液中,
D.25℃时 的 ,在足量的 溶液中滴加少量 溶液,
发生反应:
9.(2023·北京朝阳·统考三模)室温下,向10.0mL纯碱(可能含有 )的稀溶液中逐滴加入
0.100mol/L盐酸,滴定曲线如图,其中p、q为滴定终点,下列分析正确的是
A.p→q,选用酚酞做指示剂,到达滴定终点时溶液由红色变为无色
B.由滴定数据可知,原纯碱中
C.p点 的主要原因:
D.q点溶液中:
10..(2023·北京海淀·北京市十一学校校考三模)为探究温度、浓度对铝和碳酸钠溶液反应的影响,某兴
趣小组查询了相关资料,并进行了实验探究。以下三组实验均采用了相同形状且等质量的打磨后的铝片。
【文献资料】
(I)铝和碱液的反应实质是铝先和水反应生成 和 ,生成的 和 反应生成 -而
溶解。
(II)碳酸氢钠溶液常温下就能缓慢分解,温度越高分解速率越大。温度/ 溶液
实验 实验现象
① 25 0.5 5 有细小的气泡
有较多气泡,气体不能使澄清石灰水变浑
② 25 a 5
浊;用试管收集的气体靠近火焰有爆鸣声
有大量白色絮状沉淀和气泡,气体可使澄
③ 80 2.0 5 清石灰水变浑浊;气体通过 溶液除
杂后用试管收集,靠近火焰有爆鸣声
下列说法不正确的是
A.
B.实验③的反应速率比实验②更大的原因之一是实验③中 浓度更大
C.实验③中的气体为 混合气体,白色沉淀的产生可能是由于 往溶液上方移动时与
反应生成
D.将实验②中的 溶液换成相同浓度的 溶液,无白色沉淀生成
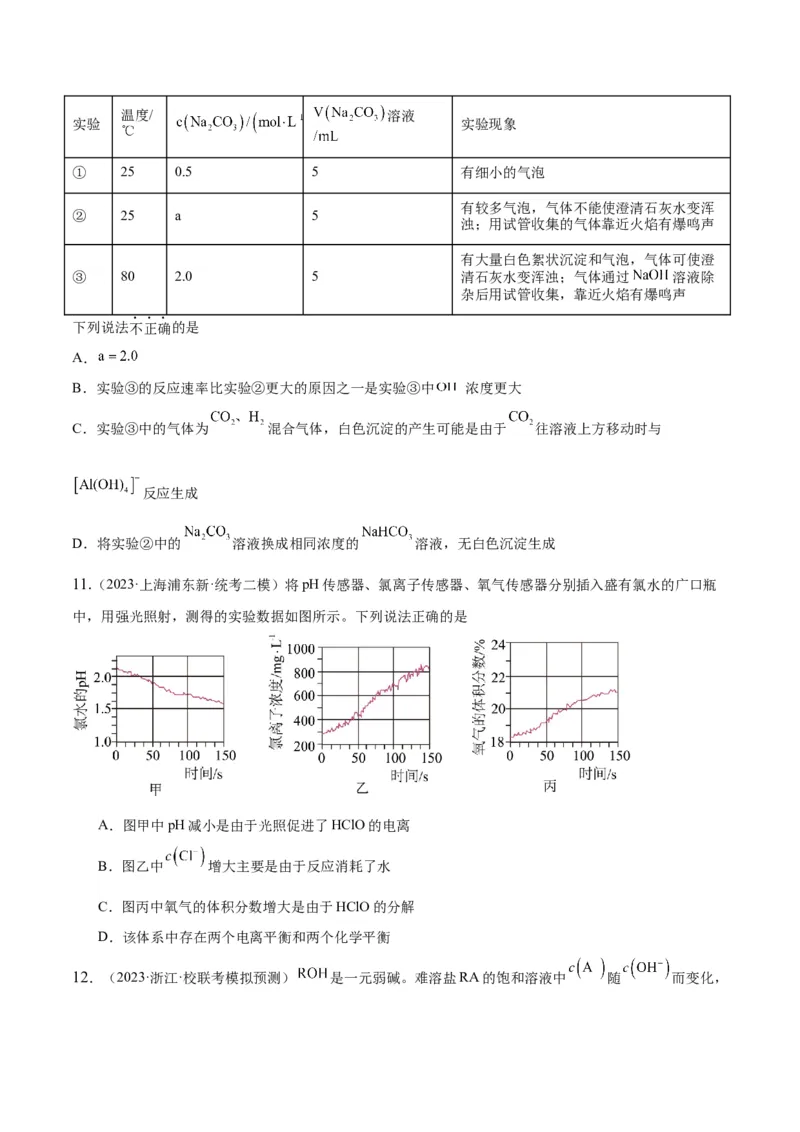
11.(2023·上海浦东新·统考二模)将pH传感器、氯离子传感器、氧气传感器分别插入盛有氯水的广口瓶
中,用强光照射,测得的实验数据如图所示。下列说法正确的是
A.图甲中pH减小是由于光照促进了HClO的电离
B.图乙中 增大主要是由于反应消耗了水
C.图丙中氧气的体积分数增大是由于HClO的分解
D.该体系中存在两个电离平衡和两个化学平衡
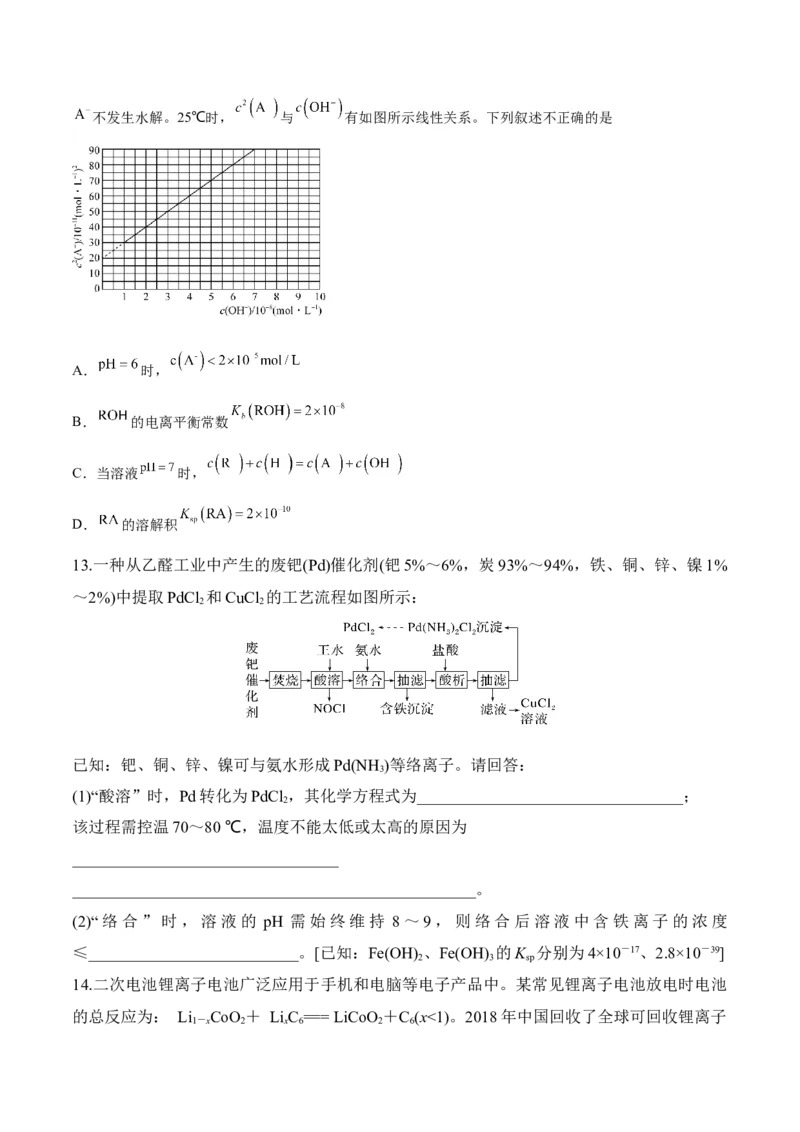
12.(2023·浙江·校联考模拟预测) 是一元弱碱。难溶盐RA的饱和溶液中 随 而变化,不发生水解。25℃时, 与 有如图所示线性关系。下列叙述不正确的是
A. 时,
B. 的电离平衡常数
C.当溶液 时,
D. 的溶解积
13.一种从乙醛工业中产生的废钯(Pd)催化剂(钯5%~6%,炭93%~94%,铁、铜、锌、镍1%
~2%)中提取PdCl 和CuCl 的工艺流程如图所示:
2 2
已知:钯、铜、锌、镍可与氨水形成Pd(NH )等络离子。请回答:
3
(1)“酸溶”时,Pd转化为PdCl ,其化学方程式为_________________________________;
2
该过程需控温70~80 ℃,温度不能太低或太高的原因为
_________________________________
__________________________________________________。
(2)“络合”时,溶液的 pH 需始终维持 8~9,则络合后溶液中含铁离子的浓度
≤__________________________。[已知:Fe(OH) 、Fe(OH) 的K 分别为4×10-17、2.8×10-39]
2 3 sp
14.二次电池锂离子电池广泛应用于手机和电脑等电子产品中。某常见锂离子电池放电时电池
的总反应为: Li CoO + Li C === LiCoO +C (x<1)。2018年中国回收了全球可回收锂离子
1-x 2 x 6 2 6电池总量的69%。但现阶段我国废旧电池回收仍属于劳动密集型产业,效率仍需提高。一种
回收该锂离子电池中的锂和钴的流程:
已知:①Na S O 是一种中等强度的还原剂,遇强酸分解
2 2 3
② Li CO 溶解度随温度升高而减小
2 3
(1)控制氢离子浓度为4 mol/L,反应温度90 ℃,测得相同时间内离子的浸出率与Na S O 溶液
2 2 3
的变化关系如图。则酸浸时应选用浓度为________mol/L的Na S O 溶液。Na S O 溶液浓度
2 2 3 2 2 3
增 至 0.3 mol/L 时 , LiCoO 的 浸 出 率 明 显 下 降 , 可 能 的 原 因 是
2
__________________________________________________(用化学方程式结合文字说明)。
(2)已知15 ℃左右 Li CO 的K 为3.2×10-2,该温度下 Li CO 的溶解度约为________g。将萃
2 3 sp 2 3
取后的 Li SO 溶液加热至95 ℃,加入饱和Na CO 溶液,反应10 min,________________(填
2 4 2 3
操作)得 Li CO 粉末。
2 3
15.(2023秋·广东湛江·高三湛江一中校考开学考试)糠酸(熔点133℃,沸点231℃,在热水中溶解度较
大,微溶于冷水)和糠醇(熔点-29℃,沸点171℃)均为重要的化工中间体,工业上可利用糠醛(沸点
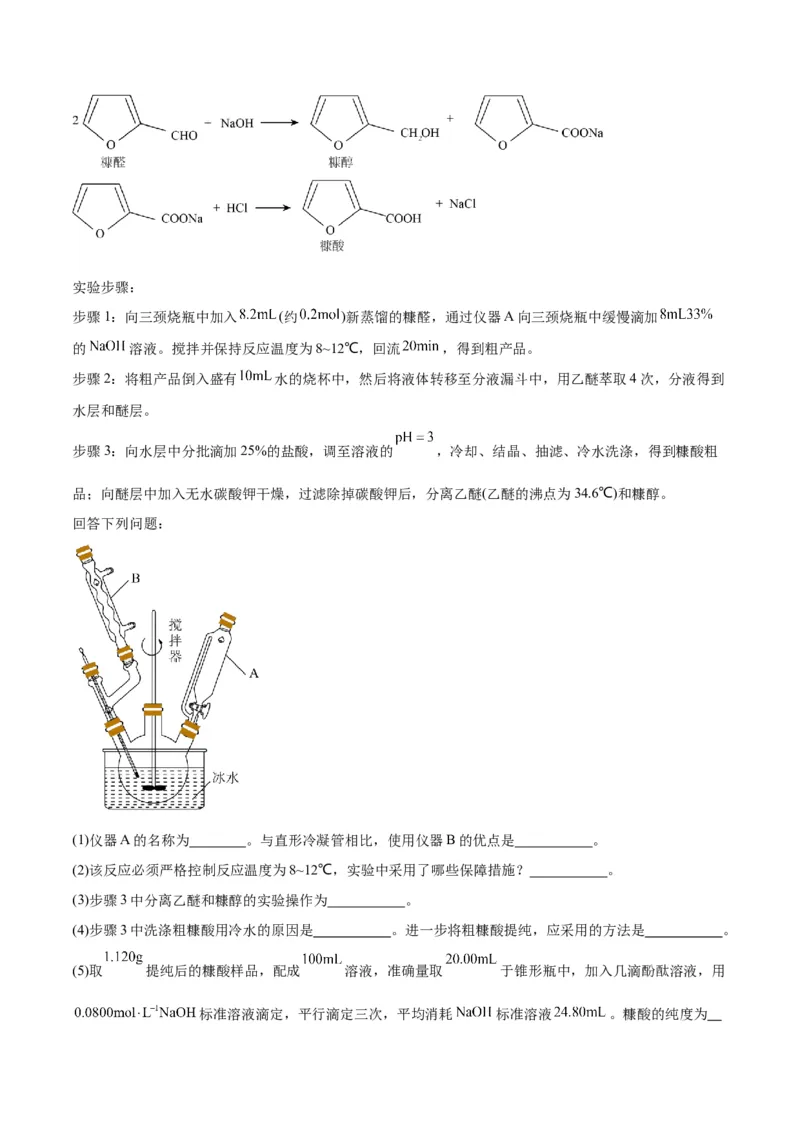
161.7℃,易被氧化)发生歧化反应制取这两种物质(该反应为强放热反应),反应原理如下:实验步骤:
步骤1:向三颈烧瓶中加入 (约 )新蒸馏的糠醛,通过仪器A向三颈烧瓶中缓慢滴加
的 溶液。搅拌并保持反应温度为8~12℃,回流 ,得到粗产品。
步骤2:将粗产品倒入盛有 水的烧杯中,然后将液体转移至分液漏斗中,用乙醚萃取4次,分液得到
水层和醚层。
步骤3:向水层中分批滴加25%的盐酸,调至溶液的 ,冷却、结晶、抽滤、冷水洗涤,得到糠酸粗
品;向醚层中加入无水碳酸钾干燥,过滤除掉碳酸钾后,分离乙醚(乙醚的沸点为34.6℃)和糠醇。
回答下列问题:
(1)仪器A的名称为 。与直形冷凝管相比,使用仪器B的优点是 。
(2)该反应必须严格控制反应温度为8~12℃,实验中采用了哪些保障措施? 。
(3)步骤3中分离乙醚和糠醇的实验操作为 。
(4)步骤3中洗涤粗糠酸用冷水的原因是 。进一步将粗糠酸提纯,应采用的方法是 。
(5)取 提纯后的糠酸样品,配成 溶液,准确量取 于锥形瓶中,加入几滴酚酞溶液,用
标准溶液滴定,平行滴定三次,平均消耗 标准溶液 。糠酸的纯度为。该中和滴定实验中,若其他实验操作均正确,则下列实验操作造成测得的糠酸的纯度比实际偏低的是
(填标号)。
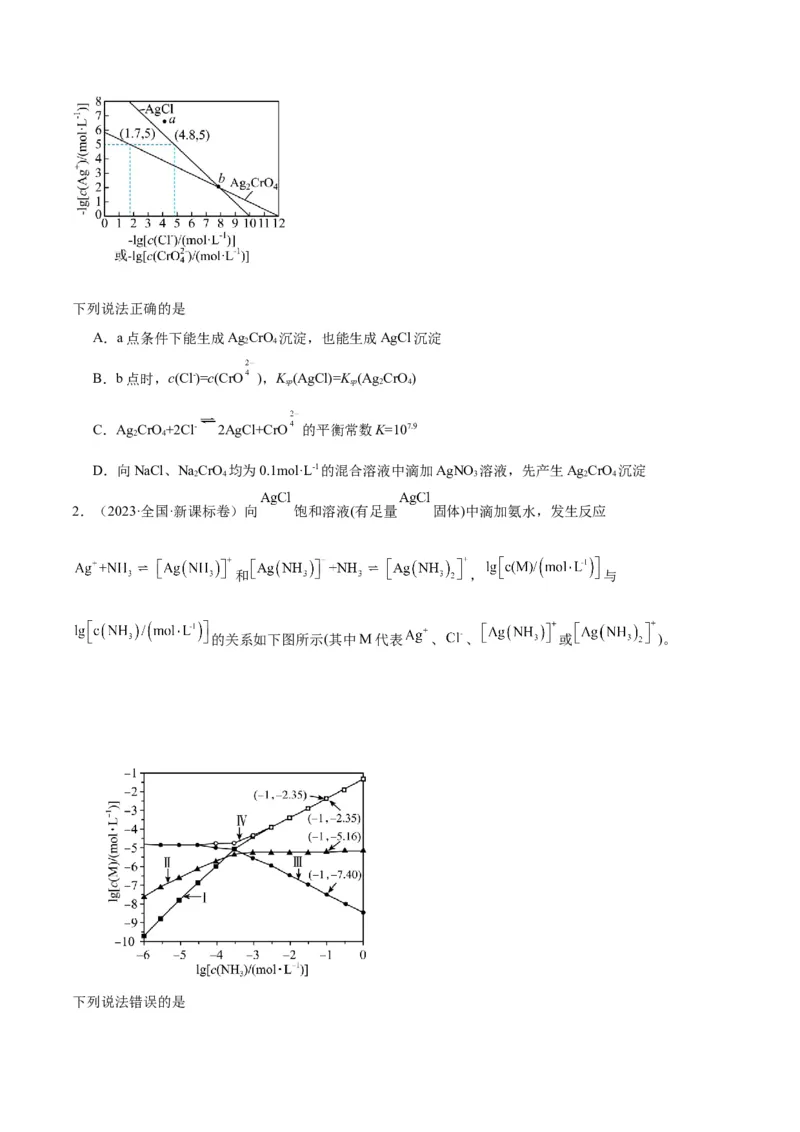
A.蒸馏水洗净后,末用 标准溶液润洗碱式滴定管
B.指示剂酚酞溶液滴加过多(酚酞是一种弱酸)
C.锥形瓶内壁用蒸馏水洗净后,再用配制好的糠酸样品溶液润洗2~3次,将润洗液倒掉,再装入
糠酸样品溶液,进行中和滴定
D.滴定前仰视碱式滴定管液面读数,滴定后俯视碱式滴定管液面读数