文档内容
专题 10 化学反应速率与平衡
第 29 练 化学反应的调控
1.合成氨反应中催化剂的作用是( )
A.使逆反应不发生
B.使平衡向正反应方向移动
C.加快正、逆反应速率,缩短达到平衡的时间
D.提高原料的转化率
2.下列生活和生产中的做法或事实,与调控反应速率无关的是( )
A.牛奶放在冰箱中冷藏
B.使用加酶洗衣粉洗涤衣物
C.汽车的橡胶轮胎中要添加抑制剂
D.工业合成氨时,及时将氨气液化分离
3.不符合工业合成氨生产实际的是
A.铁触媒作催化剂 B.N、H 循环使用
2 2
C.NH 液化分离 D.反应在常压下进行
3
4.下列有关合成氨工业的叙述,可用勒夏特列原理来解释的是
A.使用铁触媒,使N 和H 混合气体有利于合成氨
2 2
B.高压比常压条件更有利于合成氨的反应
C.700K左右比室温更有利于合成氨的反应
D.合成氨时采用循环操作,可提高原料的利用率
5.在合成氨工业中,为增加NH 的日产量,下列操作与平衡移动无关的是( )
3
A.不断将氨分离出来
B.使用催化剂
C.采用500 ℃左右的高温而不是700 ℃的高温
D.采用2×107~5×107 Pa的压强
6.下图为工业合成氨的流程图。图中为提高原料转化率而采取的措施是( )A.①②③ B.①③⑤ C.②④⑤ D.②③④
7.关于工业合成氨的叙述中,错误的是( )
A.在动力、设备、材料允许的情况下,反应尽可能在高压下进行
B.温度越高越有利于工业合成氨
C.在工业合成氨中N、H 的循环利用可提高其利用率,降低成本
2 2
D.及时从反应体系中分离出氨气有利于平衡向正反应方向移动
8.下列有关合成氨工业的说法中正确的是( )
A.从合成塔出来的混合气体,其中NH 只占15%,所以生产氨的效率都很低
3
B.由于氨易液化,N、H 是循环使用的,总体来说氨的产率很高
2 2
C.合成氨反应温度控制在400~500 ℃,目的是使化学平衡向正反应方向移动
D.合成氨采用的压强是10~30 MPa,因为该压强下铁触媒的活性最大
9.对于可逆反应N(g)+3H(g) 2NH (g) ΔH<0,下列说法中正确的是( )
2 2 3
A.达到平衡后充入N,当重新达到平衡时,NH 的浓度比原平衡的大,N 的浓度比原平衡的小
2 3 2
B.达到平衡后,升高温度,既加快了正、逆反应速率,又提高了NH 的产率
3
C.达到平衡后,缩小容器体积,既有利于加快正、逆反应速率,又有利于提高氢气的转化率
D.加入催化剂可以缩短达到平衡的时间,是因为正反应速率增大,而逆反应速率减小
10.将等物质的量的N 、H 充入某密闭容器中,在一定条件下,发生如下反应并达到平衡:N(g)
2 2 2
+3H (g) 2NH (g) ΔH<0。当改变某个条件并维持新条件直至新的平衡时,下表中关于新平衡与原
2 3
平衡的比较正确的是( )。
改变条件 新平衡与原平衡比较
A 压缩体积 N 的浓度一定变小
2
B 升高温度 N 的转化率变小
2
C 充入一定量H H 的转化率不变,N 的转化率变大
2 2 2
D 使用适当催化剂 NH 的体积分数增大
31.在合成氨反应中使用催化剂和增大压强,下列叙述中正确的是( )
A.都能增大反应速率,都对化学平衡无影响
B.都对化学平衡有影响,但都不影响达到平衡状态所用的时间
C.都能缩短达到平衡状态所用的时间,只有增大压强对化学平衡有影响
D.使用催化剂能缩短反应达到平衡状态所用的时间,而增大压强无此效果
2.下列有关合成氨工业的说法中正确的是( )
A.铁触媒作催化剂可加快反应速率,且有利于化学平衡向合成氨的方向移动
B.升高温度可以加快反应速率,且有利于化学平衡向合成氨的方向移动
C.增大压强能缩短达到平衡状态所用的时间
D.合成氨采用的压强是10~30 MPa,因为该压强下铁触媒的活性最高
3.合成氨反应的正反应是气体体积减小的放热反应。合成氨工业的生产流程如下:
关于合成氨工业的说法中不正确的是( )
A.混合气进行循环利用遵循绿色化学思想
B.合成氨反应须在低温下进行
C.对原料气进行压缩是为了增大原料气的转化率
D.使用催化剂可以提高反应的速率,但是不能使平衡向正反应方向移动
4.在一定条件下,对于密闭容器中的反应:N+3H 2NH ,下列说法正确的是( )
2 2 3
A.当氮气和氢气投料比(物质的量之比)为1∶3时,达到平衡时氨的体积分数最大
B.增加铁触媒的接触面积,不可能提高合成氨工厂的年产量
C.达到平衡时,氢气和氨气的浓度比一定为3∶2
D.分别用氮气和氢气来表示该反应的转化率时,数值大小一定相同
5.SO 在400~600℃下的催化氧化:2SO +O 2SO ,已知此正反应放热。如果反应在密闭容器
2 2 2 3
中进行,下列有关说法中错误的是( )
A.在上述条件下,SO 不可能完全转化为SO
2 3
B.达到平衡时,SO 的浓度与SO 的浓度一定相等
2 3
C.使用催化剂是为了加快反应速率,提高生产效率
D.为了提高SO 的转化率,可适当提高O 的浓度
2 2
6.4NH (g)+5O(g) 4NO(g)+6H O(g) 是工业上制硝酸的重要反应,下列有关说法错误的是
3 2 2A.使用催化剂可以加快反应速率
B.增大压强可以加快反应速率
C.达到平衡时,V =V
(正) (逆)
D.增大O 的浓度可以使NH 全部转变为NO
2 3
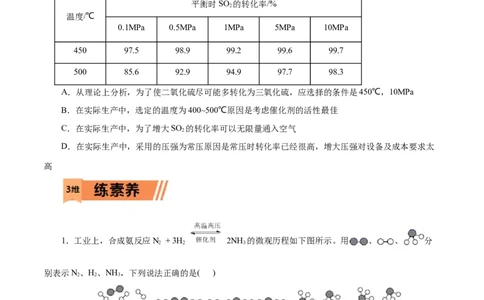
7.在硫酸工业中,通过下列反应使SO 氧化为SO :2SO (g)+O(g) 2SO (g)
2 3 2 2 3
H=-196.6kJ/mol。下表列出了在不同温度和压强下,反应达到平衡时SO 的转化率。下列说法错误的是(
2
△)
平衡时SO 的转化率/%
2
温度/℃
0.1MPa 0.5MPa 1MPa 5MPa 10MPa
450 97.5 98.9 99.2 99.6 99.7
500 85.6 92.9 94.9 97.7 98.3
A.从理论上分析,为了使二氧化硫尽可能多转化为三氧化硫,应选择的条件是450℃,10MPa
B.在实际生产中,选定的温度为400~500℃原因是考虑催化剂的活性最佳
C.在实际生产中,为了增大SO 的转化率可以无限量通入空气
2
D.在实际生产中,采用的压强为常压原因是常压时转化率已经很高,增大压强对设备及成本要求太
高
1.工业上,合成氨反应N + 3H 2NH 的微观历程如下图所示。用 、 、 分
2 2 3
别表示N、H、NH ,下列说法正确的是( )
2 2 3
A.①→② 催化剂在吸附N、H 时,形成新的化学键
2 2
B.②→③ 形成N原子和H原子是放热过程
C.①→⑤ N 和H 全部化合成氨气
2 2
D.使用合适的催化剂,能提高合成氨反应的效率
2.已知:2SO (g)+ O (g)= 2SO (g) H =-197.8kJ•mol—1。起始反应物为SO 和 O(物质的量之比为2:
2 2 3 2 2
△1,且总物质的量不变)。SO 的平衡转化率(%)随温度和压强的变化如下表,下列说法不正确的是( )
2
压强/(105Pa)
温度/K
1.01 5.07 10.1 25.3 50.7
673 99.2 99.6 99.7 99.8 99.9
723 97.5 98.9 99.2 99.5 99.6
773 93.5 96.9 97.8 98.6 99.0
A.一定压强下降低温度,SO 的转化率增大
2
B.在不同温度、压强下,转化相同物质的量的SO 所需要的时间相等
2
C.使用催化剂可以缩短反应达到平衡所需的时间
D.工业生产通常不采取加压措施是因为常压下SO 的转化率已相当高
2
3.(2022·浙江省6月选考)关于反应Cl(g)+HO(l) HClO(aq)+ H+(aq)+ Cl-(aq) ΔH<0,达到平
2 2
衡后,下列说法不正确的是( )
A.升高温度,氯水中的c(HClO)减小
B.氯水中加入少量醋酸钠固体,上述平衡正向移动,c(HClO)增大
C.取氯水稀释,c(Cl-)/ c(HClO)增大
D.取两份氯水,分别滴加AgNO 溶液和淀粉KI溶液,若前者有白色沉淀,后者溶液变蓝色,可以
3
证明上述反应存在限度
4.硫在不同温度下的状态和分子结构不同,单质硫S 环状分子的结构如图。把硫加热超过其熔点就
8
变成黄色流动性液休;433K以上液态硫颜色变深,黏度增加;523K以上黏度下降;717.6K时硫变为蒸气,
蒸气中存在3S 4S 6S 12S,温度越高,蒸气的平均相对分子质量越小。下列说法正确
8 6 4 2
的是( )
A.对于3S 4S 6S 12S H<0
8 6 4 2
B.温度越高,S 蒸气中的含量越低 △
2
C.可用酒精洗涤试管中残留的硫单质
D.433K以上液态硫颜色变深,黏度增加,可能与S 的环状结构断裂变为无限长链状结构有关
8
5.接触法制硫酸的工艺流程中的关键步骤是SO 的催化氧化:2SO +O 2SO ΔH<0,在催化剂
2 2 2 3表面的反应历程如下:
下列说法正确的是( )
A.过程中既有V—O键的断裂,又有V—O键的形成
B.该反应的中间产物是VO
2 5
C.反应①的活化能比反应②小
D.反应放热,为提高SO 转化率,应尽可能在较低温度下反应
2
6.五氧化二氮(化学式:NO)又称硝酐,是硝酸的酸酐,在一定温度下可发生以下反应:2NO
2 5 2 5
4NO +O 。某温度下,向恒容密闭容器中充入NO,发生上述反应,部分实验数据见下表:
2 2 2 5
下列说法正确的是( )
时间/s 0 500 1000 1500
5.00 3.52 2.50 2.50
A.0~1000s内,v(O )=1.0×102mol·L-1·s-1
2
B.当气体密度不变时,反应达到平衡状态
C.该温度下反应的平衡常数K=125
D.反应达到平衡后,保持其他条件不变,加入合适的催化剂,ΔH变大
7.已知反应:CO(g)+2H(g) CHOH (g) ΔH<0,在起始温度均为T℃、容积均为2L的密
2 3
闭容器中发生反应的部分数据如下表所示。下列说法正确的是( )
反应条件 反应时间/min CO/mol
0 3 6 0
5 5
反应Ⅰ:恒温
恒容
12 2
15 1反应Ⅱ:绝热
0 0 0 3
恒容
A.对于反应Ⅰ,达到平衡时H 的转化率为40%
2
B.达到平衡时,反应Ⅰ和Ⅱ的平衡常数
C.15min时,向反应Ⅰ的容器中再充入CO和CHOH各1mol,H 的转化率不变
3 2
D.选择高效的催化剂,可以提高CHOH的产率
3
8.在2个初始温度均为T℃的密闭容器中发生反应:2SO (g)+O(g) 2SO (g)(正反应放热 。下
2 2 3
列说法正确的是( )
起始物质的量/mol 平衡时SO 物质的量/mol
3
容器编号 容器类型 初始体积
SO O SO
2 2 3
Ⅰ 恒温恒容 1.0L 2 1 0 1.6
Ⅱ 恒温恒压 1.0L 2 1 0 a
A.a>1.6
B.选择不同的催化剂,该反应的反应速率和平衡转化率都将不同
C.随反应进行SO 的浓度逐渐减小,达到平衡时,正反应速率最小,此时v正(SO )=0
2 2
D.若起始时向容器Ⅰ中充入1molSO (g)、0.2molO(g)和4molSO (g),则反应将向正反应方向进行
2 2 3