文档内容
训练(三十九) 水的电离和溶液的酸碱性
1.(2021·宁夏青铜峡中学检测)下列液体均处于25 ℃,有关叙述正确的是( )
A.某物质的溶液pH<7,则该物质一定是酸
B.相同条件下,pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍
C.将1 L 0.1 mol/L的Ba(OH) 溶液稀释为2 L,pH=12
2
D.pH=8的NaOH溶液稀释100倍,其pH=6
B [25 ℃时溶液pH<7,该溶液呈酸性,但不一定是酸,可以是酸式盐等,如NaHSO 等,
4
A错误;pH=4.5的番茄汁中c(H+)=10-4.5 mol/L,pH=6.5的牛奶中c(H+)=10-6.5mol/L,故
前者是后者的100倍,B正确;将1 L 0.1 mol/L的Ba(OH) 溶液稀释为2 L,c(OH-)=0.1
2
mol/L,该溶液的pH=13,C错误;pH=8的NaOH溶液稀释100倍,所得溶液仍呈碱性,其
pH接近于7,但大于7,D错误。]
2.(2021·山东实验中学检测)X、Y、Z三种液体的近似pH如图,下列判断正确的是( )
A.X可能是醋酸钠溶液
B.Y可能是90 ℃时的纯水
C.Y一定是正盐溶液
D.Z可使甲基橙试液变黄
D [溶液X的pH=1,溶液呈酸性,而醋酸钠溶液由于CHCOO-的水解而使溶液呈碱
3
性,A错误;升高温度,水的电离程度增大,水的离子积K 增大,水的pH减小,故90 ℃时纯
w
水的pH<7,B错误;Y点溶液pH=7,由于题目未指明温度,无法判断溶液的酸碱性和种类,
C错误;Z点溶液的pH=10,溶液呈碱性,可使甲基橙试液变黄,D正确。]
3.(2021·河北辛集中学检测)溶液的酸碱性是衡量人体健康状况的重要指标,下列有关
溶液的酸碱性及pH的应用说法正确的是( )
A.某溶液中c(H+)小于10-7 mol·L-1,则该溶液呈碱性
B.测溶液的pH时,pH试纸若用蒸馏水润湿,测定结果一定会偏低
C.常温下,pH=11的氨水稀释100倍后,其pH=9
D.常温下,pH=12的KOH溶液与pH=2的甲酸溶液等体积混合后,滴入石蕊溶液呈
红色
D [常温下,c(H+)小于10-7 mol·L-1的溶液呈碱性,但未知温度,A错误;若用蒸馏水润湿的pH试纸测中性溶液的pH,无影响,B错误;稀释过程中,一水合氨继续电离,pH>9,
测酸性溶液的pH偏高,C错误;KOH与HCOOH反应后HCOOH有剩余,显酸性,滴入石蕊
溶液呈红色,D正确。]
4.(2021·湖北沙市中学检测)现有常温下0.1 mol/L的NaSO 溶液。欲使此溶液中水的电
2 4
离平衡向右移动,且pH<7,有下列措施:①给溶液加热;②加入少量稀硫酸;③加入NH Cl
4
晶体;④加入CHCOONa固体;⑤加入BaCl 溶液;⑥加入FeCl 溶液。其中能达到目的是(
3 2 3
)
A.①③⑥ B.①②③
C.②③④ D.③⑤⑥
A [①水电离过程为吸热过程,加热促进水的电离,溶液中氢离子浓度增大,pH<7,①
正确;②加入少量稀硫酸抑制水的电离,②错误;③加入NH Cl晶体溶解后NH与OH-反应,
4
水的电离平衡向右移动,且pH<7,③正确;④加入CHCOONa固体,溶解后醋酸根离子水
3
解促进水的电离,溶液显碱性,PH>7,④错误;⑤加入BaCl 溶液,氯化钡是强酸强碱盐对水
2
的电离无影响,⑤错误;⑥加入FeCl 溶液,铁离子水解促进水的电离,溶液显酸性,pH<7,
3
⑥正确。]
5.(2021·山东聊城调研)关于室温下pH=2的盐酸和0.01 mol·L-1的醋酸溶液,下列说法
正确的是( )
A.两溶液中溶质的物质的量:n(CHCOOH)=n(HCl)
3
B.两溶液中阴离子的浓度:c(CHCOO-)<c(Cl-)
3
C.相同体积的两溶液均用水稀释100倍后,盐酸的pH比醋酸的大
D.相同体积的两溶液分别与足量镁条反应,盐酸产生的气体比醋酸的多
B [醋酸是弱电解质,pH=2的盐酸中c(HCl)=0.01 mol/L,与醋酸等体积时所含溶质的
物质的量相等,否则不相等,A错误;醋酸部分电离,则c(CHCOO-)<0.01 mol/L,盐酸中c(Cl
3
-)=0.01 mol/L,B正确;相同体积两溶液均稀释100倍,盐酸中c(H+)仍大于醋酸,故盐酸的
pH小,C错误;相同体积时,n(CHCOOH)=n(HCl),则与足量镁条反应,产生气体的量相等,
3
D错误。]
6.(2021·贵州思南中学检测)已知室温时,0.1 mol·L-1某一元酸HA在水中有0.1%发生
电离,下列叙述错误的是( )
A.该溶液的pH=4
B.升高温度,溶液的pH增大
C.此酸的电离常数约为1×10-7D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍
B [室温时,0.1 mol·L-1一元酸HA在水中有0.1%发生电离,则电离产生的c(H+)=0.1
mol·L-1×0.1%=1×10-4 mol·L-1,pH=-lg 1×10-4=4,A正确;升高温度,HA的电离程
度增大,电离产生的c(H+)增大,溶液的pH减小,B错误;HA的电离常数为K(HA)=,此时
a
c(H+)=c(A-)≈1×10-4 mol·L-1,c(HA)≈0.1 mol·L-1,故K(HA)==1×10-7,C正确;HA
a
电离产生的c(H+)=1×10-4 mol·L-1,而HA溶液中由水电离出的 c(H+) =c(OH-) =
水 水
(1×10-14)/( 1×10-4)=1×10-10 mol·L-1,故由HA电离出的c(H+)约为水电离出的c(H+)的
106倍,D正确。]
7.(2021·陕西西安检测)25 ℃时,甲、乙两烧杯均盛有5 mL pH=3的某一元酸溶液,向乙
烧杯中加水稀释至pH=4。下列关于甲烧杯和稀释后的乙烧杯中的溶液的描述中,不正确的
是( )
A.溶液的体积:10V ≤V
甲 乙
B.水电离出的OH-浓度:10c(OH-) =c(OH-)
甲 乙
C.若分别用等浓度的NaOH溶液完全中和,所得溶液的pH:甲≤乙
D.若分别与5 mL pH=11的NaOH溶液反应,所得溶液的pH:甲≤乙
C [若为强酸,则应加水稀释到体积是原来的10倍,若为弱酸,由于有电离平衡的移动,
加水的体积要多,稀释的倍数大于10,A项正确;在甲溶液中水电离的c(OH-)=10-11 mol·L
-1,乙溶液中,水电离的c(OH-)=10-10 mol·L-1,B项正确;由于甲和乙中含有的一元酸的物
质的量相等,用NaOH中和后得到盐的物质的量也相等,若为强酸,则溶液为中性,若为弱酸,
溶液显碱性,而且浓度越小,其pH越小,C项错误;根据酸碱混合时的规律,当pH加和等于
14的酸碱等体积混合时,谁弱显谁性。若酸为强酸,则反应后溶液为中性,甲反应后再加水稀
释得到乙反应后的溶液,溶液也为中性;若酸为弱酸,则反应后溶液显酸性,浓度越小,其pH
越大,D项正确。]
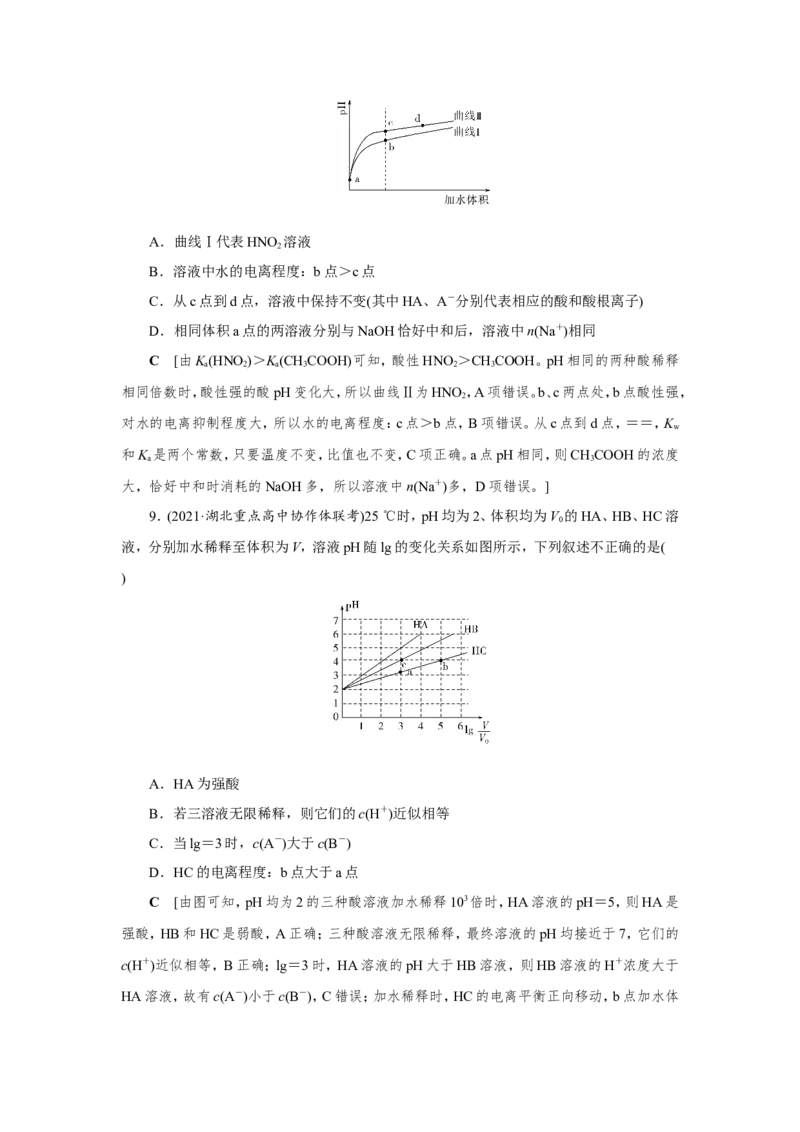
8.(2019·天津卷)某温度下,HNO 和CHCOOH的电离常数分别为5.0×10-4和1.7×10
2 3
-5。将pH和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙
述正确的是( )A.曲线Ⅰ代表HNO 溶液
2
B.溶液中水的电离程度:b点>c点
C.从c点到d点,溶液中保持不变(其中HA、A-分别代表相应的酸和酸根离子)
D.相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同
C [由K(HNO)>K(CHCOOH)可知,酸性HNO>CHCOOH。pH相同的两种酸稀释
a 2 a 3 2 3
相同倍数时,酸性强的酸pH变化大,所以曲线Ⅱ为HNO,A项错误。b、c两点处,b点酸性强,
2
对水的电离抑制程度大,所以水的电离程度:c点>b点,B项错误。从c点到d点,==,K
w
和K 是两个常数,只要温度不变,比值也不变,C项正确。a点pH相同,则CHCOOH的浓度
a 3
大,恰好中和时消耗的NaOH多,所以溶液中n(Na+)多,D项错误。]
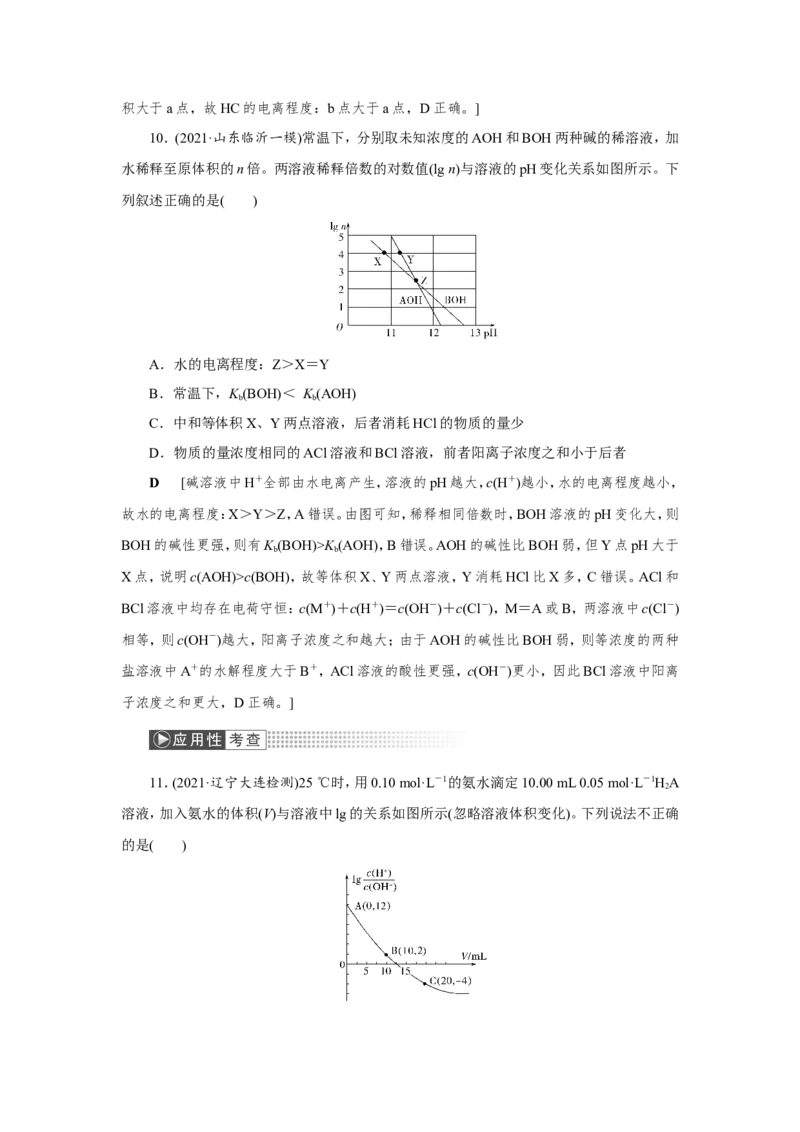
9.(2021·湖北重点高中协作体联考)25 ℃时,pH均为2、体积均为V 的HA、HB、HC溶
0
液,分别加水稀释至体积为V,溶液pH随lg的变化关系如图所示,下列叙述不正确的是(
)
A.HA为强酸
B.若三溶液无限稀释,则它们的c(H+)近似相等
C.当lg=3时,c(A-)大于c(B-)
D.HC的电离程度:b点大于a点
C [由图可知,pH均为2的三种酸溶液加水稀释103倍时,HA溶液的pH=5,则HA是
强酸,HB和HC是弱酸,A正确;三种酸溶液无限稀释,最终溶液的pH均接近于7,它们的
c(H+)近似相等,B正确;lg=3时,HA溶液的pH大于HB溶液,则HB溶液的H+浓度大于
HA溶液,故有c(A-)小于c(B-),C错误;加水稀释时,HC的电离平衡正向移动,b点加水体积大于a点,故HC的电离程度:b点大于a点,D正确。]
10.(2021·山东临沂一模)常温下,分别取未知浓度的AOH和BOH两种碱的稀溶液,加
水稀释至原体积的n倍。两溶液稀释倍数的对数值(lg n)与溶液的pH变化关系如图所示。下
列叙述正确的是( )
A.水的电离程度:Z>X=Y
B.常温下,K (BOH)< K (AOH)
b b
C.中和等体积X、Y两点溶液,后者消耗HCl的物质的量少
D.物质的量浓度相同的ACl溶液和BCl溶液,前者阳离子浓度之和小于后者
D [碱溶液中H+全部由水电离产生,溶液的pH越大,c(H+)越小,水的电离程度越小,
故水的电离程度:X>Y>Z,A错误。由图可知,稀释相同倍数时,BOH溶液的pH变化大,则
BOH的碱性更强,则有K (BOH)>K (AOH),B错误。AOH的碱性比BOH弱,但Y点pH大于
b b
X点,说明c(AOH)>c(BOH),故等体积X、Y两点溶液,Y消耗HCl比X多,C错误。ACl和
BCl溶液中均存在电荷守恒:c(M+)+c(H+)=c(OH-)+c(Cl-),M=A或B,两溶液中c(Cl-)
相等,则c(OH-)越大,阳离子浓度之和越大;由于AOH的碱性比BOH弱,则等浓度的两种
盐溶液中A+的水解程度大于B+,ACl溶液的酸性更强,c(OH-)更小,因此BCl溶液中阳离
子浓度之和更大,D正确。]
11.(2021·辽宁大连检测)25 ℃时,用0.10 mol·L-1的氨水滴定10.00 mL 0.05 mol·L-1HA
2
溶液,加入氨水的体积(V)与溶液中lg的关系如图所示(忽略溶液体积变化)。下列说法不正确
的是( )A.A点溶液的pH等于1
B.由图中数据可知,HA为弱酸
2
C.B点水电离出的H+浓度为1.0×10-6 mol·L-1
D.C点溶液中c(NH)>c(A2-)>c(OH-)>c(H+)
B [A点:根据c(H+) ·c(OH-)=K =1×10-14,lg=12,计算得c(H+)=10-1 mol·L-1,
w
则pH=1,0.05 mol·L-1HA完全电离,HA为强酸,A正确,B错误;B点酸碱恰好完全中和
2 2
生成盐(NH )A,lg=2,计算得c(H+)=10-6 mol·L-1,则水电离出的H+浓度为1.0×10-6
4 2
mol·L-1,C正确;C点为(NH )A与NH ·HO的混合物,根据lg=-4,计算得c(H+)=10-
4 2 3 2
9mol·L-1,则pH=9,呈碱性,考虑氨水的电离平衡,则溶液中c(NH)>c(A2-)>c(OH-)>c(H+),
D正确。]
12.(2021·天津和平区检测)(1)常温下,将1 mL pH=1的HSO 溶液加水稀释到100
2 4
mL,稀释后的溶液中=________。
(2)某温度时,测得0.01 mol·L-1的NaOH溶液的pH为11,则该温度下水的离子积常数
K =________。该温度________(填“高于”或“低于”)25 ℃。
w
(3)常温下,设pH=5的HSO 溶液中由水电离出的H+浓度为c;pH=5的Al (SO ) 溶
2 4 1 2 4 3
液中由水电离出的H+浓度为c,则=________。
2
(4)常温下,pH=13的Ba(OH) 溶液a L与pH=3的HSO 溶液b L混合(混合后溶液体
2 2 4
积变化忽略不计)。若所得混合溶液呈中性,则a∶b=________。若所得混合溶液pH=12,则
a∶b=________。
(5)在(2)所述温度下,将pH=a的NaOH溶液V L与pH=b的硫酸V L混合。
a b
①若所得混合液为中性,且a=12,b=2,则V∶V=________。
a b
②若所得混合液的pH=10,且a=12,b=2,则V∶V=________。
a b
解析 (3)c=c(OH-)=10-9 mol·L-1,c=c(H+)=10-5 mol·L-1。(4)若呈中性,则0.1 a
1 2
=10-3b,a∶b=1∶100;若pH=12,则c(OH-)==0.01 mol·L-1,a∶b=11∶90。(5)K =
w
1×10-13,①若呈中性,则10-13+a·V=10-b·V,将a=12,b=2代入,得V∶V=1∶10。②
a b a b
若pH=10,则呈碱性,c(OH-) ==10-3 mol·L-1,而c(OH-) =,将a=12,b=2代入,得
混 混
V∶V=1∶9。
a b
答案 (1)108 (2)1×10-13 高于 (3)10-4 (4)1∶100 11∶90 (5)①1∶10
②1∶9