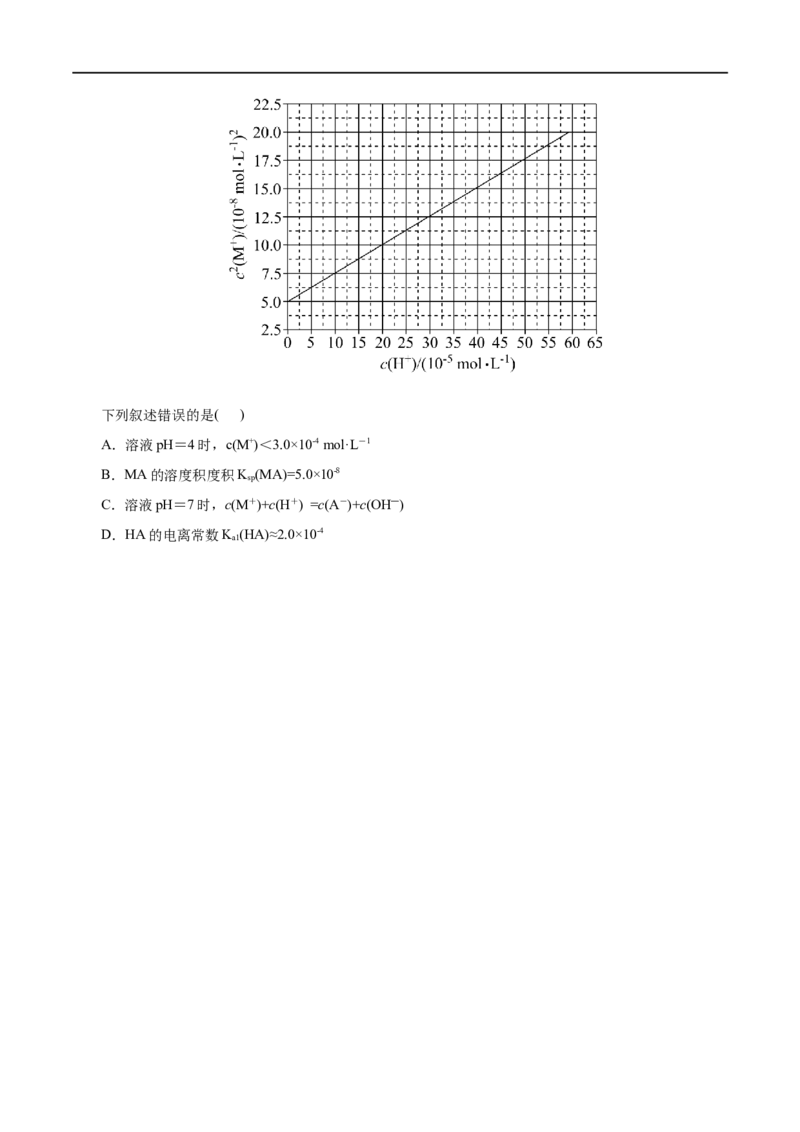文档内容
专题 11 水溶液中的离子反应与平衡
第 33 练 沉淀溶解平衡
1.下列对“难溶”的理解正确的是( )
A.在水中难溶的物质,在其他溶剂中也是难溶的
B.难溶就是绝对不溶
C.难溶就是溶解度相对较小,没有绝对不溶于水的电解质
D.如果向某溶液中加入足量另一种试剂时,生成了难溶性的电解质,则说明原溶液中的相应离子已
沉淀完全
2.下列有关AgCl沉淀的溶解平衡状态的说法中,正确的是( )
A.AgCl沉淀的生成和溶解不断进行,但速率相等
B.AgCl难溶于水,溶液中没有Ag+和Cl-
C.升高温度,AgCl的溶解度不变
D.向AgCl沉淀的溶解平衡体系中加入NaCl固体,AgCl的溶解度不变
3.为除去MgCl 酸性溶液中的Fe3+,可在加热搅拌的条件下加入的一种试剂是( )
2
A.NH ·H O B.NaOH C.NaCO D.MgCO
3 2 2 3 3
4.在下列溶液中,AgCl的溶解度最小的是( )
A.0.5mol/L AgNO 溶液 B.0.5mol/LKClO 溶液
3 3
C.0.1mol/LNaCl溶液 D.0.3mol/L AlCl 溶液
3
5.在CaCO 饱和溶液中,加入NaCO 固体,达到平衡时( )
3 2 3
A.c(Ca2+)=c(CO2-)
3
B.c(Ca2+)=c(CO2-)=
3
C.c(Ca2+)≠c(CO2-),c(Ca2+)·c(CO2-)=K (CaCO)
3 3 sp 3
D.c(Ca2+)≠c(CO2-),c(Ca2+)·c(CO2-)≠K (CaCO)
3 3 sp 3
6.已知25℃时,K [Mg(OH) ]=1.8×10-11、K [Cu(OH) ]=2.2×10-20。在c(Mg2+)=c(Cu2+)的酸性溶液中,
sp 2 sp 2
逐滴加入NaOH稀溶液使pH慢慢増大,下列判断正确的是( )
A.Mg2+先沉淀 B.Cu2+先沉淀
C.同时沉淀 D.Mg2+和Cu2+均不可能沉淀
7.在1L0.01mol·L-1MgCl 溶液中,加入1mL0.01mol·L-1的NaCO 溶液,下列说法正确的是(已知
2 2 3MgCO 的K =6.8×10-6mol2·L-2) ( )
3 sp
A.有MgCO 沉淀析出 B.无MgCO 沉淀析出
3 3
C.无法确定 D.有沉淀但不是MgCO
3
8.一定温度下,将有缺角的BaSO 晶体置于饱和BaSO 溶液中,一段时间后缺角消失得到有规则的
4 4
BaSO 晶体。下列说法中正确的是( )
4
A.BaSO 晶体质量会增加 B.BaSO 晶体质量会减小
4 4
C.溶液中c(Ba2+)增大 D.溶液中c(Ba2+)保持不变
9.下列有关溶度积常数K 的说法正确的是( )
sp
A.常温下,向BaCO 饱和溶液中加入NaCO 固体,BaCO 的K 减小
3 2 3 3 sp
B.溶度积常数K 只受温度影响,温度升高K 减小
sp sp
C.溶度积常数K 只受温度影响,温度升高K 增大
sp sp
D.常温下,向Mg(OH) 饱和溶液中加入NaOH固体,Mg(OH) 的K 不变
2 2 sp
10.已知:K (AgCl)=1.8×10-10 ,K (AgI)=1.5×10-16,K (Ag CrO)=2.0×10-12,则下列难溶盐的饱
sp sp sp 2 4
和溶液中,Ag+浓度大小顺序正确的是( )
A.AgCl>AgI>Ag CrO B.AgCl> Ag CrO>AgI
2 4 2 4
C.Ag CrO>AgCl>AgI D.Ag CrO>AgI>AgCl
2 4 2 4
11.在BaSO 饱和溶液中加入少量的BaCl 溶液产生BaSO 沉淀,若以K 表示BaSO 的溶度积常数,
4 2 4 sp 4
则平衡后溶液中( )
A.c(Ba2+)=c(SO)=(K )
sp
B.c(Ba2+)·c(SO)>K ,c(Ba2+)=c(SO)
sp
C.c(Ba2+)·c(SO)=K ,c(Ba2+)>c(SO)
sp
D.c(Ba2+)·c(SO)≠K ,c(Ba2+)T)。下列说法不正确的是( )
4 2 1A.温度为T 时,K (FeAsO)=10-2a
2 sp 4
B.c(FeAsO ):Z>W=X
4
C.FeAsO 的溶解过程吸收能量
4
D.将Z溶液升温一定可以得到Y溶液
1.不法分子曾用含有可溶性钡盐的工业废盐腌制咸鸭蛋而引发了钡盐中毒事件。根据资料得知,当
胃液中Ba2+浓度小于10-4mol·Lˉ1时,可以达到解毒目的。已知:K (BaSO)=1.1×10-10、K (BaCO)=2.6×10-
sp 4 sp 3
9。下列有关说法错误的是( )
A.可溶性钡盐使人体蛋白质变性引起中毒
B.误食碳酸钡不会引起中毒
C.医学上用0.38mol·Lˉ1的硫酸钠溶液给患者洗胃,可以达到有效解毒效果
D.BaSO 在一定条件下也可以转化为BaCO
4 3
2.下列说法中正确的是( )
A.钡中毒患者可尽快使用苏打溶液洗胃,随即导泻使Ba2+转化为BaCO 而排出
3
B.工业上可以用NaHS、(NH )S等可溶性硫化物作沉淀剂除去废水中的Hg2+、Cu2+等,但不能使用
4 2
FeS等不溶性硫化物作沉淀剂
C.水中的Mg(HCO ) 、Ca(HCO ) 受热易分解生成难溶性的MgCO 、CaCO ,故水垢的主要成分是
3 2 3 2 3 3
MgCO 、CaCO
3 3
D.珊瑚虫从周围海水中获取Ca2+和HCO,经反应形成石灰石(CaCO)外壳,从而逐渐形成珊瑚
3
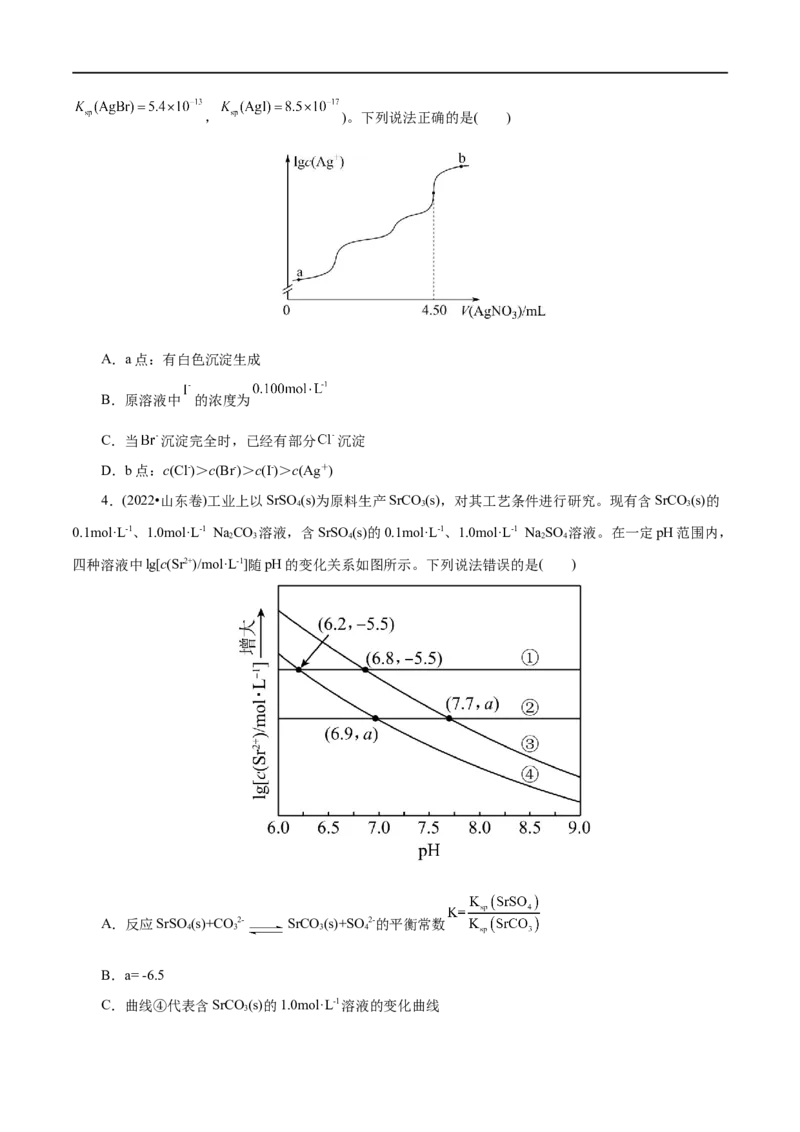
3.(2022•湖南选择性考试)室温时,用0.100 mol·L-1的标准AgNO 溶液滴定 浓度相等的Cl-、
3
Br-和 I-混合溶液,通过电位滴定法获得 与 的关系曲线如图所示(忽略沉淀对离子的吸
附作用。若溶液中离子浓度小于1.0×10-5mol·L-1时,认为该离子沉淀完全。 ,, )。下列说法正确的是( )
A.a点:有白色沉淀生成
B.原溶液中 的浓度为
C.当 沉淀完全时,已经有部分 沉淀
D.b点:c(Cl-)>c(Br-)>c(I-)>c(Ag+)
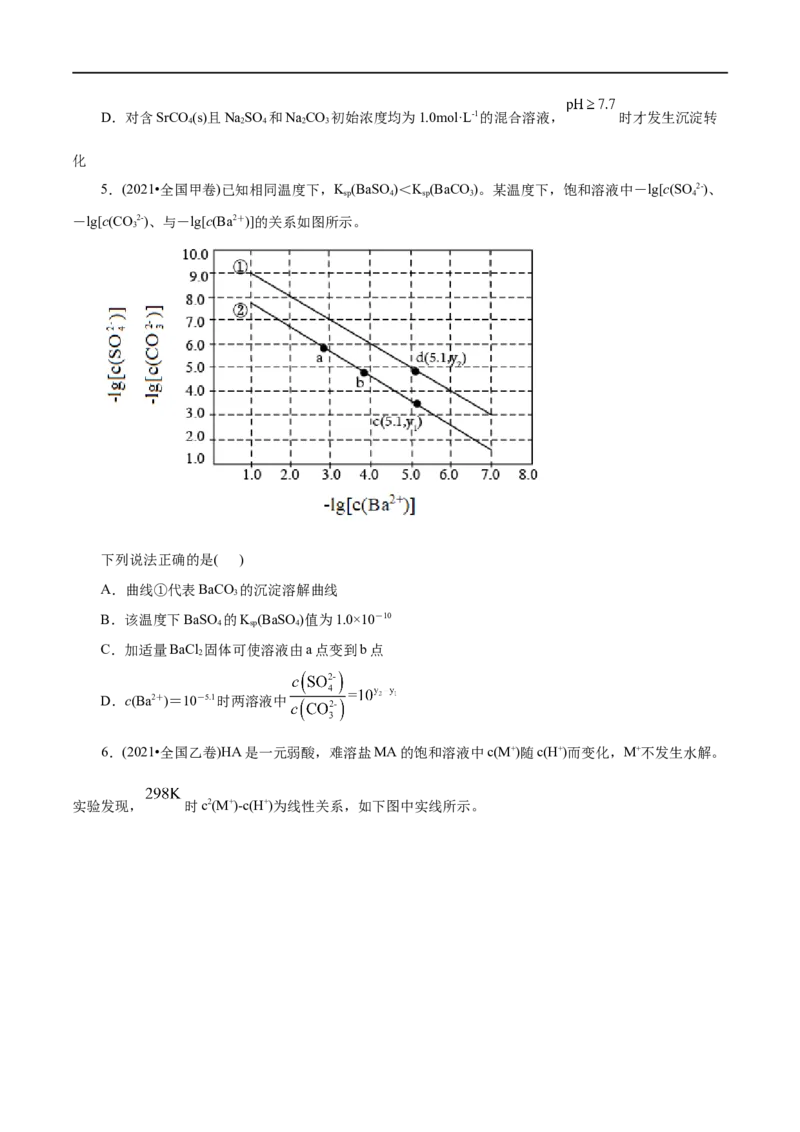
4.(2022•山东卷)工业上以SrSO (s)为原料生产SrCO (s),对其工艺条件进行研究。现有含SrCO (s)的
4 3 3
0.1mol·L-1、1.0mol·L-1 Na CO 溶液,含SrSO (s)的0.1mol·L-1、1.0mol·L-1 Na SO 溶液。在一定pH范围内,
2 3 4 2 4
四种溶液中lg[c(Sr2+)/mol·L-1]随pH的变化关系如图所示。下列说法错误的是( )
A.反应SrSO (s)+CO2- SrCO (s)+SO 2-的平衡常数
4 3 3 4
B.a= -6.5
C.曲线④代表含SrCO (s)的1.0mol·L-1溶液的变化曲线
3D.对含SrCO (s)且NaSO 和NaCO 初始浓度均为1.0mol·L-1的混合溶液, 时才发生沉淀转
4 2 4 2 3
化
5.(2021•全国甲卷)已知相同温度下,K (BaSO)<K (BaCO)。某温度下,饱和溶液中-lg[c(SO 2-)、
sp 4 sp 3 4
-lg[c(CO2-)、与-lg[c(Ba2+)]的关系如图所示。
3
下列说法正确的是( )
A.曲线①代表BaCO 的沉淀溶解曲线
3
B.该温度下BaSO 的K (BaSO)值为1.0×10-10
4 sp 4
C.加适量BaCl 固体可使溶液由a点变到b点
2
D.c(Ba2+)=10-5.1时两溶液中
6.(2021•全国乙卷)HA是一元弱酸,难溶盐MA的饱和溶液中c(M+)随c(H+)而变化,M+不发生水解。
实验发现, 时c2(M+)-c(H+)为线性关系,如下图中实线所示。下列叙述错误的是( )
A.溶液pH=4时,c(M+)<3.0×10-4mol·L-1
B.MA的溶度积度积K (MA)=5.0×10-8
sp
C.溶液pH=7时,c(M+)+c(H+) =c(A-)+c(OH―)
D.HA的电离常数K (HA)≈2.0×10-4
a1