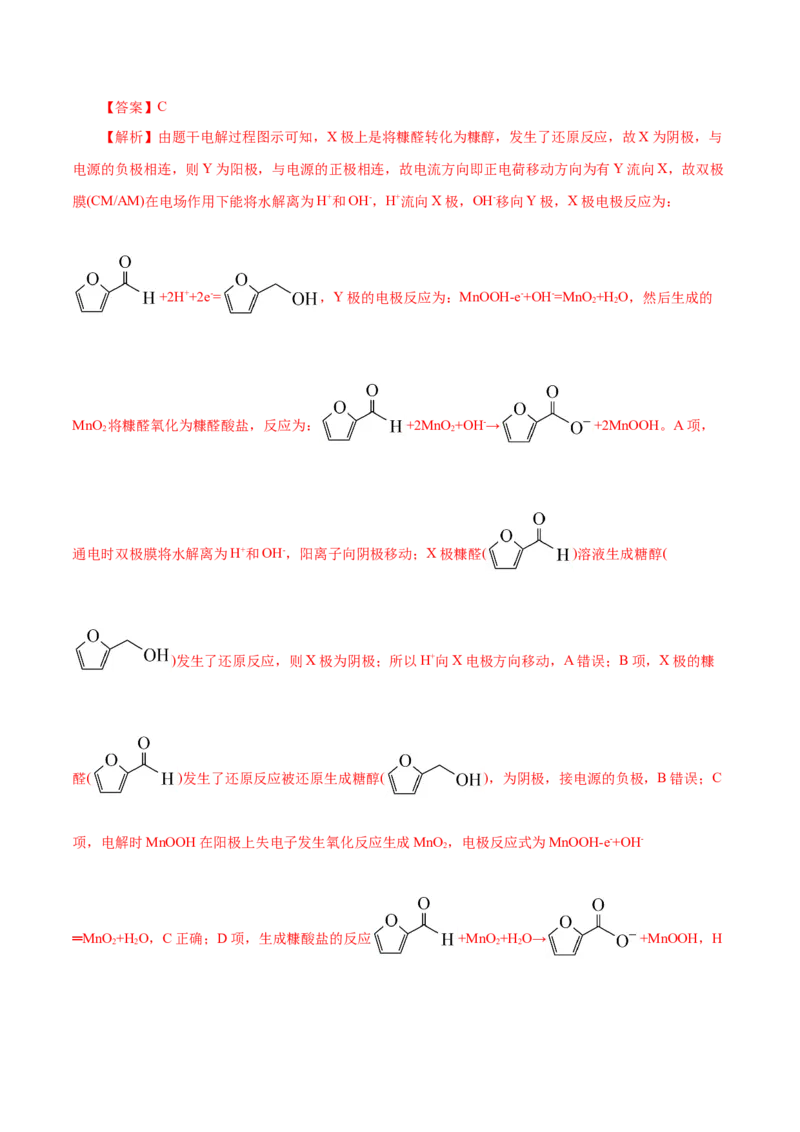
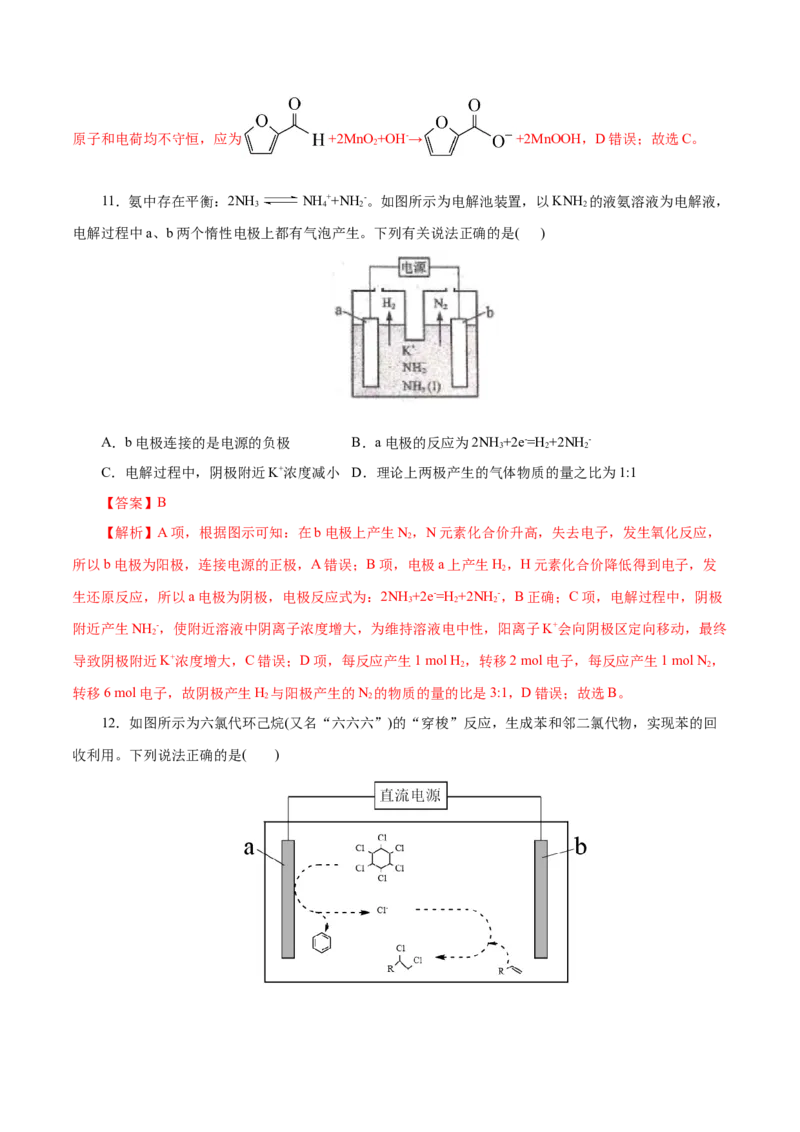
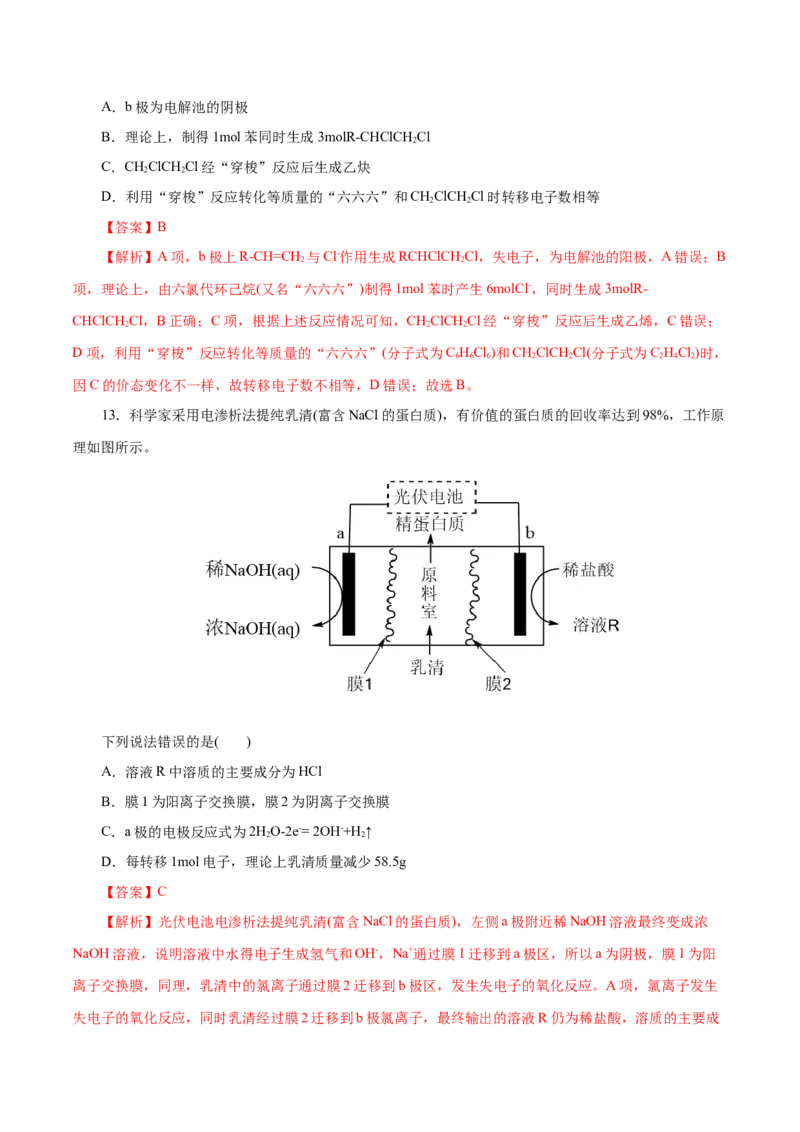
文档内容
专题 12 化学反应与电能
第 35 练 电解池
1.电解池中,阳极的电极材料一定( )
A.发生氧化反应 B.与电源正极相连
C.是铂电极 D.得电子
【答案】B
【解析】阳极材料若为活泼金属则直接发生氧化反应;若为惰性电极,则为电解质溶液中最易失电子
的阴离子发生氧化反应。
2.下列关于电解槽的叙述中不正确的是( )
A.与电源正极相连的是电解槽的阴极
B.与电源负极相连的是电解槽的阴极
C.在电解槽的阳极发生氧化反应
D.电子从电源的负极沿导线流入电解槽的阴极
【答案】A
【解析】电解槽的电极名称是由电极材料与电源的连接方式决定的,与电源正极相连的是电解槽的阳
极。
3.电解CuCl 和NaCl的混合溶液,阴极和阳极上首先析出的物质分别是( )
2
A.Cu和Cl B.H 和Cl
2 2 2
C.H 和O D.Cu和O
2 2 2
【答案】A
【解析】在CuCl 和NaCl溶液中,Cu2+、Na+、H+向阴极移动,因Cu2+氧化性最强,则阴极反应为:
2
Cu2++2e-===Cu,而Cl-、OH-向阳极移动,因Cl-的还原性比OH-强,所以阳极反应为:2Cl--2e-
===Cl↑,故电解时阴极、阳极首先析出的物质分别为Cu和Cl。
2 2
4.下图是电解CuCl 溶液的装置,其中c、d为石墨电极( )
2
A.a为负极 B.b为阳极
C.c电极上有氯气产生 D.d电极上发生氧化反应【答案】C
【解析】A项,有电流流出的是正极,a为正极,故A错误;B项,b是负极,故B错误;C项,c与
正极相连是阳极,吸引阴离子,使Cl-变成氯气,故C正确;D项,d与负极相连是阴极,阴极发生还原反
应,故D错误;故选C。
5.用石墨作电极,电解1 mol·L-1下列物质的溶液,溶液中的pH保持不变的是( )
A.HCl B.NaOH C.Na SO D.NaCl
2 4
【答案】C
【解析】用石墨作电极,电解HCl(aq)时,H+放电产生H,使溶液中c(H+)减小,pH增大,所以A不
2
符合;用石墨作电极,电解NaOH(aq)时,实质为电解水,使溶液中c(OH-)增大,pH增大,所以B不符合;
用石墨作电极,电解NaCl(aq)时,生成NaOH,溶液中c(OH-)增大,pH增大,则D不符合;只有电解
NaSO (aq)时,实质为电解水,溶液仍为中性,pH不变,故选项C正确。
2 4
6.若某装置发生如下反应:Cu+2H+===Cu2++H↑,关于该装置的有关说法正确的是( )
2
A.该装置一定为原电池 B.该装置为电解池
C.若为原电池,Cu为正极 D.电解质溶液可能是硝酸溶液
【答案】B
【解析】已知反应为非自发的氧化还原反应,故该装置应为电解池,而非原电池,但电解质不能为
HNO,否则得电子的为NO,而非H+得电子放出H。
3 2
7.用石墨做电极电解CuCl 溶液,下列说法正确的是( )
2
A.在阳极上析出金属铜 B.在阴极上析出金属铜
C.在阴极上产生有刺激性气味的气体 D.阳极上发生还原反应
【答案】B
【解析】根据电解原理,阳极发生氧化反应:2Cl--2e-=Cl↑,阴极发生还原反应:Cu2++2e-=Cu。
2
因此阳极上产生有刺激性气味的气体氯气,在阴极上析出铜。故B符合题意。
8.如图为直流电源电解稀NaSO 水溶液的装置。下列说法正确的是( )
2 4
A.a为阳极,b为阴极 B.a发生氧化反应,b发生还原反应
C.溶液中Na+向b极移动 D.a极产生H,b极产生O
2 2
【答案】D
【解析】电解NaSO 溶液实际上是电解水,电解时发生的反应为:a(阴极):4H++4e-===2H ↑(还原
2 4 2
反应);b(阳极):4OH--4e-===2H O+O↑(氧化反应),故A、B错误;溶液中阳离子(Na+)移向阴极(a极),
2 2
C错误。9.用石墨作电极电解CuSO 溶液。通电一段时间后,欲使电解液恢复到起始状态,应向溶液中加入
4
适量的( )
A.CuSO B.HO C.CuO D.CuSO ·5H O
4 2 4 2
【答案】C
【解析】由硫酸铜溶液的电解方程式:2CuSO +2HO=====2Cu+O +2HSO 可知,加入CuO才可
4 2 2 2 4
与生成的HSO 反应生成CuSO 而使电解液恢复到原浓度,故C正确。
2 4 4
10.关于电解NaCl水溶液,下列叙述正确的是( )
A.若在阴极附近的溶液中滴入石蕊试液,溶液呈无色
B.若在阳极附近的溶液中滴入KI溶液,溶液呈棕色
C.电解时在阳极得到氯气,在阴极得到金属钠
D.电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液呈中性
【答案】B
【解析】电解食盐水时发生的反应:阳极:2Cl--2e-===Cl,阴极:2HO+2e-===H +2OH-(或2H
2 2 2
++2e-===H ),总反应:2NaCl+2HO=====2NaOH+H +Cl 。阴极显碱性,滴入石蕊溶液变蓝,A错误;
2 2 2 2
阳极附近的溶液中会溶有少量的 Cl ,滴加KI溶液后发生反应:Cl +2I-===I +2Cl-,溶液呈棕色,B正
2 2 2
确;阴极上是HO电离产生的H+放电产生H ,不是Na+放电生成钠,C错误;电解后生成NaOH溶液呈
2 2
碱性,D错误。
11.用惰性电极进行电解,下列说法正确的是( )
A.电解稀硫酸,实质上是电解水,故溶液pH不变
B.电解稀NaOH溶液,要消耗OH-,故溶液pH减小
C.电解NaSO 溶液,在阴极上和阳极上生成气体产物的物质的量之比为1:2
2 4
D.电解氯化铜溶液,在阴极上和阳极上生成产物的物质的量之比为1:1
【答案】D
【解析】A项,电解稀硫酸时,实质上是电解水,溶剂的质量减少,溶质的质量不变,所以溶液的
浓度增大,氢离子的浓度增大,溶液的pH变小,故A错误;B项,电解稀氢氧化钠溶液时,实质上是电
解水,溶剂的质量减少,溶质的质量不变,所以溶液的浓度增大,氢氧根离子的浓度增大,溶液的pH变
大,故B错误;C项,电解硫酸钠溶液时,实质上是电解水,阴极上氢离子得电子生成氢气,阳极上氢氧
根离子失电子生成氧气,根据得失电子守恒,在阴极上和阳极上析出产物的物质的量之比为2:1,故C错
误;D项,电解氯化铜溶液时,阴极上铜离子得电子生成铜,阳极上氯离子失电子生成氯气,根据得失电
子守恒,在阴极上和阳极上析出产物的物质的量之比为1:1,故D正确;故选D。
12.用惰性电极电解下列溶液一段时间后再加入一定量的某种纯净物(方括号内的物质),能使溶液恢
复到原来的成分和浓度的是( )
A.AgNO[AgNO] B.NaOH[HO]
3 3 2C.KCl[KCl] D.CuSO [Cu(OH) ]
4 2
【答案】B
【解析】A项:4AgNO +2HO=====4Ag+O↑+4HNO ,脱离反应体系的物质是4Ag+O ,相当于
3 2 2 3 2
2Ag O,所以应当加入适量Ag O才能复原。(加入AgNO ,会使NO的量增加);B项:2HO=====2H↑+
2 2 3 2 2
O↑ 脱离反应体系的是2H+O,相当于2HO,加入适量水可以复原。C项:2KCl+2HO=====2KOH+
2 2 2 2 2
H↑+Cl↑,脱离反应体系的是H+Cl,相当于2HCl,应通入适量HCl气体才能复原。(加入盐酸时,同时
2 2 2 2
也增加了水) D项:2CuSO +2HO=====2HSO +2Cu+O↑,脱离反应体系的是 2Cu+O ,相当于
4 2 2 4 2 2
2CuO,加入适量CuO可以复原。
1.用惰性电极电解AgNO 溶液,下列说法不正确的是( )
3
A.电解过程中阴极质量不断增加
B.电解过程中溶液的pH不断降低
C.此时向溶液中加入适量的Ag O固体可使溶液恢复到电解前的状况
2
D.电解后两极产生的气体体积比为2∶1
【答案】D
【解析】用惰性电极电解AgNO 溶液,电解反应方程式为4AgNO+2HO=====4Ag+O↑+4HNO。
3 3 2 2 3
阴极上析出Ag,阳极上放出O ,故A正确、D错误;由于生成HNO 溶液,pH应不断降低,B正确;要
2 3
使溶液恢复到电解前的状况要看加入的物质在溶液中的反应:2Ag O+4HNO===4AgNO +2HO,得到的
2 3 3 2
物质恰好是反应掉的物质,可以使溶液恢复到电解前的状况,C正确。
2.用如图所示装置用石墨电极电解氯化铜溶液,Y电极上产生能使湿润的淀粉KI试纸变蓝的黄绿
色气体。下列判断正确的是( )
A.a为电源正极 B.X电极质量增加
C.Y电极若换成Cu,电极反应质量不变 D.X电极表面发生氧化反应
【答案】B
【解析】Y电极上产生能使湿润的淀粉KI试纸变蓝的黄绿色气体,即产生氯气,则Y为阳极,与Y
相连的b为电源正极,X为阴极,与X相连的a为电源负极。A项,根据分析可知a为电源负极,故A错
误;B项,X为阴极,铜离子在阴极被还原生成铜单质,所以X电极质量增加,故B正确;C项,Y为阳极,若换成Cu,则Cu被氧化生成铜离子,电极质量减小,故C错误;D项,X为阴极,电极表面得电子
发生还原反应,故D错误;故选B。
3.如图中X、Y分别是直流电源的两极,通电后发现a极板增重,b极板有无色无味气体放出,符合
这一情况的是( )
选项 a极板 b极板 X电极 Z溶液
A 锌 石墨 负极 CuSO
4
B 石墨 石墨 负极 NaOH
C 银 铁 正极 AgNO
3
D 铜 石墨 负极 CuCl
2
【答案】A
【解析】a极质量增加,必定是金属在a极析出,a极一定是阴极。B选项Z溶液为NaOH,无金属析
出,被排除。又因为b极有无色无味气体生成,只能是O ,而D选项电解CuCl 溶液,阳极要析出Cl ,D
2 2 2
选项被排除。在A、C选项中,根据电极名称,X应当作为电源的负极。
4.氯碱工业用离子交换膜法电解饱和食盐水,装置示意图如图。下列说法错误的是( )
A.a为阳极,发生氧化反应生成氯气
B.b极的电极反应式为2HO+2e-=H ↑+2OH-
2 2
C.电解时,Na+穿过离子交换膜进入阴极室
D.饱和食盐水从c处进入,淡盐水从e处流出
【答案】D
【解析】A项,a和电源的正极相连,为阳极,溶液中的Cl-在阳极失去电子发生氧化反应生成氯气,
故A正确;B项,b为阴极,溶液中水电离出来的H+得到电子生成氢气,电极反应式为2HO+2e-
2
=H ↑+2OH-,故B正确;C项,离子交换膜为阳离子交换膜,电解时,阳离子移向阴极,所以Na+穿过离子
2
交换膜进入阴极室,故C正确;D项,由于溶液中的Cl-在阳极放电,所以饱和食盐水从c处进入阳极室,
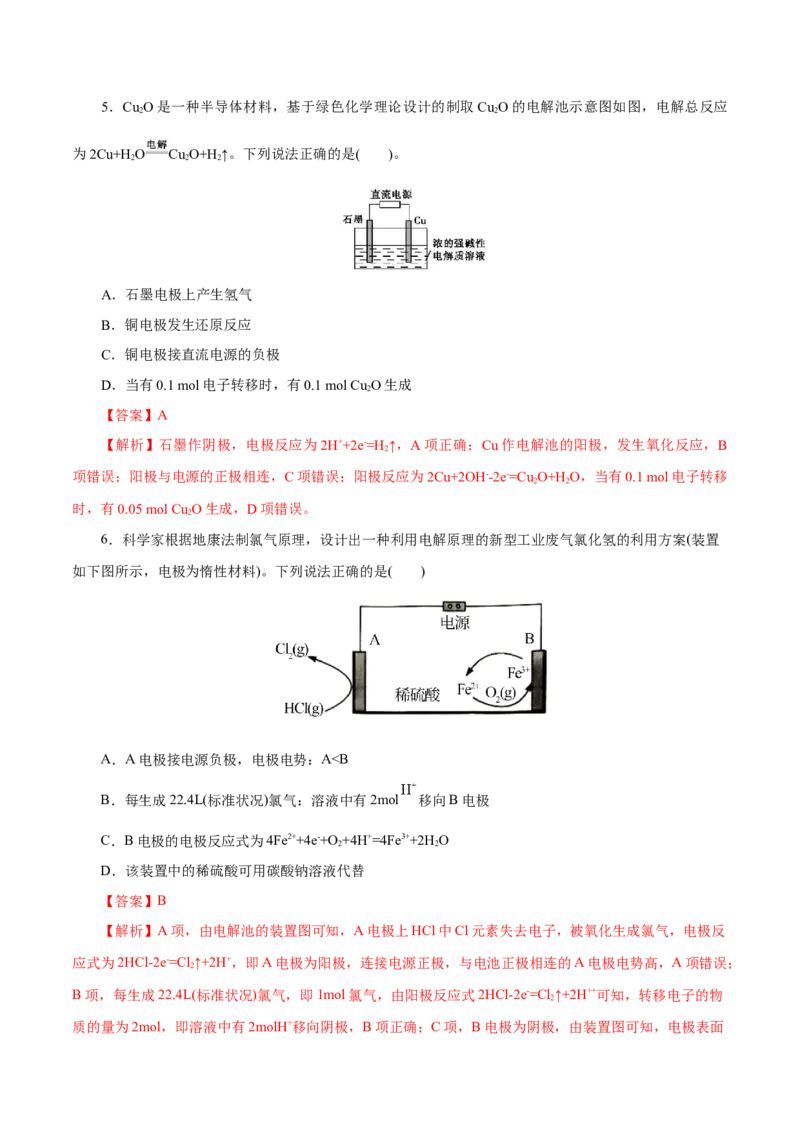
Cl-放电生成氯气逸出,Na+穿过离子交换膜进入阴极室,所以淡盐水从d处流出,故D错误;故选D。5.Cu O是一种半导体材料,基于绿色化学理论设计的制取Cu O的电解池示意图如图,电解总反应
2 2
为2Cu+H O Cu O+H↑。下列说法正确的是( )。
2 2 2
A.石墨电极上产生氢气
B.铜电极发生还原反应
C.铜电极接直流电源的负极
D.当有0.1 mol电子转移时,有0.1 mol Cu O生成
2
【答案】A
【解析】石墨作阴极,电极反应为2H++2e-=H ↑,A项正确;Cu作电解池的阳极,发生氧化反应,B
2
项错误;阳极与电源的正极相连,C项错误;阳极反应为2Cu+2OH--2e-=Cu O+HO,当有0.1 mol电子转移
2 2
时,有0.05 mol Cu O生成,D项错误。
2
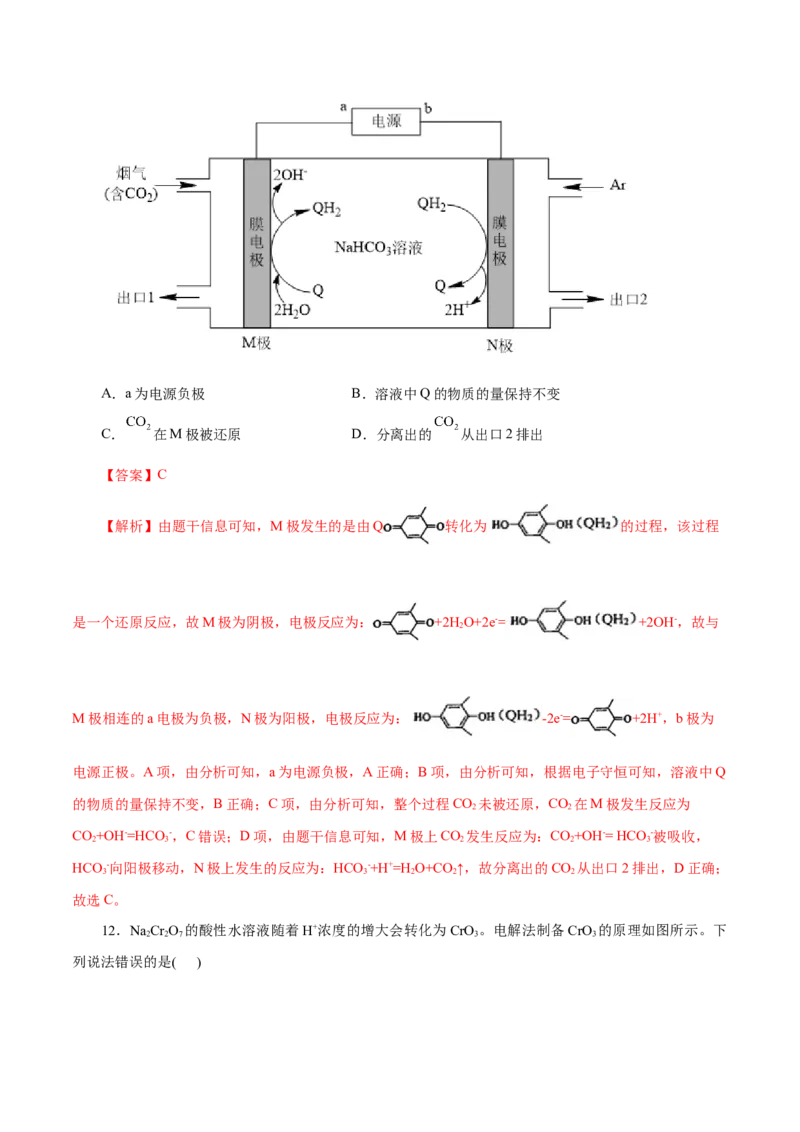
6.科学家根据地康法制氯气原理,设计出一种利用电解原理的新型工业废气氯化氢的利用方案(装置
如下图所示,电极为惰性材料)。下列说法正确的是( )
A.A电极接电源负极,电极电势:A