文档内容
第 32 讲 化学键
[复习目标] 1.了解化学键的定义,了解离子键、共价键的形成。2.了解共价键的类型及键
参数。
考点一 化学键与化合物类型 电子式
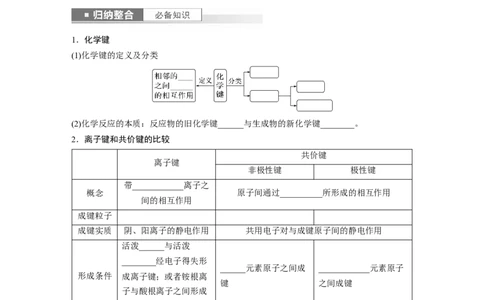
1.化学键
(1)化学键的定义及分类
(2)化学反应的本质:反应物的旧化学键______与生成物的新化学键________。
2.离子键和共价键的比较
共价键
离子键
非极性键 极性键
带____________离子之
概念 原子间通过__________所形成的相互作用
间的相互作用
成键粒子
成键实质 阴、阳离子的静电作用 共用电子对与成键原子间的静电作用
活泼______与活泼
________经电子得失形
______元素原子之间成 ____________元素原子
形成条件 成离子键;或者铵根离
键 之间成键
子与酸根离子之间形成
离子键
3.离子化合物和共价化合物
项目 离子化合物 共价化合物
定义 含有________的化合物 只含有________的化合物
构成微粒
化学键类型 一定含有______,可能含有
只含有________
________4.化学键的表示方法——电子式
(1)概念:在元素符号周围用“·”或“×”来表示原子的____________的式子。
(2)常见物质电子式的书写
①原子:Na ________,Cl ________。
②简单离子:Na+ ____,F- ________。
③复杂离子:NH ____________________,OH- ________________。
④离子化合物:MgCl _____________________,
2
NaO ________________________,
2
NaO ________________________。
2 2
⑤非金属单质及共价化合物:N _________________________________________,
2
HO ________________,HO ________________________。
2 2 2
(3)用电子式表示化合物的形成过程
①离子化合物
如NaCl:____________________________________________________。
②共价化合物
如HCl:______________________________________________________。
一、化学键与离子化合物、共价化合物的判断
1.一定条件下,氨与氟气发生反应:4NH +3F===NF +3NH F,其中NF 的空间结构与
3 2 3 4 3
NH 相似。下列有关说法错误的是( )
3
A.除F 单质外,反应物和生成物均为共价化合物
2
B.NF 中各原子均满足8电子稳定结构
3
C.NF 中只含极性共价键
3
D.NH F中既含有离子键又含有共价键
4
2.有以下 8 种物质:① Ne ② HCl ③ P ④ HO ⑤ NaS ⑥ NaOH ⑦ NaO
4 2 2 2 2 2
⑧NH Cl
4
请用上述物质的序号填空:
(1)不存在化学键的是________。
(2)只存在极性共价键的是________。
(3)只存在非极性共价键的是________。
(4)既存在非极性共价键又存在极性共价键的是________。
(5)只存在离子键的是________。
(6)既存在离子键又存在共价键的是________。
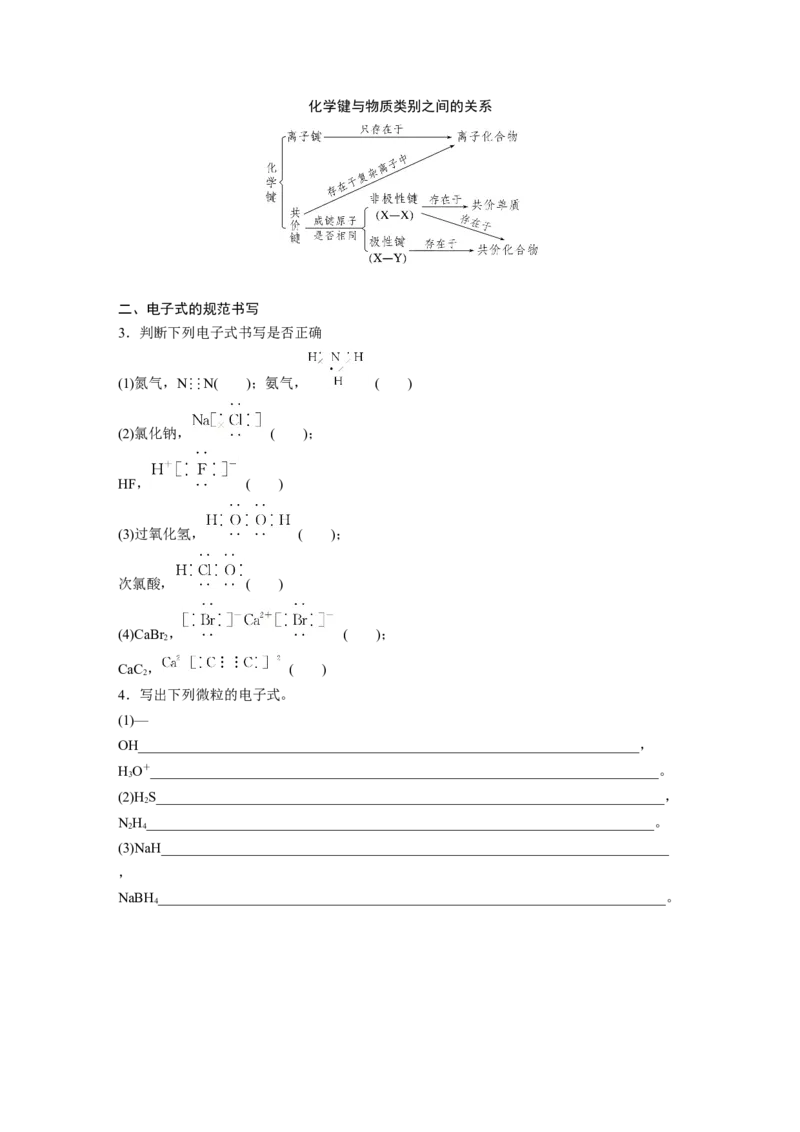
(7)属于离子化合物的是__________。化学键与物质类别之间的关系
二、电子式的规范书写
3.判断下列电子式书写是否正确
(1)氮气,N⋮⋮N( );氨气, ( )
(2)氯化钠, ( );
HF, ( )
(3)过氧化氢, ( );
次氯酸, ( )
(4)CaBr , ( );
2
CaC , ( )
2
4.写出下列微粒的电子式。
(1)—
OH_______________________________________________________________________,
HO+________________________________________________________________________。
3
(2)H S________________________________________________________________________,
2
NH________________________________________________________________________。
2 4
(3)NaH________________________________________________________________________
,
NaBH ________________________________________________________________________。
4考点二 共价键及其参数
1.共价键的本质及特征
共价键是原子间通过____________所形成的相互作用,其特征是具有________和________。
2.分类
分类依据 类型
____键 轨道“________”重叠
形成共价键的原子轨道重叠方式
____键 轨道“________”重叠
______键 共用电子对______偏移
形成共价键的电子对是否偏移
________键 共用电子对________偏移
____键 原子间有______共用电子对
原子间共用电子对的数目 ____键 原子间有______共用电子对
____键 原子间有______共用电子对
3.键参数
(1)概念
(2)键参数对分子性质的影响
①键能越____,键长越____,分子越稳定。
②
1.共价键的成键原子只能是非金属原子( )
2.在任何情况下,都是σ键比π键强度大( )
3.σ键能单独形成,而π键一定不能单独形成( )
4.σ键可以绕键轴旋转,π键一定不能绕键轴旋转( )
5.碳碳三键和碳碳双键的键能分别是碳碳单键键能的3倍和2倍( )
6.分子的稳定性与分子间作用力的大小无关( )一、共价键的类型及数目判断
1.分析下列物质中含有哪些不同类型的共价键,在对应的空格处打“√”(σ键、π键需填
写1 mol该物质所含σ键、π键的物质的量)。
物质 极性键 非极性键 σ键 π键 单键 双键 三键
N
2
C H
2 4
SiO
2
BF
3
HCN
二、键能、键长与物质稳定性
2.Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或
三键。从原子结构角度分析,原因是________________________________________
________________________________________________________________________。
3.硅是重要的半导体材料,构成了现代电子工业的基础。碳和硅的有关化学键键能如表所
示,简要分析和解释下列有关事实:
化学键 C—C C—H C—O Si—Si Si—H Si—O
键能/ (kJ·mol-1) 365 413 336 226 318 452
(1)硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是
________________________________________________________________________
________________________________________________________________________。
(2)SiH 的稳定性小于CH,更易生成氧化物,原因是_________________________
4 4
________________________________________________________________________ 。
1.正误判断,正确的打“√”,错误的打“×”。
(1)钠与N、O、Cl分别形成的化合物中只含有离子键(2018·全国卷Ⅱ,10B改编)( )
(2)1 mol乙烷和1 mol乙烯中,化学键数相同(2018·全国卷Ⅲ,8D)( )
(3)Na O 与ClO 均含有非极性共价键(2018·全国卷Ⅲ,13C改编)( )
2 2 2
(4)氢元素与其他元素可形成共价化合物或离子化合物(2017·天津,5B)( )(5)甲基的电子式: (2020·浙江7月选考,5D)( )
(6)B NH(无机苯)的结构与苯类似,也有大π键。B NH 的熔点主要取决于所含化学键的键
3 3 6 3 3 6
能 (2020·山东,7A)( )
(7)键能C—C>Si—Si、C—H>Si—H,因此C H 稳定性大于Si H(2020·山东,4A)( )
2 6 2 6
(8)28 g C H 分子中含有的σ键数目为4N (2022·辽宁,3B)( )
2 4 A
2. (2022·北京,9)由键能数据大小,不能解释下列事实的是( )
化学键 C—H Si—H C==O C—O Si—O C—C Si—Si
键能/kJ·mol-1 411 318 799 358 452 346 222
A.稳定性:CH>SiH
4 4
B.键长:C==O晶体硅
3.[2020·浙江7月选考,26(1)(2)](1)气态氢化物热稳定性HF大于HCl的主要原因是
________________________________________________________________________
________________________________________________________________________。
(2)CaCN 是离子化合物,各原子均满足 8 电子稳定结构,CaCN 的电子式是
2 2
________________________________________________________________________。