文档内容
1.下列有关AgCl沉淀溶解平衡的说法正确的是( )
A.AgCl沉淀生成和溶解不断进行,但速率相等
B.AgCl难溶于水,溶液中没有Ag+和Cl-
C.升高温度,AgCl沉淀的溶解度减小
D.在有AgCl沉淀生成的溶液中加入NaCl固体,AgCl沉淀溶解的量不变
2.(2022·保定模拟)在一定温度下,当过量的 Mg(OH) 固体在水溶液中达到平衡时:
2
Mg(OH) (s)Mg2+(aq)+2OH-(aq),要使Mg(OH) 固体增加,c(OH-)增加,可采取的措
2 2
施是( )
A.加适量的水
B.通入少量HCl气体
C.加少量NaOH固体
D.加少量MgSO 固体
4
3.(2022·首都师范大学附中模拟)25 ℃时,在含有大量PbI 的饱和溶液中存在沉淀溶解平
2
衡:PbI (s)Pb2+(aq)+2I-(aq),加入KI固体,下列说法正确的是( )
2
A.溶液中Pb2+和I-的浓度都增大
B.K (PbI )增大
sp 2
C.PbI 的沉淀溶解平衡向右移动
2
D.溶液中c(Pb2+)减小
4.关于沉淀溶解平衡和溶度积常数,下列说法不正确的是( )
A.K 只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关
sp
B . 将 饱 和 NaSO 溶 液 加 入 到 饱 和 石 灰 水 中 , 有 白 色 沉 淀 产 生 , 说 明
2 4
K [Ca(OH) ]>K (CaSO)
sp 2 sp 4
C.已知25 ℃时K [Fe(OH) ]=2.8×10-39,则该温度下反应 Fe(OH) +3H+Fe3++
sp 3 3
3HO的平衡常数K=2.8×103
2
D.已知25 ℃时,K [Mg(OH) ]=1.8×10-11,在MgCl 溶液中加入氨水调混合液的pH=
sp 2 2
11,产生沉淀,则此时溶液中的c(Mg2+)=1.8×10-5 mol·L-1
5.往锅炉注入NaCO 溶液浸泡,将水垢中的CaSO 转化为CaCO ,再用盐酸去除,下列
2 3 4 3
叙述正确的是( )
A.温度升高,NaCO 溶液的K 增大,c(OH-)减小
2 3 w
B.CaSO 能转化为CaCO ,说明K (CaCO)>K (CaSO)
4 3 sp 3 sp 4
C.CaCO 溶解于盐酸而CaSO 不溶,是因为硫酸酸性强于盐酸
3 4
D.沉淀转化的离子方程式为CO(aq)+CaSO(s)CaCO (s)+SO(aq)
4 36.为研究沉淀的生成及转化,某小组进行如图实验。下列关于该实验的分析不正确的是(
)
A.①浊液中存在平衡:AgSCN(s)Ag+(aq)+SCN-(aq)
B.②中颜色变化说明上层清液中含有SCN-
C.③中颜色变化说明有AgI生成
D.该实验可以证明AgI比AgSCN更难溶
7.(2021·江苏,11)室温下,通过下列实验探究NaHCO 、NaCO 溶液的性质。
3 2 3
实验1:用pH试纸测量0.1 mol·L-1NaHCO 溶液的pH,测得pH约为8
3
实验2:将0.1 mol·L-1NaHCO 溶液与0.1 mol·L-1 CaCl 溶液等体积混合,产生白色沉淀
3 2
实验3:向0.1 mol·L-1NaCO 溶液中通入CO,溶液pH从12下降到约为9
2 3 2
实验4:向0.1 mol·L-1NaCO 溶液中滴加新制饱和氯水,氯水颜色褪去
2 3
下列说法正确的是( )
A.由实验1可得出:K (H CO)>
a2 2 3
B.实验2中两溶液混合时有:c(Ca2+)·c(CO)6
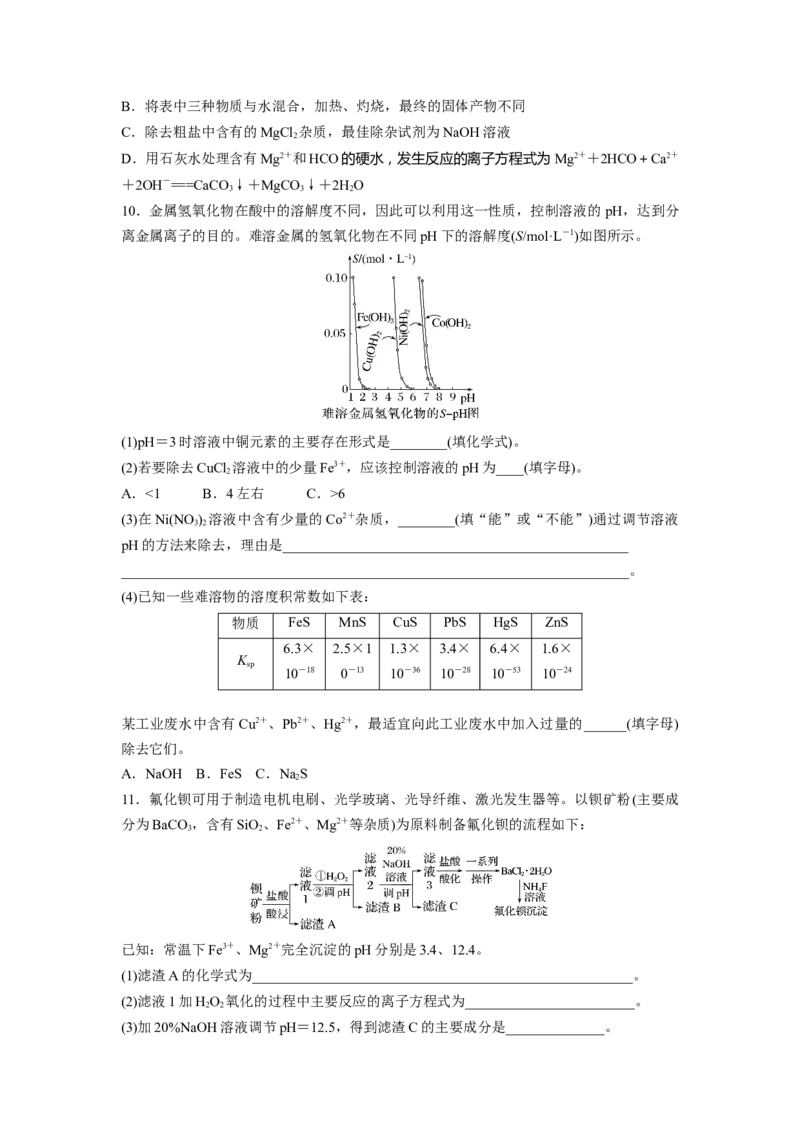
(3)在Ni(NO ) 溶液中含有少量的Co2+杂质,________(填“能”或“不能”)通过调节溶液
3 2
pH的方法来除去,理由是_________________________________________________
________________________________________________________________________。
(4)已知一些难溶物的溶度积常数如下表:
物质 FeS MnS CuS PbS HgS ZnS
6.3× 2.5×1 1.3× 3.4× 6.4× 1.6×
K
sp
10-18 0-13 10-36 10-28 10-53 10-24
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的______(填字母)
除去它们。
A.NaOH B.FeS C.NaS
2
11.氟化钡可用于制造电机电刷、光学玻璃、光导纤维、激光发生器等。以钡矿粉(主要成
分为BaCO ,含有SiO、Fe2+、Mg2+等杂质)为原料制备氟化钡的流程如下:
3 2
已知:常温下Fe3+、Mg2+完全沉淀的pH分别是3.4、12.4。
(1)滤渣A的化学式为______________________________________________________。
(2)滤液1加HO 氧化的过程中主要反应的离子方程式为________________________。
2 2
(3)加20%NaOH溶液调节pH=12.5,得到滤渣C的主要成分是______________。(4)滤液3加入盐酸酸化后再经__________、冷却结晶、__________、洗涤、真空干燥等一
系列操作后得到BaCl ·2H O。
2 2
(5)常温下,用BaCl ·2H O配制成0.2 mol·L-1水溶液与等浓度的氟化铵溶液反应,可得到
2 2
氟化钡沉淀。请写出该反应的离子方程式:____________________________________
________________________________________________________________________。
已知K (BaF )=1.84×10-7,当钡离子完全沉淀时(即钡离子浓度≤10-5 mol·L-1),至少需
sp 2
要的氟离子浓度是________ mol·L-1(结果保留三位有效数字,已知=1.36)。
(6)已知:K (BaCO)=2.58×10-9,K (BaSO)=1.07×10-10。将氯化钡溶液滴入等物质的
sp 3 sp 4
量浓度的硫酸钠和碳酸钠的混合溶液中,当BaCO 开始沉淀时,溶液中=________(结果保
3
留三位有效数字)。