文档内容
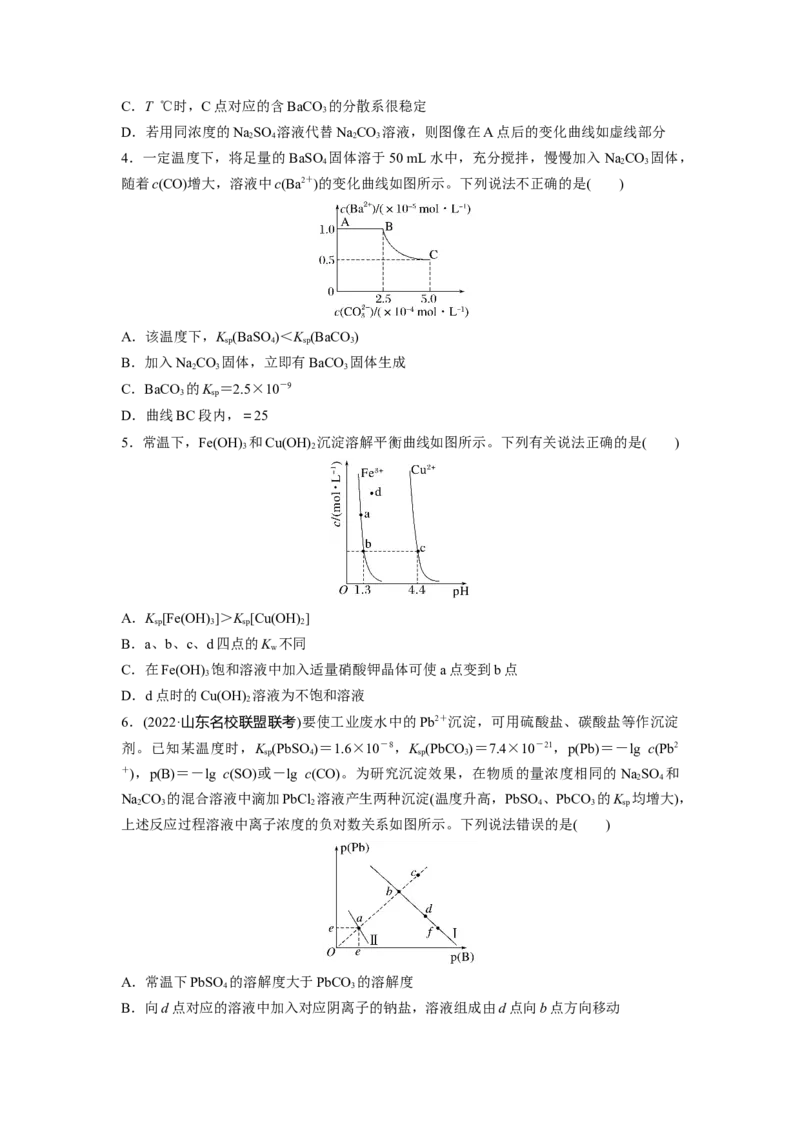
1.常温下,K (CaCO)=2.8×10-9,CaSO 在水中的沉淀溶解平衡曲线如图所示。下列判
sp 3 4
断错误的是( )
A.a点是CaSO 的饱和溶液而b点不是
4
B.蒸发水可使溶液由b点变化到a点
C.常温下,CaCO (s)+SO(aq)CaSO(s)+CO(aq)的K=3.1×10-4
3 4
D.除去锅炉中的CaSO 时,可用NaCO 溶液将其转化为CaCO
4 2 3 3
2.常温下,取一定量的PbI 固体配成饱和溶液,t时刻改变某一条件,离子浓度变化如图
2
所示。下列有关说法正确的是( )
A.常温下,PbI 的K 为2×10-6
2 sp
B.温度不变,向PbI 饱和溶液中加入少量硝酸铅浓溶液,平衡向左移动,Pb2+的浓度减
2
小
C.温度不变,t时刻改变的条件可能是向溶液中加入了KI固体,PbI 的K 增大
2 sp
D.常温下,K (PbS)=8×10-28,向PbI 的悬浊液中加入NaS溶液,反应PbI (s)+S2-
sp 2 2 2
(aq) PbS(s)+2I-(aq)的平衡常数为5×1018
3.T ℃时,向5 mL a mol·L-1 BaCl 溶液中逐滴加入0.1 mol·L-1 Na CO 溶液,滴加过程
2 2 3
中溶液的-lg c(Ba2+)与NaCO 溶液体积(V)的关系如图所示,下列说法正确的是[已知:lg
2 3
5=0.7,K (BaSO)=1.0×10-10]( )
sp 4
A.A、B两点溶液中c(Ba2+)之比为2 000∶3
B.a=10-4.3C.T ℃时,C点对应的含BaCO 的分散系很稳定
3
D.若用同浓度的NaSO 溶液代替NaCO 溶液,则图像在A点后的变化曲线如虚线部分
2 4 2 3
4.一定温度下,将足量的BaSO 固体溶于50 mL水中,充分搅拌,慢慢加入NaCO 固体,
4 2 3
随着c(CO)增大,溶液中c(Ba2+)的变化曲线如图所示。下列说法不正确的是( )
A.该温度下,K (BaSO)<K (BaCO)
sp 4 sp 3
B.加入NaCO 固体,立即有BaCO 固体生成
2 3 3
C.BaCO 的K =2.5×10-9
3 sp
D.曲线BC段内,=25
5.常温下,Fe(OH) 和Cu(OH) 沉淀溶解平衡曲线如图所示。下列有关说法正确的是( )
3 2
A.K [Fe(OH) ]>K [Cu(OH) ]
sp 3 sp 2
B.a、b、c、d四点的K 不同
w
C.在Fe(OH) 饱和溶液中加入适量硝酸钾晶体可使a点变到b点
3
D.d点时的Cu(OH) 溶液为不饱和溶液
2
6.(2022·山东名校联盟联考)要使工业废水中的Pb2+沉淀,可用硫酸盐、碳酸盐等作沉淀
剂。已知某温度时,K (PbSO )=1.6×10-8,K (PbCO )=7.4×10-21,p(Pb)=-lg c(Pb2
sp 4 sp 3
+),p(B)=-lg c(SO)或-lg c(CO)。为研究沉淀效果,在物质的量浓度相同的NaSO 和
2 4
NaCO 的混合溶液中滴加PbCl 溶液产生两种沉淀(温度升高,PbSO 、PbCO 的K 均增大),
2 3 2 4 3 sp
上述反应过程溶液中离子浓度的负对数关系如图所示。下列说法错误的是( )
A.常温下PbSO 的溶解度大于PbCO 的溶解度
4 3
B.向d点对应的溶液中加入对应阴离子的钠盐,溶液组成由d点向b点方向移动C.e约为4且对应的阴离子是SO
D.对于曲线Ⅰ,对b点的溶液加热(忽略水分蒸发),溶液组成由b点向c点移动
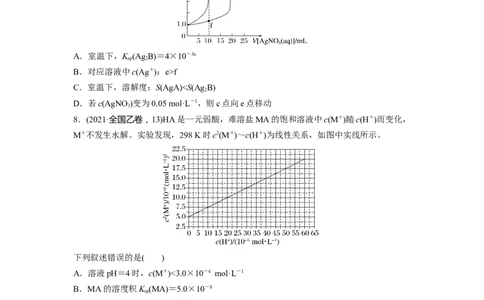
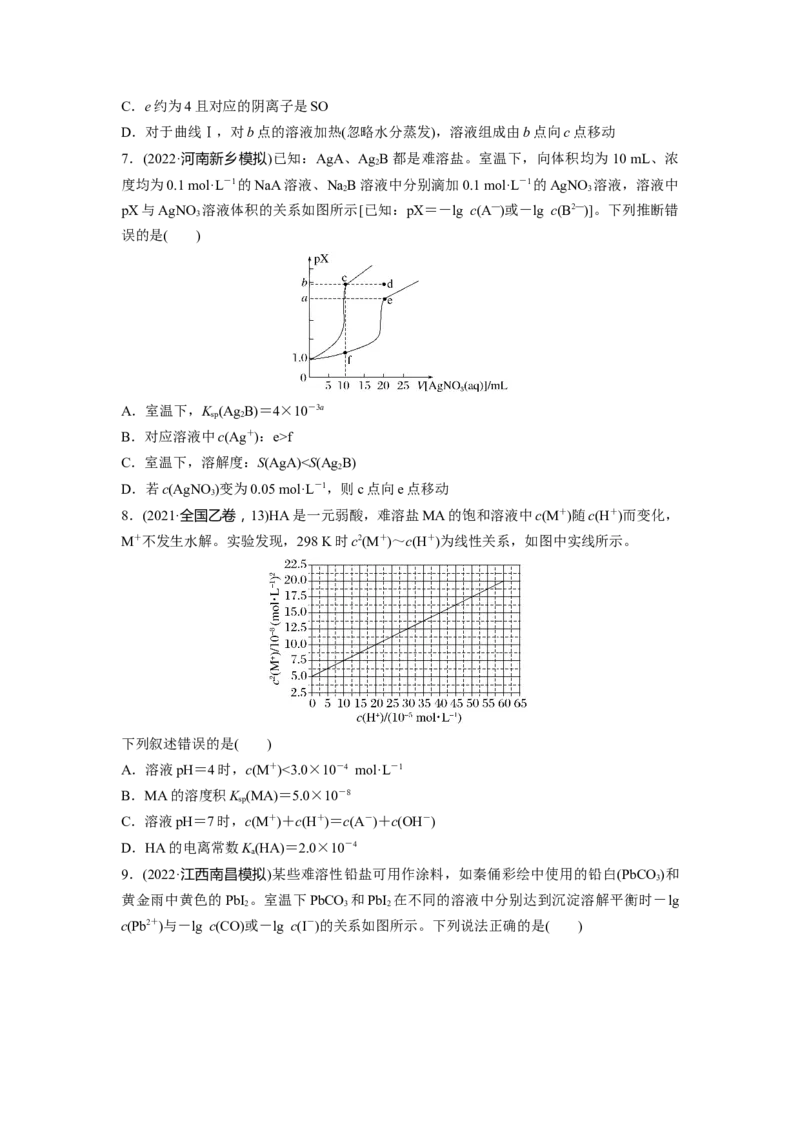
7.(2022·河南新乡模拟)已知:AgA、Ag B都是难溶盐。室温下,向体积均为10 mL、浓
2
度均为0.1 mol·L-1的NaA溶液、NaB溶液中分别滴加0.1 mol·L-1的AgNO 溶液,溶液中
2 3
pX与AgNO 溶液体积的关系如图所示[已知:pX=-lg c(A—)或-lg c(B2—)]。下列推断错
3
误的是( )
A.室温下,K (Ag B)=4×10-3a
sp 2
B.对应溶液中c(Ag+):e>f
C.室温下,溶解度:S(AgA)