文档内容
第 57 讲 难溶电解质的沉淀溶解平衡
[复习目标] 1.了解难溶电解质的沉淀溶解平衡。2.理解溶度积(K )的含义,并能进行相关
sp
计算。3.了解沉淀的生成、溶解与转化,并能应用化学平衡原理解释。
考点一 沉淀溶解平衡及影响因素
1.物质的溶解性与溶解度的关系
20 ℃时,电解质在水中的溶解度与溶解性存在如下关系:
2.沉淀溶解平衡
(1)概念
在一定温度下,当沉淀和溶解的速率______时,形成____________,达到平衡状态,把这
种平衡称为沉淀溶解平衡。
(2)沉淀溶解平衡的影响因素
①内因:难溶电解质本身的性质,即难溶电解质的溶解能力。
②外因:难溶电解质在水溶液中会建立动态平衡,改变温度和某离子浓度,会使沉淀溶解
平衡发生移动。
以AgCl为例:AgCl(s)Ag+(aq)+Cl-(aq) ΔH>0完成下表。
外界条件 移动方向 c(Ag+)
升高温度
加水(固体有剩余)
加入少量AgNO
3
加入NaS
2
通入HCl
通入NH
3
1.难溶电解质在水溶液中达到沉淀溶解平衡时,沉淀和溶解即停止( )
2.相同温度下,AgCl在水中的溶解能力与在NaCl溶液中的相同( )
3.难溶电解质达到沉淀溶解平衡时,增加难溶电解质的量,平衡向溶解方向移动( )1.将足量BaCO 固体分别加入:
3
①30 mL水;②10 mL 0.2 mol·L-1NaCO 溶液;③50 mL 0.01 mol·L-1 BaCl 溶液;④100
2 3 2
mL 0.01 mol·L-1盐酸中溶解至溶液饱和。
所得溶液中c(Ba2+)由大到小的顺序为____________________________。
2.已知溶液中存在平衡:Ca(OH) (s)Ca2+(aq)+2OH-(aq) ΔH<0,下列有关该平衡体
2
系的说法正确的是( )
①升高温度,平衡逆向移动
②向溶液中加入少量碳酸钠粉末能增大钙离子的浓度
③除去氯化钠溶液中混有的少量钙离子,可以向溶液中加入适量的NaOH溶液
④恒温下,向溶液中加入CaO,溶液的pH升高
⑤给溶液加热,溶液的pH升高
⑥向溶液中加入NaCO 溶液,其中固体质量增加
2 3
⑦向溶液中加入少量NaOH固体,Ca(OH) 固体质量不变
2
A.①⑥ B.①⑥⑦
C.②③④⑥ D.①②⑥⑦
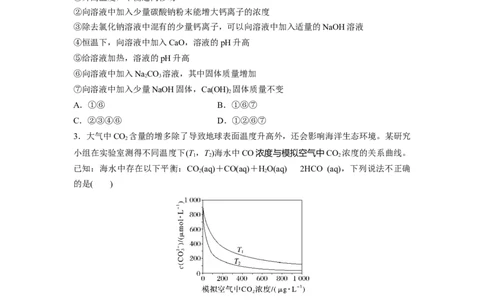
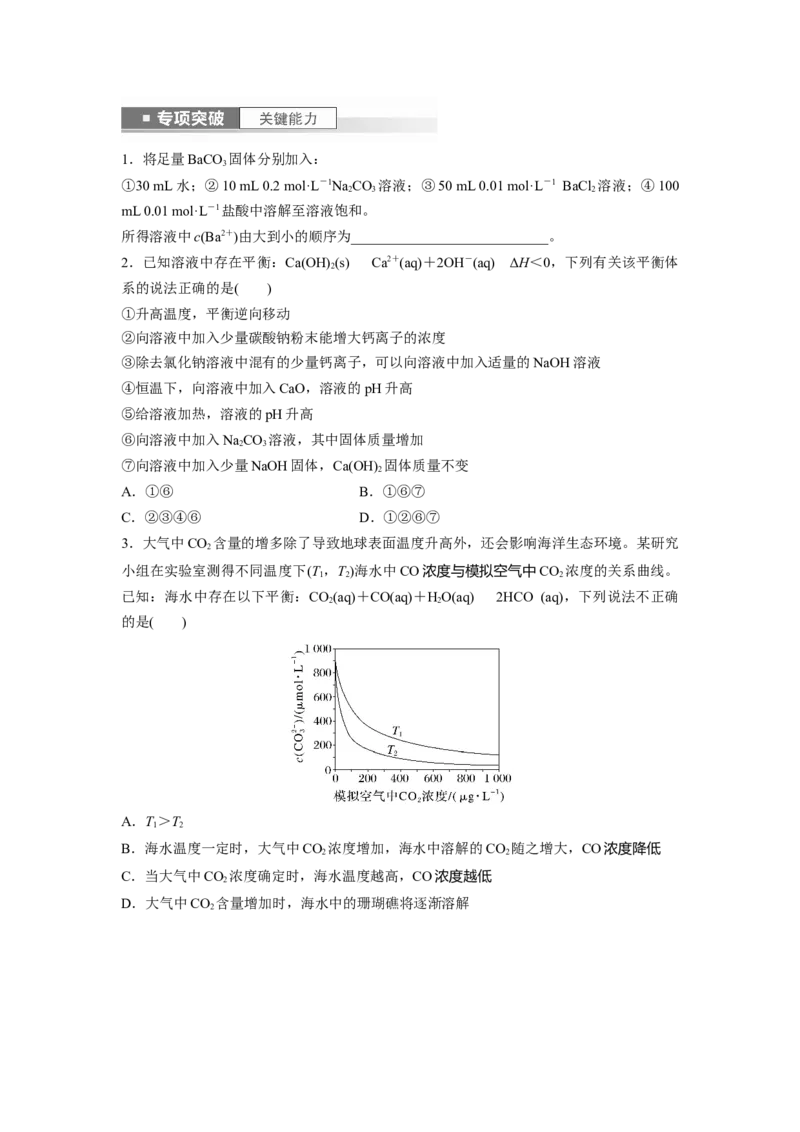
3.大气中CO 含量的增多除了导致地球表面温度升高外,还会影响海洋生态环境。某研究
2
小组在实验室测得不同温度下(T ,T)海水中CO浓度与模拟空气中CO 浓度的关系曲线。
1 2 2
已知:海水中存在以下平衡:CO(aq)+CO(aq)+HO(aq)2HCO (aq),下列说法不正确
2 2
的是( )
A.T>T
1 2
B.海水温度一定时,大气中CO 浓度增加,海水中溶解的CO 随之增大,CO浓度降低
2 2
C.当大气中CO 浓度确定时,海水温度越高,CO浓度越低
2
D.大气中CO 含量增加时,海水中的珊瑚礁将逐渐溶解
2考点二 溶度积常数及应用
1.溶度积常数和离子积
以A B (s)mAn+(aq)+nBm-(aq)为例:
m n
溶度积 离子积
含义 沉淀溶解平衡的平衡常数 溶液中有关离子浓度幂的乘积
符号 K Q
sp
K (A B )=__________________, Q(A B )=__________________,
sp m n m n
表达式
式中的浓度是平衡浓度 式中的浓度是任意浓度
判断在一定条件下沉淀能否生成或溶解
①Q>K :溶液过饱和,有______析出;
sp
应用
②Q=K :溶液饱和,处于______状态;
sp
③Q<K :溶液________,无沉淀析出
sp
2.K 的影响因素
sp
(1)内因:溶度积与难溶电解质溶解能力的关系:阴、阳离子个数比相同的难溶电解质,溶
度积______,其溶解能力____;不同类型的难溶电解质,应通过计算才能进行比较溶解能
力。
(2)外因:仅与______有关,与浓度、压强、催化剂等无关。
一、溶度积的概念及影响因素
1.下列说法正确的是( )
A.难溶电解质的溶度积K 越小,则它的溶解度越小
sp
B.K (Ag CrO)