文档内容
第一章 化学计量在实验中的应用
能力提升检测卷
时间:90分钟 分值:100分
可能用到的相对原子质量:H 1 Li 7 C 12 O16 Na 23 P 31 S 32 Cl 35.5 K 39 Ca 40
Fe 56 Cu 64
一、选择题(每小题只有一个正确选项,共16*3分)
1.(2022·北京石景山·一模)下列说法正确的是
A.室温下,pH相同的盐酸和醋酸溶液,溶质的物质的量浓度相同
B.等物质的量的NaO和NaO 含有相同数目的离子
2 2 2
C.同温同压下,O 和O 的密度相同
2 3
D.0.5mol/LNa SO 溶液中约含有3.01×1023个Na+
2 4
【答案】B
【解析】A. pH相同的盐酸和醋酸溶液,氢离子的物质的量浓度相同,盐酸是强酸,醋酸是弱酸,醋酸
的物质的量浓度大于盐酸的,故A错误;B. NaO和NaO 所含阴阳离子个数比都是1:2,所以等物质的
2 2 2
量的二者含有相同数目的离子,故B正确;C.同温同压下,密度之比等于摩尔质量之比,所以O 和O 的
2 3
密度不同,故C错误;D.溶液体积未知,无法求算 Na+的物质的量和个数,故D错误;故答案为:B
2.(2022·浙江·安吉县高级中学模拟预测)关于反应4Li+2SOCl =4LiCl+S+SO ,下列有关说法正确的是
2 2
A.还原剂只有Li
B.SOCl 既是氧化剂又是还原剂
2
C.氧化产物与还原产物的物质的量之比为2:1
D.每转移4mol电子,生成SO 的体积为22.4L
2
【答案】A
【解析】在反应4Li+2SOCl =4LiCl+S+SO 中,Li的化合价升高,做还原剂,生成的LiCl是氧化产物;
2 2
SOCl 中的S是+4价,反应后部分变为0价,生成单质硫,所以SOCl 做氧化剂,S为还原产物。A.由以
2 2
上分析可知,还原剂只有Li,故A正确;B.由以上分析可知,SOCl 中只有S的化合价发生变化,Cl和
2
O的化合价都没有发生变化,所以SOCl 只做氧化剂,故B错误;C.由以上分析可知,氧化产物LiCl与
2
还原产物S的物质的量之比为4:1,故C错误;D.没有指明温度和压强,无法计算生成的SO 的体积,
2
故D错误;故选A。
3.(2022·湖南师大附中模拟预测)科学家发现金星大气中存在 ,据此推断金星大气层或存在生命。利用下列反应可制备 : 。下列说法正确的是
A. 中化学键为非极性键
B.中子数为10的氧原子可表示为
C.每1mol 参加反应理论上可生成22.4L
D.每消耗12.4g的 ,则过程中转移电子数为0.3N
A
【答案】D
【解析】A. 中化学键为不同原子间形成的键,为极性键,A错误;B.核素的表示方法为:元素符号
左下角为质子数,左上角为质量数;中子数为10的氧原子可表示为 ,B错误;C.没有说明是否为标
况,不能判断生成 的体积,C错误;D.反应前后 中有1个磷原子得到3个电子,化合价由0变
为-3,另一部分磷原子失去电子,电子转移为 ~3e-,12.4g的 的物质的量为0.1mol,则过程中转移电
子数为0.3N ,D正确;故选D。
A
4.(2022·福建省龙岩第一中学模拟预测)过硫酸钾 常用作强氧化剂,可发生反应:
。过硫酸根 的离子结构如图所示。下列说法正确的是
A. 中氧元素的化合价有: 、
B. 中含 极性共价键C. 固体中阴阳离子总数为
D. 和水反应产生
【答案】A
【解析】A.由结构可知, 分子结构的中间存在过氧根,过氧根中氧为-1价氧,与每个硫相连的其
它氧为-2价氧, A正确;B.过氧根中氧氧键为非极性键,1个过硫酸根中含有12个极性共价键,
中含 极性共价键,B错误;C. 固体中含有K+和HSO 两种离子,则
固体中阴阳离子总数为 ,C错误;D.没有说明是否为标况,不能计算生成氧气的体积,D错误;故
选A。
5.(2022·天津市新华中学一模)设 为阿伏加德罗常数的值,下列有关叙述正确的是
A. 白磷 中白磷分子总数为
B. 含 为 的矿泉水含 数目为
C.由乙烯制备一氯乙烷若获得 产品需 个 分子
D.标准状况下, 与足量水反应可获得 个 分子
【答案】B
【解析】A.31g白磷(P )的物质的量为 =0.25mol,则白磷分子总数为0.25N ,A错误;B.
4 A
2L 含 K+ 19.5 mg/L 的矿泉水中 K+的物质的量为 =10−3mol,则K+数目为 10-3 N ,B
A
正确;C.由乙烯制备一氯乙烷,生成 1 mol 产品理论上需HCl分子数为 N ,C错误;D.标准状况下,
A
SO 不是气体,不能用气体摩尔体积进行计算,D错误;故选:B。
3
6.(2022·北京育才学校三模)下列各项比较中,正确的是
A.7.8g Na O 中含有的离子数为0.4N
2 2 AB.标准状况下,等体积乙烷和苯,所含分子数相等
C.等物质的量的Fe和Cu分别与足量的Cl 反应,转移的电子数相等
2
D.质量相同的 HO 和 DO(重水)所含的原子数不相同
2 2
【答案】D
【解析】A.7.8g Na O 的物质的量为0.1mol,1个NaO 含有2个Na+和1个O ,所以7.8g Na O 中含有
2 2 2 2 2 2
的离子数为0.3N ,故A错误;B.同温同压条件下,相同体积的任何气体具有相同分子数,苯标况下为液
A
体,不能使用阿伏加德罗定律,所以标准状况下,等体积乙烷和苯,所含分子数不相等,故B错误;C.
1mol铁与足量氯气反应生成氯化铁,转移3mol电子,1mol铜与足量氯气反应生成氯化铜,转移2mol电子,
故C错误;D.HO 和 DO(重水)的摩尔质量不同,所以质量相同的 HO 和 DO(重水)的物质的量不同,
2 2 2 2
所含的原子数不相同,故D正确;故答案选D。
7.(2022·辽宁·模拟预测)下列叙述中正确的是
A.钠与水,铁与水蒸气反应均得到相应的碱和氢气
B.1mol Cu分别与足量浓硝酸和稀硝酸反应,生成气体的物质的量相等
C.1mol Fe分别与足量Cl、S充分反应,转移电子数相等
2
D.向饱和NaCO 溶液中通入足量CO,有NaHCO 结晶析出
2 3 2 3
【答案】D
【解析】A.铁与水蒸气反应生成四氧化三铁和氢气,A叙述错误;B.Cu与浓硝酸反应生成NO ,与稀
2
硝酸反应生成NO,根据电子得失守恒知1molCu分别与足量浓硝酸和稀硝酸反应,生成气体的物质的量不
相等,B叙述错误;C.1molFe分别与足量Cl、S充分反应,分别生成FeCl 、FeS,转移电子数不相等,
2 3
C叙述错误;D.NaHCO 在水中的溶解度小于NaCO,因此向饱和NaCO 溶液中通入CO,有NaHCO
3 2 3 2 3 2 3
结晶析出,D叙述正确;故答案选D。
8.(2022·北京海淀·二模)下列说法正确的是
A.室温下,1L0.1mol·L-1盐酸中H+的数目约为6.02×1022
B.标准状况下,5.6LCCl 中所含C—Cl键的数目约为6.02×1023
4
C.5.6gFe和足量Cl 反应转移电子的物质的量为0.2mol
2
D.室温下,pH相同的盐酸和硫酸中,溶质的物质的量浓度相同
【答案】A
【解析】A.1L0.1mol·L-1盐酸中H+的物质的量为0.1mol,H+的个数约为: ,
A正确;B.标准状况下CCl 为液态,无法计算其物质的量,也无法计算含C-Cl键个数,B错误;C.Fe
4和足量Cl 反应生成三氯化铁,铁元素化合价为+3价,转移电子的物质的量为0.3mol,C错误;D.室温下,
2
pH相同的盐酸和硫酸中,氢离子浓度相同,盐酸的浓度是硫酸浓度的2倍,溶质的物质的量浓度不相同,
D错误;故选A。
9.(2022·黑龙江·哈尔滨三中模拟预测)设N 为阿伏加德罗常数的值,下列叙述正确的是
A
A.12gNaHSO 晶体中阳离子和阴离子的总数为0.3N
4 A
B.标准状况下,33.6L氟化氢的原子数为3N
A
C.标准状况下,2.24LD35Cl分子中所含有的中子数目为1.9N
A
D.含4.8g碳元素的石墨晶体中的共价键数为1.2N 个
A
【答案】C
【解析】A.NaHSO 晶体由钠离子和硫酸氢根离子构成,12gNaHSO 晶体的物质的量为
4 4
=0.1mol,阳离子和阴离子的总数为0.2N ,A错误;B.标准状况下,氟化氢为液体,不能用V =22.4L/
A m
mol计算,B错误;C.标准状况下,2.24LD35Cl的物质的量为 =0.1mol,含中子的物质的量为
0.1mol (1+35-17)=1.9,个数为1.9N ,C正确;D.石墨中每个碳原子参与形成3个共价键,每个碳原子
A
形成的共价键数为 =1.5,含4.8g碳元素的石墨晶体的物质的量为 =0.4mol,含碳原子0.4mol,共
价键为0.4mol 1.5=0.6mol,个数为0.6N ,D错误;答案选C。
A
10.(2022·北京·模拟预测)下列关于“100 mL 0.1 mol·L-1 BaCl 溶液”的说法正确的是
2
A.该溶液中含有的微粒主要有:BaCl 、Ba2+、Cl-、HO
2 2
B.若取该溶液10 mL,其中c(Ba2+)=0.01 mol·L-1
C.若取该溶液10 mL,恰好能与10 mL 0.1 mol·L-1 Na SO 溶液完全反应
2 4
D.该溶液与0.1 mol·L-1 NaCl溶液中的c(Cl-)相等
【答案】C
【解析】A.BaCl 是强电解质,在水中完全电离为Ba2+、Cl-,不存在BaCl ,同时该溶液中还含有溶剂
2 2
HO分子,A错误;B.溶液的浓度与溶液体积大小无关,所以从该溶液中取该溶液10 mL,物质的浓度不
2
变,其中c(Ba2+)=0.1 mol·L-1,B错误;C.BaCl 、NaSO 发生反应:BaCl +Na SO =BaSO ↓+2NaCl,二者
2 2 4 2 2 4 4
恰好反应时物质的量相等,由于两种溶液浓度相同、体积相等,因此10 mL0.1 mol/L BaCl 溶液恰好能与
2
10 mL 0.1 mol·L-1 Na SO 溶液完全反应,C正确;D.该溶液中c(Cl-)=2c(BaCl )=0.2 mol/L,0.1 mol·L-1
2 4 2NaCl溶液中的c(Cl-)=0.1 mol·L-1,可见两种溶液中c(Cl-)不相等,D错误;故合理选项是C。
11.(2022·重庆市天星桥中学一模)溶质均为 的 两种酸, 与足量铝反应生成 体
积为 (标准状况,下同): 与足量锌反应生成 体积为 。下列说法错误的是
A. 和 生成氢气的物质的量之比一定为
B. 和 消耗铝和锌的物质的量之比一定为
C.
D.由题给条件无法确定m和n的具体数值
【答案】B
【解析】A.由H X生成H 的物质的量n= ,由HY生成H 的物质的量n= ,则两种酸
m 2 1 n 2 2
生成H 物质的量之比为 (或者根据相同条件下,气体物质的量之比等于体积比也可得出),A正
2
确;B.设消耗Al的物质的量为x mol,由得失电子守恒得:3x mol=2× ,解得x= ,设
消耗Zn的物质的量为y mol,由得失电子守恒得:2y mol=2× ,解得y= ,故消耗的铝和
锌物质的量之比为 ,B错误;C.由于金属足量,故两种酸都完全反应,根据氢元素守恒得:0.1
mol×m=2× ,解得m= ,同理0.1 mol×n=2× ,解得n= ,故 ,C正确;
D.由C选项分析知,m= 、n= ,由于V、V 具体数值未知,故无法确定m、n具体数值,D正确;
1 2故答案选B。
12.(2022·广西·南宁二中模拟预测)2021年,我国科学家首次在实验室实现 到淀粉的全合成,其合
成路线如下:设 为阿伏伽德罗常数,下列有关说法不正确的是
A.标况下,11.2L 中含有共用电子对数目为2
B.反应②、③无法在高温下进行
C.反应②中,3.2g 生成HCHO时转移电子数目为0.2
D.1mol DHA与乙酸发生取代反应,可消耗乙酸分子数目为
【答案】D
【解析】A. 的结构式为O=C=O,标况下11.2L 中含有共用电子对数目为 ,
故A正确;B.反应②、③需要用酶作2催化剂,反应②、③无法在高温下进行,故B正确;C.反应②中,
3.2g 生成HCHO时转移电子数目为 ,故C正确;D.DHA含有2个羟基,
1mol DHA与乙酸发生取代反应,可消耗2mol乙酸,故D错误;选D。
13.(2022·山东潍坊·三模)南京大学科研团队首次发现氨还原过程中的多米诺效应:即一旦完成第①步,
将自发完成后续步骤,反应过程示意图如下。N 表示阿伏伽德罗常数的值,下列说法正确的是
AA. 含有N 个价电子 B. 中含有3N 个共价键
A A
C.若 参与第②步反应转移电子数为0.1N D.①②③步反应均为氧化还原反应
A
【答案】C
【解析】A. 的物质的量不确定,无法计算含有的价电子个数,A错误;B. 是离子化合物,
只有离子键,B错误;C. 的物质的量是0.1mol,参与第②步反应时化合价从0价升高到+1价,则
转移电子数为0.1N ,C正确;D.第③步反应是氢离子和氨气反应生成铵根,是非氧化还原反应,D错误;
A
答案选C。
14.(2022·辽宁·沈阳二中模拟预测)纯碱在生产、生活中有广泛应用。例如可用足量的纯碱溶液吸收含
氯气的尾气,生成三种盐(反应1);工业上也可用纯碱溶液从海水中提取溴,其主要原理如下:
反应2: ;反应3:
。
下列说法正确的是
A.反应2中氧化剂与还原剂的质量之比为1∶5
B.标准状况下,22.4L溴单质中含有2mol溴原子
C.反应1中生成的三种盐是NaClO, 和
D.反应2中的 与反应1中的 表现出了相似的化学性质
【答案】D
【解析】A.反应2中溴既是氧化剂又是还原剂,其中氧化剂与还原剂的质量之比为 ,A项错误;B.
标准状况下,溴单质呈液态, 项错误;C.根据氧化还原反应原理及纯碱足量,氯元素一部分化合价升
高,另一部分化合价降低,三种盐是次氯酸钠、氯化钠、碳酸氢钠,C项错误;D.反应2中的溴单质和
反应1中的氯气都表现氧化性和还原性,D项正确;故选D。
15.(2022·浙江嘉兴·二模)关于反应2KMnO KMnO +MnO+O ↑,下列说法正确的是
4 2 4 2 2
A.Mn元素被氧化B.氧化产物与还原产物物质的量之比为2:1
C.该反应中氧化性最强的是KMnO
4
D.生成2.24L O 时,转移0.4mol电子
2
【答案】C
【解析】Mn元素的化合价由KMnO 中的+7价降至KMnO 中的+6价和MnO 中的+4价,O元素的化合价
4 2 4 2
由-2价升至O 中的0价,KMnO 既是氧化剂、又是还原剂,KMnO 和MnO 是还原产物,O 是氧化产物;
2 4 2 4 2 2
据此分析作答。A.Mn元素的化合价由KMnO 中的+7价降至KMnO 中的+6价和MnO 中的+4价,Mn
4 2 4 2
元素化合价降低,Mn元素被还原,A错误;B.Mn元素的化合价由KMnO 中的+7价降至KMnO 中的+6
4 2 4
价和MnO 中的+4价,KMnO 和MnO 是还原产物,O元素的化合价由-2价升至O 中的0价,O 是氧化
2 2 4 2 2 2
产物,氧化产物与还原产物物质的量之比为1:2,B错误;C.该反应中KMnO 既是氧化剂、又是还原剂,
4
KMnO 和MnO 是还原产物,O 是氧化产物,根据同一氧化还原反应中,氧化剂的氧化性强于氧化产物,
2 4 2 2
该反应中氧化性最强的是KMnO ,C正确;D.O 所处温度和压强未知,无法计算2.24LO 物质的量,无
4 2 2
法计算转移电子物质的量,D错误;答案选C。
16.(2022·天津红桥·一模)下列说法正确的是
A.标准状况下, 中所含 键的数目为
B.质量相同的 和 (重水)所含的原子数相同
C.室温下, 的氨水中, 的物质的量为
D.室温下, 溶液中 的数目为
【答案】A
【解析】A.1个CH 分子含4个C-H键,标准状况下,5.6L CH 的物质的量为 =0.25mol,所含
4 4
C-H键的数目为0.25mol 4 6.02 1023/mol= ,故A正确;B.HO的相对分子质量为18,DO的
2 2
相对分子质量为20,二者的摩尔质量不同,质量相同的HO和DO,物质的量不同,所含的原子数不同,
2 2
故B错误;C.pH=12的氨水中,c(OH-)=0.01mol/L,因溶液的体积未知,故无法计算OH-的物质的量,故
C错误;D. 的物质的量为1L 0.1mol/L =0.1mol,但醋酸为弱酸,部分电离,故的数目小于 ,故D错误;答案选A。
二、主观题(共5小题,共52分)
17.(10分)(2022·山东聊城市·高三二模)过氧化钙 是一种用途广泛的优良供氧剂,常温下为
白色固体,能溶于酸,难溶于水、乙醇,且本身无毒,不污染环境,某实验小组制备 过程如下。
Ⅰ.制备
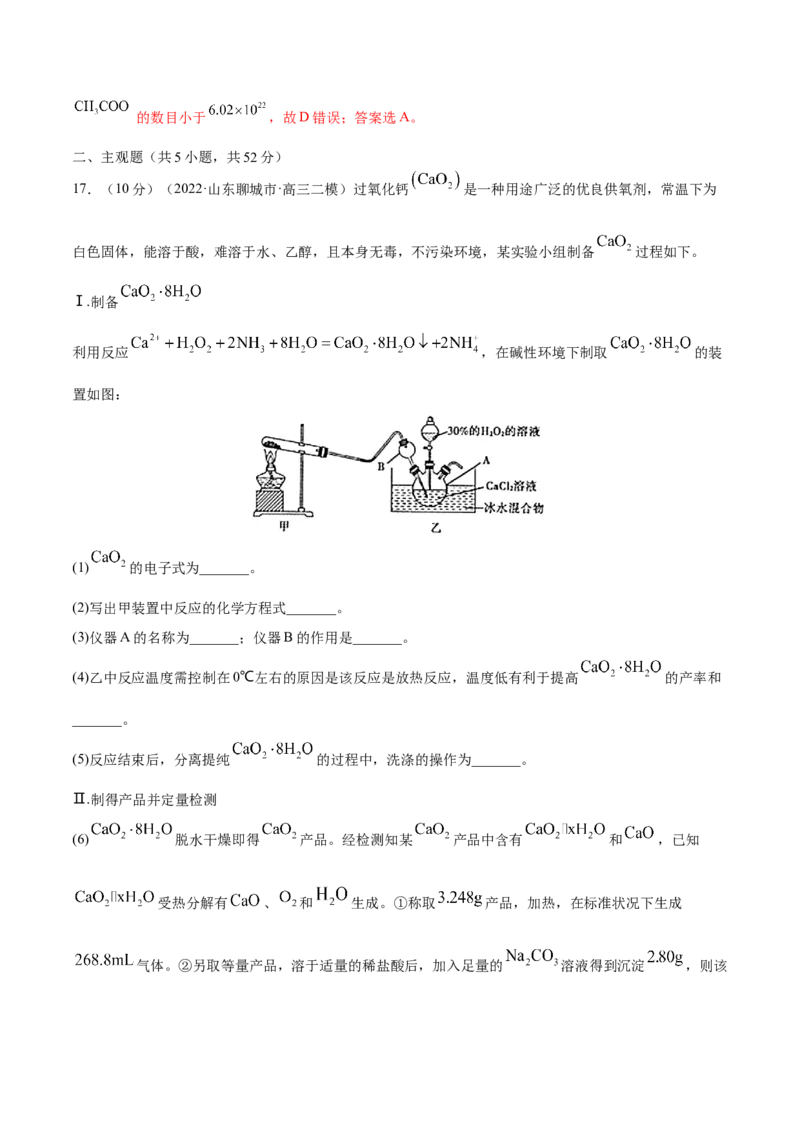
利用反应 ,在碱性环境下制取 的装
置如图:
(1) 的电子式为_______。
(2)写出甲装置中反应的化学方程式_______。
(3)仪器A的名称为_______;仪器B的作用是_______。
(4)乙中反应温度需控制在0℃左右的原因是该反应是放热反应,温度低有利于提高 的产率和
_______。
(5)反应结束后,分离提纯 的过程中,洗涤的操作为_______。
Ⅱ.制得产品并定量检测
(6) 脱水干燥即得 产品。经检测知某 产品中含有 和 ,已知
受热分解有 、 和 生成。①称取 产品,加热,在标准状况下生成
气体。②另取等量产品,溶于适量的稀盐酸后,加入足量的 溶液得到沉淀 ,则该产品中 的x值为_______。
【答案】(1) (1分)(2) (2分)(3) 三颈烧瓶(1
分) 防倒吸(1分) (4)过氧化氢的利用率(1分) (5) 向过滤器中加入蒸馏水浸没沉淀,待水自然流
出后,重复操作2—3次(2分) (6) 3 (2分)
【解析】由实验装置图可知,装置甲中氯化铵固体和氢氧化钙共热反应制备氨气,装置乙中,在冰水浴的
条件下,三颈烧瓶中发生的反应为氯化钙、过氧化氢和氨气反应生成八水过氧化钙和氯化铵,氨气极易溶
于水,长颈漏斗在实验中起防倒吸的作用。
(1)过氧化钙是由钙离子和过氧根离子形成的离子化合物,电子式为 ,故答案为:
;
(2) 甲装置中发生的反应为氯化铵固体和氢氧化钙共热反应生成氯化钙、氨气和水,反应的化学方程式为
,故答案为: ;
(3)由分析可知,装置乙中仪器A的名称为三颈烧瓶,装置B为长颈漏斗,用于防止因实验时氨气极易溶于
水产生倒吸,故答案为:三颈烧瓶;防倒吸;
(4) 乙中反应温度需控制在0℃左右的原因是该反应是放热反应,温度低,可以降低八水过氧化钙,便于晶
体析出,通过八水过氧化钙的产率,同时也能减少过氧化氢分解,提高过氧化氢的利用率,故答案为:过
氧化氢的利用率;
(5)洗涤八水过氧化钙的操作为向过滤器中加入蒸馏水浸没沉淀,待水自然流出后,重复操作2—3次即可,
故答案为:向过滤器中加入蒸馏水浸没沉淀,待水自然流出后,重复操作2—3次;
(6)由①可得:2CaO▪xH O—O ,266.8mL氧气的物质的量为 =0.012mol,则CaO▪xH O的物质
2 2 2 2 2
的量为0.012mol×2=0.024mol;由②可知,反应生成2.80g碳酸钙的物质的量为 =0.028mol,则样
品中CaO▪xH O和CaO的物质的量之和为0.028mol,则CaO的物质的量为0.028mol—
2 2
0.024mol=0.004mol;由样品的质量为3.248g可得:0.024mol×(72+18x)g/mol+ 0.004mol×56g/mol=3.248g,
解得x=3,故答案为:3。18.(12分)(2021·黑龙江哈尔滨市·哈尔滨三中高三一模)碱式碳酸铜又名孔雀石,主要成分为
Cu (OH) CO,呈绿色,是一种具有广泛用途的化工产品。某化学小组探究制备碱式碳酸铜的反应条件并
2 2 3
制备少量碱式碳酸铜。
试剂:0.25 mol·L-1 Na CO 溶液、0.5 mol·L-1 NaOH溶液、0.5 mol·L-1 Cu(NO ) 溶液各100mL
2 3 3 2
实验1:探究Cu(NO ) 与NaOH和NaCO 溶液配比
3 2 2 3
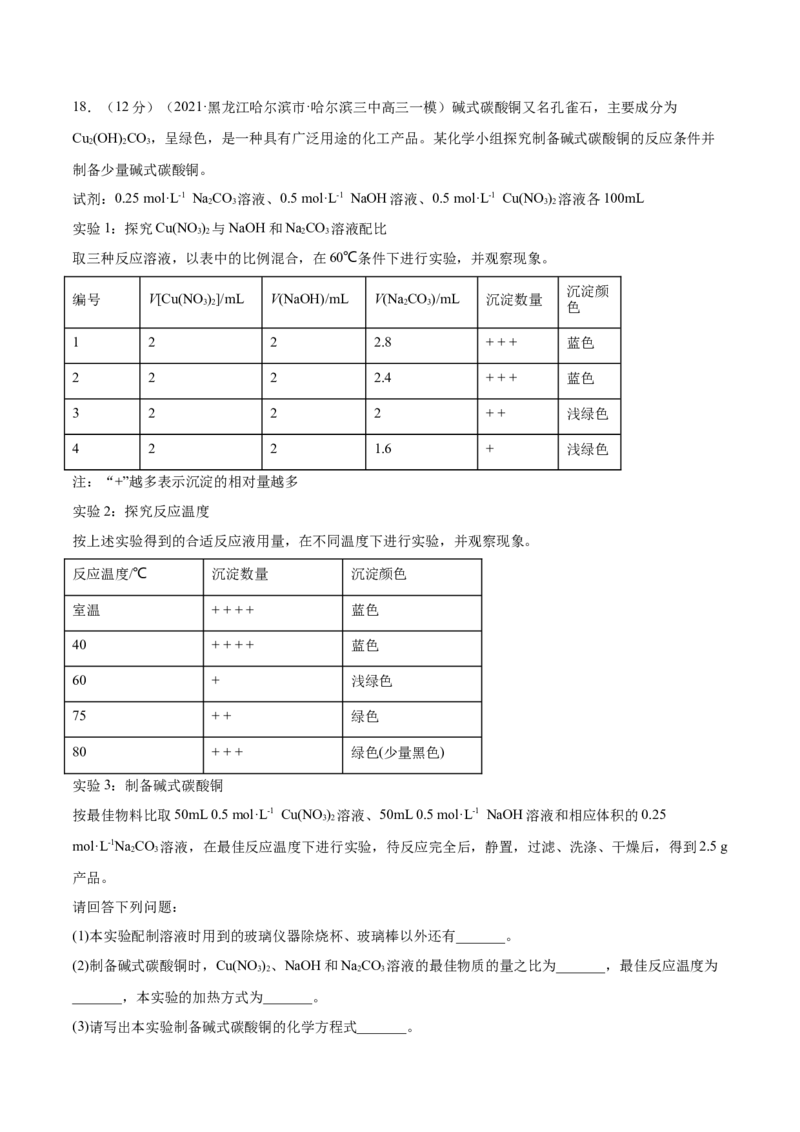
取三种反应溶液,以表中的比例混合,在60℃条件下进行实验,并观察现象。
沉淀颜
编号 V[Cu(NO )]/mL V(NaOH)/mL V(Na CO)/mL 沉淀数量
3 2 2 3 色
1 2 2 2.8 + + + 蓝色
2 2 2 2.4 + + + 蓝色
3 2 2 2 + + 浅绿色
4 2 2 1.6 + 浅绿色
注:“+”越多表示沉淀的相对量越多
实验2:探究反应温度
按上述实验得到的合适反应液用量,在不同温度下进行实验,并观察现象。
反应温度/℃ 沉淀数量 沉淀颜色
室温 + + + + 蓝色
40 + + + + 蓝色
60 + 浅绿色
75 + + 绿色
80 + + + 绿色(少量黑色)
实验3:制备碱式碳酸铜
按最佳物料比取50mL 0.5 mol·L-1 Cu(NO ) 溶液、50mL 0.5 mol·L-1 NaOH溶液和相应体积的0.25
3 2
mol·L-1NaCO 溶液,在最佳反应温度下进行实验,待反应完全后,静置,过滤、洗涤、干燥后,得到2.5 g
2 3
产品。
请回答下列问题:
(1)本实验配制溶液时用到的玻璃仪器除烧杯、玻璃棒以外还有_______。
(2)制备碱式碳酸铜时,Cu(NO )、NaOH和NaCO 溶液的最佳物质的量之比为_______,最佳反应温度为
3 2 2 3
_______,本实验的加热方式为_______。
(3)请写出本实验制备碱式碳酸铜的化学方程式_______。(4)实验2中在80℃反应生成的沉淀中有少量黑色的物质,产生该物质的原因可能是_______。
(5)计算本实验的产率_______%(保留三位有效数字)。
【答案】(1)100mL 容量瓶、胶头滴管 (2分)
(2)2:2:1(2分) 75℃ (1分) 水浴加热 (1分)
(3)2NaOH+Na CO+2Cu(NO) = Cu (OH) CO+4NaNO (2分)
2 3 3 2 2 2 3 3
(4)碱式碳酸铜受热分解生成黑色的氧化铜(2分)
(5)90.1 (2分)
【解析】(1)本实验配制溶液时用到的玻璃仪器除烧杯、玻璃棒以外还有100mL 容量瓶、胶头滴管;
(2)由实验1表格数据可知,当Cu(NO )、NaOH和NaCO 溶液的体积均为2mL时,生成碱式碳酸铜最多,
3 2 2 3
又Cu(NO )、NaOH和NaCO 溶液的浓度分别为0.5 mol·L-1、0.5 mol·L-1、0.25 mol·L-1,则制备碱式碳酸铜
3 2 2 3
时,Cu(NO )、NaOH和NaCO 溶液的最佳物质的量之比为2:2:1;由实验2表格数据可知,当温度为
3 2 2 3
75℃时,生成碱式碳酸铜最多,则最佳反应温度为75℃,故本实验的加热方式为水浴加热;
(3)制备碱式碳酸铜的化学方程式为2NaOH+Na CO+2Cu(NO) = Cu (OH) CO+4NaNO ;
2 3 3 2 2 2 3 3
(4)实验2中在80℃反应生成的沉淀中有少量黑色的物质,产生该物质的原因可能是碱式碳酸铜受热分解生
成黑色的氧化铜;
(5)由反应方程式可知,理论上生成碱式碳酸铜的物质的量为 ,质量为 ,
则本实验的产率为 。
19.(10分)(2021·浙江宁波市·高三二模)硫粉和 溶液反应可以生成多硫化钠( ),离子反
应为: 、 …
(1)在 溶液中加入 硫粉,只发生 ,反应后溶液中 和 无剩余,则原
_______ 。
(2)在一定体积和浓度的 溶液中加入 硫粉,控制一定条件使硫粉完全反应,反应后溶液中的阴离子有 、 、 (忽略其他阴离子),且物质的量之比为 。则反应后溶液中的
_______ 。(写出计算过程)
【答案】(1)0.25 (2) 0.1
【解析】(1) 硫粉的物质的量为 =0.025mol,只发生 ,则
, 0.25 ;
(2) , ,根据 , ,
,
, 。
20.(10分)(2021·浙江衢州市·高三二模)混合碱(Na CO 与NaHCO ,或NaCO 与NaOH的混合物)的
2 3 3 2 3
成分及含量可用双指示剂法测定。步骤如下:取混合碱溶液25.00 mL,滴加2滴酚酞为指示剂,用0.2000
mol·L−1的盐酸滴定液滴定至溶液呈微红色,记下消耗盐酸体积为22.50 mL;再滴加2滴甲基橙,继续滴定
至溶液由黄色变为橙色,记下第二次滴定消耗盐酸的体积12.50 mL。(已知:HCO 的K =4.3×10-7;K
2 3 a1 a2
=5.6× 10-11)
请计算:
(1)混合碱成分及物质的量之比为___________。
(2)混合碱溶液中NaCO 的浓度为___________mol·L−1.(写出计算过程)
2 3
【答案】(1)5:4 (2)0.1000 mol·L−1
【解析】滴酚酞为指示剂,发生的反应为:OH-+H+=H O,CO +H+=HCO ,或只发生CO +H+=HCO
2
,甲基橙为指示剂时,发生HCO +H+=H O+CO ↑。由于两次消耗的酸的体积不相同,且第一次多于第二
2 2
次,混合碱成分是NaCO 与NaOH。
2 3
(1)由分析可知:混合碱成分是NaCO 与NaOH及物质的量之比为12.50 mL:(22.50 mL-12.50 mL)=5 :4。
2 3
故答案为:5:4;(2)n(Na CO)+n(NaOH)=0.2000mol·L−1×22.50mL=4.5×10-3mol,n(Na CO)= 4.5×10-3mol=2.5×10-3mol, 混
2 3 2 3
合碱溶液中NaCO 的浓度为 =0.1000 mol·L−1。故答案为:0.1000 mol·L−1。
2 3
21.(10分)(2022·浙江·模拟预测)向70.4g由 、 、 三种物质组成的固体混合物加入2L一
定浓度的稀硫酸后固体恰好溶解,可收集到标准状况下气体2.24L,再向反应后的溶液中滴入 溶液,
无明显现象。(忽略反应前后溶液的体积变化)
(1)反应后溶液中 的物质的量浓度为_______;
(2)原固体中 的质量取值范围为_______。
【答案】(1)0.5
(2)
【解析】(1)根据题意可以将铁和 看成 和铁单质,根据稀硫酸后固体恰好溶解,可收集到标准状
况下气体2.24L,收集氢气0.1mol,可知与酸反应生成氢气的铁单质为0.1mol即5.6g,氧化亚铁为70.4-
5.6=64.8g,即0.9mol,根据铁元素守恒可知 ,故 的物质的量
浓度为0.5mol/L。
(2)向70.4g由 、 、 三种物质组成的固体混合,根据上述计算可知铁元素的总量为1mol,其中
0.1mol参与反应生成氢气,假设剩下的0.9mol铁元素全部来自铁单质和 ,铁单质能将 正好转化
为亚铁离子, ,故铁单质与Fe3+为1:2, ,
,根据题意,混合物中还含有氧化亚铁,故 质量范围为
。