文档内容
第一章 化学计量在实验中的应用综合练习
【基础巩固】
1.某硫原子的质量是a g,12C原子的质量是b g,若N 表示阿伏加德罗常数的值,则下列说法正确
A
的是( )
①该硫原子的相对原子质量为 ②m g该硫原子的物质的量为 mol ③该硫原子的摩尔质量是aN
A
g ④a g该硫原子所含的电子数为16N
A
A.①③ B.②④ C.①② D.②③
2.设N 为阿伏加德罗常数的值,如果a g某气态双原子分子的分子数为p,则b g该气体在标准状
A
况下的体积V(L)是( )
A. B. C. D.
3.据央视新闻报道,在政府工作报告中指出,建设一批光网城市,推进 5万个行政村通光纤,让更
多城乡居民享受数字化生活。光缆的主要成分为SiO 。下列叙述正确的是( )
2
A.6 g光缆由0.1 mol SiO 分子构成
2
B.标准状况下,15 g SiO 的体积为5.6 L
2
C.SiO 中Si与O的质量之比为7∶8
2
D.相同质量的SiO 和CO 中含有的氧原子数相同
2 2
4.在150 ℃时碳酸铵受热可完全分解,则其完全分解后所产生的气态混合物的密度是相同条件下
氢气密度的( )
A.96倍 B.48倍 C.12倍 D.32倍
5.如图表示1 g O 与1 g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体可能是(
2
)
A.C H B.CH C.CO D.NO
2 4 4 2
6.一定温度和压强下,用m g的CH 、CO 、O 、SO 四种气体分别吹出四个体积大小不同的气球。
4 2 2 2
下列说法正确的是( )
A.气球②中装的是O
2
B.气球①和气球③中气体分子数相等
C.气球①和气球④中气体物质的量之比为4∶1
D.气球③和气球④中气体密度之比为2∶1
7.(2023·西宁质检)下列判断正确的是( )A.同温、同压下,相同体积的氮气和氦气所含的原子数相等
B.标准状况下,5.6 L以任意比例混合的氯气和氧气所含的原子数为0.5N
A
C.1 mol氯气和足量NaOH溶液反应转移的电子数为2N
A
D.常温、常压下,22.4 L的NO 和CO 混合气体含有2N 个O原子
2 2 A
8.配制250 mL 0.5 mol·L-1的NaOH溶液,在下列仪器中:①量筒、②250 mL容量瓶、③托盘天
平和砝码、④500 mL容量瓶、⑤烧杯、⑥玻璃棒、⑦漏斗、⑧药匙、⑨胶头滴管、⑩250 mL烧
瓶,需要用到的仪器按使用先后顺序排列正确的是( )
A.⑧③⑤⑥②⑨ B.②③⑦⑤⑥ C.②⑤⑦⑥① D.④③⑦⑤⑥
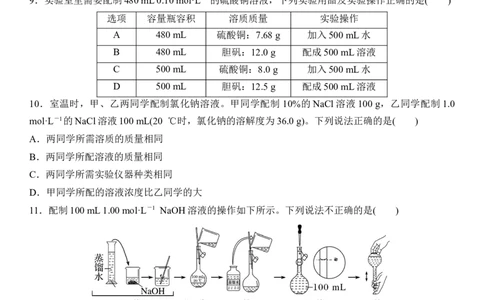
9.实验室里需要配制480 mL 0.10 mol·L-1的硫酸铜溶液,下列实验用品及实验操作正确的是( )
选项 容量瓶容积 溶质质量 实验操作
A 480 mL 硫酸铜:7.68 g 加入500 mL水
B 480 mL 胆矾:12.0 g 配成500 mL溶液
C 500 mL 硫酸铜:8.0 g 加入500 mL水
D 500 mL 胆矾:12.5 g 配成500 mL溶液
10.室温时,甲、乙两同学配制氯化钠溶液。甲同学配制 10%的NaCl溶液100 g,乙同学配制1.0
mol·L-1的NaCl溶液100 mL(20 ℃时,氯化钠的溶解度为36.0 g)。下列说法正确的是( )
A.两同学所需溶质的质量相同
B.两同学所配溶液的质量相同
C.两同学所需实验仪器种类相同
D.甲同学所配的溶液浓度比乙同学的大
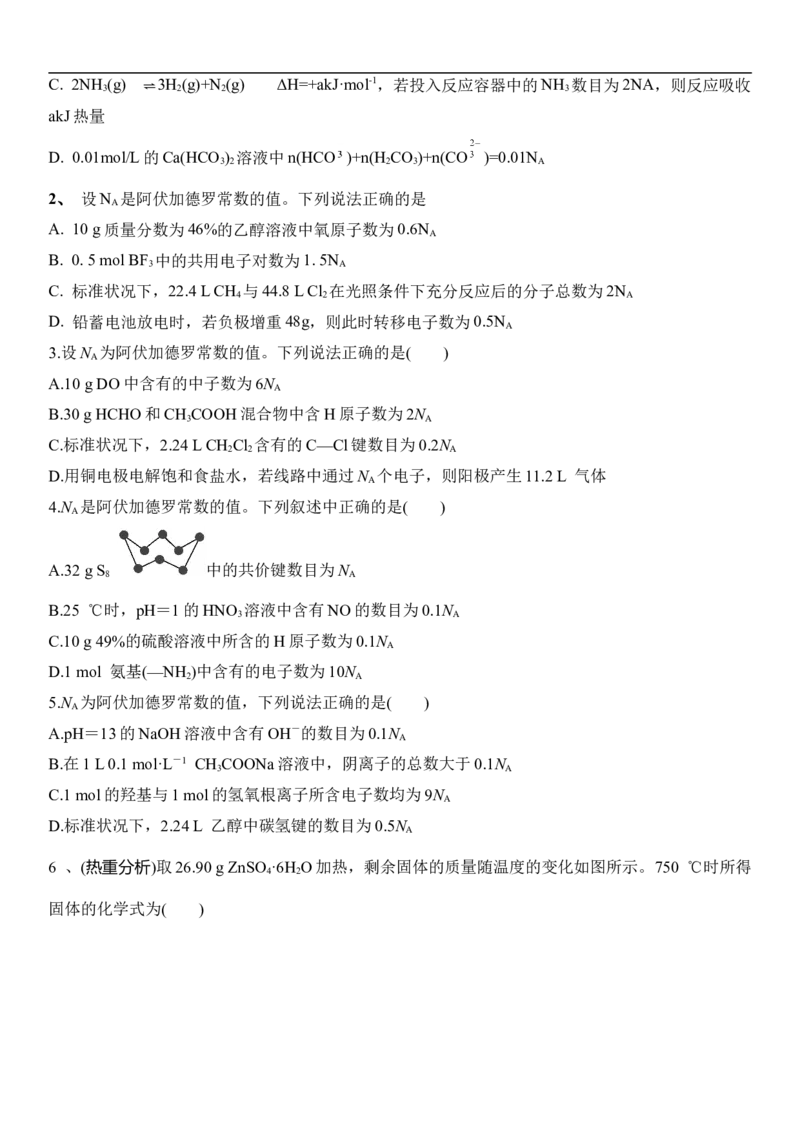
11.配制100 mL 1.00 mol·L-1 NaOH溶液的操作如下所示。下列说法不正确的是( )
A.操作1前称取NaOH的质量为4.0 g
B.操作2前NaOH溶液需恢复至室温
C.操作4若俯视刻度线定容,结果偏大
D.操作5后液面下降,需补充少量水至刻度线
【拔高练习】
1. N 代表阿伏加德罗常数的值,下列说法正确的是
A
A. 标况下,4.48LCH Cl中所含分子数为0.2N
3 A
B. 足量单质Cu与0.2mol浓硫酸在加热条件下反应,转移电子数为0.2N
AC. 2NH (g) 3H (g)+N (g) ΔH=+akJ·mol-1,若投入反应容器中的NH 数目为2NA,则反应吸收
3 ⇌ 2 2 3
akJ热量
D. 0.01mol/L的Ca(HCO ) 溶液中n(HCO )+n(H CO )+n(CO )=0.01N
3 2 2 3 A
2、 设N 是阿伏加德罗常数的值。下列说法正确的是
A
A. 10 g质量分数为46%的乙醇溶液中氧原子数为0.6N
A
B. 0. 5 mol BF 中的共用电子对数为1. 5N
3 A
C. 标准状况下,22.4 L CH 与44.8 L Cl 在光照条件下充分反应后的分子总数为2N
4 2 A
D. 铅蓄电池放电时,若负极增重48g,则此时转移电子数为0.5N
A
3.设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.10 g DO中含有的中子数为6N
A
B.30 g HCHO和CH COOH混合物中含H原子数为2N
3 A
C.标准状况下,2.24 L CH Cl 含有的C—Cl键数目为0.2N
2 2 A
D.用铜电极电解饱和食盐水,若线路中通过N 个电子,则阳极产生11.2 L 气体
A
4.N 是阿伏加德罗常数的值。下列叙述中正确的是( )
A
A.32 g S 中的共价键数目为N
8 A
B.25 ℃时,pH=1的HNO 溶液中含有NO的数目为0.1N
3 A
C.10 g 49%的硫酸溶液中所含的H原子数为0.1N
A
D.1 mol 氨基(—NH )中含有的电子数为10N
2 A
5.N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.pH=13的NaOH溶液中含有OH-的数目为0.1N
A
B.在1 L 0.1 mol·L-1 CH COONa溶液中,阴离子的总数大于0.1N
3 A
C.1 mol的羟基与1 mol的氢氧根离子所含电子数均为9N
A
D.标准状况下,2.24 L 乙醇中碳氢键的数目为0.5N
A
6 、(热重分析)取26.90 g ZnSO ·6H O加热,剩余固体的质量随温度的变化如图所示。750 ℃时所得
4 2
固体的化学式为( )A.ZnO B.ZnSO C.Zn O(SO ) D.ZnSO ·H O
4 3 4 2 4 2
7.(原子守恒)(1)MnCO 可用作电讯器材元件材料,还可用作瓷釉、颜料及制造锰盐的原料。它在空
3
气中加热易转化为不同价态锰的氧化物,其固体残留率随温度的变化,如图所示。则 300 ℃时,剩
余固体中n(Mn)∶n(O)为________;图中C点对应固体的成分为________(填化学式)。
(2)某工厂用m kg铬铁矿粉(含Cr O 40%)制备K Cr O ,最终得到产品m kg,产率为________。
1 2 3 2 2 7 2
8.(得失电子守恒)(1)以硅藻土为载体的五氧化二钒(V O )是接触法生产硫酸的催化剂。从废钒催化剂
2 5
中回收V O 既避免污染环境又有利于资源综合利用。
2 5
以下是一种废钒催化剂回收工艺路线:
“氧化”中欲使3 mol的VO2+变为VO,则需要氧化剂KClO 至少为________ mol。
3
(2)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是每克含氯消毒剂的氧化能力相当于
多少克Cl 的氧化能力。NaClO 的有效氯含量为________(计算结果保留两位小数)。
2 2【真题演练】
1.(2022·辽宁,3)设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.1.8 g 18O中含有的中子数为N B.28 g C H 分子中含有的σ键数目为4N
A 2 4 A
C.标准状况下,22.4 L HCl气体中H+数目为N D.pH=12的Na CO 溶液中OH-数目为0.01N
A 2 3 A
2.(2022·浙江6月选考,12)N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.12 g NaHSO 中含有0.2N 个阳离子
4 A
B.11.2 L乙烷和丙烯的混合气体中所含碳氢键数为3N
A
C.8 g CH 含有中子数为3N
4 A
D.0.1 mol H 和0.1 mol I 于密闭容器中充分反应后,HI分子总数为0.2N
2 2 A
3.(2022·海南,7)在2.8 g Fe中加入100 mL 3 mol·L-1 HCl,Fe完全溶解。N 代表阿伏加德罗常数
A
的值,下列说法正确的是( )
A.反应转移电子为0.1 mol B.HCl溶液中Cl-数为3N
A
C.2.8 g 56Fe含有的中子数为1.3N D.反应生成标准状况下气体3.36 L
A
4.(2022·全国甲卷,11)N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.25 ℃,101 kPa下,28 L氢气中质子的数目为2.5N
A
B.2.0 L 1.0 mol·L-1 AlCl 溶液中,Al3+的数目为2.0N
3 A
C.0.20 mol苯甲酸完全燃烧,生成CO 的数目为1.4N
2 A
D.电解熔融CuCl ,阴极增重6.4 g,外电路中通过电子的数目为0.10N
2 A
5.(2021·广东,11)设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.1 mol CHCl 含有C—Cl键的数目为3N
3 A
B.1 L 1.0 mol·L-1的盐酸含有阴离子总数为2N
A
C.11.2 L NO与11.2 L O 混合后的分子数目为N
2 A
D.23 g Na与足量H O反应生成的H 分子数目为N
2 2 A
6.(2021·浙江6月选考,18)设N 为阿伏加德罗常数的值。下列说法不正确的是( )
A
A.标准状况下,1.12 L 18O 中含有中子数为N
2 A
B.31 g P 中的共价键数目为1.5N
4 A
C.100 mL 0.1 mol·L-1的NaOH水溶液中含有氧原子数为0.01N
A
D.18.9 g 三肽C H N O (相对分子质量:189)中的肽键数目为0.2N
6 11 3 4 A
7.(2021·湖南,5)N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.18 g H 18O含有的中子数为10N
2 A
B.0.1 mol·L-1 HClO 溶液中含有的H+数为0.1N
4 A
C.2 mol NO与1 mol O 在密闭容器中充分反应后的分子数为2N
2 A
D.11.2 L CH 和22.4 L Cl (均为标准状况)在光照下充分反应后的分子数为1.5N
4 2 A8.(2021·河北,7)N 是阿伏加德罗常数的值。下列说法错误的是( )
A
A.22.4 L(标准状况)氟气所含的质子数为18N
A
B.1 mol碘蒸气和1 mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2N
A
C.电解饱和食盐水时,若阴阳两极产生气体的总质量为73 g,则转移电子数为N
A
D.1 L 1 mol·L-1溴化铵水溶液中NH与H+离子数之和大于N
A