文档内容
第4讲 难溶电解质的溶解平衡
【2020·备考】
最新考纲:1.了解难溶电解质的沉淀溶解平衡。2.理解溶度积的含义及其表达式,
能进行相关的计算。
核心素养:1.变化观念与平衡思想:认知难溶电解质的溶解平衡有一定限度,是可
以调控的。能多角度、动态地分析难溶电解质的溶解平衡,并运用难溶电解质的溶
解平衡原理解决实际问题(利用沉淀生成处理污水等)。2.科学探究与创新意识:能
发现和提出有关难溶电解质的溶解平衡的判断问题;能从问题和假设出发,确定
探究目的,设计探究方案,进行沉淀转化等实验探究。
考点一 沉淀的溶解平衡及应用
(频数:★☆☆ 难度:★★★)
INCLUDEPICTURE "名师课堂.tif" \* MERGEFORMAT INCLUDEPICTURE
" 名 师 课 堂 .tif" \* MERGEFORMAT
INCLUDEPICTURE " 书名号 .TIF " \* MERGEFORMAT INCLUDEPICTURE
" 书名号 .TIF" \* MERGEFORMAT 名师课堂导语 本考点主要考查沉淀溶解平
衡的影响因素,沉淀的生成、溶解及转化的理解;特别是沉淀的转化问题,是高考
常考点,复习时加以关注.
1.沉淀溶解平衡
(1)含义
在一定温度下的水溶液中,当沉淀溶解和生成的速率相等时,即建立了溶解平衡
状态。
(2)建立过程INCLUDEPICTURE "5H596.tif" \* MERGEFORMAT
(3)特征
INCLUDEPICTURE "5H597.TIF" \* MERGEFORMAT
2.影响沉淀溶解平衡的因素
(1)内因
难溶电解质本身的性质,这是决定因素。
(2)外因
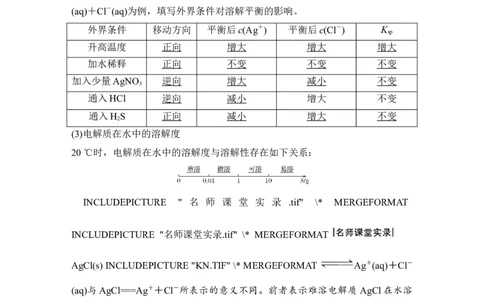
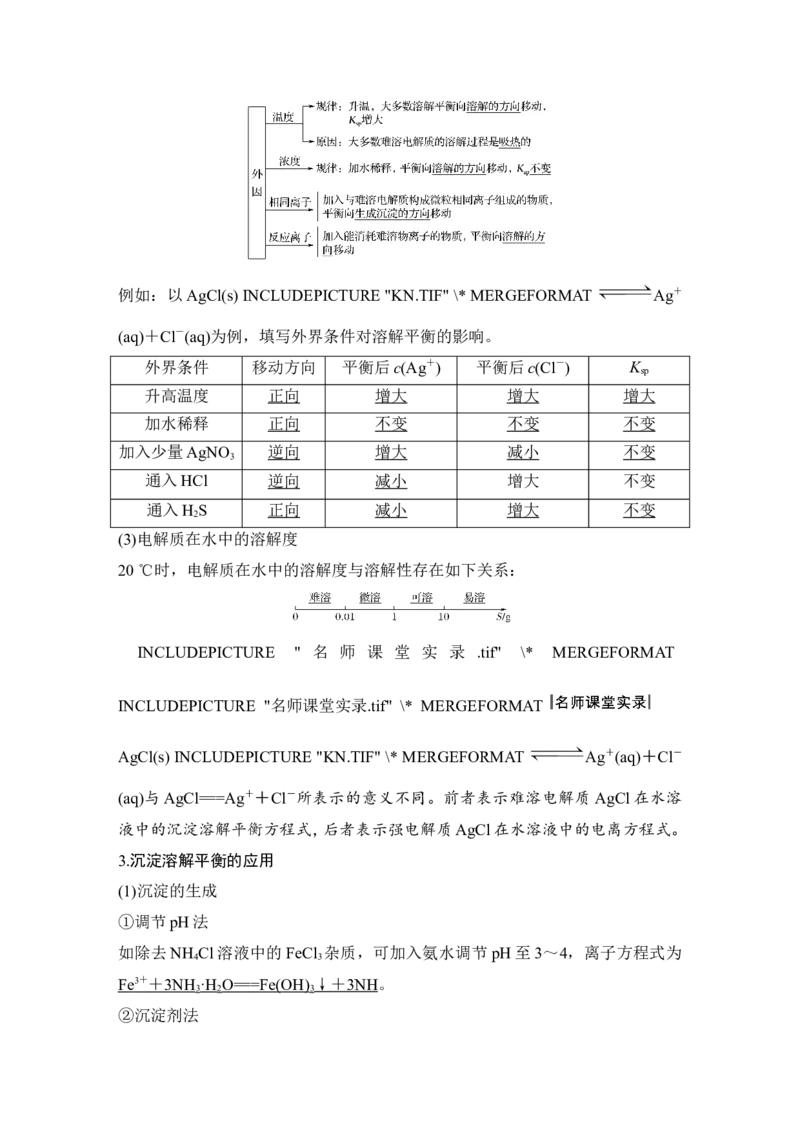
INCLUDEPICTURE "P871.TIF" \* MERGEFORMAT例如:以AgCl(s) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT Ag+
(aq)+Cl-(aq)为例,填写外界条件对溶解平衡的影响。
外界条件 移动方向 平衡后c(Ag+) 平衡后c(Cl-) K
sp
升高温度 正向 增大 增大 增大
加水稀释 正向 不变 不变 不变
加入少量AgNO 逆向 增大 减小 不变
3
通入HCl 逆向 减小 增大 不变
通入H S 正向 减小 增大 不变
2
(3)电解质在水中的溶解度
20 ℃时,电解质在水中的溶解度与溶解性存在如下关系:
INCLUDEPICTURE " 名 师 课 堂 实 录 .tif" \* MERGEFORMAT
INCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
AgCl(s) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT Ag+(aq)+Cl-
(aq)与AgCl===Ag++Cl-所表示的意义不同。前者表示难溶电解质 AgCl在水溶
液中的沉淀溶解平衡方程式,后者表示强电解质AgCl在水溶液中的电离方程式。
3.沉淀溶解平衡的应用
(1)沉淀的生成
①调节pH法
如除去NH Cl溶液中的FeCl 杂质,可加入氨水调节pH至3~4,离子方程式为
4 3
Fe 3 + + 3NH ·H O == =Fe(OH) ↓ + 3NH 。
3 2 3
②沉淀剂法如用H S沉淀Cu2+,离子方程式为H S + Cu 2 + == =CuS ↓ + 2H + 。
2 2
(2)沉淀的溶解
①酸溶解法
如CaCO 溶于盐酸,离子方程式为CaCO + 2H + == =C a 2 + + H O + CO ↑。
3 3 2 2
②盐溶液溶解法
如 Mg(OH) 溶于 NH Cl 溶液,离子方程式为 Mg(OH) + 2NH == =M g 2 + +
2 4 2
2NH ·H O。
3 2
③氧化还原溶解法
如不溶于盐酸的硫化物Ag S溶于稀HNO 。
2 3
④配位溶解法
如AgCl溶于氨水,离子方程式为 AgCl + 2NH ·H O == =[Ag(NH ) ] + + Cl - + 2H O。
3 2 3 2 2
(3)沉淀的转化
①实质:沉淀溶解平衡的移动(沉淀的溶解度差别越大,越容易转化)。
②应用:锅炉除垢、矿物转化等。
INCLUDEPICTURE " 名 师 课 堂 实 录 .tif" \* MERGEFORMAT
INCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
1.一般说来,溶解度小的沉淀转化成溶解度更小的沉淀容易实现,但溶解度小的沉
淀转化成溶解度稍大的沉淀也能实现。
2.用沉淀法除杂不可能将杂质离子全部通过沉淀除去。一般认为残留在溶液中的
离子浓度小于1×10-5 mol·L-1时,沉淀已经完全。
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)沉淀达到溶解平衡时,溶液中溶质离子浓度一定相等,且保持不变(×)
(2)升高温度,沉淀溶解平衡一定正向移动(×)
(3)室温下,AgCl在水中的溶解度小于在食盐水中的溶解度(×)
(4)BaSO 在同物质的量浓度的Na SO 溶液和Al (SO ) 溶液中的溶解度相同(×)
4 2 4 2 4 3
(5)为减少洗涤过程中固体的损耗,最好选用稀H SO 代替H O来洗涤BaSO 沉淀
2 4 2 4
(√)
2.(教材改编题)(RJ选修4·P 2改编)下列叙述中正确的是( )
67A.升高温度,沉淀溶解平衡都是向促进沉淀溶解的方向移动
B.绝对不溶解的物质是不存在的
C.难溶电解质在水溶液中达到沉淀溶解平衡时,沉淀和溶解即停止
D.BaSO (s) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT SO(aq)+
4
Ba2 + (aq) 表 示 溶 解 平 衡 ; H O + HSO INCLUDEPICTURE "KN.TIF" \*
2
MERGEFORMAT SO+H O+表示水解平衡
3
答案 B
3.(规范答题专练)试用平衡移动原理解释下列事实:
(1)BaCO 不溶于水,为什么不能作钡餐?
3
_____________________________________________________________________
。
(2)CaCO 难溶于稀H SO ,却能溶于醋酸中;
3 2 4
_____________________________________________________________________
。
(3)分别用等体积的蒸馏水和 0.01 mol·L-1的盐酸洗涤AgCl沉淀,用水洗涤造成
AgCl的损失大于用稀盐酸洗涤的损失量。
____________________________________________________________________。
答案 (1)BaCO (s) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
3
Ba2+(aq)+CO(aq),HCl===H++Cl-,2H++CO===H O+CO ↑,盐酸电离的H+
2 2
与BaCO 产生的CO结合生成CO 和H O,破坏了BaCO 的溶解平衡,c(Ba2+)增
3 2 2 3
大,引起人体中毒
(2)CaCO (s) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT Ca2+(aq)
3
+CO(aq),H SO ===SO+2H+,Ca2++SO===CaSO ↓,因为生成的CaSO 溶解度
2 4 4 4
较小,会附着在CaCO 的表面,阻止平衡右移。而CH COOH INCLUDEPICTURE
3 3
"KN.TIF" \* MERGEFORMAT CH COO-+H+,Ca2+与CH COO-不产生
3 3
沉淀;当H+与CO结合生成CO 和H O时,CaCO 的溶解平衡右移
2 2 3(3)用水洗涤 AgCl,AgCl(s) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
Ag+(aq)+Cl-(aq)平衡右移,AgCl的质量减少,用盐酸洗涤AgCl,稀释的
同时HCl电离产生的Cl-会使平衡左移,AgCl减少的质量要小些。
INCLUDEPICTURE "题组诊断.tif" \* MERGEFORMAT INCLUDEPICTURE
" 题 组 诊 断 .tif" \* MERGEFORMAT
[A组 基础知识巩固]
1.已知溶液中存在平衡:
Ca(OH) (s) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT Ca2+(aq)+
2
2OH-(aq) ΔH<0,下列有关该平衡体系的说法正确的是( )
①升高温度,平衡逆向移动
②向溶液中加入少量碳酸钠粉末能增大钙离子的浓度
③除去氯化钠溶液中混有的少量钙离子,可以向溶液中加入适量的NaOH溶液
④恒温下向溶液中加入CaO,溶液的pH升高
⑤给溶液加热,溶液的pH升高
⑥向溶液中加入Na CO 溶液,其中固体质量增加
2 3
⑦向溶液中加入少量NaOH固体,Ca(OH) 固体质量不变
2
A.①⑥ B.①⑥⑦
C.②③④⑥ D.①②⑥⑦
解析 加入碳酸钠粉末会生成CaCO ,使Ca2+浓度减小,②错;加入氢氧化钠溶液
3
会使平衡左移,有Ca(OH) 沉淀生成,但Ca(OH) 的溶度积较大,要除去Ca2+,应
2 2
把Ca2+转化为更难溶的CaCO ,③错;恒温下K 不变,加入CaO后,溶液仍为
3 sp
Ca(OH) 的饱和溶液,pH不变,④错;加热,Ca(OH) 的溶解度减小,溶液的pH降
2 2
低,⑤错;加入Na CO 溶液,沉淀溶解平衡向右移动,Ca(OH) 固体转化为CaCO
2 3 2 3
固体,固体质量增加,⑥正确;加入NaOH固体平衡向左移动,Ca(OH) 固体质量增
2
加,⑦错。
答案 A2.下列化学原理的应用,主要用沉淀溶解平衡原理来解释的是( )
①热纯碱溶液去油污能力强 ②误将钡盐[BaCl 、Ba(NO ) ]当作食盐混用后,常用
2 3 2
0.5%的Na SO 溶液解毒 ③溶洞、珊瑚的形成 ④碳酸钡不能作“钡餐”而硫酸
2 4
钡则能 ⑤泡沫灭火器灭火的原理
A.②③④ B.①②③
C.③④⑤ D.①②③④⑤
解析 ①⑤是水解平衡原理。
答案 A
3.(2018·北京西城区期中)为研究沉淀的生成及其转化,某小组进行如下实验。关
于该实验的分析不正确的是( )
INCLUDEPICTURE "10X643.TIF" \* MERGEFORMAT
A.① 浊 液 中 存 在 平 衡 : AgSCN(s) INCLUDEPICTURE "KN.TIF" \*
MERGEFORMAT Ag+(aq)+SCN-(aq)
B.②中颜色变化说明上层清液中含有SCN-
C.③中颜色变化说明有AgI生成
D.该实验可以证明AgI比AgSCN更难溶
解析 0.01 mol·L-1 AgNO 溶液中加入0.005 mol·L-1 KSCN溶液,产生白色沉淀
3
AgSCN,该沉淀在溶液中存在溶解平衡:AgSCN(s) INCLUDEPICTURE "KN.TIF"
\* MERGEFORMAT Ag+(aq)+SCN-(aq),A正确;取①上层清液加入2mol·L-1 Fe(NO ) 溶液,溶液变成红色,说明有Fe(SCN) 生成,从而推知上层清液
3 3 3
中含有SCN-,B正确;①中余下浊液中加入2 mol·L-1KI 溶液,产生黄色沉淀,该
沉淀应为AgI,C正确;①中反应后AgNO 溶液有剩余,则余下浊液中除含有
3
AgSCN外,还有AgNO ,再加入2 mL 2 mol·L-1 KI溶液生成AgI沉淀,不能说明
3
AgSCN转化为AgI,故不能证明AgI比AgSCN更难溶,D错误。
答案 D
【归纳总结】
沉淀生成的两大应用
(1)分离离子:同一类型的难溶电解质,如AgCl、AgBr、AgI,溶度积小的物质先析
出,溶度积大的物质后析出。
(2)控制溶液的pH来分离物质,如除去MgCl 中的FeCl 就可向溶液中加入MgO
2 3
或Mg(OH) 等物质,将Fe3+转化为Fe(OH) 而除去。
2 3
[B组 考试能力过关]
4.下列说法正确的是( )
A.(2018·全国卷Ⅱ) 碳酸钡可用于胃肠X射线造影检查
B.(天津卷)在同浓度的盐酸中,ZnS可溶而CuS不溶,说明CuS的溶解度比ZnS的
小
C.(天津卷)含有AgCl和AgI固体的悬浊液:c(Ag+)>c(Cl-)=c(I-)
D.(浙江卷)相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、
②0.1 mol/L盐酸、③0.1 mol/L氯化镁溶液、④0.1 mol/L硝酸银溶液中,Ag+浓度:
①>④=②>③
答案 B
5.(2016·海南化学,5)向含有MgCO 固体的溶液中滴加少许浓盐酸(忽略体积变
3
化),下列数值变小的是( )
A.c(CO) B.c(Mg2+)
C.c(H+) D.K (MgCO )
sp 3
解 析 含 有 MgCO 固 体 的 溶 液 中 存 在 沉 淀 溶 解 平 衡 : MgCO (s)
3 3
INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT Mg2+(aq)+CO(aq),滴
加少许浓盐酸可与CO反应,促使平衡向右移动,则c(Mg2+)和c(H+)增大,c(CO)减小;温度不变,K (MgCO )不变,故A正确。
sp 3
答案 A
考点二 沉淀溶解平衡常数及其应用
(频数:★★★ 难度:★★★)
INCLUDEPICTURE "名师课堂.tif" \* MERGEFORMAT INCLUDEPICTURE
" 名 师 课 堂 .tif" \* MERGEFORMAT
INCLUDEPICTURE " 书名号 .TIF " \* MERGEFORMAT INCLUDEPICTURE
" 书名号 .TIF" \* MERGEFORMAT 名师课堂导语 溶度积常数属于常考点,一
方面考查对溶度积曲线的理解;另一方面考查有关溶度积的计算;另外借助溶度
积分析沉淀溶解平衡移动,及沉淀生成、溶解和转化问题在考题中也经常涉及。
1.溶度积和离子积
以A B (s) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT mAn+(aq)+
m n
nBm-(aq)为例:
溶度积 离子积
概念 沉淀溶解的平衡常数 溶液中有关离子浓度幂的乘积
符号 K Q
sp c
K (A B )= c m (A n + )· c n (B m - ) , Q (A B )= c m (A n + )· c n (B m - ) ,式中
表达式 sp m n c m n
式中的浓度都是平衡浓度 的浓度都是任意浓度
判断在一定条件下沉淀能否生成或溶解
①Q >K :溶液过饱和,有沉淀析出
c sp
应用
②Q =K :溶液饱和,处于平衡状态
c sp
③Q <K :溶液未饱和,无沉淀析出
c sp
2.K 的影响因素
sp
(1)内因:难溶物质本身的性质,这是主要决定因素。
(2)外因
①浓度:加水稀释,平衡向溶解方向移动,但K 不变。
sp
②温度:绝大多数难溶盐的溶解是吸热过程,升高温度,平衡向溶解方向移动,K
sp增大。
③其他:向平衡体系中加入可与体系中某些离子反应生成更难溶物质或更难电离
物质或气体的离子时,平衡向溶解方向移动,但K 不变。
sp
INCLUDEPICTURE " 名 师 课 堂 实 录 .tif" \* MERGEFORMAT
INCLUDEPICTURE "名师课堂实录.tif" \* MERGEFORMAT
(1)溶解平衡一般是吸热的,温度升高平衡右移,K 增大,但Ca(OH) 相反。
sp 2
(2)对于沉淀溶解平衡:A B (s) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
m n
mAn+(aq)+nBm-(aq),K =cm(An+)·cn(Bm-),对于相同类型的物质,K 的大
sp sp
小反映了难溶电解质在溶液中溶解能力的大小,也反映了该物质在溶液中沉淀的
难易。
3.有关 K 的相关计算
sp
(1)已知溶度积求溶液中的某种离子的浓度,如 K =a的饱和AgCl溶液中c(Ag+)
sp
=__ mol·L - 1 。
(2)已知溶度积、溶液中某离子的浓度,求溶液中的另一种离子的浓度,如某温度下
AgCl的K =a,在0.1 mol·L-1的NaCl溶液中加入过量的AgCl固体,达到平衡后
sp
c(Ag+)= 10 a __ mol·L - 1 。
(3)计算反应的平衡常数,如对于反应 Cu2+(aq)+MnS(s) INCLUDEPICTURE
"KN.TIF" \* MERGEFORMAT CuS(s)+Mn2+(aq),K (MnS)=c(Mn2+)·c(S2
sp
-),K (CuS)=c(Cu2+)·c(S2-)。而平衡常数K==。
sp
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)K 既与难溶电解质的性质和温度有关,也与沉淀的量和溶液中离子浓度有关
sp
(×)
(2)在一定条件下,溶解度较小的沉淀也可以转化成溶解度较大的沉淀(√)
(3)常温下,向BaCO 饱和溶液中加入Na CO 固体,BaCO 的K 减小(×)
3 2 3 3 sp
(4)溶度积常数K 只受温度的影响,温度升高K 增大(×)
sp sp
(5)常温下,向Mg(OH) 饱和溶液中加入NaOH固体,Mg(OH) 的K 不变(√)
2 2 sp(6)K (AB )小于K (CD),则AB 的溶解度小于CD的溶解度(×)
sp 2 sp 2
2.(识图能力专练)不同温度下(T 、T ),CaCO 在水中的沉淀溶解平衡曲线如图所示,
1 2 3
回答下列问题(注:CaCO 均未完全溶解)。
3
INCLUDEPICTURE "10X644.TIF" \* MERGEFORMAT
(1)T ________(填“>”“<”或“=”)T 。
1 2
(2)保持T 不变,怎样使A点变成B点?
1
(3)在B点,若温度从T 升到T ,则B点变到________点(填“C”“D”或“E”)。
1 2
答案 (1)<
(2)保持T 不变,向悬浊液中加入Na CO 固体。
1 2 3
(3)D INCLUDEPICTURE " 题 组 诊 断 .tif" \* MERGEFORMAT
INCLUDEPICTURE " 题 组 诊 断 .tif" \* MERGEFORMAT
[A组 基础知识巩固]
1.可溶性钡盐有毒,医院中常用硫酸钡这种钡盐作为内服造影剂。医院抢救钡离子
中毒患者时,除催吐外,还需要向中毒者胃中灌入硫酸钠溶液。已知:某温度下,
K (BaCO )=5.1×10-9 mol2·L-2;K (BaSO )=1.1×10-10 mol2·L-2。下列推断正确
sp 3 sp 4
的是( )
A.不用碳酸钡作为内服造影剂,是因为K (BaCO )>K (BaSO )
sp 3 sp 4
B.抢救钡离子中毒患者时,若没有硫酸钠,可以用碳酸钠溶液代替
C.若误饮c(Ba2+)=1.0×10-5mol·L-1的溶液时,会引起钡离子中毒
D.可以用0.36 mol·L-1的Na SO 溶液给钡离子中毒患者洗胃
2 4
解析 因胃酸可与CO反应生成水和二氧化碳,使 CO浓度降低,从而使平衡
BaCO (s) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT Ba2+(aq)+
3
CO(aq)向溶解方向移动,使Ba2+浓度增大,Ba2+有毒,与K 大小无关,故A错误;
sp
BaCO 溶于胃酸,起不到解毒的作用,故B错误;c(Ba2+)=1.0×10-5 mol·L-1的溶
3液钡离子浓度很小,不会引起钡离子中毒,故C错误;用0.36 mol·L-1的Na SO 溶
2 4
液给钡离子中毒患者洗胃,反应后
c(Ba2+)= mol·L-1,浓度很小,可起到解毒的作用,故D正确。
答案 D
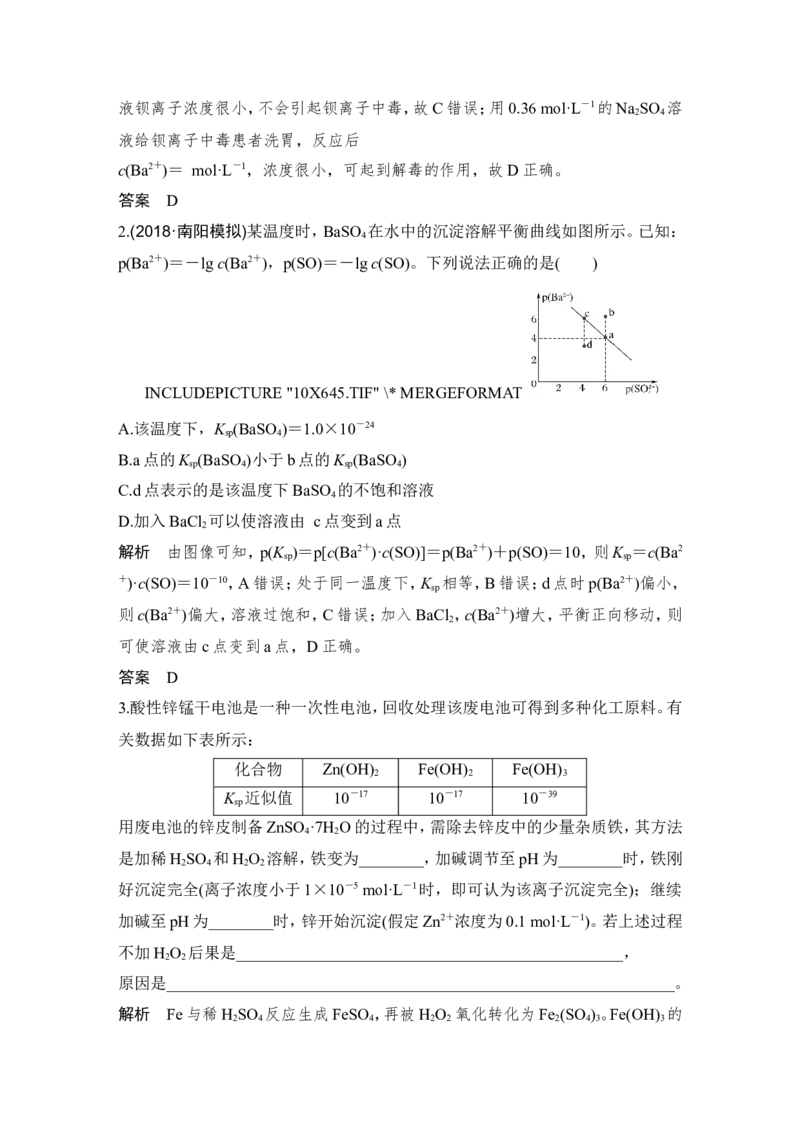
2.(2018·南阳模拟)某温度时,BaSO 在水中的沉淀溶解平衡曲线如图所示。已知:
4
p(Ba2+)=-lg c(Ba2+),p(SO)=-lg c(SO)。下列说法正确的是( )
INCLUDEPICTURE "10X645.TIF" \* MERGEFORMAT
A.该温度下,K (BaSO )=1.0×10-24
sp 4
B.a点的K (BaSO )小于b点的K (BaSO )
sp 4 sp 4
C.d点表示的是该温度下BaSO 的不饱和溶液
4
D.加入BaCl 可以使溶液由 c点变到a点
2
解析 由图像可知,p(K )=p[c(Ba2+)·c(SO)]=p(Ba2+)+p(SO)=10,则K =c(Ba2
sp sp
+)·c(SO)=10-10,A错误;处于同一温度下,K 相等,B错误;d点时p(Ba2+)偏小,
sp
则c(Ba2+)偏大,溶液过饱和,C错误;加入BaCl ,c(Ba2+)增大,平衡正向移动,则
2
可使溶液由c点变到a点,D正确。
答案 D
3.酸性锌锰干电池是一种一次性电池,回收处理该废电池可得到多种化工原料。有
关数据如下表所示:
化合物 Zn(OH) Fe(OH) Fe(OH)
2 2 3
K 近似值 10-17 10-17 10-39
sp
用废电池的锌皮制备ZnSO ·7H O的过程中,需除去锌皮中的少量杂质铁,其方法
4 2
是加稀H SO 和H O 溶解,铁变为________,加碱调节至pH为________时,铁刚
2 4 2 2
好沉淀完全(离子浓度小于1×10-5 mol·L-1时,即可认为该离子沉淀完全);继续
加碱至pH为________时,锌开始沉淀(假定Zn2+浓度为0.1 mol·L-1)。若上述过程
不加H O 后果是________________________________________________,
2 2
原因是_______________________________________________________________。
解析 Fe与稀H SO 反应生成FeSO ,再被H O 氧化转化为Fe (SO ) 。Fe(OH) 的
2 4 4 2 2 2 4 3 3K =c(Fe3+)·c3 (OH-),则Fe3+恰好沉淀完全时,c(OH-)=≈10-11.3 mol·L-1,则溶
sp
液的pH=2.7。Zn(OH) 的K =c(Zn2+)·c2(OH-),则Zn2+开始沉淀时,c(OH-)==
2 sp
10-8 mol·L-1,溶液的pH=6。Fe(OH) 和Zn(OH) 的K 相近,不加入H O 将Fe2+
2 2 sp 2 2
转化为Fe3+,很难将Zn2+和Fe2+分开。
答案 Fe3+ 2.7 6 Zn2+和Fe2+分离不开 Fe(OH) 和Zn(OH) 的K 相近
2 2 sp
【方法规律】
解沉淀溶解平衡图像题三步骤
第一步:明确图像中纵、横坐标的含义
纵、横坐标通常是难溶物溶解后电离出的离子浓度。
第二步:理解图像中线上点、线外点的含义
INCLUDEPICTURE "10X646.TIF" \* MERGEFORMAT
(1)以氯化银为例,在该沉淀溶解平衡图像上,曲线上任意一点都达到了沉淀溶解
平衡状态,此时Q =K 。在温度不变时,无论改变哪种离子的浓度,另一种离子的
c sp
浓度只能在曲线上变化,不会出现在曲线以外。
(2)曲线上方区域的点均为过饱和溶液,此时Q >K 。
c sp
(3)曲线下方区域的点均为不饱和溶液,此时Q <K 。
c sp
第三步:抓住K 的特点,结合选项分析判断
sp
(1)溶液在蒸发时,离子浓度的变化分两种情况:
①原溶液不饱和时,离子浓度都增大;
②原溶液饱和时,离子浓度都不变。
(2)溶度积常数只是温度的函数,与溶液中溶质的离子浓度无关,在同一曲线上的
点,溶度积常数相同。
[B组 考试能力过关]
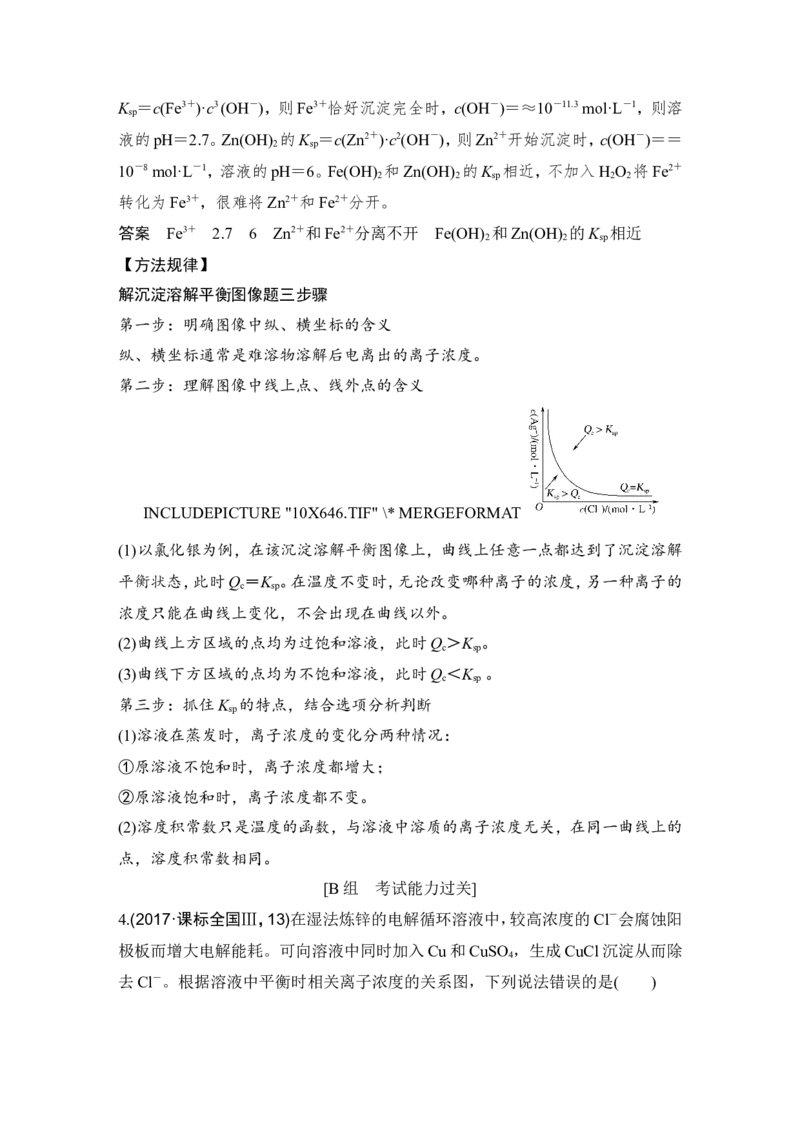
4.(2017·课标全国Ⅲ,13)在湿法炼锌的电解循环溶液中,较高浓度的Cl-会腐蚀阳
极板而增大电解能耗。可向溶液中同时加入Cu和CuSO ,生成CuCl沉淀从而除
4
去Cl-。根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是( )INCLUDEPICTURE "17GH18.tif" \* MERGEFORMAT
A.K (CuCl)的数量级为10-7
sp
B.除Cl-反应为Cu+Cu2++2Cl-===2CuCl
C.加入Cu越多,Cu+浓度越高,除Cl-效果越好
D.2Cu+=== Cu2++Cu平衡常数很大,反应趋于完全
解析 A 项,根据 CuCl(s) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
Cu+(aq)+Cl-(aq)可知K (CuCl)=c(Cu+)·c(Cl-),从Cu+图像中任取一点
sp
代入计算可得K (CuCl)≈10-7,正确;B项,由题干中“可向溶液中同时加入Cu
sp
和CuSO ,生成CuCl沉淀从而除去Cl-”可知Cu、Cu2+与Cl― 可以发生反应生成
4
CuCl 沉淀,正确;C 项,Cu(s)+Cu2+(aq) INCLUDEPICTURE "KN.TIF" \*
MERGEFORMAT 2Cu+(aq),固体对平衡无影响,故增加固体Cu的物质的
量,平衡不移动,Cu+的浓度不变,错误;D项,2Cu+(aq) INCLUDEPICTURE
"KN.TIF" \* MERGEFORMAT Cu(s)+Cu2+(aq),反应的平衡常数K=,从
图中两条曲线上任取横坐标相同的c(Cu2+)、c(Cu+)两点代入计算可得K≈106,反
应平衡常数较大,反应趋于完全,正确。
答案 C
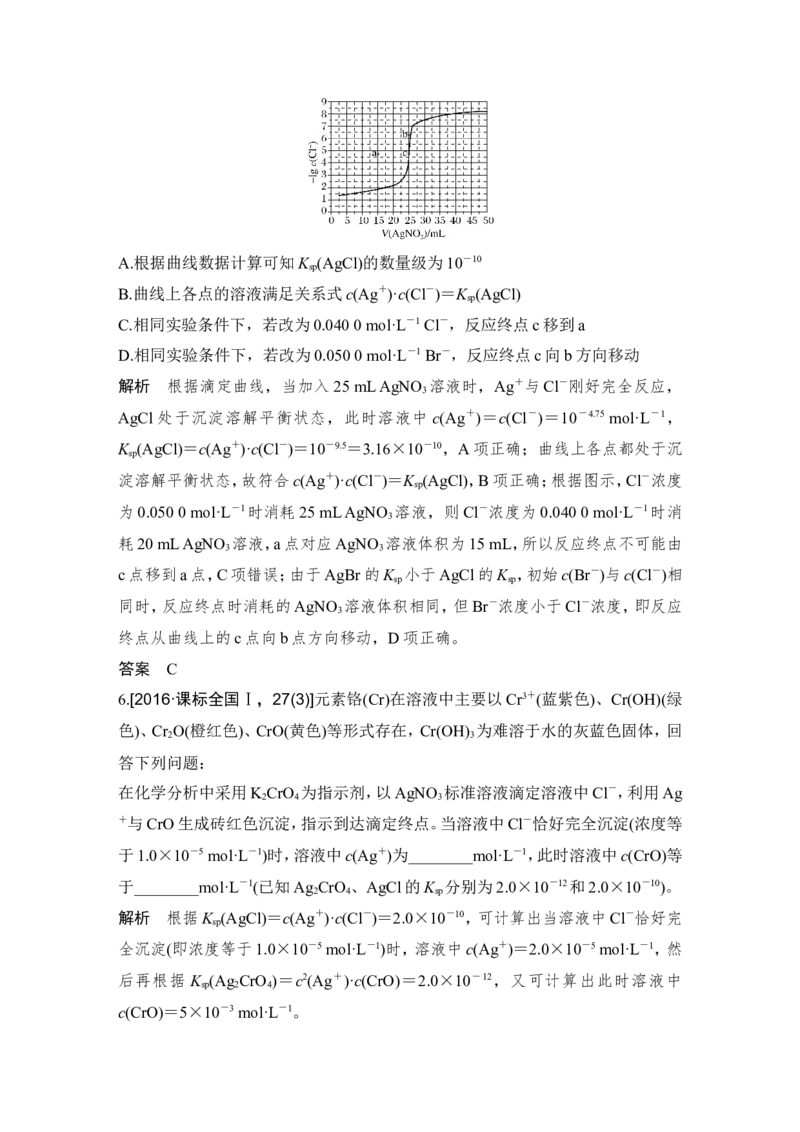
5.(2018·课标全国Ⅲ,12)用0.100 mol·L-1 AgNO 滴定50.0 mL 0.050 0 mol·L-1 Cl
3
-溶液的滴定曲线如图所示。下列有关描述错误的是( )
INCLUDEPICTURE "18GK20.TIF" \* MERGEFORMATA.根据曲线数据计算可知K (AgCl)的数量级为10-10
sp
B.曲线上各点的溶液满足关系式c(Ag+)·c(Cl-)=K (AgCl)
sp
C.相同实验条件下,若改为0.040 0 mol·L-1 Cl-,反应终点c移到a
D.相同实验条件下,若改为0.050 0 mol·L-1 Br-,反应终点c向b方向移动
解析 根据滴定曲线,当加入25 mL AgNO 溶液时,Ag+与Cl-刚好完全反应,
3
AgCl 处于沉淀溶解平衡状态,此时溶液中 c(Ag+)=c(Cl-)=10-4.75 mol·L-1,
K (AgCl)=c(Ag+)·c(Cl-)=10-9.5=3.16×10-10,A项正确;曲线上各点都处于沉
sp
淀溶解平衡状态,故符合c(Ag+)·c(Cl-)=K (AgCl),B项正确;根据图示,Cl-浓度
sp
为0.050 0 mol·L-1时消耗25 mL AgNO 溶液,则Cl-浓度为0.040 0 mol·L-1时消
3
耗20 mL AgNO 溶液,a点对应AgNO 溶液体积为15 mL,所以反应终点不可能由
3 3
c点移到a点,C项错误;由于AgBr的K 小于AgCl的K ,初始c(Br-)与c(Cl-)相
sp sp
同时,反应终点时消耗的AgNO 溶液体积相同,但Br-浓度小于Cl-浓度,即反应
3
终点从曲线上的c点向b点方向移动,D项正确。
答案 C
6.[2016·课标全国Ⅰ,27(3)]元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)(绿
色)、Cr O(橙红色)、CrO(黄色)等形式存在,Cr(OH) 为难溶于水的灰蓝色固体,回
2 3
答下列问题:
在化学分析中采用K CrO 为指示剂,以AgNO 标准溶液滴定溶液中Cl-,利用Ag
2 4 3
+与CrO生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好完全沉淀(浓度等
于1.0×10-5 mol·L-1)时,溶液中c(Ag+)为________mol·L-1,此时溶液中c(CrO)等
于________mol·L-1(已知Ag CrO 、AgCl的K 分别为2.0×10-12和2.0×10-10)。
2 4 sp
解析 根据K (AgCl)=c(Ag+)·c(Cl-)=2.0×10-10,可计算出当溶液中Cl-恰好完
sp
全沉淀(即浓度等于1.0×10-5 mol·L-1)时,溶液中c(Ag+)=2.0×10-5 mol·L-1,然
后再根据 K (Ag CrO )=c2(Ag+)·c(CrO)=2.0×10-12,又可计算出此时溶液中
sp 2 4
c(CrO)=5×10-3 mol·L-1。答案 2.0×10-5 5×10-3
INCLUDEPICTURE "分层课时作业.TIF" \* MERGEFORMAT
INCLUDEPICTURE "分层课时作业.TIF" \* MERGEFORMAT
[A级 全员必做题]
1.在AgCl饱和溶液中尚有AgCl固体存在,当向溶液中加入0.1 mol/L的盐酸时,
下列说法正确的是( )
A.AgCl沉淀溶解平衡正向移动
B.AgCl溶解度增大
C.溶液中c(Ag+)增大
D.溶液中c(Cl-)增大
解析 AgCl饱和溶液中尚有AgCl固体存在,则溶液存在沉淀溶解平衡:AgCl(s)
INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT Ag+(aq)+Cl-(aq),当
向溶液中加入0.1 mol/L的盐酸时,c(Cl-)增大,平衡逆向移动,所以溶液中c(Ag+)
变小,AgCl溶解度减小。
答案 D
2.(2018·湖南怀化统一考试,17)往锅炉注入Na CO 溶液浸泡,将水垢中的CaSO
2 3 4
转化为CaCO ,再用盐酸去除,下列叙述中正确的是( )
3
A.温度升高,Na CO 溶液的K 和c(H+)均会增大
2 3 W
B.CaSO 能转化为CaCO ,说明K (CaCO )>K (CaSO )
4 3 sp 3 sp 4
C.CaCO 溶解于盐酸而CaSO 不溶,是因为硫酸酸性强于盐酸
3 4
D.沉淀转化的离子方程式为 CO(aq)+CaSO (s) INCLUDEPICTURE "KN.TIF" \*
4
MERGEFORMAT CaCO (s)+SO(aq)
3
解析 温度升高,水的电离平衡正向移动,K 增大;温度升高,Na CO 的水解平衡
W 2 3
正向移动,c(OH-)增大,c(H+)减小,A项错误。K (CaCO )13,D错误。
答案 D
8.常温时,Ca(OH) 和CaWO (钨酸钙)的沉淀溶解平衡曲线如图所示。下列分析不
2 4
正确的是( )
INCLUDEPICTURE "10X648.TIF" \* MERGEFORMATA.常温时K [Ca(OH) ]>K (CaWO )
sp 2 sp 4
B.a点表示无Ca(OH) 沉淀、有CaWO 沉淀
2 4
C.加热饱和Ca(OH) 溶液有白色沉淀生成
2
D.常温时这两种饱和溶液中c(Ca2+)相等
解析 Ca(OH) 沉淀溶解平衡曲线起点的定量信息是 c(Ca2+)=1.0×10-7mol/L、
2
c(OH-)=1.0 mol/L,K [Ca(OH) ]=c(Ca2+)·c2(OH-)=1.0×10-7,CaWO 的沉淀溶
sp 2 4
解平衡曲线起点的定量信息是 c(Ca2+)=1.0×10-7mol/L、c(WO)=1.0×10-
3mol/L , K (CaWO ) = c(Ca2 + )·c(WO) = 1.0×10 - 10<1.0×10 - 7 , 故
sp 4
K [Ca(OH) ]>K (CaWO ),A项正确。a点的定量信息是c(Ca2+)=1.0×10-4mol/L、
sp 2 sp 4
c(OH-)=1.0×10-3mol/L或c(WO)=1.0×10-3mol/L,Q [Ca(OH) ]=
c 2
c(Ca2+)·c2(OH-)=1.0×10-10K (CaWO ),有钨酸钙沉淀生成,B项正确。氢氧化钙
sp 4
的溶解度随温度升高而降低,故加热饱和Ca(OH) 溶液有白色氢氧化钙沉淀生成,
2
C项正确。设饱和氢氧化钙溶液中钙离子浓度为x mol/L,则氢氧根离子浓度为2x
mol/L,x×(2x)2=1.0×10-7,4x3=1.0×10-7,x=×10-3,饱和钨酸钙溶液中钙离子
浓度为y mol/L,钨酸根离子浓度也为y mol/L,则y2=1.0×10-10,y=1.0×10-5,
x>y,D项不正确。
答案 D
9.以硫铁矿为原料生产硫酸所得的酸性废水中砷元素含量极高,为控制砷的排放,
采用化学沉降法处理含砷废水,相关数据如下表,若混合溶液中Ca2+、Al3+、
Fe3+的浓度均为1.0×10-4mol·L-1,c(AsO)最大是( )
难溶物 K
sp
Ca (AsO ) 6.8×10-19
3 4 2
AlAsO 1.6×10-16
4
FeAsO 5.7×10-21
4
A.5.7×10-16 mol·L-1 B.8.2×10-3mol·L-1
C.1.6×10-12mol·L-1 D.5.7×10-17mol·L-1
解析 若混合溶液中Ca2+、Al3+、Fe3+的浓度均为1.0×10-4mol·L-1,依据表中难
溶物的 K 大小可知,反应过程中 Fe3+先形成沉淀,依据 K (FeAsO )=c(Fe3
sp sp 4
+)·c(AsO)=5.7×10-21可得,c(AsO)==5.7×10-17mol·L-1。答案 D
10.已知下列物质在20 ℃下的K 如下,试回答下列问题:
sp
化学式 AgCl AgBr AgI Ag S Ag CrO
2 2 4
颜色 白色 浅黄色 黄色 黑色 红色
K 2.0×10-10 5.4×10-13 8.3×10-17 2.0×10-48 2.0×10-12
sp
(1)20 ℃时,上述五种银盐饱和溶液中,Ag+物质的量浓度由大到小的顺序是
____________________________________________________________________。
(2)向BaCl 溶液中加入AgNO 和KBr,当两种沉淀共存时,=________。
2 3
(3)测定水体中氯化物的含量,常用标准硝酸银法进行滴定,滴定时,应加入的指示
剂是________。
A.KBr B.KI
C.K S D.K CrO
2 2 4
解析 (1)AgCl、AgBr、AgI均是AB型,c(Ag+)分别为×10-5mol·L-1≈1.4×
10-5mol·L-1、×10-7mol·L-1≈7.3×10-7mol·L-1、×10-9mol·L-1≈9.1×
10-9mol·L-1;后两种是A B型,c2(Ag+)·c(Ag+)=K ,则c(Ag+)=,Ag S、Ag CrO
2 sp 2 2 4
中c(Ag+)分别为1.59×10-16mol·L-1、1.59×10-4mol·L-1。故Ag+物质的量浓度由
大到小的顺序为Ag CrO >AgCl>AgBr>AgI>Ag S。
2 4 2
(2)出现共沉淀,此时必须同时发生两个平衡:
AgCl(s) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT Ag+(aq)+Cl-
(aq)
c(Ag+)·c(Cl-)=K (AgCl)=2.0×10-10①
sp
AgBr(s) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT Ag+(aq)+Br-
(aq)
c(Ag+)·c(Br-)=K (AgBr)=5.4×10-13②
sp
两者相比得:==2.7×10-3。
(3)由c(Ag+)大小知,饱和时只有Ag CrO 中的c(Ag+)比AgCl中的c(Ag+)大,在
2 4
AgCl沉淀完全后再产生Ag CrO 沉淀,其他均在AgCl之前沉淀,不能作指示剂,
2 4另外这里作指示剂时,生成的沉淀必须有颜色。
答案 (1)Ag CrO >AgCl>AgBr>AgI>Ag S
2 4 2
(2)2.7×10-3 (3)D
11.(1)已知常温时CuS的K =1.3×10-36,向100 mL 2×10-18 mol·L-1的K S溶液
sp 2
中加入100 mL 2×10-18 mol·L-1的CuCl 溶液,试通过计算说明有无CuS沉淀生
2
成 ( 写 出 计 算 推 理 过 程 , 忽 略 溶 液 混 合 时 的 体 积 变 化 ) :
_____________________________________________________________________
_____________________________________________________________________
。
(2)甲同学向某Na S样品(含Na CO 、Na SO 杂质)的溶液中加入少量BaCl 溶液,
2 2 3 2 4 2
产生白色沉淀,过滤,向滤渣中加入过量盐酸,沉淀完全溶解。
① 沉 淀 溶 于 盐 酸 的 离 子 方 程 式 是
_____________________________________________________________________
_____________________________________________________________________
。
②仅由上述实验无法判断 K (BaCO )与 K (BaSO )的大小关系,理由是
sp 3 sp 4
______________________________________________________________________
_____________________________________________________________________
。
(3)在0.10 mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜
沉淀生成,当溶液的pH=8时,c(Cu2+)=________mol·L-1{已知K [Cu(OH) ]=
sp 2
2.2×10-20} 。
解析 (2)①由题意知生成的含钡离子的沉淀可完全溶于稀盐酸,故应为BaCO 。
3
(3)K [Cu(OH) ]=c(Cu2+)×c2(OH-)=c(Cu2+)×(1×10-6)2=2.2×10-20,c(Cu2+)=
sp 2
2.2×10-8mol·L-1。
答案 (1)c(S2-)·c(Cu2+)=1×10-18×1×10-18=1×10-36<1.3×10-36,无CuS沉淀
生成
(2)①BaCO +2H+===Ba2++H O+CO ↑
3 2 2
②沉淀的形成除了与K 有关外,还与溶液中沉淀组分的离子浓度大小有关
sp
(3)2.2×10-8[B级 拔高选做题]
12.在一定温度下,AgCl与AgI的饱和溶液中存在如图所示关系,下列说法正确的
是( )
INCLUDEPICTURE "10X650.TIF" \* MERGEFORMAT
A.向0.1 mol/L KI溶液中加入AgNO 溶液,当I-恰好完全沉淀时,c(Ag+)=2×10
3
-12mol/L
B.向AgI的饱和溶液中加入HI溶液,可使溶液由A点移到B点
C.AgCl(s)+I-(aq) INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT
AgI(s)+Cl-(aq),在该温度下的平衡常数K=2.5×106
D.向2 mL 0.01 mol/L AgNO 溶液中加几滴0.01 mol/L NaCl溶液,静置片刻,再向
3
溶液中加几滴0.01 mol/L KI溶液,有黄色沉淀生成,说明K (AgCl)>K (AgI)
sp sp
解析 A 点对应的银离子浓度和碘离子浓度分别为 1×10-5mol/L 和 8×10-
12mol/L,K (AgI)=c(Ag+)·c(I-)=8×10-17,I-恰好完全沉淀时 c(I-)=1×10-5
sp
mol/L,此时c(Ag+)==8×10-12mol/L,A项错误。由于溶度积常数只随温度变化
而变化,所以当碘离子浓度增大时银离子浓度应减小,故不能由A点移到B点,B
项错误。K=====2.5×106,C项正确。向2 mL 0.01 mol/L AgNO 溶液中加几
3
滴0.01 mol/L NaCl溶液时,银离子过量,再向溶液中加几滴0.01 mol/L KI溶液,
有黄色沉淀生成,是因为过量的银离子与碘离子反应生成 AgI,不能据此说明
K (AgCl)>K (AgI),D项错误。
sp sp
答案 C
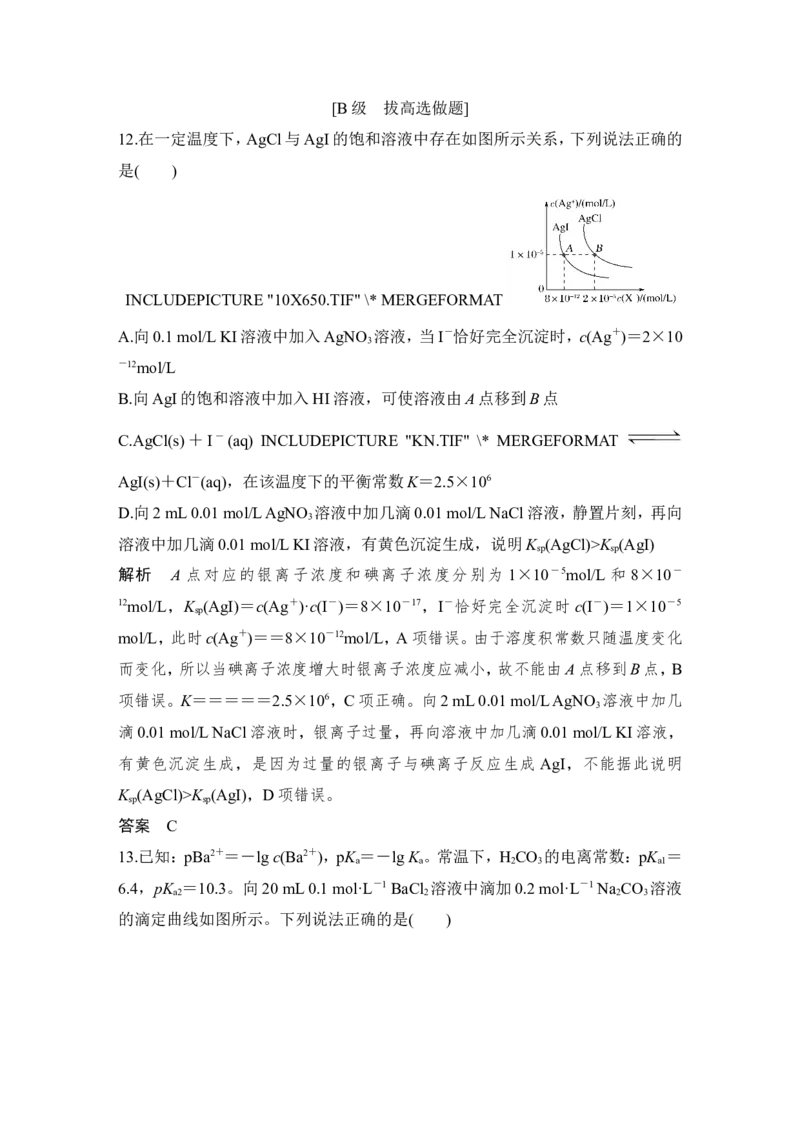
13.已知:pBa2+=-lg c(Ba2+),pK =-lg K 。常温下,H CO 的电离常数:pK =
a a 2 3 a1
6.4,pK =10.3。向20 mL 0.1 mol·L-1 BaCl 溶液中滴加0.2 mol·L-1 Na CO 溶液
a2 2 2 3
的滴定曲线如图所示。下列说法正确的是( )A.只有F点对应的溶液中存在BaCO 的沉淀溶解平衡
3
B.其他条件相同时,用MgCl 溶液替代BaCl 溶液,可使F点向G点迁移
2 2
C.常温下,K (BaCO )=1.0×10-9
sp 3
D.常温下,Na CO 溶液的pK =7.6
2 3 h1
解析 从一开始有碳酸钡生成,就有沉淀溶解平衡存在,A项错误;碳酸镁微溶于
水,碳酸钡难溶于水,若氯化镁溶液替代氯化钡溶液,恰好完全反应时,pMg2+减
小,F点向下方移动,B项错误;F点表示氯化钡溶液和碳酸钠溶液恰好完全反应
生成碳酸钡和氯化钠,c(Ba2+)=c(CO),K (BaCO )=1.0×10-9,C项正确;CO+
sp 3
H O INCLUDEPICTURE "KN.TIF" \* MERGEFORMAT HCO+OH-,K
2 h1
=,pK =14-10.3=3.7,D项错误。
h1
答案 C
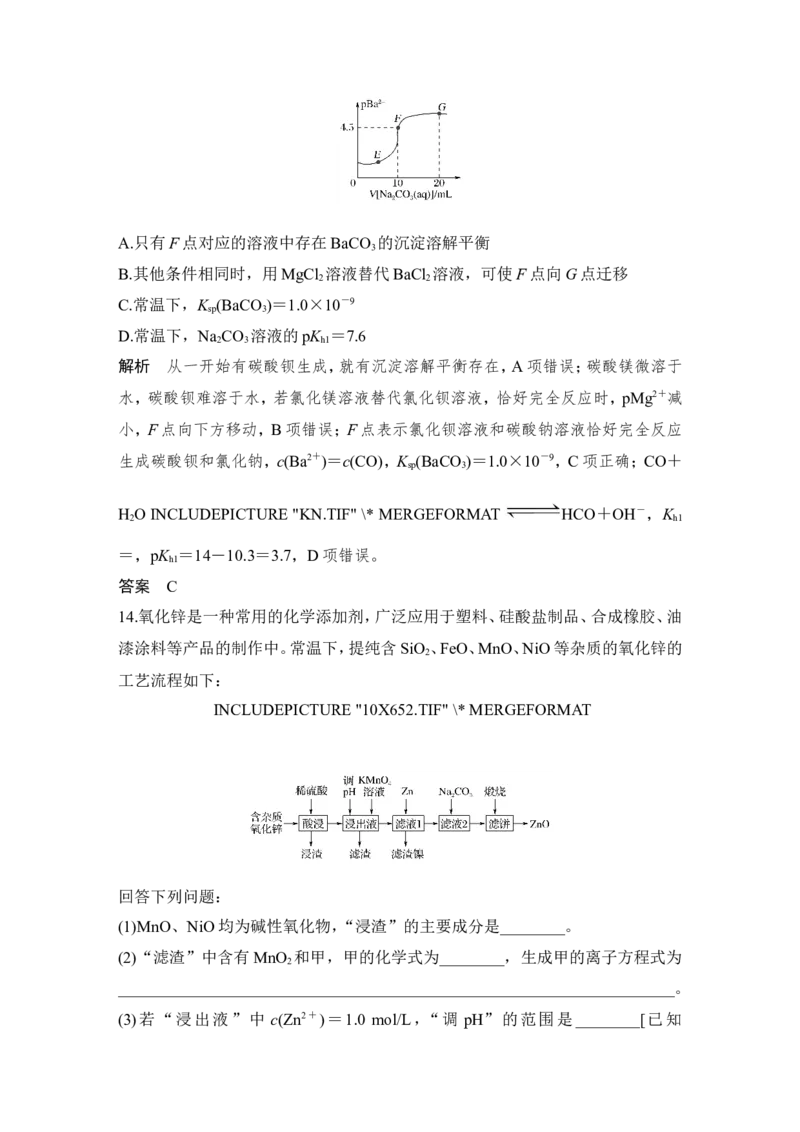
14.氧化锌是一种常用的化学添加剂,广泛应用于塑料、硅酸盐制品、合成橡胶、油
漆涂料等产品的制作中。常温下,提纯含SiO 、FeO、MnO、NiO等杂质的氧化锌的
2
工艺流程如下:
INCLUDEPICTURE "10X652.TIF" \* MERGEFORMAT
回答下列问题:
(1)MnO、NiO均为碱性氧化物,“浸渣”的主要成分是________。
(2)“滤渣”中含有MnO 和甲,甲的化学式为________,生成甲的离子方程式为
2
_____________________________________________________________________。
(3)若“浸出液”中 c(Zn2+)=1.0 mol/L,“调 pH”的范围是________[已知Fe(OH) 、Zn(OH) 、Ni(OH) 的K 分别为1.0×10-38、1.0×10-17、1.0×10-16]。在加
3 2 2 sp
高锰酸钾溶液前,若pH较低,对除杂的影响是________。
(4)加入锌的目的是________,Mn2+的还原性________Ni2+(填“强于”或“弱
于”),理由是______________________________________________________。
(5)若滤饼的成分为Zn(OH) ·ZnCO ,写出“滤液2”中加入Na CO 发生反应的化
2 3 2 3
学方程式:_________________________________________________________。
解析 (1)FeO、MnO和NiO均为碱性氧化物,可以溶于稀硫酸,不溶的是酸性氧
化物SiO ,故“浸渣”的主要成分是SiO 。(2)加入高锰酸钾是为了把杂质离子Fe2
2 2
+和Mn2+分别氧化成氢氧化铁和二氧化锰沉淀除去,信息中说明“滤渣”中含有
MnO ,暗示高锰酸根离子的还原产物为MnO ,根据得失电子守恒、电荷守恒及反
2 2
应溶液显酸性写出的离子方程式为MnO+3Fe2++7H O===3Fe(OH) ↓+MnO ↓
2 3 2
+5H+。(3)调pH是为了使氧化生成的Fe3+完全沉淀除去且Zn2+尚未沉淀,c(Fe3
+)<1.0×10-5mol/L 时 Fe3+完全沉淀:c(Fe3+)·c3(OH-)=1.0×10-38,c(OH
-)>1.0×10-11mol/L,c(H+)<1.0×10-3mol/L,pH>3;Zn2+尚未沉淀:c(Zn2+)·c2(OH
-)<1.0×10-17,将 c(Zn2+)=1.0 mol/L 代入得 c(OH-)<1.0×10-8.5mol/L,c(H
+)>1.0×10-5.5mol/L,pH<5.5;若pH较低,铁离子和锰离子不能生成沉淀,从而无
法除去铁和锰杂质。(4)由“提纯”知整个工艺流程要除去杂质“SiO 、FeO、
2
MnO、NiO等”,“酸浸”和“氧化”分别除去了SiO 和FeO、MnO,结合加锌后生
2
成“滤渣镍”知,加入锌的目的是将“滤液1”中的Ni2+置换还原除去;由于高锰
酸钾可以氧化“浸出液”中的Mn2+但不能氧化其中的Ni2+,所以Mn2+的还原性
强于Ni2+。(5)根据“滤饼的成分为Zn(OH) ·ZnCO ”可判断该反应为非氧化还原
2 3
反应,结合元素守恒推出有硫酸钠和二氧化碳生成:2ZnSO +2Na CO +
4 2 3
H O===Zn(OH) ·ZnCO ↓+2Na SO +CO ↑。
2 2 3 2 4 2
答案 (1)SiO (或二氧化硅) (2)Fe(OH) MnO+3Fe2++7H O===3Fe(OH) ↓+
2 3 2 3
MnO ↓+5H+
2
(3)3