文档内容
考点 17 原子结构和核外电子排布
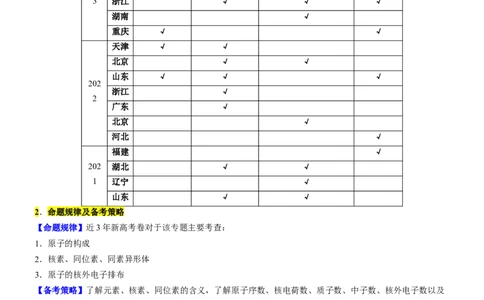
1.3年真题考点分布
年 考点分布
卷区
份 原子的构成 核素和同位素 原子的核外电子排布 综合应用
江苏 √
广东 √ √
202 湖南 √ √
3 浙江 √ √ √
湖南 √
重庆 √ √
天津 √ √
北京 √ √
山东 √ √ √
202
浙江 √
2
广东 √
北京 √
河北 √
福建 √
202 湖北 √ √
1 辽宁 √
山东 √ √
2.命题规律及备考策略
【命题规律】近3年新高考卷对于该专题主要考查:
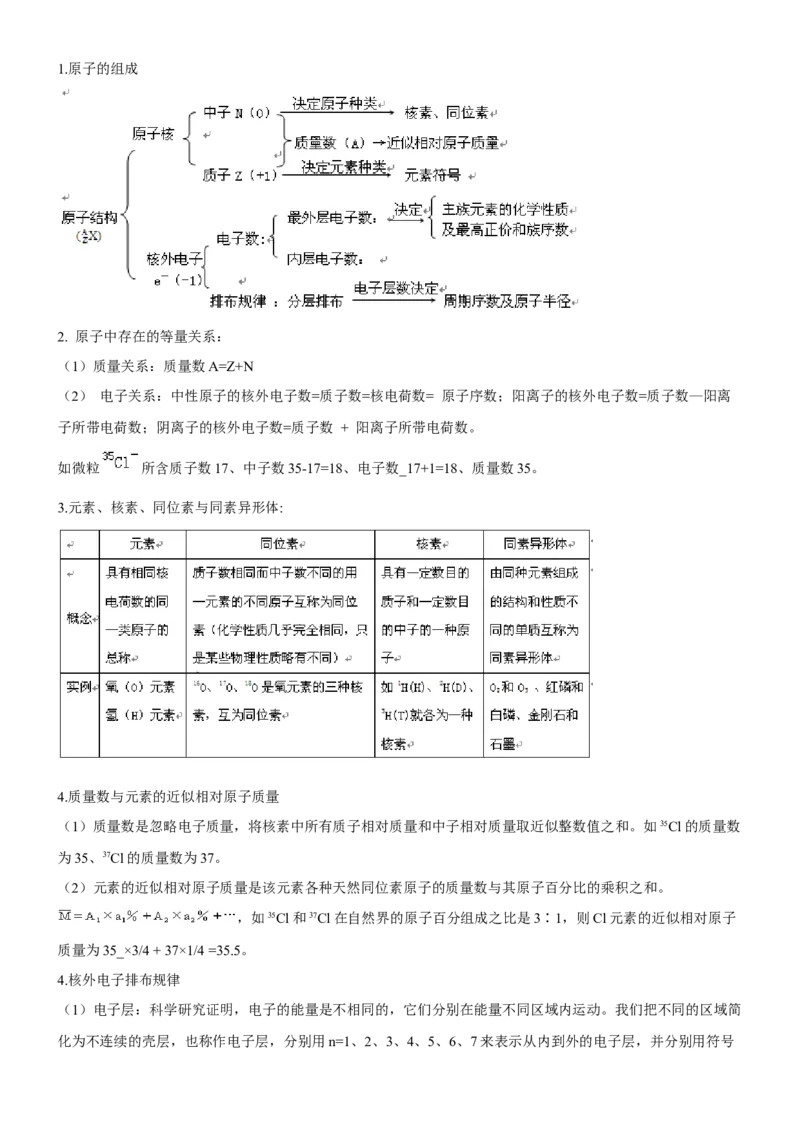
1.原子的构成
2.核素、同位素、同素异形体
3.原子的核外电子排布
【备考策略】了解元素、核素、同位素的含义,了解原子序数、核电荷数、质子数、中子数、核外电子数以及
它们之间的相互关系;原子的微观结构;能从能层、能级等不同层次认识原子的结构以及核外电子的排布规律,
能从宏观和微观相结合的视角分析原子结构与元素性质的关系。
【命题预测】原子结构与元素的性质是高中化学的基础,也是每年高考的热点,以高科技、新成果、诺贝尔奖等
为载体考查原子的各种量的关系考查原子结构,原子核外电子的能级分布及常见元素的基态原子或离子电子排
布式是必考知识点,常见题型为选择题和填空题,本部分考查内容的规律性强,命题空间广阔,考查方式会向
多方位、多层次发展。
考法 1 原子的构成1.原子的组成
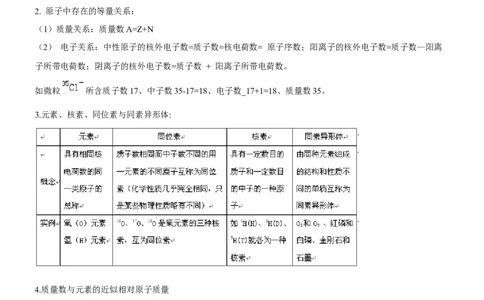
2. 原子中存在的等量关系:
(1)质量关系:质量数A=Z+N
(2) 电子关系:中性原子的核外电子数=质子数=核电荷数= 原子序数;阳离子的核外电子数=质子数—阳离
子所带电荷数;阴离子的核外电子数=质子数 + 阳离子所带电荷数。
如微粒 所含质子数17、中子数35-17=18、电子数_17+1=18、质量数35。
3.元素、核素、同位素与同素异形体:
4.质量数与元素的近似相对原子质量
(1)质量数是忽略电子质量,将核素中所有质子相对质量和中子相对质量取近似整数值之和。如35Cl的质量数
为35、37Cl的质量数为37。
(2)元素的近似相对原子质量是该元素各种天然同位素原子的质量数与其原子百分比的乘积之和。
,如35Cl和37Cl在自然界的原子百分组成之比是3∶1,则Cl元素的近似相对原子
质量为35_×3/4 + 37×1/4 =35.5。
4.核外电子排布规律
(1)电子层:科学研究证明,电子的能量是不相同的,它们分别在能量不同区域内运动。我们把不同的区域简
化为不连续的壳层,也称作电子层,分别用n=1、2、3、4、5、6、7来表示从内到外的电子层,并分别用符号K、L、M、N、O、P、Q来表示。
符号 K L M N O P Q
层数 1 2 3 4 5 6 7
(2)核外电子的排布规律:核外电子排布遵循的规律是能量最低原理,电子总是尽先占满能量低的电子层,然
后由里到外,依次排布在能量逐步升高的电子层上。
【典例1】(2023·上海中学高三月考)下列有关说法正确的是( )
A.煤油是可再生能源
B.H 燃烧过程中热能转化为化学能
2
C.火星陨石中的20Ne质量数为20
D.月壤中的3He与地球上的3H互为同位素
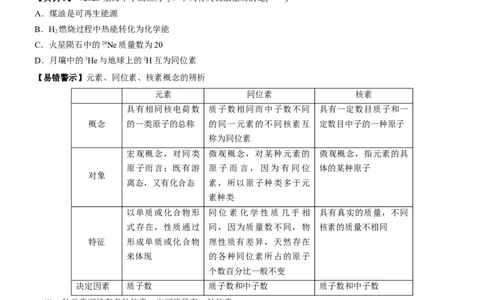
【易错警示】元素、同位素、核素概念的辨析
元素 同位素 核素
具有相同核电荷数 质子数相同而中子数不同 具有一定数目质子和一
概念 的一类原子的总称 的同一元素的不同核素互 定数目中子的一种原子
称为同位素
宏观概念,对同类 微观概念,对某种元素的 微观概念,指元素的具
原子而言;既有游 原子而言,因为有同位 体的某种原子
对象
离态,又有化合态 素,所以原子种类多于元
素种类
以单质或化合物形 同位素化学性质几乎相 具有真实的质量,不同
式存在,性质通过 同,因为质量数不同,物 核素的质量不相同
特征 形成单质或化合物 理性质有差异,天然存在
来体现 的各种同位素所占的原子
个数百分比一般不变
决定因素 质子数 质子数和中子数 质子数和中子数
(1)一种元素可能有多种核素,也可能只有一种核素;
(2)有多少种核素就有多少种原子;
(3)不同的核素可能具有相同的质子数,如H与H;也可能具有相同的中子数,如C与O;也可能具有相同的
质量数,如C与N;也可能质子数、中子数、质量数均不相同,如H与C;
(4)在区别同位素、同素异形体的概念时,可从概念的字面加深理解。同位素的研究对象是原子,“同位”是
指同一种元素的几种核素在元素周期表中的位置相同,即质子数相同,中子数不同;同素异形体的研究对象为
单质,“同素”是指元素种类相同。
【典例2】(2023·中山一中高三月考)1934年约里奥-居里夫妇在核反应中用α粒子(即氦核He)轰击金属原子
X,得到核素Y,开创了人造放射性核素的先河: X+He―→Y+n,其中元素X、Y的最外层电子数之和为8。下列叙述正确的是( )
A.X的相对原子质量为26
B.X、Y均可形成三氯化物
C.X的原子半径小于Y的
D.Y仅有一种含氧酸
1.(2023·浙江·校联考二模)门捷列夫曾预测镓、钪、锗元素的存在及性质,莫塞莱也曾预测一种“类锰”元
素。现该元素单质是从核燃料裂变产物中提取,它是与锰同为ⅦB族的放射线元素锝( ),其一种核素在临
床医学诊断中应用很广。下列有关推测不正确的是
A. 、 、 三种核素互为同位素,都是放射性元素
B.用于显像的 注射液是处方药,必须有许可证单位才能使用
C.用氘核轰击钼( )靶也能得到 ,此过程属于化学变化
D. 能与水反应,反应后溶液显酸性
2.(2023·河北·校联考一模)下列化学用语正确的是
A.四氯化碳分子的比例模型:
B. 分子中S原子的VSEPR模型:V形
C.次氯酸钠的电子式:
D.含有8个中子的碳原子可表示为:
3.(2023·黑龙江大庆·统考一模)我国科学家成功合成出新核素 ,熔合反应为
。下列叙述正确的是
A. 和 的物理性质完全相同
B.上述熔合反应为氧化还原反应
C.上述熔合反应中a=203、b=103
D. 核内中子数和质子数之差为47
考法 2 原子核外电子排布原理1. 能层和能级:在多电子原子中,电子的排布分成不同的能层,同一能层的电子能量也可能不同,还可以分成
不同的能级。
电子层(能层) 原子轨道类型(能级) 原子轨道数目 最多容纳电子数
K(1) 1s 1 2
L(2) 2s 2p 4 8
M(3) 3s 3p 3d 9 18
N (4) 4s 4p 4d 4f 16 32
O(5) 5s 5p 5d 5f 5g 25 50
……(n) n 2 2n 2
(1)任一能层,能级数等于能层序数;
(2)s、p、d、f……的轨道数依次是1、3、5、7……,s、p、d、f……可容纳的电子数依次是其轨道数1、
3、5、7……的两倍;
(3)各电子层最多容纳的电子数为2n2个。最外层最多容纳8个电子;次外层最多容纳18个(若此外层为1
或2,最多只能有2或8个电子);倒数第三层最多只有32个电子(若该层n=1,2,3,最多只能有2,8,18
个电子)
2. 原子轨道:不同能级上的电子出现概率约为90%的电子云空间轮廓图 称为原子轨道。
(1)s电子的原子轨道呈球形对称,ns能级各有1个原子轨道;p电子的原子轨道呈纺锤形,np能级各有3个
原子轨道,相互垂直(用p、p、p 表示);nd能级各有5个原子轨道;nf能级各有7个原子轨道。
x y z
(2)相同能层上原子轨道能量的高低:ns X >Q
C.气态氢化物分子的键角:Q>X>Y D.最高价氧化物对应的水化物的酸性:X>Q>M
【基础过关】
1.(2023·上海·统考模拟预测)2022年6月,由来自德国、日本、美国和中国等国的科学家组成的国际科研团
队在《自然》杂志发表论文证实“四中子态”物质的存在。该物质只由四个中子组成,则其质量数是
A.1 B.2 C.3 D.4
2.(2023·广东汕头·统考三模)氧族元素是人类生存的必需元素,下列有关氧族元素及其化合物说法错误的是
A.基的电子式: B.原子核内有46个中子数的硒原子:C. 的结构示意图: D. 的 模型:
3.(2022·广东江门·校考模拟预测)2022年2月27日,长征八号遥二运载火箭—“快八”在西昌卫星发射中
心成功将22颗卫星发射升空。液氢-液氧、煤油-液氧都是常用的火箭推进剂,下列说法错误的是
A.1H、2H、3H互为同位素 B.分离液态空气可获取液氧
C.氢能属于二次能源 D.煤的液化是生产煤油的主要方法
4.(2023·广东梅州·统考三模)下列化学用语的表示不正确的是
A.中子数为2的氢核素:
B. 的电子式:
C.基态铬原子的价电子排布式:
D. 的空间结构模型:
5.(2023·河北沧州·校考三模)现代宇宙学理论认为现今的宇宙起源于一次“大爆炸”,该过程中发生“碳燃
烧”形成了其他元素,可表示为 (γ为高能量光子), ,
,下列说法错误的是
A.a=24
B.Y的基态原子的电子排布式为
C. 是
D.金属性:XX
B.简单离子半径:X>Z>W
C.电负性:X>Y>Z
D.Z的最高价氧化物对应水化物的碱性大于W
7.(2023贺兰县景博中学高三月考)元素周期表前四周期A、B、C、D、E五种元素,A元素的原子最外层电
子排布式为ns1;B元素的原子价电子排布式为ns2np2;C元素位于第二周期且原子中p能级与s能级电子总数相
等;D元素原子的M能层的p能级中有3个未成对电子;E元素原子有5个未成对电子。
(1)写出元素名称:C___________;D___________;E___________。
(2)C基态原子的电子排布图为___________。(3)当n=2时,B的最简单气态氢化物的电子式为___________,BC 分子的结构式是___________;当n=3时,B
2
与C形成的化合物与氢氧化钠溶液反应的离子方程式是___________。
(4)若A元素的原子最外层电子排布式为2s1,B元素的原子价电子排布式为3s23p2,A、B、C、D四种元素的第
一电离能由大到小的顺序是___________。(用元素符号表示)
(5)E元素原子的价电子排布式是___________,在元素周期表中的位置是___________,其最高价氧化物的化学
式___________。
8.(2023定兴第三中学高三月考)X 、Y 、Z、 W 为元素周期表前四周期的元素,原子序数依次增大,X原
子核外有6种不同运动状态的电子,Y原子的基态时2p原子轨道上有3个未成对的电子;Z有多种氧化物,其
中一种红棕色氧化物可作涂料;W位于第四周期,其原子最外层只有1个电子,且内层都处于全充满状态。回
答下列问题
(1)X 在元素周期表中的位置是:___________;Y的最高价氧化物对应水化物与Y的最简单气态氢化物反应的
化学方程式:___________。
(2)X、Y最简单气态氢化物的稳定性:X ___________Y(填“大于”或“小于”)。
(3)Z原子核外电子排布式为:___________。
(4)W位于元素周期表的___________区,与W处于同一周期且最外层电子数相同的元素的基态原子共有
___________种、这些元素分别为___________(填元素符号)。
(5)在发生焰色反应时,W的4s电子会跃迁到4p轨道,写出此激发态W原子的价层电子排布式: ___________。
(6)与钛位于同一周期且含有相同未成对电子数的过渡元素为___________ (填元素符号)
(7)基态砷原子N电子层中的成对电子与单电子的数量比为___________。
【真题感知】
1.(2023·江苏·统考高考真题)氢元素及其化合物在自然界广泛存在且具有重要应用。 、 、 是氢元素
的3种核素,基态H原子 的核外电子排布,使得H既可以形成 又可以形成 ,还能形成 、 、
、 、 等重要化合物;水煤气法、电解水、光催化分解水都能获得 ,如水煤气法制氢反应中,
与足量 反应生成 和 吸收131.3kJ的热量。 在金属冶炼、新能源开发、碳
中和等方面具有重要应用,如 在催化剂作用下与 反应可得到 。我国科学家在氢气的制备和应用
等方面都取得了重大成果。下列说法正确的是
A. 、 、 都属于氢元素B. 和 的中心原子轨道杂化类型均为
C. 分子中的化学键均为极性共价键
D. 晶体中存在Ca与 之间的强烈相互作用
2.(2023·广东·统考高考真题)科教兴国,“可上九天揽月,可下五洋捉鳖”。下列说法正确的是
A.“天舟六号”为中国空间站送去推进剂 气, 是第 族元素
B.火星全球影像彩图显示了火星表土颜色,表土中赤铁矿主要成分为
C.创造了可控核聚变运行纪录的“人造太阳”,其原料中的 与 互为同位素
D.“深地一号”为进军万米深度提供核心装备,制造钻头用的金刚石为金属晶体
3.(2023·湖南·统考高考真题)下列化学用语表述错误的是
A.HClO的电子式:
B.中子数为10的氧原子: O
C.NH 分子的VSEPR模型:
3
D.基态N原子的价层电子排布图:
4.(2022·北京·高考真题) (锶)的 、 稳定同位素在同一地域土壤中 值不变。土壤生物中
值与土壤中 值有效相关。测定土壤生物中 值可进行产地溯源。下列说法不正确的
是
A. 位于元素周期表中第六周期、第ⅡA族
B.可用质谱法区分 和
C. 和 含有的中子数分别为49和48
D.同一地域产出的同种土壤生物中 值相同
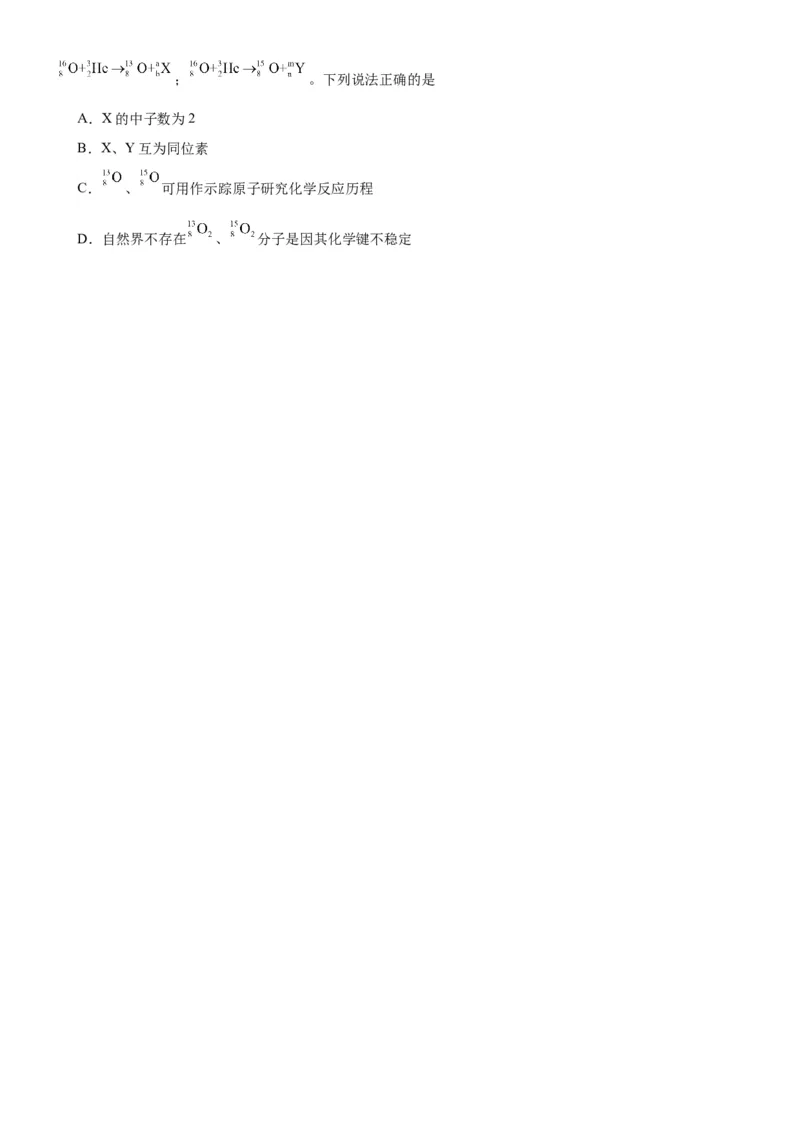
5.(2022·山东·高考真题) 、 的半衰期很短,自然界中不能稳定存在。人工合成反应如下:; 。下列说法正确的是
A.X的中子数为2
B.X、Y互为同位素
C. 、 可用作示踪原子研究化学反应历程
D.自然界不存在 、 分子是因其化学键不稳定