文档内容
考点 28 盐类的水解
高考中主要以盐类水解为载体考查溶液的酸碱性、溶液的pH计算及粒子浓度的大小比较等,通过图
像分析、反应条件控制等考查难溶电解质的溶解平衡,题型为选择题和非选择题。
预测2023年应重点关注水解平衡常数的计算、影响水解平衡的因素、电解质溶液中电荷守恒关系的应
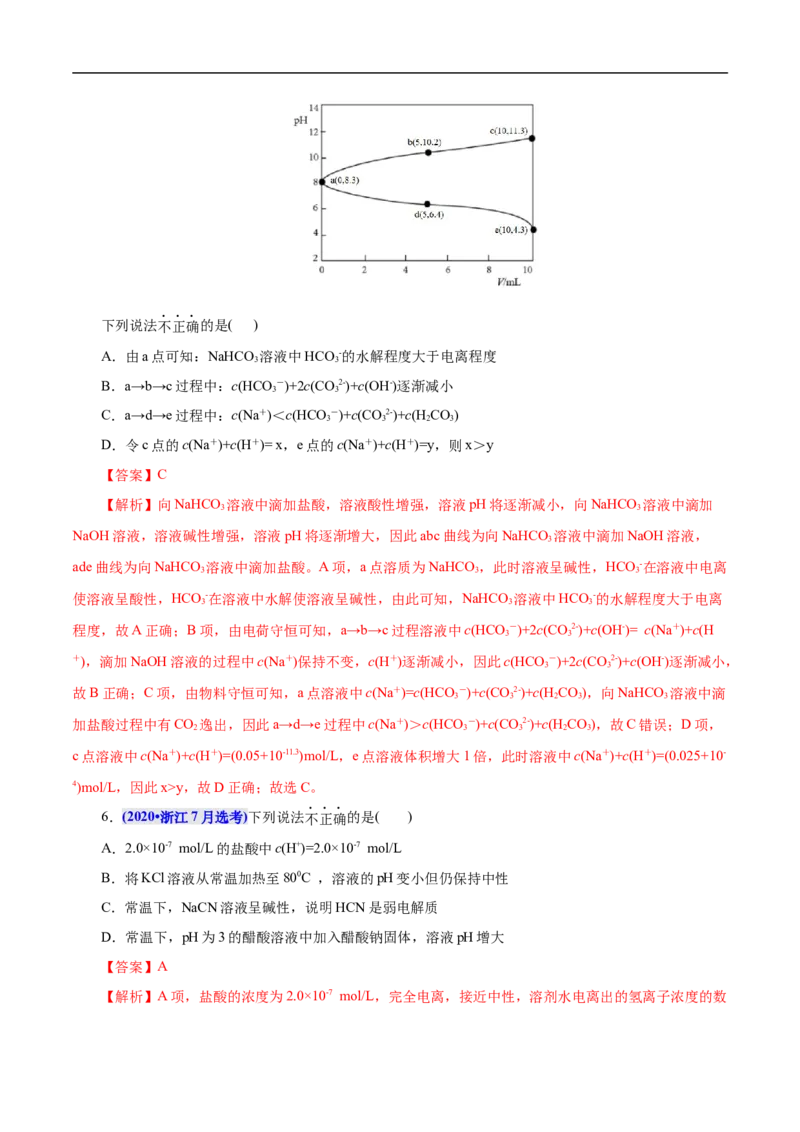
用;要加强数形结合题的训练力度,提高分析问题的能力,积极应对高考命题的灵活性与创新性。
一、盐类水解及规律
二、影响盐类水解的因素
三、盐类水解的应用
四、粒子”浓度关系的比较
盐类水解及规律
4..盐类水解离子方程式的书写要求(1)一般来说,盐类水解的程度不大,应该用可逆号“ ”表示。盐类水解一般不会产生沉淀和气
体,所以不用符号“↓”和“↑”表示水解产物。
(2)多元弱酸盐的水解是分步进行的,水解离子方程式要分步表示。
(3)多元弱碱阳离子的水解简化成一步完成。
(4)水解分别显酸性和碱性的离子组由于相互促进水解程度较大,书写时要用“===”“↑”“↓”等。
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)盐类水解的实质是促进水电离,水电离平衡右移( )
(2)酸式盐溶液可能呈酸性,也可能呈碱性( )
(3)某盐溶液呈酸性,该盐一定发生了水解反应( )
(4)离子能够发生水解的盐溶液一定呈酸性或碱性( )
(5)溶液呈中性的盐一定是强酸、强碱生成的盐( )
(6)常温下,pH=10的CHCOONa溶液与pH=4的NH Cl溶液,水的电离程度相同( )
3 4
(7)常温下,pH=11的CHCOONa溶液与pH=3的CHCOOH溶液,水的电离程度相同( )
3 3
(8)NaHCO 、NaHSO 都能促进水的电离( )
3 4
(9)向NaAlO 溶液中滴加NaHCO 溶液,有沉淀和气体生成( )
2 3
(10)Na CO 的水解:CO+2HO===H CO+2OH-( )
2 3 2 2 3
(11)FeCl 溶液与NaHCO 溶液混合:Fe3++3HCO===Fe(OH) ↓+3CO↑( )
3 3 3 2
(12)同浓度的NaCO 溶液和CHCOONa溶液相比前者pH大;同浓度的NaCO 和NaHCO 溶液相比后
2 3 3 2 3 3
者pH小( )
答案:(1)√ (2)√ (3)× (4)× (5)× (6)√ (7)× (8)× (9)× (10)× (11)√ (12)√
【典例】
例1
例2
例1 广义的水解观认为:无论是盐的水解还是非盐的水解,其最终结果是反应中各物质和水分别离
解成两部分,然后两两重新组合成新的物质。根据上述观点,下列说法不正确的是( )
A.BaO 的水解产物是Ba(OH) 和HO
2 2 2 2
B.PCl 的水解产物是HClO和HPO
3 3 4
C.Al C 的水解产物是Al(OH) 和CH
4 3 3 4
D.CHCOCl的水解产物是两种酸
3
【答案】B
【解析】BaO 的水解产物是Ba(OH) 和HO,该反应中没有元素化合价升降,符合水解原理,故A项
2 2 2 2正确;该反应中Cl元素的化合价由-1变为+1,有电子转移,不符合水解原理,故B项错误;Al C 水解
4 3
得到氢氧化铝和甲烷,符合水解原理,故 C项正确;CHCOCl的水解产物是两种酸,为CHCOOH和
3 3
HCl,符合水解原理,故D项正确。
例2 25 ℃时浓度都是1 mol·L-1的四种正盐溶液:AX、BX、AY、BY;AX的溶液pH=7且溶液中
c(X-)=1 mol·L-1,BX的溶液pH=4,BY的溶液pH=6。下列说法正确的是( )
A.电离平衡常数K(BOH)小于K(HY)
B.AY溶液的pH小于BY溶液的pH
C.稀释相同倍数,溶液pH变化BX等于BY
D.将浓度均为1 mol·L-1的HX和HY溶液分别稀释10倍后,HX溶液的pH大于HY
【答案】A
【解析】A项,根据BY溶液的pH=6,B+比Y-更易水解,则BOH比HY更难电离,因此电离平衡
常数K(BOH)小于K(HY);B项,根据AX、BX、BY溶液的pH,则AX为强酸强碱盐,BX为强酸弱碱盐,
BY为弱酸弱碱盐,则AY为弱酸强碱盐,溶液的pH>7,故AY溶液的pH大于BY溶液的pH;C项,稀
释相同倍数,BX、BY溶液的pH均增大,且BX溶液的pH变化大于BY溶液;D项,HX为强酸,HY为
弱酸,浓度相同时,稀释10倍后,HY的电离程度增大,但仍不可能全部电离,故HX溶液的酸性强,pH
小。
【对点提升】
对点1 NH Cl溶于重水(D O)后,产生的一水合氨和水合氢离子为( )
4 2
A.NH D·H O和DO+ B.NH ·D O和HD O+
2 2 3 3 2 2
C.NH ·HDO和DO+ D.NH D·HDO和HDO+
3 3 2 2
【答案】C
【解析】NH
Cl水解的实质是其电离出的NH+
与重水电离出的OD-结合生成一水合氨,即DO
4 4 2
D++OD-,NH+
+OD-→NH ·HDO,D+与DO结合生成DO+。
4 3 2 3
对点2 常温下,浓度均为0.1 mol·L-1的下列四种盐溶液,其pH测定如下表所示:
序号 ① ② ③ ④
溶液 CHCOONa NaHCO NaCO NaClO
3 3 2 3
pH 8.8 9.7 11.6 10.3
下列说法正确的是( )
A.四种溶液中,水的电离程度:①>②>④>③
B.NaCO 和NaHCO 溶液中,粒子种类相同
2 3 3C.将等浓度的CHCOOH和HClO溶液比较,pH小的是HClO
3
D.NaCO 溶液中,c(Na+)=c(CO)+c(HCO)+c(H CO)
2 3 2 3
【答案】B
【解析】A项,四种盐溶液均促进了水的电离,根据越弱越水解,水解显碱性,水解程度越大,pH越
大,则四种溶液中,水的电离程度:③>④>②>①,A错误;B项,NaCO 和NaHCO 溶液中都存在着
2 3 3
H+、OH-、CO、HCO、HCO 、Na+、HO,B正确;C项,醋酸的酸性强于次氯酸,在物质的量浓度相
2 3 2
等的情况下,pH小的是醋酸,C错误;D项,根据物料守恒,NaCO 溶液中,c(Na+)=2c(CO)+2c(HCO)
2 3
+2c(H CO),D错误。
2 3
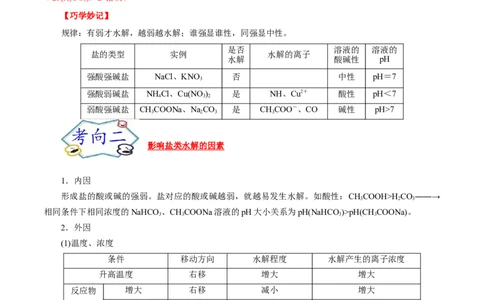
【巧学妙记】
规律:有弱才水解,越弱越水解;谁强显谁性,同强显中性。
是否 溶液的 溶液的
盐的类型 实例 水解的离子
水解 酸碱性 pH
强酸强碱盐 NaCl、KNO 否 中性 pH=7
3
强酸弱碱盐 NH Cl、Cu(NO ) 是 NH、Cu2+ 酸性 pH<7
4 3 2
弱酸强碱盐 CHCOONa、NaCO 是 CHCOO-、CO 碱性 pH>7
3 2 3 3
影响盐类水解的因素
1.内因
形成盐的酸或碱的强弱。盐对应的酸或碱越弱,就越易发生水解。如酸性:CHCOOH>H CO――→
3 2 3
相同条件下相同浓度的NaHCO 、CHCOONa溶液的pH大小关系为pH(NaHCO)>pH(CHCOONa)。
3 3 3 3
2.外因
(1)温度、浓度
条件 移动方向 水解程度 水解产生的离子浓度
升高温度 右移 增大 增大
反应物 增大 右移 减小 增大
浓度 减小(稀释) 右移 增大 减小
(2)外加物质:外加物质对水解反应的影响取决于该物质的性质。
①外加酸、碱
水解程度
外加物质
弱酸阴离子 弱碱阳离子
酸 增大 减小
碱 减小 增大
②外加能水解的盐【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)外界条件对盐水解程度的大小起决定作用( )
(2)影响盐类水解的因素有温度、浓度、压强等( )
(3)能水解的盐的浓度越低,水解程度越大,溶液的酸碱性越强( )
(4)盐溶液显酸碱性,一定是由水解引起的( )
(5)水解平衡右移,盐的离子的水解程度一定增大( )
(6)NaHCO 和NaHSO 都能促进水的电离( )
3 4
(7)水解反应NH+HO NH ·H O+H+达到平衡后,升高温度平衡逆向移动( )
2 3 2
(8)Na CO 溶液加水稀释,促进水的电离,溶液的碱性增强( )
2 3
(9)稀溶液中,盐的浓度越小,水解程度越大,其溶液酸性(或碱性)也越强( )
(10)在滴有酚酞的NaCO 溶液中慢慢滴入BaCl 溶液,溶液的红色逐渐退去( )
2 3 2
(11)pH相等的①NaHCO 、②NaCO、③NaOH溶液的物质的量浓度大小:①>②>③( )
3 2 3
(12)在NH Cl溶液中加入稀HNO,能抑制NH水解( )
4 3
(13)在CHCOONa溶液中加入冰醋酸,能抑制CHCOO-水解( )
3 3
答案:(1)× (2)× (3)× (4)× (5)× (6)× (7)√ (8)× (9)× (10)√ (11)√ (12)√
【典例】
例1 在一定条件下,NaCO 溶液存在水解平衡:CO+HO HCO+OH-。下列说法正确的是(
2 3 2
)
A.稀释溶液,水解平衡常数增大
B.通入CO,平衡向正反应方向移动
2
C.升高温度,减小
D.加入NaOH固体,溶液pH减小
【答案】B
【解析】水解平衡常数只受温度的影响,A错误;通入的CO 与OH-反应,使平衡向正反应方向移动,
2
B正确;温度升高,CO的水解程度增大,c(HCO)增大,c(CO)减小,C错误;加入NaOH固体,溶液的
pH增大,D错误。
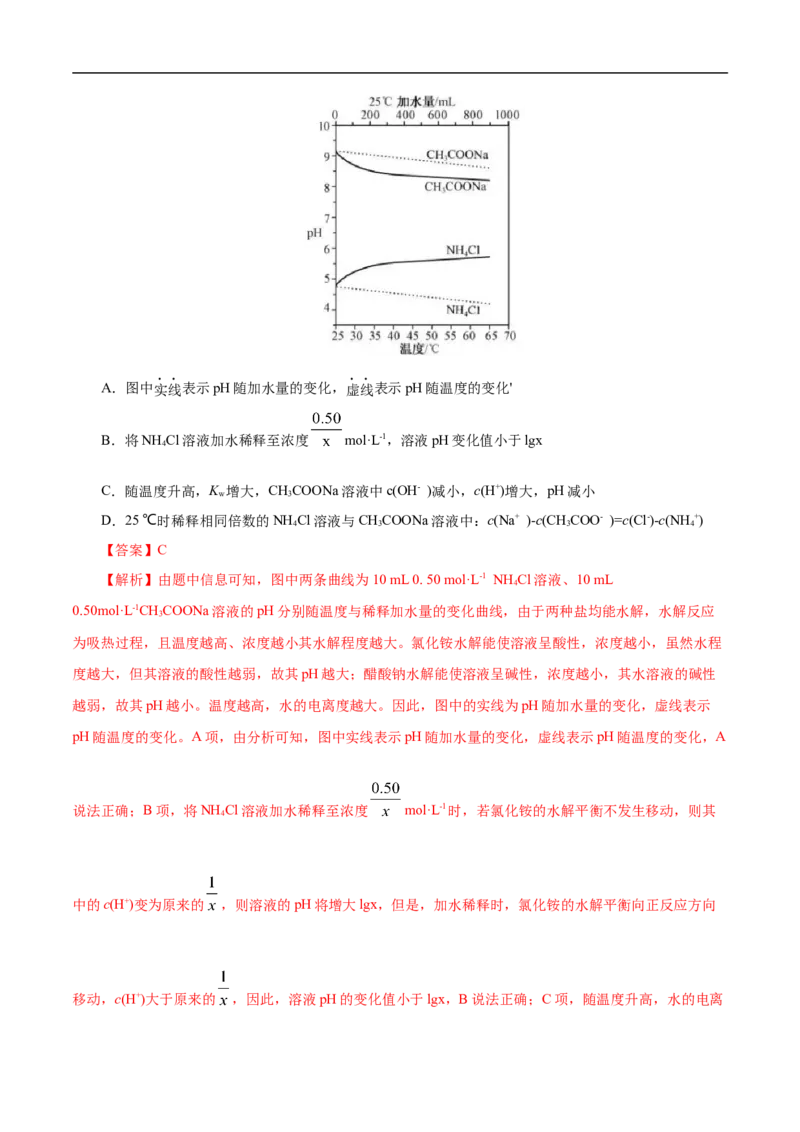
例2 (2021年1月浙江选考)实验测得10 mL 0.50 mol·L-1NH Cl溶液、10 mL 0.50mol·L-1CHCOONa溶
4 3
液的pH分别随温度与稀释加水量的变化如图所示。已知25 ℃时CHCOOH和NH ·H O的电离常数均为
3 3 2
1.8×10-5.下列说法不正确的是( )A.图中实线表示pH随加水量的变化,虚线表示pH随温度的变化'
B.将NH Cl溶液加水稀释至浓度 mol·L-1,溶液pH变化值小于lgx
4
C.随温度升高,K 增大,CHCOONa溶液中c(OH- )减小,c(H+)增大,pH减小
w 3
D.25 ℃时稀释相同倍数的NH Cl溶液与CHCOONa溶液中:c(Na+ )-c(CHCOO- )=c(Cl-)-c(NH +)
4 3 3 4
【答案】C
【解析】由题中信息可知,图中两条曲线为10 mL 0. 50 mol·L-1 NH Cl溶液、10 mL
4
0.50mol·L-1CHCOONa溶液的pH分别随温度与稀释加水量的变化曲线,由于两种盐均能水解,水解反应
3
为吸热过程,且温度越高、浓度越小其水解程度越大。氯化铵水解能使溶液呈酸性,浓度越小,虽然水程
度越大,但其溶液的酸性越弱,故其pH越大;醋酸钠水解能使溶液呈碱性,浓度越小,其水溶液的碱性
越弱,故其pH越小。温度越高,水的电离度越大。因此,图中的实线为pH随加水量的变化,虚线表示
pH随温度的变化。A项,由分析可知,图中实线表示pH随加水量的变化,虚线表示pH随温度的变化,A
说法正确;B项,将NH Cl溶液加水稀释至浓度 mol·L-1时,若氯化铵的水解平衡不发生移动,则其
4
中的c(H+)变为原来的 ,则溶液的pH将增大lgx,但是,加水稀释时,氯化铵的水解平衡向正反应方向
移动,c(H+)大于原来的 ,因此,溶液pH的变化值小于lgx,B说法正确;C项,随温度升高,水的电离程度变大,因此水的离子积变大,即K 增大;随温度升高,CHCOONa的水解程度变大,溶液中c(OH-)
w 3
增大,因此,C说法不正确;D项, 25℃时稀释相同倍数的NH C1溶液与CHCOONa溶液中均分别存在
4 3
电荷守恒,c(Na+ ) +c(H+) =c(OH-)+c(CHCOO- ) ,c(NH +)+c(H+ ) =c(Cl-)+c(OH- )。因此,氯化铵溶液中,
3 4
c(Cl-)-c(NH +) =c(H+ )-c(OH- ),醋酸钠溶液中,c(Na+ )-c(CHCOO- )= c(OH-) -c(H+) 。由于25 ℃时
4 3
CHCOOH和NH ·H O的电离常数均为1.8 ×10-5,因此,由于原溶液的物质的量浓度相同,稀释相同倍数
3 3 2
后的NH C1溶液与CHCOONa溶液,溶质的物质的量浓度仍相等,由于电离常数相同,其中盐的水解程
4 3
度是相同的,因此,两溶液中c(OH-) -c(H+)(两者差的绝对值)相等,故c(Na+ )-c(CHCOO- )=c(Cl-)-
3
c(NH +),D说法正确。故选C。
4
【对点提升】
对点1 下列溶液中,操作和现象对应正确的是( )
选项 溶液 操作 现象
A 滴有酚酞的明矾溶液 加热 颜色变深
B 滴有酚酞的氨水 加入少量NH Cl固体 颜色变浅
4
C 滴有酚酞的CHCOONa溶液 加入少量的CHCOONa固体 颜色变浅
3 3
D 氯化铁溶液 加热 颜色变浅
【答案】B
【解析】明矾溶液中Al3+水解使溶液呈酸性,加热,Al3+的水解程度增大,溶液的酸性增强,无颜色
变化,A项错误;加入NH Cl固体,氨水的电离程度减小,碱性减弱,溶液颜色变浅,B项正确;加入少
4
量CHCOONa固体会使CHCOO-+HO CHCOOH+OH-平衡向右移动,c(OH-)增大,颜色变深,
3 3 2 3
C项错误;加热氯化铁溶液时促进FeCl 水解为红褐色的Fe(OH) ,颜色加深,D项错误。
3 3
对点2 25℃,向20mL0.1mol•L-1的弱碱BOH溶液(K =1.0×10-5)中逐滴加入0.1mol•L-1盐酸,pH~V
b
曲线如图所示,下列说法正确的是
A.a点到b点,水的电离程度先减小后增大
B.a点时,c(Cl-)+c(OH-)=c(H+)+c(BOH)C.b点时,c(Cl-)=c(BOH)+c(B+)+c(H+)
D.V=20mL时,c(Cl-)>c(B+)>c(OH-)>c(H+)
【答案】B
【解析】A项,当BOH与盐酸恰好完全反应时,溶液中的溶质为0.05mol/LBCl,此时溶液中存在
B+的水解,BOH的电离平衡常数K =1.0×10-5,则B+的水解平衡常数为K = =10-9;则此时溶液中满
b h
足K =c(H+)c(BOH)/c(B+)≈c(H+)c(BOH)/0.05mol·L−1,c(H+)=c(BOH),解得c(H+)= ×10-5.5mol/L,所以此时
h
溶液的pH>5,即b点BOH已经完全反应,a点到b点,BOH逐渐和盐酸完全反应,然后盐酸过量,则水
的电离程度先增大后减小,A错误;B项,a点时,溶液中存在电荷守恒c(Cl-)+c(OH-)=c(H+)+c(B+),此时
pH=9,则c(OH-)=10-5mol/L,BOH的电离平衡常数K = =1.0×10-5,所以此时c(BOH)=c(B+),
b
则c(Cl-)+c(OH-)=c(H+)+c(BOH),B正确;C项,当BOH和盐酸恰好完全反应时,溶液中存在物料守恒:
c(Cl-)=c(BOH)+c(B+),b点时盐酸过量,所加入的盐酸中存在c′(Cl-)=c′(H+),若加入到混合溶液中后,B+的
水解不受影响,则c(Cl-)=c(BOH)+c(B+)+c(H+),但盐酸的电离会抑制B+,所以c(Cl-)>c(BOH)+c(B+)
+c(H+),C错误;D项,V=20mL时,溶液中溶质为BCl,溶液存在B+的水解,溶液显酸性,但水解是微弱
的,所以c(Cl-)>c(B+)>c(H+)>c(OH-),D错误;故选B。
【巧学妙记】
利用平衡移动原理解释问题的思维模板
(1)解答此类题的思维过程
①找出存在的平衡体系(即可逆反应或可逆过程)
②找出影响平衡的条件
③判断平衡移动的方向
④分析平衡移动的结果及移动结果与所解答问题的联系
(2)答题模板
……存在……平衡,……(条件)……(变化),使平衡向……(方向)移动,……(结论)。
盐类水解的应用1.判断离子能否大量共存
若阴、阳离子发生相互促进的水解反应,水解程度较大而不能大量共存,有的甚至水解完全。常见的
相互促进的水解反应进行完全的有:Fe3+、Al3+与[Al(OH) ]-、CO、HCO。
4
2.判断盐溶液蒸干时所得的产物
(1)盐溶液水解生成难挥发性酸和酸根阴离子易水解的强碱盐,蒸干后一般得原物质,如 CuSO (aq)蒸
4
干得CuSO ;NaCO(aq)蒸干得NaCO(s)。
4 2 3 2 3
(2)盐溶液水解生成挥发性酸时,蒸干灼烧后一般得对应的氧化物,如 AlCl (aq)蒸干得Al(OH) ,灼烧
3 3
得Al O。
2 3
(3)考虑盐受热时是否分解,如Ca(HCO )、NaHCO 、KMnO 、NH Cl固体受热易分解,因此蒸干灼烧
3 2 3 4 4
后分别为Ca(HCO )→CaCO (CaO);NaHCO →NaCO;KMnO →
3 2 3 3 2 3 4
KMnO 和MnO ;NH Cl→NH 和HCl。
2 4 2 4 3
(4)还原性盐在蒸干时会被O 氧化。如NaSO (aq)蒸干得NaSO (s)。
2 2 3 2 4
(5)弱酸的铵盐蒸干后无固体。如:NH HCO 、(NH )CO。
4 3 4 2 3
3.保存、配制某些盐溶液
如配制FeCl 溶液时,为防止出现Fe(OH) 沉淀,常加几滴盐酸来抑制FeCl 的水解;在实验室盛放
3 3 3
NaCO、CHCOONa、NaS等溶液的试剂瓶不能用玻璃塞,应用橡胶塞。
2 3 3 2
4.利用盐类的水解反应制取胶体、净水
如实验室制备Fe(OH) 胶体的原理为FeCl +3HO=====Fe(OH) (胶体)+3HCl。
3 3 2 3
明矾净水的原理:Al3+水解生成氢氧化铝胶体,胶体具有很大的表面积,吸附水中悬浮物而聚沉。
5.解释热的纯碱溶液去污能力强
碳酸钠溶液中存在水解平衡CO+HO HCO+OH-,升高温度,水解平衡右移,c(OH-)增大。
2
6.解释泡沫灭火器的反应原理
成分NaHCO 、Al (SO ) 发生反应Al3++3HCO===Al(OH) ↓+3CO↑。
3 2 4 3 3 2
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)明矾能水解生成Al(OH) 胶体,可用作净水剂( )
3
(2)制备AlCl 、FeCl 、CuCl 均不能采用将溶液直接蒸干的方法( )
3 3 2
(3)实验室保存NaS溶液用带有玻璃塞的试剂瓶 ( )
2
(4)泡沫灭火器中的试剂是Al (SO ) 溶液与NaCO 溶液( )
2 4 3 2 3
(5)焊接时用NH Cl溶液除锈与盐类水解无关( )
4
(6)生活中用电解食盐水的方法制取消毒液,运用了盐类的水解原理( )
(7)实验室配制FeCl 溶液时,需将FeCl (s)溶解在较浓盐酸中,然后加水稀释( )
3 3答案:(1)√ (2)× (3)× (4)× (5)× (6)√
【典例】
例1 下列有关问题与盐的水解有关的是( )
①NH Cl与ZnCl 溶液可作焊接金属时的除锈剂
4 2
②NaHCO 与Al (SO ) 两种溶液可作泡沫灭火剂
3 2 4 3
③草木灰与铵态氮肥不能混合施用
④实验室中盛放NaCO 溶液的试剂瓶不能用磨口玻璃塞
2 3
⑤加热蒸干CuCl 溶液得到Cu(OH) 固体
2 2
⑥要除去FeCl 溶液中混有的Fe2+,可先通入氧化剂Cl,再调节溶液的pH
3 2
A.①②③ B.②③④ C.①④⑤ D.①②③④⑤
【答案】D
【解析】①NH Cl和ZnCl 均为强酸弱碱盐,溶液中NH与Zn2+均发生水解反应,溶液显酸性,可以
4 2
除去金属表面的锈;②HCO与Al3+发生相互促进的水解反应,产生CO ,可作灭火剂;③草木灰的主要
2
成分为KCO,水解显碱性,而铵态氮肥水解显酸性,因而二者不能混合施用;④NaCO 溶液水解显碱性,
2 3 2 3
而磨口玻璃塞中的二氧化硅会与碱反应生成NaSiO ,将瓶塞与瓶口黏合在一起,因此实验室盛放NaCO
2 3 2 3
溶液的试剂瓶应用橡胶塞;⑤CuCl 溶液中存在水解平衡,CuCl +2HOCu(OH) +2HCl,加热时,HCl
2 2 2 2
挥发使平衡不断右移,最终得到Cu(OH) 固体;⑥Cl 能将Fe2+氧化成Fe3+,且没有引入杂质,与盐的水
2 2
解无关。
例2 下列实验操作不能达到实验目的的是( )
实验目的 实验操作
A 实验室配制FeCl 水溶液 将FeCl 溶于少量浓盐酸中,再加水稀释
3 3
B 由MgCl 溶液制备无水MgCl 将MgCl 溶液加热蒸干
2 2 2
将0.1mol·L-1MgSO 溶液滴入NaOH溶液
证明Cu(OH) 的溶度积比 4
C 2 至不再有沉淀产生,再滴加
Mg(OH) 的小
2 0.1mol·L-1CuSO 溶液
4
D 除去MgCl 酸性溶液中的Fe3+ 加入过量MgO充分搅拌,过滤
2
【答案】B
【解析】A项,配制FeCl 水溶液时,铁离子的水解平衡正向进行,加入适量的浓盐酸可使水解平衡
3
逆向移动,A与题意不符;B项,将MgCl 溶液加热蒸干时,镁离子的水解平衡正向移动,加热可使HCl
2
挥发增强,蒸干、灼烧得到MgO,B符合题意;C项,将0.1mol·L-1MgSO 溶液滴入NaOH溶液至不再有
4
沉淀产生,沉淀为氢氧化镁,再滴加0.1mol·L-1CuSO 溶液,若有蓝色沉淀生成,说明Cu(OH) 的溶度积比
4 2Mg(OH) 的小,C与题意不符;D项,Fe3+完全沉淀时溶液的pH为3.2左右,此时MgCl 不会产生沉淀,
2 2
可通过加入MgO调节pH的方法除去Fe3+,D与题意不符;故选B。
【对点提升】
对点1 合理利用某些盐能水解的性质,能解决许多生产、生活中的问题,下列叙述的事实与盐类水
解的性质无关的是( )
A.金属焊接时可用NH Cl溶液做除锈剂
4
B.配制FeSO 溶液时,加入一定量Fe粉
4
C.长期施用铵态氮肥会使土壤酸化
D.向FeCl 溶液中加入CaCO 粉末后有气泡产生
3 3
【答案】B
【解析】NH Cl水解溶液显酸性,能和铁锈反应从而除去铁锈,故和盐类水解有关,A不合题意;亚
4
铁离子易被氧化,配制FeSO 溶液时,加入一定量Fe粉的目的是防止Fe2+被氧化,与盐类的水解无关,B
4
符合题意;铵根离子水解显酸性,所以长期施用铵态氮肥会使土壤酸化,与盐类的水解有关,C不合题意;
FeCl 是强酸弱碱盐,水解显酸性,故加入碳酸钙后有气泡产生,和盐类的水解有关,D不合题意。
3
对点2 下列指定溶液中一定能大量共存的离子组是( )
A.pH=1的溶液中:NH、Na+、Fe3+、SO
B.含有大量AlO的溶液中:Na+、K+、HCO、NO
C.中性溶液中:K+、Al3+、Cl-、SO
D.NaS溶液中:SO、K+、Cu2+、Cl-
2
【答案】A
【解析】A 项,酸性条件下,H+抑制 NH、Fe3+的水解,能大量共存;B 项,AlO+HCO+
HO===Al(OH) ↓+CO,不能大量共存;C项,Al3+水解呈酸性,因而在中性溶液中不存在;D项,Cu2++
2 3
S2-===CuS↓,不能大量共存。
【巧学妙记】
1.熟记下列因水解相互促进不能大量共存的离子组合
(1)Al3+与HCO、CO、AlO、SiO、HS-、S2-、ClO-。
(2)Fe3+与HCO、CO、AlO、SiO、ClO-。
(3)NH与SiO、AlO。
(4)NH与CHCOO-、HCO虽能发生水解相互促进的反应,但能大量共存。
3
2.盐溶液蒸干灼烧时所得产物的几种判断类型
(1)盐溶液水解生成难挥发性酸时,蒸干后一般得原物质,如CuSO (aq)――→CuSO (s)。盐溶液水解
4 4
生成易挥发性酸时,蒸干灼烧后一般得对应的氧化物,如FeCl (aq) ――→Fe(OH) ――→Fe O。
3 3 2 3
(2)酸根阴离子易水解的强碱盐,如NaCO 溶液等蒸干后可得到原物质。
2 3
(3)考虑盐受热时是否分解。Ca(HCO ) 、NaHCO 、KMnO 固体受热易分解,因此蒸干后分别为
3 2 3 4Ca(HCO )→CaCO 、NaHCO →NaCO、KMnO →KMnO +MnO 。
3 2 3 3 2 3 4 2 4 2
(4)还原性盐在蒸干时会被O 氧化,如NaSO (aq)――→NaSO (s)。
2 2 3 2 4
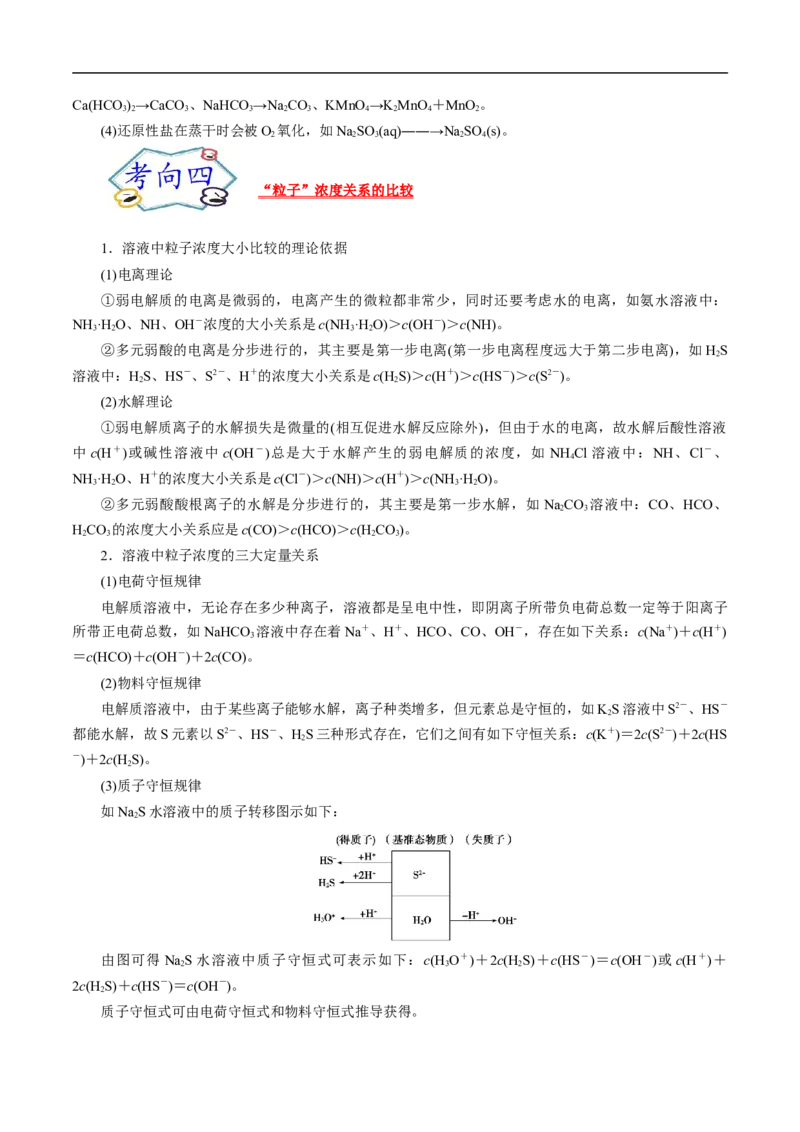
“粒子”浓度关系的比较
1.溶液中粒子浓度大小比较的理论依据
(1)电离理论
①弱电解质的电离是微弱的,电离产生的微粒都非常少,同时还要考虑水的电离,如氨水溶液中:
NH ·H O、NH、OH-浓度的大小关系是c(NH ·H O)>c(OH-)>c(NH)。
3 2 3 2
②多元弱酸的电离是分步进行的,其主要是第一步电离(第一步电离程度远大于第二步电离),如HS
2
溶液中:HS、HS-、S2-、H+的浓度大小关系是c(H S)>c(H+)>c(HS-)>c(S2-)。
2 2
(2)水解理论
①弱电解质离子的水解损失是微量的(相互促进水解反应除外),但由于水的电离,故水解后酸性溶液
中c(H+)或碱性溶液中 c(OH-)总是大于水解产生的弱电解质的浓度,如 NH Cl溶液中:NH、Cl-、
4
NH ·H O、H+的浓度大小关系是c(Cl-)>c(NH)>c(H+)>c(NH ·H O)。
3 2 3 2
②多元弱酸酸根离子的水解是分步进行的,其主要是第一步水解,如NaCO 溶液中:CO、HCO、
2 3
HCO 的浓度大小关系应是c(CO)>c(HCO)>c(H CO)。
2 3 2 3
2.溶液中粒子浓度的三大定量关系
(1)电荷守恒规律
电解质溶液中,无论存在多少种离子,溶液都是呈电中性,即阴离子所带负电荷总数一定等于阳离子
所带正电荷总数,如NaHCO 溶液中存在着Na+、H+、HCO、CO、OH-,存在如下关系:c(Na+)+c(H+)
3
=c(HCO)+c(OH-)+2c(CO)。
(2)物料守恒规律
电解质溶液中,由于某些离子能够水解,离子种类增多,但元素总是守恒的,如KS溶液中S2-、HS-
2
都能水解,故S元素以S2-、HS-、HS三种形式存在,它们之间有如下守恒关系:c(K+)=2c(S2-)+2c(HS
2
-)+2c(H S)。
2
(3)质子守恒规律
如NaS水溶液中的质子转移图示如下:
2
由图可得 NaS水溶液中质子守恒式可表示如下:c(H O+)+2c(H S)+c(HS-)=c(OH-)或c(H+)+
2 3 2
2c(H S)+c(HS-)=c(OH-)。
2
质子守恒式可由电荷守恒式和物料守恒式推导获得。【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)Na S溶液:c(Na+)>c(HS-)>c(OH-)>c(H S) ( )
2 2
(2)Na C O 溶液:c(OH-)=c(H+)+c(HC O)+2c(H C O) ( )
2 2 4 2 2 2 4
(3)Na CO 溶液:c(Na+)+c(H+)=2c(CO)+c(OH-) ( )
2 3
(4)0.1 mol·L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H A)>c(A2-) ( )
2
(5)常温下,pH=9的NaHA溶液:c(Na+)>c(HA-)>c(A2-)>c(H A) ( )
2
(6)新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-) ( )
(7)pH=8.3的NaHCO 溶液:c(Na+)>c(HCO)>c(CO)>c(H CO) ( )
3 2 3
(8)Na CO 溶液:c(H+)-c(OH-)=c(HCO)+2c(CO)-c(Na+) ( )
2 3
(9)向NaOH溶液中滴入HCOOH溶液后溶液显碱性:c(HCOO-)>c(OH-)>c(H+) ( )
(10)浓度均为0.1 mol·L-1的HF溶液与KF溶液等体积混合:c(F-)+c(HF)=0.2 mol·L-1( )
(11)pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH)>c(OH-)=c(H+) ( )
(12)0.2 mol/L CH COOH溶液与0.1 mol/L NaOH溶液等体积混合:2c(H+)-2c(OH-)=c(CHCOO-)-
3 3
c(CHCOOH) ( )
3
(13)0.1 mol/L NaHCO 溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO)>c(HCO)
3
>c(OH-) ( )
(14)20 mL 0.1 mol/L CH COONa溶液与10 mL 0.1 mol/L HCl溶液混合后溶液呈酸性,所得溶液中:
3
c(CHCOO-)>c(Cl-)>c(CHCOOH)>c(H+) ( )
3 3
(15)室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH)+c(OH
-)( )
(16)0.1 mol/L CH COOH溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+
3
c(CHCOOH)( )
3
答案:(1)× (2)√ (3)× (4)× (5)× (6)× (7)× (8)√ (9)× (10)× (11)× (12)√ (13)×
(14)√ (15)× (16)×
【典例】
例1 (2020•江苏卷)室温下,将两种浓度均为0.1mol·L-1的溶液等体积混合,若溶液混合引起的体积变
化可忽略,下列各混合溶液中微粒物质的量浓度关系正确的是( )
A.NaHCO -Na CO 混合溶液(pH=10.30):NaHCO 溶液中:c(Na+)>c(HCO)>c(CO2-)>c(OH-)
3 2 3 3 3
B.氨水-NH Cl混合溶液(pH=9.25):c(NH)+ c(H+)= c(NH ∙HO)+c(OH-)
4 3 2
C.CHCOOH - CHCOONa混合溶液(pH=4.76):c(Na+)>c(CHCOOH)>c(CHCOO−)>c(H+)
3 3 3 3
D.HC O-NaHC O 混合溶液(pH=1.68,HC O 为二元弱酸):c(H+)+c(H C O)= c(Na+)+c(OH—)+
2 2 4 2 4 2 2 4 2 2 4
c(C O)
2
【答案】AD【解析】A项,NaHCO 水溶液呈碱性,说明HCO -的水解程度大于其电离程度,等浓度的NaHCO 和
3 3 3
NaCO 水解关系为:CO2->HCO -,溶液中剩余微粒浓度关系为:c(HCO)>c(CO2-),CO2-和HCO -水解程
2 3 3 3 3 3 3
度微弱,生成的OH-浓度较低,由NaHCO 和NaCO 化学式可知,该混合溶液中Na+浓度最大,则混合溶
3 2 3
液中微粒浓度大小关系为:c(Na+)>c(HCO)>c(CO2-)>c(OH-),故A正确;B项,该混合溶液中电荷守恒
3
为:c(NH)+ c(H+)= c(Cl−)+c(OH-),物料守恒为:c(CHCOOH)+c(NH)=2c(Cl−),两式联立消去c(Cl-)可得:
3
c(NH)+2c(H+)= c(NH ∙HO)+2c(OH-),故B错误;C项,若不考虑溶液中相关微粒行为,则
3 2
c(CHCOOH)=c(CHCOO-)=c(Na+),该溶液呈酸性,说明CHCOOH电离程度大于CHCOONa水解程度,
3 3 3 3
则溶液中微粒浓度关系为:c(CHCOO-)>c(Na+)>c(CHCOOH)>c(H+),故C错误;D项,该混合溶液中物料
3 3
守恒为:2c(Na+)=c(H C O)+c(HC O-)+c(C O),电荷守恒为:c(H+)+c(Na+)=c(OH—)+c(HC O-)
2 2 4 2 4 2 2 4
+2c(C O),两式相加可得:c(H+)+c(H C O)= c(Na+)+c(OH—)+c(C O),故D正确;故选AD。
2 2 2 4 2
例 2 (2021•湖南选择性考试)常温下,用 0.1000mol•L﹣1的盐酸分别滴定 20.00mL 浓度均为
0.1000mol•L﹣1的三种一元弱酸的钠盐(NaX、NaY、NaZ)溶液,滴定曲线如图所示。下列判断错误的是(
)
A.该NaX溶液中:c(Na+)>c(X﹣)>c(OH﹣)>c(H+)
B.三种一元弱酸的电离常数:K(HX)>K(HY)>K(HZ)
a a a
C.当pH=7时,三种溶液中:c(X﹣)=c(Y﹣)=c(Z﹣)
D.分别滴加20.00mL盐酸后,再将三种溶液混合:c(X﹣)+c(Y﹣)+c(Z﹣)=c(H+)﹣c(OH﹣)
【答案】C
【解析】A项,因为HX为弱酸,NaX溶液存在水解:X﹣+H O HX+OH﹣,所以c(Na+)>c(X﹣)>
2
c(OH﹣)>c(H+),故A正确;B项,根据盐类水解的规律:越弱越水解可⇌知,相同浓度的强碱弱酸盐溶液中,
一元弱酸越弱,则其盐溶液碱性越强,结合图片可知溶液碱性强弱为:NaX<NaY<NaZ,则酸性强弱为:
HX>HY>HZ,一元弱酸中,酸性越强,电离程度越大,电离平衡常数 K越大,所以有:K(HX)>
a
K(HY)>K(HZ),故B正确;C项,当pH=7时,c(H+)=c(OH﹣),根据电荷守恒,NaX溶液中有:c(H+)
a a
+c(Na+)=c(OH﹣)+c(X﹣)+c(Cl﹣),则有:c(X﹣)=c(Na+)﹣c(Cl﹣),同理有:c(Y﹣)=c(Na+)﹣c(Cl﹣),c(Z﹣)=c(Na+)﹣c(Cl﹣),又因三种溶液滴定到pH=7时,消耗的HCl的量是不一样的,即溶液中的c(Cl﹣)是不一样
的,所以c(X﹣)≠c(Y﹣)≠c(Z﹣),故C错误;D项,分别滴加20.00mL盐酸后,再将三种溶液混合后存在电荷
0.1mol/L×20mL×3
守恒:c(X﹣)+c(Y﹣)+c(Z﹣)+c(OH﹣)+c(Cl﹣)=c(H+)+c(Na+),又混合溶液中c(Na+)= =
40mL×3
0.1mol/L×20mL×3
0.05mol/L,混合溶液中c(Cl﹣)= =0.05mol/L,代入电荷守恒表达式,有c(X﹣)+c(Y
40mL×3
﹣)+c(Z﹣)=c(H+)﹣c(OH﹣),故D正确。故选C。
【对点提升】
对点1 下列溶液中粒子的物质的量浓度关系正确的是( )
A.0.1 mol·L-1 NaHCO 溶液与0.1 mol·L-1 NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO)>
3
c(HCO)>c(OH-)
B.20 mL 0.1 mol·L-1 CHCOONa溶液与10 mL 0.1 mol·L-1 HCl溶液混合后溶液呈酸性,所得溶液中:
3
c(CHCOO-)>c(Cl-)>c(CHCOOH)>c(H+)
3 3
C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH)+c(OH
-)
D.0.1 mol·L-1 CHCOOH溶液与0.1 mol·L-1 NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)
3
+c(CHCOOH)
3
【答案】B
【解析】A项,等浓度等体积的NaHCO 与NaOH混合时,两者恰好反应生成NaCO,在该溶液中
3 2 3
CO能进行两级水解:CO+HOHCO+OH-、HCO+HO HCO+OH-,故溶液中c(OH
2 2 2 3
-)>c(HCO),该项错误;B项,CHCOONa与HCl混合时反应后生成的溶液中含有等量的CHCOONa、
3 3
CHCOOH、NaCl,因溶液显酸性,故溶液中CHCOOH的电离程度大于CHCOO-的水解程度,该项正确;
3 3 3
C项,在混合前两溶液的pH之和为14,则氨水过量,所得溶液为少量NH Cl和过量NH ·H O的混合溶液,
4 3 2
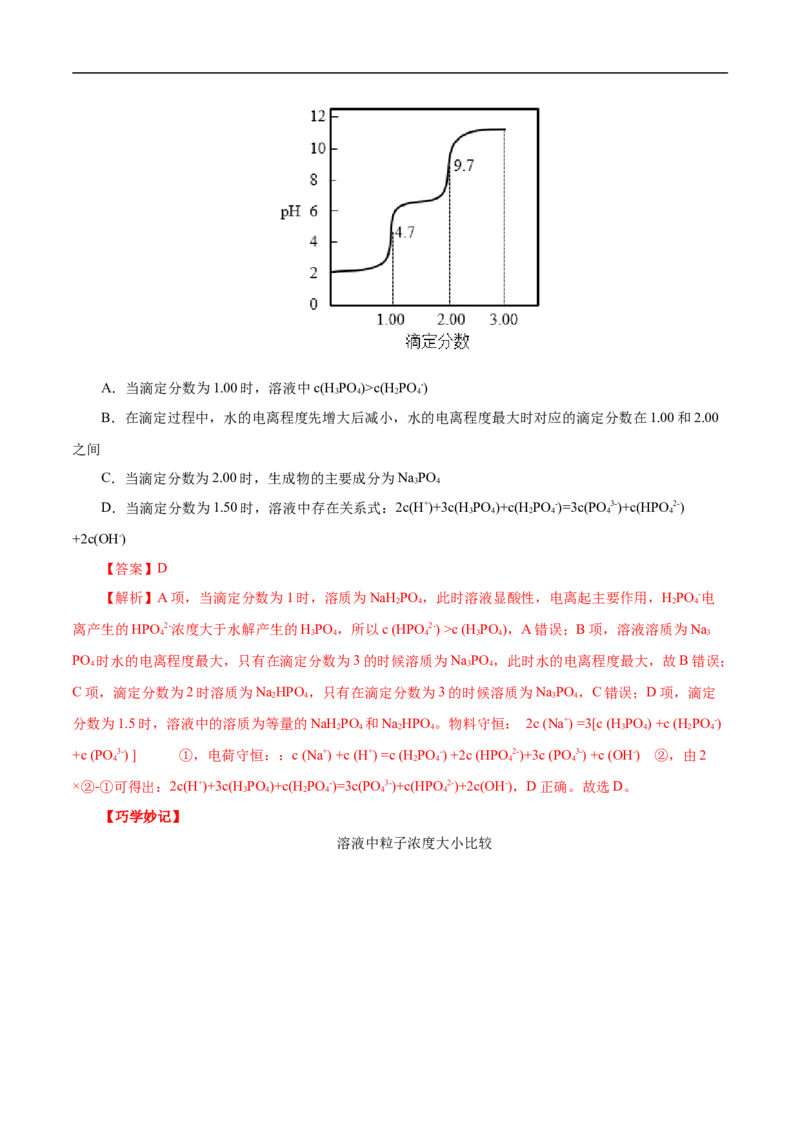
则c(Cl-)c(H PO -)
3 4 2 4
B.在滴定过程中,水的电离程度先增大后减小,水的电离程度最大时对应的滴定分数在1.00和2.00
之间
C.当滴定分数为2.00时,生成物的主要成分为NaPO
3 4
D.当滴定分数为1.50时,溶液中存在关系式:2c(H+)+3c(H PO )+c(H PO -)=3c(PO3-)+c(HPO 2-)
3 4 2 4 4 4
+2c(OH-)
【答案】D
【解析】A项,当滴定分数为1时,溶质为NaH PO ,此时溶液显酸性,电离起主要作用,HPO -电
2 4 2 4
离产生的HPO 2-浓度大于水解产生的HPO ,所以c (HPO2-) >c (H PO ),A错误;B项,溶液溶质为Na
4 3 4 4 3 4 3
PO 时水的电离程度最大,只有在滴定分数为3的时候溶质为NaPO ,此时水的电离程度最大,故B错误;
4 3 4
C项,滴定分数为2时溶质为NaHPO ,只有在滴定分数为3的时候溶质为NaPO ,C错误;D项,滴定
2 4 3 4
分数为1.5时,溶液中的溶质为等量的NaH PO 和NaHPO 。物料守恒: 2c (Na+) =3[c (H PO ) +c (H PO -)
2 4 2 4 3 4 2 4
+c (PO 3-) ] ①,电荷守恒::c (Na+) +c (H+) =c (H PO -) +2c (HPO 2-)+3c (PO 3-) +c (OH-) ②,由2
4 2 4 4 4
×②-①可得出:2c(H+)+3c(H PO )+c(H PO -)=3c(PO3-)+c(HPO 2-)+2c(OH-),D正确。故选D。
3 4 2 4 4 4
【巧学妙记】
溶液中粒子浓度大小比较1.下列关于盐类水解的说法错误的是( )
A.在纯水中加入能水解的盐一定促进水的电离
B.同温时,等浓度的NaHCO 和NaCO 溶液,NaHCO 溶液的pH大
3 2 3 3
C.在NH Cl溶液中加入稀HNO 能抑制NH水解
4 3
D.加热CHCOONa溶液,溶液中 的值将减小( )
3
【答案】B
【解析】盐类水解促进水的电离,A对;同温下,等浓度的NaCO 中CO水解程度大于HCO,所以
2 3
NaCO 溶液的碱性强,pH大,B错;NH水解使溶液显酸性,加入 HNO 抑制NH水解,C对;加热
2 3 3
CHCOONa溶液,CHCOO-水解程度增大,c(CHCOO-)减小,c(Na+)不变,则 变小,D对。
3 3 3
2.25 ℃时,某一元酸(HB)对应的盐NaB的水溶液呈碱性,下列叙述正确的是( )
A.HB的电离方程式为HB===H++B-
B.NaB溶液中:c(Na+)>c(B-)>c(H+)>c(OH-)
C.NaB溶液中:c(Na+)+c(H+)=c(HB)+c(B-)
D.0.1 mol/L NaB溶液中水电离出的OH-浓度大于10-7 mol/L
【答案】D
【解析】NaB的水溶液呈碱性,说明HB是弱酸,A项中的电离方程式中应用“”;B项应为
c(Na+)>c(B-)>c(OH-)>c(H+);C项应为c(Na+)+c(H+)=c(OH-)+c(B-);D项中B-水解促进了水的电离,
故水电离出的OH-浓度大于10-7 mol/L。
3.相同物质的量浓度的NaCN和NaClO相比,NaCN溶液的pH较大,则同温同体积同浓度的HCN
和HClO说法正确的是( )A.酸性:HCN>HClO
B.pH:HClO>HCN
C.酸根离子浓度:c(CN-)HCN
【答案】C
【解析】A项,等浓度的两盐溶液中NaCN溶液pH较大,说明酸性HClO>HCN ,故A错误;B项,
HClO电离程度大,其水溶液的pH:HClO<HCN,故B错误;C项,酸根离子的物质的量浓度c(ClO - )>
c(CN - ),故C正确;D项,等物质的量的一元酸(无论酸性强弱)必中和等物质的量的NaOH,故D错误。
4.25℃时,浓度均为0.2mol•L-1的NaHCO 和NaCO 溶液中,下列判断不正确的是( )
3 2 3
A.均存在水解平衡和电离平衡
B.由水电离出的c(OH-)前者小于后者
C.存在的离子种类相同
D.分别加入NaOH固体,恢复至室温,水解平衡均受到抑制,溶液的pH均减小
【答案】D
【解析】A项,NaHCO 溶液中存在的HCO -电离平衡和水解平衡、水的电离平衡,NaCO 溶液中存
3 3 2 3
在CO2-的水解平衡和水的电离平衡,故不选A;B项,CO2-的水解程度远远大于HCO -水解程度,二者水
3 3 3
解均显碱性,根据水解规律:谁强显谁性,所以NaCO 中的氢氧根浓度大于NaHCO 溶液中的氢氧根浓度,
2 3 3
故不选B;C项,HCO -能电离和水解,电离生成CO2-和H+,水解生成HCO 和OH-,CO2-第一步水解生
3 3 2 3 3
成HCO -和OH-,第二步水解生成HCO 和OH-,溶液中还存在H+,所以两种溶液中粒子种类相同,故不
3 2 3
选C;D项,分别加入NaOH固体,恢复到原温度,碳酸氢根和氢氧根在溶液反应会生成碳酸根和水,氢
氧根对它们的水解均起到抑制作用,但由于加入了强碱,溶液的pH均增大,故选D。
5.有四位同学分别设计实验证明:某种盐的水解是吸热的,不正确的是( )
A.甲同学:将硝酸铵晶体溶于水,若水温下降,说明硝酸铵水解是吸热的
B.乙同学:用加热的方法可除去KNO 溶液中混有的Fe3+,说明含Fe3+的盐水解是吸热的
3
C.丙同学:通过实验发现同浓度的热的纯碱液比冷的纯碱液去油污效果好,说明碳酸钠水解是吸热
的
D.丁同学:在醋酸钠溶液中滴入酚酞溶液,加热(不考虑水蒸发)后若红色加深,说明醋酸钠水解是吸
热的
【答案】A
【解析】A项,因硝酸铵晶体溶于水吸收热量,则不能说明盐水解为吸热反应,故A错误;B项,温
度升高,三价铁转化为氢氧化铁沉淀下来,说明升高温度有利于三价铁离子的水解平衡向右移动,故B正确;C项,温度升高,去油污效果好,说明温度升高有利于碳酸根的水解平衡正向移动,生成的氢氧根浓
度越大,碱性越强,酯的水解越彻底,故C正确;D项,醋酸钠溶液中滴入酚酞试液,加热后若红色加深,
则说明升高温度促进水解,即水解反应为吸热反应,故D正确。
6.一般较强酸可制取较弱酸,这是复分解反应的规律之一。已知在常温下测得浓度均为0.1mol/L的
下列 3 种溶液的 pH:
溶质 NaHCO NaCO NaClO
3 2 3
pH 8.34 11.6 10.3
下列有关说法正确的是( )
A.以上溶液的 pH 是用广泛 pH 试纸测定的
B.反应CO+H O+2NaClO=Na CO+2HClO可以发生
2 2 2 3
C.室温下,电离常数: K( H CO)>K( HClO)
2 2 3
D.在新制氯水中加入少量 NaHCO 固体可以提高溶液中 HClO 的浓度
3
【答案】D
【解析】根据“越弱越水解”并结合表格数据知,酸性的强弱顺序为HCO>HClO >HCO -。A项,pH
2 3 3
试纸不能用于测量具有氧化性和漂白性的溶液的pH,NaClO具有强氧化性,故A错误;B项,正确的反应
方程式为NaClO+CO +H O═NaHCO+HClO,故B错误;C项,酸性HClO >HCO -,电离常数:
2 2 3 3
K( H CO)c(H+)>c(NH+)>c(OH-)
4
C.0.1mol/L Na CO 与0.1mol/L NaHCO 溶液等体积混合: 2c(Na+)=3c(CO 2-)+3c(HCO-)+3c(H CO)
2 3 3 3 3 2 3
D.0.1mol/L Na C O 与0.1mol/L 的盐酸等体积混合(H C O 为二元弱酸):2c(C O2-)+c(HC O-)
2 2 4 2 2 4 2 4 2 4
+c(OH-)=c(Na+)+c(H+)
【答案】C
【解析】A项,NaHCO 溶液中:HCO -的水解程度大于其电离程度,所以溶液显碱性,根据质子守恒
3 3
可得c(OH-)=c(H+)+c(H CO),A错误;B项,HCl是一元强酸,完全电离,c(H+)与盐酸的浓度相等,而
2 3
NH ·HO是一元弱碱,只有很少一部分电离,在溶液中存在电离平衡,所以c(NH ·HO)>c(OH-),室温下,
3 2 3 2
将pH=2的盐酸与pH=12的氨水等体积混合,电离产生的OH-恰好与H+中和,但c(NH ·HO)> c(OH-),电
3 2
解质分子进一步电离产生OH-和NH +,因此溶液显碱性,所得溶液中:c(NH +)>c(Cl-),c(OH-)>c(H+),盐
4 4电离产生的离子浓度远大于弱碱电离产生的离子浓度所以微粒浓度关系为c(NH +) >c(Cl-)>c(OH-) >c(H+),
4
B错误;C项,0.1mol/L Na CO 与0.1mol/L NaHCO 溶液等体积混合,根据物料守恒可得: 2c(Na+)
2 3 3
=3c(CO 2-)+3c(HCO-)+3c(H CO),C正确;D项,0.1mol/L Na C O 与0.1mol/L 的盐酸等体积混合(H C O
3 3 2 3 2 2 4 2 2 4
为二元弱酸,二者发生反应:NaC O+HCl=NaCl+NaHC O,根据电荷守恒可得2c(C O2-)+c(HC O-)+
2 2 4 2 4 2 4 2 4
c(OH-)+c(Cl-)=c(Na+)+c(H+),D错误。
8.已知:常温下浓度均为0.1 mol·L-1的下列各溶液的pH如下表所示,下列有关说法正确的是( )
溶质 NaF NaClO NaCO
2 3
pH 7.5 9.7 11.6
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HCO<HClO<HF
2 3
B.若将CO 通入0.1 mol·L-1 Na CO 溶液中至溶液呈中性,则溶液中2c(CO2-)+c(HCO -)=0.1
2 2 3 3 3
mol·L-1(忽略溶液体积变化)
C.根据上表,水解方程式ClO-+HO HClO+OH-的平衡常数K≈10-7.6
2
D.向上述NaClO溶液中通过量CO 气体的离子方程式为:2ClO-+CO+H O === 2HClO+CO2-
2 2 2 3
【答案】C
【解析】A项,0.1 mol·L-1溶液的pH:NaFHClO>HCO -。又酸性HCO>HCO-,A项错误。B项,CO 通入0.1 mol·L-1
3 2 3 3 2
NaCO 溶液后,符合电荷守恒2c(CO2-)+c(HCO -)+c(OH-)=c(Na+)+c(H+),其中c(Na+)=0.2 mol·L-1。
2 3 3 3
溶液呈中性时c(OH-)=c(H+),得2c(CO2-)+c(HCO -)=0.2 mol·L-1,B项错误;C项,0.1 mol·L-1NaClO
3 3
溶液pH=9.7,则c(H+)=10-9.7mol·L-1,c(OH-)=10-4.3mol·L-1。c(ClO-)≈10-4.3mol·L-1,
c(HClO)≈0.1mol·L-1,则水解平衡常数K≈10-7.6,C项正确;D项,CO 气体过量时生成NaHCO ,离子方
2 3
程式为ClO-+CO+H O=HClO+HCO -。D项错误。
2 2 3
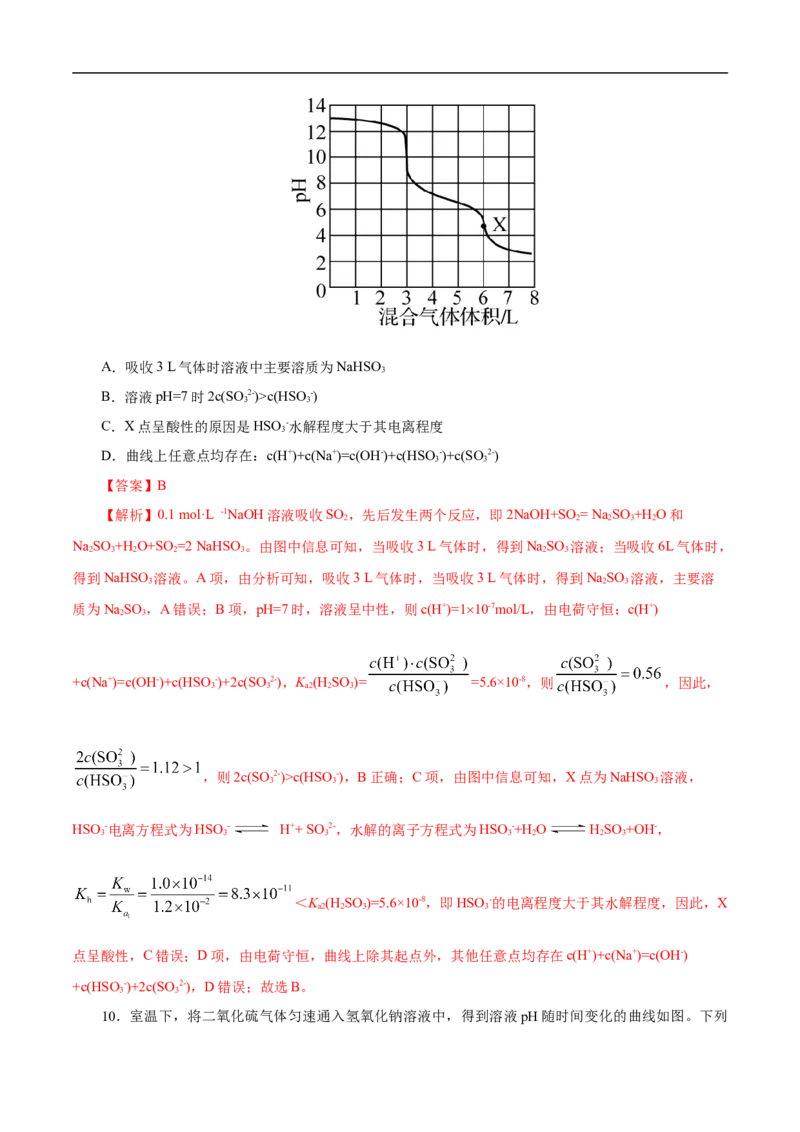
9.常温下,用200 mL 0.1 mol·L -1NaOH溶液吸收SO 与N 混合气体,所得溶液pH与吸收气体体积
2 2
的关系如图所示,已知K (H SO )=1.2×10-2,K (H SO )=5.6×10-8。下列说法正确的是( )
a1 2 3 a2 2 3A.吸收3 L气体时溶液中主要溶质为NaHSO
3
B.溶液pH=7时2c(SO 2-)>c(HSO -)
3 3
C.X点呈酸性的原因是HSO -水解程度大于其电离程度
3
D.曲线上任意点均存在:c(H+)+c(Na+)=c(OH-)+c(HSO -)+c(SO2-)
3 3
【答案】B
【解析】0.1 mol·L -1NaOH溶液吸收SO ,先后发生两个反应,即2NaOH+SO = Na SO +H O和
2 2 2 3 2
NaSO +H O+SO =2 NaHSO。由图中信息可知,当吸收3 L气体时,得到NaSO 溶液;当吸收6L气体时,
2 3 2 2 3 2 3
得到NaHSO 溶液。A项,由分析可知,吸收3 L气体时,当吸收3 L气体时,得到NaSO 溶液,主要溶
3 2 3
质为NaSO ,A错误;B项,pH=7时,溶液呈中性,则c(H+)=110-7mol/L,由电荷守恒:c(H+)
2 3
+c(Na+)=c(OH-)+c(HSO -)+2c(SO2-),K (H SO )= =5.6×10-8,则 ,因此,
3 3 a2 2 3
,则2c(SO 2-)>c(HSO -),B正确;C项,由图中信息可知,X点为NaHSO 溶液,
3 3 3
HSO -电离方程式为HSO - H++ SO 2-,水解的离子方程式为HSO -+H O HSO +OH-,
3 3 3 3 2 2 3
<K (H SO )=5.6×10-8,即HSO -的电离程度大于其水解程度,因此,X
a2 2 3 3
点呈酸性,C错误;D项,由电荷守恒,曲线上除其起点外,其他任意点均存在c(H+)+c(Na+)=c(OH-)
+c(HSO-)+2c(SO2-),D错误;故选B。
3 3
10.室温下,将二氧化硫气体匀速通入氢氧化钠溶液中,得到溶液pH随时间变化的曲线如图。下列说法正确的是( )。
A.二氧化硫与氢氧化钠按照物质的量比1∶2反应的点一定出现在图中20 min之前
B.浓度相同的①CHCOONa、②NaHCO 、③NaHSO 三份溶液中的pH:③>②>①
3 3 3
C.图中pH=7时,c(Na+)=c(HSO -)>c(OH-)=c(H+)
3
D.图中a点溶液中各离子浓度的关系是c(Na+)=c(OH-)+c(HSO -)+c(SO 2-)
3 3
【答案】A
【解析】向氢氧化钠溶液中通入二氧化硫,溶液中电荷守恒式为c(H+)+c(Na+)=c(OH-)+c(HSO -)
3
+2c(SO 2-)。A项,二氧化硫与氢氧化钠按照物质的量比1∶2反应生成亚硫酸钠,溶液pH大于7,正确;
3
B项,亚硫酸氢钠以电离为主,显酸性,则同浓度的①CHCOONa、②NaHCO 、③NaHSO 三份溶液中
3 3 3
的pH为②>①>③,错误;C项,根据电荷守恒,pH=7时:c(Na+)=c(HSO -)+2c(SO 2-)>c(OH-)=c(H+),错误;
3 3
D项,从图中a点可知此时为NaOH和NaSO 混合液,由电荷守恒式可知,错误。
2 3
11.醋酸是日常生活中最常见的调味剂和重要的化工原料,醋酸钠是其常见的盐(已知:25℃,
K(CHCOOH)=1.69×10-5)。
a 3
(1)醋酸钠溶液呈碱性的原因是_______________(写出有关的离子方程式)
(2)在CHCOONa溶液中离子浓度由大到小的顺序为_____________________(用c(Bn+)表示相应离子浓
3
度);
(3)25℃时,0.10mol/L的醋酸溶液的pH约为___________( 已知:lg1.3=0.114);
(4)对于醋酸溶液和醋酸钠溶液的下列说法正确的是____________;
A.稀释醋酸溶液,醋酸的电离程度增大,而稀释醋酸钠溶液则醋酸钠的水解程度减小.
B.升高温度可以促进醋酸电离,也可以促进醋酸钠水解.
C.醋酸和醋酸钠混合液中,醋酸抑制醋酸钠的水解、醋酸钠也抑制醋酸的电离.
D.醋酸和醋酸钠混合液中,醋酸促进醋酸钠的水解、醋酸钠也促进醋酸的电离.
(5)物质的量浓度均为0.1mol/L的CHCOONa和CHCOOH溶液等体积混合(注:混合前后溶液体积变
3 3
化忽略不计),混合液中的下列关系式正确的是_______;
A.c(CHCOOH)+2c(H+)=c(CH COO-)+2c(OH-)
3 3
B.c(Na+)+c(H+)=c(CH COO-)+c(OH-)
3
C.c(CHCOO-)+c(CH COOH)=0.1mol/L
3 3(6)常温时,有以下3种溶液,其中pH最小的是____________;
A.0.02mol•L-1CHCOOH与0.02mol•L-1NaOH溶液等体积混合液
3
B.0.03mol•L-1CHCOOH与0.01mol•L-1NaOH溶液等体积混合液
3
C.pH=2的CHCOOH与pH=12的NaOH溶液等体积混合液
3
(7)用 pH 试纸在常温下分别测定 0.10mol/L 的醋酸钠溶液和 0.10mol/L 的碳酸钠溶液,则
pH(CH COONa)_______ pH(Na CO) (填:“>”、“<”或“=”)。
3 2 3
【答案】(1)CH COO−+H O CHCOOH+OH−
3 2 3
(2)c(Na+)>c(CH COO−)>c(OH−)>c(H+)或c(Na+)、c(CHCOO−)、c(OH−)、c(H+)
3 3
(3)2.89或2.886 (4)BC (5)ABC (6)C (7)<
【解析】(1)醋酸钠是强碱弱酸盐,弱阴离子CHCOO-水解使溶液呈碱性,离子方程式为:CHCOO−
3 3
+H O CHCOOH+OH− 。 (2) 醋 酸 根 离 子 水 解 , 溶 液 显 碱 性 , 则 c(Na+)>c(CH COO−) 、
2 3 3
c(OH−)>c(H+),又因为一般水解是微弱的,所以c(Na+)和c(CHCOO−)远大于c(OH−)和c(H+),故CHCOONa
3 3
溶液中离子浓度由大到小的顺序为:c(Na+)>c(CH COO−)>c(OH−)>c(H+)或c(Na+)、c(CHCOO−)、c(OH−)、
3 3
c(H+)。(3)由已知,25℃时 K(CHCOOH)=1.69×10-5,又因为 K= ,其中
a 3 a
c(H+)=c(CH COO-),c(CHCOOH)约为0.10mol/L,所以c(H+)= =
3 3
=1.3×10-3mol/L,则pH=-lgc(H+)=3-lg1.3=2.886(或2.89)。(4)A项,稀释对电离和水解都有促进作用,则稀
释时醋酸的电离程度增大,醋酸钠的水解程度增大,故A错误;B项,电离和水解均为吸热反应,所以升
高温度,促进水解和电离,故B正确;C、D两项,醋酸电离是产生CHCOO−,CHCOO−水解是产生醋酸
3 3
二者作用相反,所以相互抑制,故 C 正确、D 错误。(5)因为 25℃,K(CHCOOH)=1.69×10-5,所以
a 3
K(CHCOO-)= = ,则 K(CHCOOH)>K (CHCOO-),物质的量浓度均为
h 3 a 3 h 3
0.1mol/L的CHCOONa和CHCOOH溶液等体积混合,溶液显酸性,电荷守恒为c(Na+)+c(H+)=c(CH COO-)
3 3 3
+c(OH-),物料守恒为 c(CHCOO-)+c(CH COOH)=2c(Na+)=2×( ×0.1mol/L),由上述两个式子可得
3 3
c(CHCOOH)+2c(H+)=c(CH COO-)+2c(OH-),综上分析A、B、C都正确。(6)A项,0.02mol•L-1CHCOOH与
3 3 30.02mol•L-1NaOH 溶液等体积混合,恰好生成醋酸钠,溶液显碱性;B 项,0.03mol•L-1CHCOOH 与
3
0.01mol•L-1NaOH溶液等体积混合,得到醋酸和醋酸钠的混合溶液,剩余0.01mol/L醋酸;C项,pH=2的
CHCOOH与pH=12的NaOH溶液等体积混合,得到醋酸和醋酸钠的混合溶液,pH=2的醋酸浓度远大于
3
0.01mol/L,所以剩余醋酸大于0.01mol/L,故C酸性最强,pH最小。(7)弱酸酸性越强,对应的钠盐溶液中
阴离子越容易水解,因为CHCOOH酸性强于HCO -,所以0.10mol/L的醋酸钠溶液和0.10mol/L的碳酸钠
3 3
溶液中,水解程度:CO2->CH COO−,弱阴离子水解溶液显碱性,水解程度越大碱性越强,pH越大,则
3 3
pH(CH COONa)<pH(Na CO)。
3 2 3
12.一般来说,较强酸可以制取较弱酸,这是复分解反应的规律之一。已知在常温下测得浓度均为
0.1 mol·L−1的下列6种溶液的pH。
溶质 CHCOONa NaHCO NaCO NaClO NaCN C HONa
3 3 2 3 6 5
pH 8.1 8.8 11.6 10.3 11.1 11.3
(1)①请根据上述信息判断下列反应不能发生的是____(填字母)。
A.CHCOOH+NaCN==CH COONa+HCN
3 3
B.CO+H O+2NaClO==Na CO+2HClO
2 2 2 3
C.2HCN+Na CO==NaCN+CO ↑+H O
2 3 2 2
D.NaCO+C HOH==NaHCO +C HONa
2 3 6 5 3 6 5
E.CO+H O+C HONa==NaHCO +C HOH
2 2 6 5 3 6 5
②已知HA、HB是两种弱酸,存在以下关系:HB(少量)+2A−==B2−+2HA,则A−、B2−、HB−三种阴离
2 2
子结合H+的难易顺序为________。
(2)一些复分解反应的发生还遵循其他规律。下列变化都属于复分解反应:
①将石灰乳与纯碱溶液混合可制得苛性钠溶液;②向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏
打固体;③蒸发KCl和NaNO 的混合溶液,首先析出NaCl晶体。根据上述反应,总结出复分解反应发生
3
的另一规律为_______________。
(3)常温下将某电解质溶解在水中后,溶液中的c(H+)=10−9 mol·L−1,则该电解质可能是____(填字母)。
A.CuSO B.HCl C.NaS D.NaOH E.K SO
4 2 2 4
(4)常温下,将a L pH=3的盐酸分别与下列三种溶液混合,所得溶液均呈中性。
①b L浓度为1.0×10−3 mol·L−1的氨水;
②c L c(OH−)=1.0×10−3 mol·L−1的氨水;
③d L c(OH−)=1.0×10−3 mol·L−1的氢氧化钠溶液。
则a、b、c、d的大小关系:__________。
【答案】(1)BC HB−B2−>HB−)(2) 由溶解度相对较大的物质向生成溶解度相对较小的物质的方向进行
(3)CD (4)b>a=d>c
【解析】(1)①六种盐都为强碱弱酸盐,盐的pH越大,说明对应的酸水解程度越大,则对应的酸越弱,
则A项,CH COOH酸性大于HCN,反应能发生,故A正确;B项,酸性H CO >HClO>HCO - ,
3 2 3 3
应生成NaHCO ,反应不能发生,故B错误;C项,酸性H CO >HClO>HCN,应生成NaHCO ,
3 2 3 3
不能生成CO ,故C错误;D项,酸性C H OH>HCO - ,反应能发生,故D正确;E项,酸性H
2 6 5 3 2
CO >C H OH>HCO - ,反应能发生,故E正确,故选BC;②据反应HB(少量)+2A-=B2-+2HA可
3 6 5 3 2
知,HA酸性小于HB,HA酸性最弱,酸性越弱,对应的酸根离子得H+能力越强,没有HB-生成,说明得
2
电子能力A-大于HB-,则得电子能力顺序为A->B2->HB-;(2)各反应均有固体生成,其溶解度更小,故复
分解反应能够向生成更难溶的物质的方向进行;(3)溶液中的c(H +)=10 -9 mol.L -1 ,说明溶液呈碱性,只
有NaS和NaOH符合;(4)一水合氨为弱电解质,不能完全电离,与盐酸反应至中性时,氨水应稍过量,
2
则b>a,c(OH-)=1.0×10 -3 mol.L -l 的氨水,一水合氨浓度远大于1.0×10 -3 mol.L -l 的氨水,反应至中性
时,a>c,氢氧化钡为强碱,与盐酸完全中和时,a=d,则b>a=d>c。
1.(2022·重庆南开中学考前模拟预测)劳动创造美好未来。下列叙述正确的是( )
A.施加适量石膏可降低盐碱地的碱性
B.铵态氮肥和草木灰混合施用可提高肥效
C.用稀硫酸清洗锅炉中的水垢
D.84消毒液和洁厕剂混合使用效果更好
【答案】A
【解析】A项,盐碱地中加石膏,可使土壤中的碳酸根转化为碳酸钙,降低土壤的碱性,A正确;B
项,铵态氮肥中铵根水解呈酸性,草木灰中碳酸根水解呈碱性,两者会反应使得铵根变成氨水,降低铵态
氮肥的肥效,B错误;C项,水垢中含有碳酸钙,加硫酸后转化为微溶物硫酸钙,阻止反应进一步进行,
水垢难除尽,C错误;D项,84消毒液成分为NaClO,洁厕剂的成分为HCl,两者混合会产生有毒气体氯
气,不可以混用,D错误;故选A。
2.(2022·上海市复旦附中高三模拟)将去掉氧化膜的铝片放入足量NaCO 溶液中,铝片表面产生气泡,
2 3
充分反应后得到无色溶液M。下列分析错误的是( )
A.产生的气体中有H B.反应与CO2-水解有关
2 3
C.Al(OH) 向酸式电离方向移动 D.M中含大量:Na+、Al3+、HCO -
3 3【答案】D
【解析】在NaCO 溶液中,CO2-发生水解,生成OH-等,OH-与Al在溶液中发生反应,生成AlO- 和
2 3 3 2
H。A项,产生的气体中有H,A正确;B项,由分析可知,与Al反应的OH-来自CO2-水解,B正确;C
2 2 3
项,NaCO 溶液呈碱性,Al(OH) 表现出酸性,发生酸式电离,C正确;D项,Al3+、HCO -在溶液中能发
2 3 3 3
生双水解反应,不能大量共存,所以M中不可能含大量Al3+、HCO -,D错误;故选D。
3
3.(2022·浙江省金华十校选考模拟)室温下,有a mol·L-1NaX和b mol·L-1NaY两种盐溶液。下列说法
正确的是( )
A.若a=b且c(X-) +c(HX)=c(Y-),则酸性HX>HY
B.若a>b且c(X-)=c(Y-),则酸性HX>HY
C.若 且 ,则酸性HX<HY
D.若a<b且c(X-)<c(Y-),则酸性HX<HY
【答案】C
【解析】A项,若a=b且c(X-) +c(HX)=c(Y-),表明NaX在水溶液中发生水解反应,离子方程式为X-
+H O HX+OH-,故在水溶液中的存在形式为X-和HX,所以HX为弱酸,而NaY不水解,故在水溶
2
液中只存在Y-,所以HY为强酸,即酸性HX<HY,A错误;B项,若a>b,则表示NaX的浓度大于
NaY,但是c(X-)=c(Y-),表明X-减少也或者减少得更多,说明X-发生了水解而减少了,或者说X-发生水解
的程度更大,减少得更多,依据盐类水解“越弱越水解”的规律,可推断酸性HX<HY,B错误;C项,
若 且 ,即NaX溶液浓度小,但是碱性强,表明X-发生了水解反应,或X-的水
解程度更大,依据盐类水解“越弱越水解”的规律,可判断酸性HX<HY,C正确;D项,若a<b且c(X-)
<c(Y-),无法判断X-和Y-是否发生了水解,则无法判断HX和HY的酸性强弱,D错误;故选C。
4.(2022·江苏省常州市考前模拟预测)常温下,通过下列实验探究NaHCO 溶液的性质。
3
实验1:用 pH计测量0.05mol·L-1 NaHCO 溶液的pH,测得pH为8.3
3
实验2:向 0.05mol·L-1 NaHCO 溶液中逐滴滴加等体积同浓度的NaOH溶液,溶液pH逐渐上升至
3
11.3
实验3:向0.05mol·L-1NaHCO 溶液中逐滴滴加等体积同浓度的盐酸,溶液pH逐渐下降至4.3
3
下列说法正确的是( )
A.由实验1可得出: K <K (H CO) ·K (H CO)
w a1 2 3 a2 2 3
B.实验2过程中,c(OH- )+c(HCO- )+2c(CO 2-- )逐渐增大
3 3
C.实验3过程中,c(Na+)逐渐小于c(HCO - )+c(CO 2-- )+c(H CO)
3 3 2 3D.实验2和3结束时,用x和y依次表示两份溶液中c(Na+ )+c(H+),则x>y
【答案】D
【解析】A项,HCO -水解平衡常数与水的离子积的关系K = ,根据实验1,碳酸氢钠溶液显碱性,
3 h
说明HCO -水解平衡常数大于HCO -电离平衡常数,有K = >K ,即有Kw>K ·K ,故A错误;B项,
3 3 h a2 a1 a2
0.05mol/LNaHCO 溶液中存在c(Na+)+c(H+)=c(OH-)+c(HCO-)+c(CO 2--)=0.05+10-8.3,向0.05moL/LNaHCO 溶
3 3 3 3
液中加入等体积等浓度的NaOH溶液,两种溶液恰好完全反应,生成NaCO,溶液中存在c(Na+)
2 3
+c(H+)=c(OH-)+c(HCO-)+c(CO 2--)=0.05+10-11.3,因此实验2过程中c(OH-)+c(HCO-)+c(CO 2--)逐渐减小,故B
3 3 3 3
错误;C项,0.05mol/LNaHCO 溶液中存在c(Na+)= c(HCO -)+c(CO 2--)+c(H CO),向0.05moL/LNaHCO 溶
3 3 3 2 3 3
液中加入等体积等浓度的盐酸,两种溶液恰好完全反应,生成NaCl和CO,CO 能溶于水,使溶液显酸性,
2 2
因此有c(Na+)= c(HCO -)+c(CO 2--)+c(H CO)+c(Cl-),推出c(Na+)>c(HCO -)+c(CO 2--)+c(H CO),实验3过程
3 3 2 3 3 3 2 3
中,c(Na+)大于c(HCO -)+c(CO 2--)+c(H CO),故C错误;D项,实验3结束后,溶液中存在c(Na+)
3 3 2 3
+c(H+)=c(OH-)+c(HCO-)+c(CO 2--)+c(Cl-)=0.025+10-4.3,根据B选项分析,推出x>y,故D正确;故选D。
3 3
5.(2022·上海市洋泾中学高三模拟)H C O 为二元弱酸,K (H C O)=5.4×10-2,K (H C O)=5.4×10-5,
2 2 4 a1 2 2 4 a2 2 2 4
NaHC O 溶液显酸性。设HC O 溶液中c(总)=c(H C O)+c(HC O-)+c(C O2-)。室温下用NaOH溶液滴定
2 4 2 2 4 2 2 4 2 4 2 4
25.00mL0.1000mol·L-1HC O 溶液至终点。滴定过程得到的下列溶液中微粒的物质的量浓度关系一定正确的
2 2 4
是( )
A.0.1000mol·L-1HC O 溶液:c(H+)=0.1000mol·L-1+c(C O2-)+c(OH-)+c(H C O)
2 2 4 2 4 2 2 4
B.c(Na+)=c(总)的溶液:c(Na+)>c(H C O)>c(H+)>c(C O2-)
2 2 4 2 4
C.pH=7的溶液:c(Na+)=0.1000mol·L-1+c(C O2-)-c(HC O)
2 4 2 2 4
D.c(Na+)=2c(总)的溶液:c(OH-)-c(H+)=2c(H C O)+c(HC O-)
2 2 4 2 4
【答案】D
【解析】A项,0.1000mol·L-1HC O 溶液中c(HC O)+c(HC O-)+c(C O2-)=0.1 mol·L-1,根据电荷守恒
2 2 4 2 2 4 2 4 2 4
c(HC O-)+2c(C O2-)+c(OH-)= c(H+),所以c(H+)=0.1000mol·L-1+c(C O2-)+c(OH-)-c(HC O),故A错误;B项,
2 4 2 4 2 4 2 2 4
根据物料守恒,c(Na+)=c(总)的溶液中溶质为NaHC O,HC O-的电离常数为5.4×10-5、水解常数为
2 4 2 4
,HC O-电离大于水解,c(C O2-)>c(H C O),故B错误;C项,加入一定体积的氢氧
2 4 2 4 2 2 4化钠溶液,c(HC O)+c(HC O-)+c(C O2-)<0.1 mol·L-1,根据电荷守恒,pH=7的溶液c(HC O-)
2 2 4 2 4 2 4 2 4
+2c(C O2-)=c(Na+),c(Na+)>0.1000mol·L-1+c(C O2-)-c(HC O),故C正确;D项,根据物料守恒
2 4 2 4 2 2 4
c(Na+)=2c(总)的溶液中溶质为NaC O,根据物料守恒c(Na+)=2[c(HC O)+c(HC O-)+c(C O2-)],根据电
2 2 4 2 2 4 2 4 2 4
荷守恒c(HC O-)+2c(C O2-)+c(OH-)=c(Na+)+ c(H+),所以c(OH-)-c(H+)=2c(H C O)+c(HC O-),故D正确;故
2 4 2 4 2 2 4 2 4
选D。
6.(2022·江苏省南京师大附中高三考前适应性测试)室温下,通过下列实验探究NaHSO、NaSO 溶液
3 2 3
的性质。
实验1:向0.1mol·L-1 NaHSO 溶液中滴加酸性KMnO 溶液,溶液紫红色褪去。
3 4
实验2:将浓度均为0.1mol·L-1的NaHSO 和Ba(OH) 溶液等体积混合,产生白色沉淀。
3 2
实验3:向0.1mol·L-1 Na SO 溶液中滴加几滴酚酞,加水稀释,溶液红色变浅。
2 3
实验4:向0.1mol·L-1 NaHSO 溶液中通入少量Cl,溶液呈弱酸性。
3 2
下列说法正确的是( )
A.实验1中发生反应的离子方程式为5SO 2-+2MnO-+6H+=5SO2-+2Mn2++3H O
3 4 4 2
B.实验2可以得出K (BaSO)>2.5×10-15的结论
sp 3
C.实验3随着水的不断加入,溶液中 的值逐渐变小
D.实验4所得溶液中存在c(H SO ) <3c(SO 2-)+c(SO 2-)
2 3 4 3
【答案】D
【解析】A项,实验1中NaHSO 被酸性K MnO 氧化,NaHSO 是弱酸的酸式盐,拆写为Na+和
3 4 3
HSO -,发生反应的离子方程式为5HSO -+2MnO-+H+=5SO2-+2Mn2++3H O,A错误;B项,实验2发生反
3 3 4 4 2
应HSO -+Ba2++OH-=BaSO ↓+H O,不知反应后的离子浓度,不可以得出K (BaSO)>2.5×10-5的结论,B错
3 3 2 sp 3
误;C项,实验3随着水的不断加入,SO 2-水解平衡:SO 2-+H O HSO -+OH-正向移动,溶液中
3 3 2 3
的值逐渐变大,C错误;D项,实验4发生反应HSO -+Cl+H O=SO 2-+2 Cl-+3H+,同时还有
3 2 2 4
NaHSO 的水解和电离,所得溶液中存在物料守恒:c(Na+)= c(H SO )+ c(HSO -)+ c(SO 2-)+c(SO 2-),存在
3 2 3 3 4 3
电荷守恒:c(Na+)+c(H+)=c(HSO -)+2 c(SO 2-)+2c(SO 2-)+ c(OH―),则有等式:c(H SO )+c(H+)=c(HSO -)+
3 4 3 2 3 3
c(SO 2-)+c(SO 2-)+ c(OH―),溶液呈弱酸性,即c(H+)>c(OH―),则c(H SO )<c(SO 2-)+c(SO 2-),故c(H SO )
4 3 2 3 4 3 2 3
<3c(SO 2-)+c(SO 2-),D正确;故选D。
4 3
7.(2022·上海市高三二模)室温下,通过下列实验探究0.1mol·L-1NaHS溶液的性质。实验 实验操作和现象
① 滴加几滴酚酞试液,溶液变红
② 加入等体积0.1molL-1NaOH溶液充分混合,无明显现象
③ 加入少量CuSO 溶⋅液,产生黑色沉淀
4
④ 加入适量NaClO溶液,有淡黄色沉淀产生
下列有关说法正确的是( )
A.实验①溶液中:c(S2-)>c(H S)
2
B.实验②所得溶液中:c(OH-)=c(H+)+c(HS-)+2c(H S)
2
C.实验③中反应的离子方程式:Cu2++HS-→CuS↓+H+
D.实验④中反应的离子方程式:2HS-+ClO-→2S↓+Cl-+H O
2
【答案】B
【解析】A项,实验①:滴加几滴酚酞试液,溶液变红,表明溶液显碱性,则HS-的水解程度大于电
离程度,所以溶液中:c(S2-)<c(H S),A不正确;B项,实验②中,NaHS与NaOH正好完全反应,所得溶
2
液为NaS溶液,溶液中存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-),物料守恒:c(Na+)=2c(HS-)
2
+2c(S2-)+2c(H S),从而得出c(OH-)=c(H+)+c(HS-)+2c(H S),B正确;C项,实验③中,HS-与Cu2+反应,生
2 2
成CuS沉淀和H+,H+再与HS-结合为HS,反应的离子方程式:Cu2++2HS-→CuS↓+HS↑,C不正确;D项,
2 2
实验④中,HS-与ClO-发生氧化还原反应,生成S、Cl-和OH-,OH-再与HS-反应生成S2-和HO,反应的离
2
子方程式:2HS-+ClO-→S↓+Cl-+S2-+H O,D不正确;故选B。
2
8.(2022·江苏省平潮高级中学模拟预测)室温下,通过下列实验探究NaCO 溶液的性质。用K 、K
2 3 a1 a2
分别表示HCO 的第一步和第二步电离常数。
2 3
实验 实验操作和现象
1 用pH试纸测定0.1mol·L-1NaCO 溶液的pH,测得pH约为12
2 3
2 向0.1mol·L-1NaCO 溶液中加入过量0.2mol·L-1CaCl 溶液,产生白色沉淀
2 3 2
3 向0.1mol·L-1NaCO 溶液中通入过量CO,测得溶液pH约为8
2 3 2
4 向含有酚酞的0.1mol·L-1NaCO 中滴加几滴0.2mol·L-1NaOH,红色加深
2 3
下列有关说法不正确的是( )
A.0.1mol·L-1NaCO 溶液中存在c(OH-)=c(H+)+2c(H CO)+c(HCO-)
2 3 2 3 3
B.实验2反应静置后的上层清液中有c(Ca2+)·c(CO2-)=K (CaCO)
3 sp 3
C.实验3得到的溶液中有c(HCO -)>c(HCO)>c(CO2-),且K K <K
3 2 3 3 a1 a2 wD.实验4中滴加的NaOH抑制了CO2-的水解, 的值变小
3
【答案】D
【解析】A项,NaCO 溶液中,根据电荷守恒可得c(OH-)+c(HCO-)+2c(CO 2-)=c(H+)+c(Na+),又根据
2 3 3 3
物料守恒可得c(Na+)=2[c(HCO-)+c(CO 2-)+c(H CO)],两式联立可得c(OH-)=c(H+)+2c(H CO)+c(HCO-),故
3 3 2 3 2 3 3
A正确;B项,NaCO 溶液中加入过量CaCl 溶液生成碳酸钙沉淀,上层清液为饱和碳酸钙溶液,故有
2 3 2
c(Ca2+)·c(CO2-)=K (CaCO),故B正确;C项,NaCO 溶液中通入过量CO,测得溶液pH约为8,即为碳
3 sp 3 2 3 2
酸氢钠溶液,溶液显碱性,水解大于电离,故有c(HCO -)>c(HCO)>c(CO2-),且水解常数大于电离常数,
3 2 3 3
故有K= >K ,故K K <K ,故C正确;D项,CO2-的水解平衡为CO2-+H O HCO -+OH-,水
h a2 a1 a2 w 3 3 2 3
解常数K= ,K 大小随温度变化而变化,故滴加NaOH平衡移动,但 不变,
h h
故D错误;故选D。
9.(2022·江苏省南通市新高考基地学校高三第二次联考)室温下,通过下列实验探究
0.100mol·L-1KC O 溶液的性质。已知:25℃时HC O 的K =10-1.22,K =10-4.19。
2 2 4 2 2 4 a1 a2
序号 实验
① 准确量取10.00mL0.100mol·L-1KC O 溶液,测得pH=8.4
2 2 4
② 向①中加入2滴0.100mol·L-1HCl盐酸,测得pH=7.0
③ 向①准确加入10.00mL0.100mol·L-1HCl溶液,pH=3.52
④ 向①中加入20.00mL0.100mol·L-1CaCl 溶液,出现白色沉淀
2
下列说法正确的是( )
A.实验①溶液中: =10-4.21
B.实验②反应所得溶液中:c(K+)=2c(C O2-)+c(HC O-)
2 4 2 4
C.实验③反应所得溶液中:c(C O2-)K (CaSO),D错误;故选C。
3 sp 3
12.(2022·福建省漳州市高毕业班一模)边搅拌边向NaCO 溶液中通入SO 制备NaHSO 溶液,水溶液
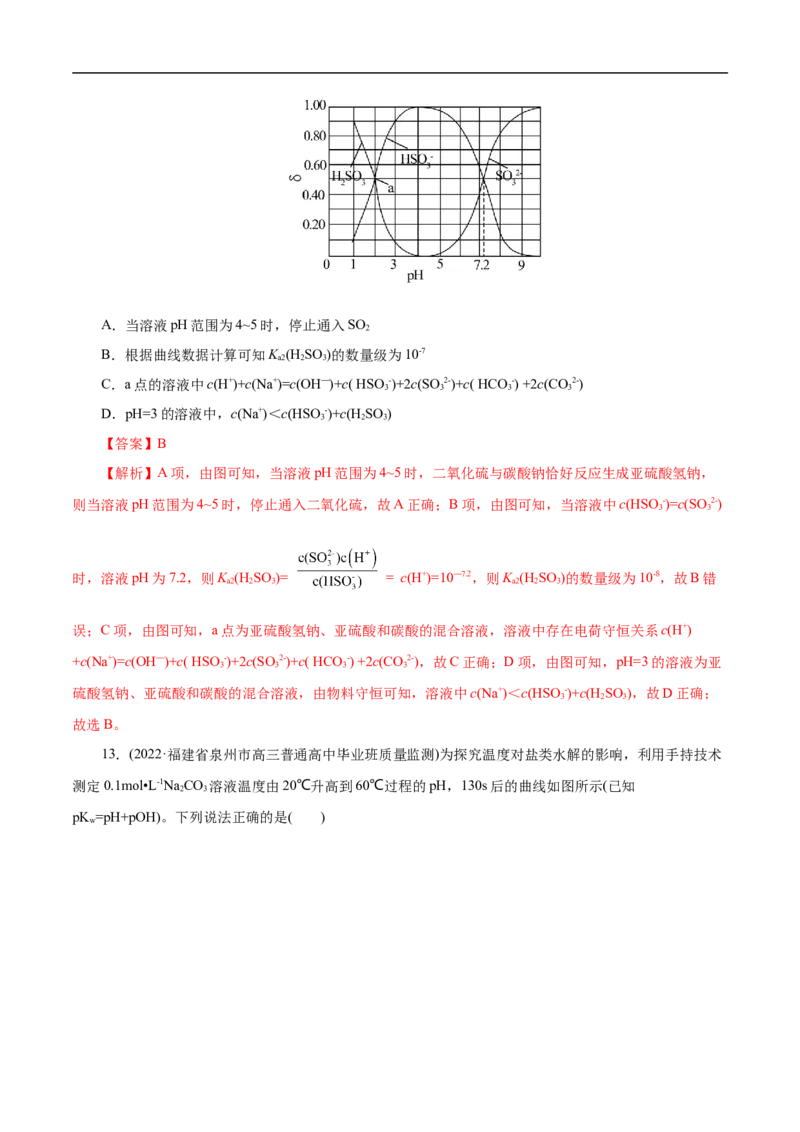
2 3 2 3
中HSO 、HSO -、SO 2-的分布系数δ随pH的变化关系如图所示。[比如HSO 的分布系数: δ (H SO ) =
2 3 3 3 2 3 2 3
],下列有关叙述错误的是( )A.当溶液pH范围为4~5时,停止通入SO
2
B.根据曲线数据计算可知K (H SO )的数量级为10-7
a2 2 3
C.a点的溶液中c(H+)+c(Na+)=c(OH—)+c( HSO -)+2c(SO 2-)+c( HCO-) +2c(CO2-)
3 3 3 3
D.pH=3的溶液中,c(Na+)<c(HSO -)+c(H SO )
3 2 3
【答案】B
【解析】A项,由图可知,当溶液pH范围为4~5时,二氧化硫与碳酸钠恰好反应生成亚硫酸氢钠,
则当溶液pH范围为4~5时,停止通入二氧化硫,故A正确;B项,由图可知,当溶液中c(HSO -)=c(SO 2-)
3 3
时,溶液pH为7.2,则K (H SO )= = c(H+)=10—7.2,则K (H SO )的数量级为10-8,故B错
a2 2 3 a2 2 3
误;C项,由图可知,a点为亚硫酸氢钠、亚硫酸和碳酸的混合溶液,溶液中存在电荷守恒关系c(H+)
+c(Na+)=c(OH—)+c( HSO -)+2c(SO 2-)+c( HCO-) +2c(CO2-),故C正确;D项,由图可知,pH=3的溶液为亚
3 3 3 3
硫酸氢钠、亚硫酸和碳酸的混合溶液,由物料守恒可知,溶液中c(Na+)<c(HSO -)+c(H SO ),故D正确;
3 2 3
故选B。
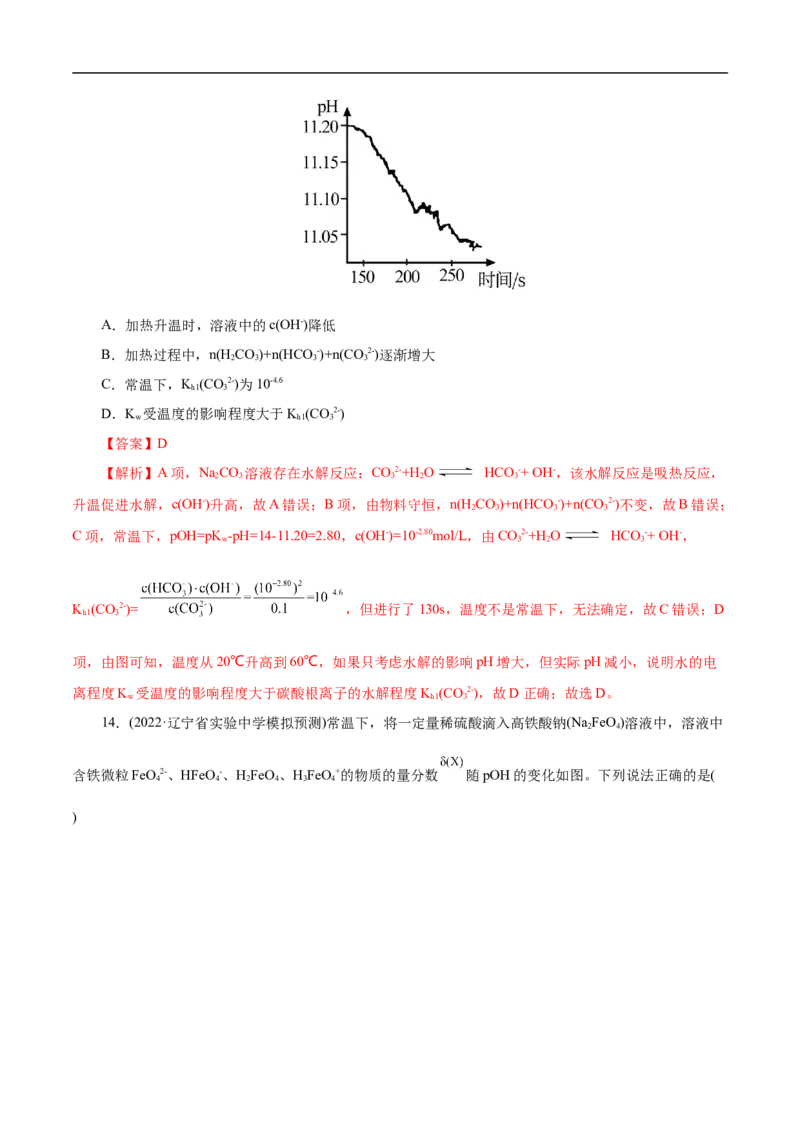
13.(2022·福建省泉州市高三普通高中毕业班质量监测)为探究温度对盐类水解的影响,利用手持技术
测定0.1mol•L-1NaCO 溶液温度由20℃升高到60℃过程的pH,130s后的曲线如图所示(已知
2 3
pK =pH+pOH)。下列说法正确的是( )
wA.加热升温时,溶液中的c(OH-)降低
B.加热过程中,n(H CO)+n(HCO-)+n(CO 2-)逐渐增大
2 3 3 3
C.常温下,K (CO2-)为10-4.6
h1 3
D.K 受温度的影响程度大于K (CO2-)
w h1 3
【答案】D
【解析】A项,NaCO 溶液存在水解反应:CO2-+H O HCO -+ OH-,该水解反应是吸热反应,
2 3 3 2 3
升温促进水解,c(OH-)升高,故A错误;B项,由物料守恒,n(H CO)+n(HCO-)+n(CO 2-)不变,故B错误;
2 3 3 3
C项,常温下,pOH=pK -pH=14-11.20=2.80,c(OH-)=10-2.80mol/L,由CO2-+H O HCO -+ OH-,
w 3 2 3
K (CO2-)= ,但进行了130s,温度不是常温下,无法确定,故C错误;D
h1 3
项,由图可知,温度从20℃升高到60℃,如果只考虑水解的影响pH增大,但实际pH减小,说明水的电
离程度K 受温度的影响程度大于碳酸根离子的水解程度K (CO2-),故D正确;故选D。
w h1 3
14.(2022·辽宁省实验中学模拟预测)常温下,将一定量稀硫酸滴入高铁酸钠(Na FeO)溶液中,溶液中
2 4
含铁微粒FeO2-、HFeO -、HFeO、HFeO+的物质的量分数 随pOH的变化如图。下列说法正确的是(
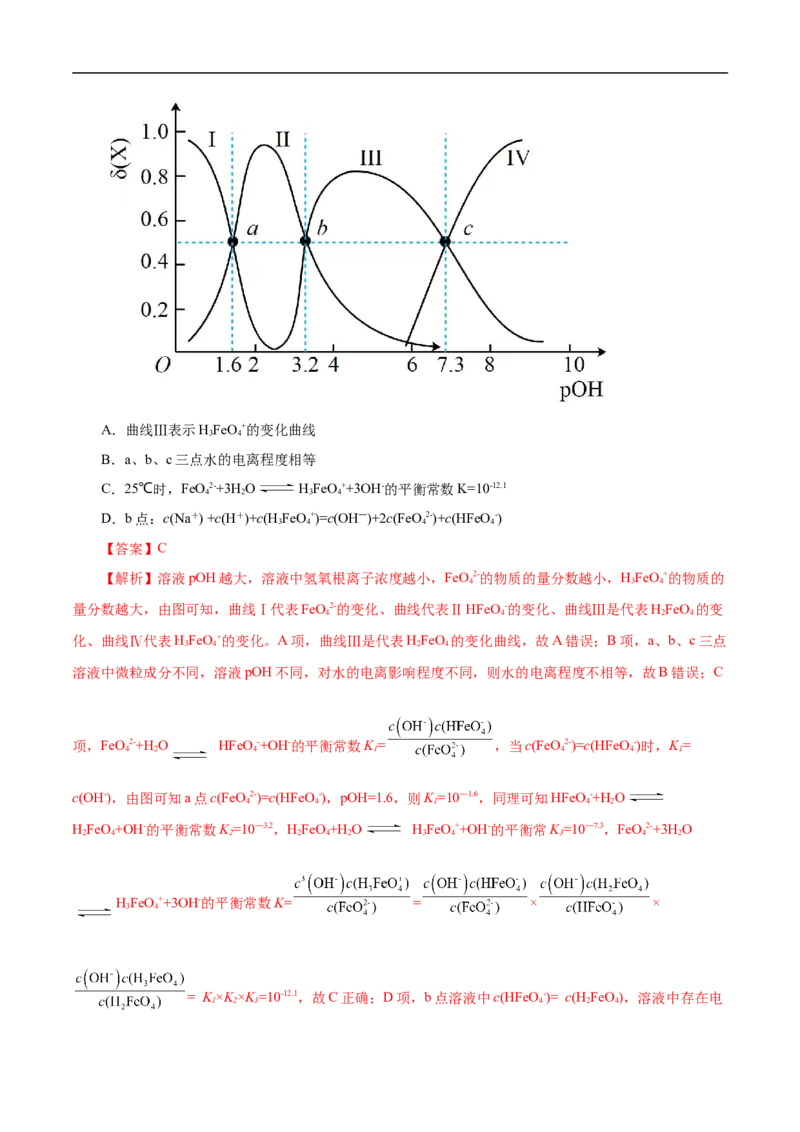
4 4 2 4 3 4
)A.曲线Ⅲ表示HFeO+的变化曲线
3 4
B.a、b、c三点水的电离程度相等
C.25℃时,FeO2-+3H O HFeO++3OH-的平衡常数K=10-12.1
4 2 3 4
D.b点:c(Na+) +c(H+)+c(H FeO+)=c(OH―)+2c(FeO 2-)+c(HFeO -)
3 4 4 4
【答案】C
【解析】溶液pOH越大,溶液中氢氧根离子浓度越小,FeO2-的物质的量分数越小,HFeO+的物质的
4 3 4
量分数越大,由图可知,曲线Ⅰ代表FeO2-的变化、曲线代表ⅡHFeO -的变化、曲线Ⅲ是代表HFeO 的变
4 4 2 4
化、曲线Ⅳ代表HFeO+的变化。A项,曲线Ⅲ是代表HFeO 的变化曲线,故A错误;B项,a、b、c三点
3 4 2 4
溶液中微粒成分不同,溶液pOH不同,对水的电离影响程度不同,则水的电离程度不相等,故B错误;C
项,FeO2-+H O HFeO -+OH-的平衡常数K = ,当c(FeO 2-)=c(HFeO -)时,K =
4 2 4 1 4 4 1
c(OH-),由图可知a点c(FeO 2-)=c(HFeO -),pOH=1.6,则K =10—1.6,同理可知HFeO -+H O
4 4 1 4 2
HFeO+OH-的平衡常数K =10—3.2,HFeO+H O HFeO++OH-的平衡常K =10—7.3,FeO2-+3H O
2 4 2 2 4 2 3 4 3 4 2
HFeO++3OH-的平衡常数K= = × ×
3 4
= K ×K ×K =10-12.1,故C正确;D项,b点溶液中c(HFeO -)= c(H FeO),溶液中存在电
1 2 3 4 2 4荷守恒关系c(Na+)+c(H+)+c(H FeO+)=c(OH-)+2c(FeO 2-)+c(HFeO -) +2c(SO 2-),溶液中c(SO 2-)≠c(HFeO -),则
3 4 4 4 4 4 4
b点溶液中c(Na+)+c(H+)+c(H FeO+)≠c(OH-)+2c(FeO 2-)+3c(HFeO -),故D错误;故选C。
3 4 4 4
15.(2022·河南省二模)向10mL0.05mol·L-1的某稀酸HA溶液中滴入0.05mol·L-1KOH溶液,溶液中由
水电离出的氢离子浓度c(H+)、溶液温度T随滴入KOH溶液体积的变化如图所示,忽略混合时溶液体积的
变化。下列说法正确的是( )
A.25℃时,HA的电离平衡常数K=2.04×10-5
B.f点后溶液温度下降的原因是中和反应放出的热量小于电解质电离吸收的热量
C.c点溶液中c(K+)=c(A-)+c(HA),e点溶液呈中性
D.a点溶液中离子浓度的大小关系:c(H+)+c(HA)>c(A-)+c(OH-);d点溶液中:2c(K+)=3[c(A-)
+c(HA)]=0.06mol·L-1
【答案】A
【解析】A项,25℃时,起点为HA溶液,水电离出的氢离子浓度c(H+)=10-11 mol·L-1,则溶液中
c(H+)=10-3 mol·L-1,此时,溶液中c(A-)=c(H+)=10-3 mol·L-1,c(HA)=0.05-10-3=0.049 mol·L-1,所以电离平衡
常数K= ,A项正确;B项,f点恰好中和反应完全,放出热量最多,f点
之后继续加入KOH,只有电解质的电离吸收热量,所以温度下降,B项错误;C项,c点为恰好中和,溶
液中c(K+)=c(A-)+c(HA),e点溶液温度不再是25℃,此时虽然水电离出的c(H+)=10-7 mol·L-1,但溶液不呈
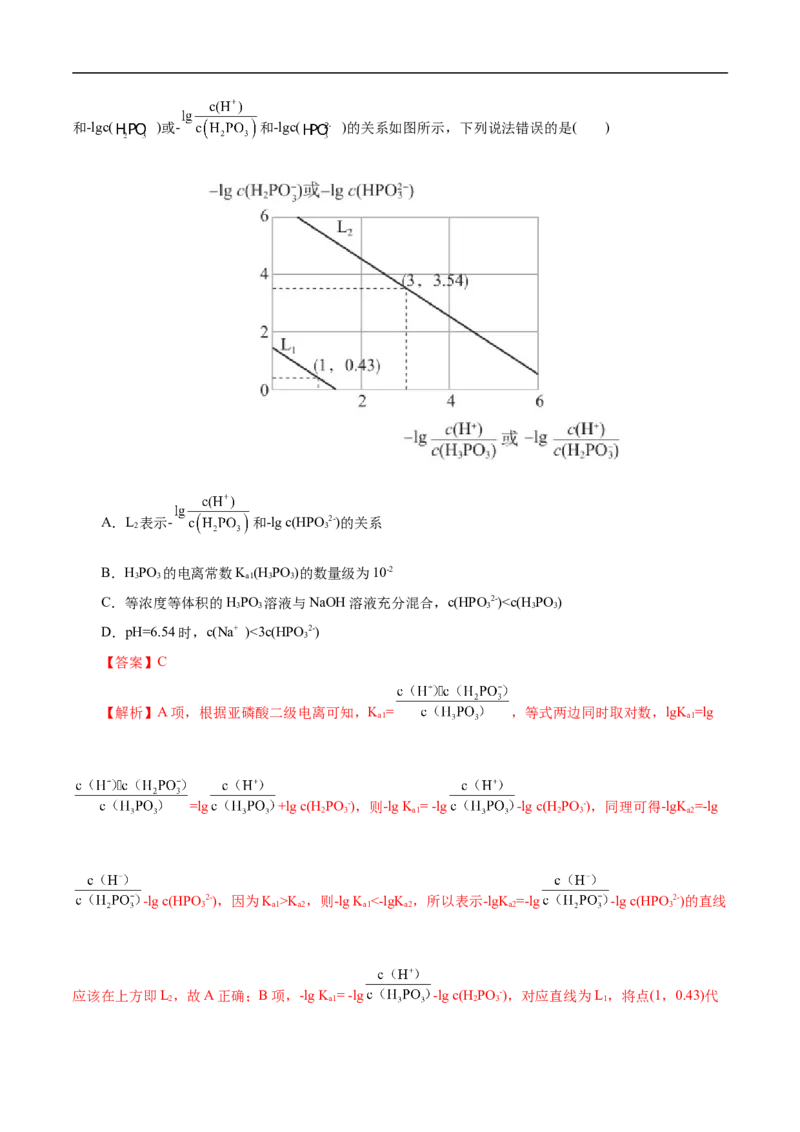
中性,C项错误;D项,a点溶液中溶质为KA和HA且为1:1,由HA的电离平衡常数可知HA的电离程
度大于KA的水解程度,所以c(K+)> c(HA),根据电荷守恒等式可得c(H+)+c(HA)K ,则-lg K <-lgK ,所以表示-lgK =-lg -lg c(HPO 2-)的直线
3 a1 a2 a1 a2 a2 3
应该在上方即L,故A正确;B项,-lg K = -lg -lg c(H PO -),对应直线为L,将点(1,0.43)代
2 a1 2 3 1入得,-lg K =1.43,K =10-1.43,K 数量级为10-2,B正确;C项,等浓度等体积的HPO 溶液与NaOH溶
a1 a1 a1 3 3
液充分混合,生成NaH PO 溶液,HPO -既电离又水解,电离平衡常数K =10-6.54,水解平衡常数K=
2 3 2 3 a2 h
=10-12.57,水解程度小于电离程度,故c(HPO 2-)>c(H PO ),C项错误;D项,将-lgK =-lg -lg
3 3 3 a2
c(HPO 2-)变形可得到 ,pH等于6.54时, c(HPO -)=c(HPO 2-),
3 2 3 3
根据电荷守恒,c(HA)+c(H+)= c(OH―)+ c(HPO -)+2c(HPO 2-)= c(OH―)+ 3c(HPO 2-),此时溶液呈酸性,
2 3 3 3
c(H+)>c(OH-),则c(Na+)<3c(HPO 2-),D项正确;故选C。
3
18.(2022·天津市二模)甘氨酸盐酸盐(HOOCCH NH Cl)的水溶液呈酸性,溶液中存在以下平衡:
2 3
HOOCCH NH + H++-OOCCH NH + K
2 3 2 3 1
-OOCCH NH + H++-OOCCH NH K
2 3 2 2 2
常温时,向10mL一定浓度的HOOCCH NH Cl的水溶液中滴入同浓度的NaOH溶液。混合溶液pH随
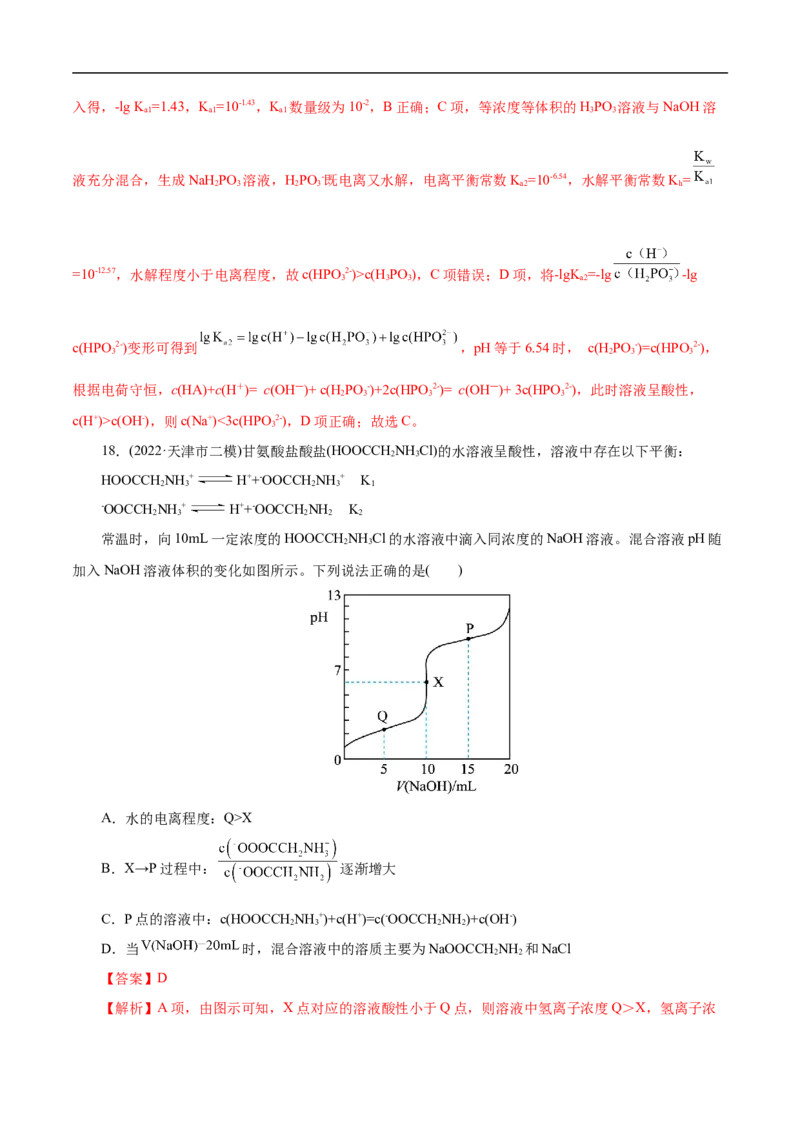
2 3
加入NaOH溶液体积的变化如图所示。下列说法正确的是( )
A.水的电离程度:Q>X
B.X→P过程中: 逐渐增大
C.P点的溶液中:c(HOOCCH NH +)+c(H+)=c(-OOCCH NH )+c(OH-)
2 3 2 2
D.当 时,混合溶液中的溶质主要为NaOOCCHNH 和NaCl
2 2
【答案】D
【解析】A项,由图示可知,X点对应的溶液酸性小于Q点,则溶液中氢离子浓度Q>X,氢离子浓度越大水的电离程度越弱,则水的电离程度Q<X,A错误;B项,由K= 可知,
2
= ,由题干图示可知,Q→P过程中溶液pH增大,即c(H+)减小,K 不变,则
2
逐渐减小,B错误;C项,由题干图示信息可知,P点对应加入的NaOH为15mL,此时
反应后的溶液中的溶质为等物质的量的NaOOCCHNH +和NaOOCCHNH ,则此时溶液中有电荷守恒式为:
2 3 2 2
c(HOOCCH NH +)+c(H+)+c(Na+)=c(-OOCCH NH )+c(OH-)+c(Cl-),且c(Na+)>c(Cl-),故c(HOOCCH NH +)
2 3 2 2 2 3
+c(H+)<c(-OOCCH NH )+c(OH-),C错误;D项,当V(NaOH)=20mL时,即甘氨酸盐酸盐
2 2
(HOOCCH NH Cl)和NaOH的物质的量之比为1:2,反应方程式为:
2 3
HOOCCH NH Cl+2NaOH=NaOOCCH NH +NaCl+2HO,故此时混合溶液中的溶质主要为NaOOCCHNH
2 3 2 2 2 2 2
和NaCl,D正确;故选C。
19.(2022·河南省安阳市考前适应性测试)室温下,某混合溶液中c(M+) +c(MOH) =c(R-) +c(HR) ,
和 随pH变化关系如图所示,已知pX = -lg X。下列说法错误的是( )
A.曲线I表示 与pH关系曲线,pK=pK -2
a b
B.b点溶液中c(M+)>c(R-),x= - 2C.MR溶液显碱性,且MR溶液溶液中c(MOH)<c( HR)
D.等物质的量的NaR与HR混合溶液中,c(HR)>c(Na+)>c(R-)>c(OH-)>c(H+)
【答案】D
【解析】由 ,当 =0即c(M+)= c(MOH)时,K= c(OH-),同理,K=
b a
c(H+),由lgX=0时,pH分别为6、10,则曲线I表示 与pH关系,曲线II表示 与pH关
系。A项,由lgX=0时,pH分别为6、10,则曲线I表示 与pH关系,K= c(H+)=10-6,常温下c点
a
c(OH-)= ,K= c(OH-)=10-4,则pK=pK -2,A正确;B项,b点溶液pH=8,溶液呈碱性,
b a b
说明MOH电离程度比HR电离程度大,则c(M+) >c(R-),c(OH-)= ,由
,则 ,则lgx=- =-2,B正确;C项,由K= 10-6,
a
K=10-4,相对而言MOH碱性较强、HR酸性较弱,则MR溶液显碱性,由越弱越水解规律可知,R-水解程
b
度大于M+,则MR溶液溶液中c(MOH) <c( HR),C正确;D项,由K= 10-6,R-水解常数为
a
< K,则HR电离程度大于R-水解程度,等物质的量的NaR与HR混合溶液中,c(R-)>
a
c(Na+)>c(HR)>c(H+)>c(OH-),D错误;故选D。
1.【2022·浙江省1月选考】某同学在两个相同的特制容器中分别加入20mL0.4mol·L-1NaCO 溶液和
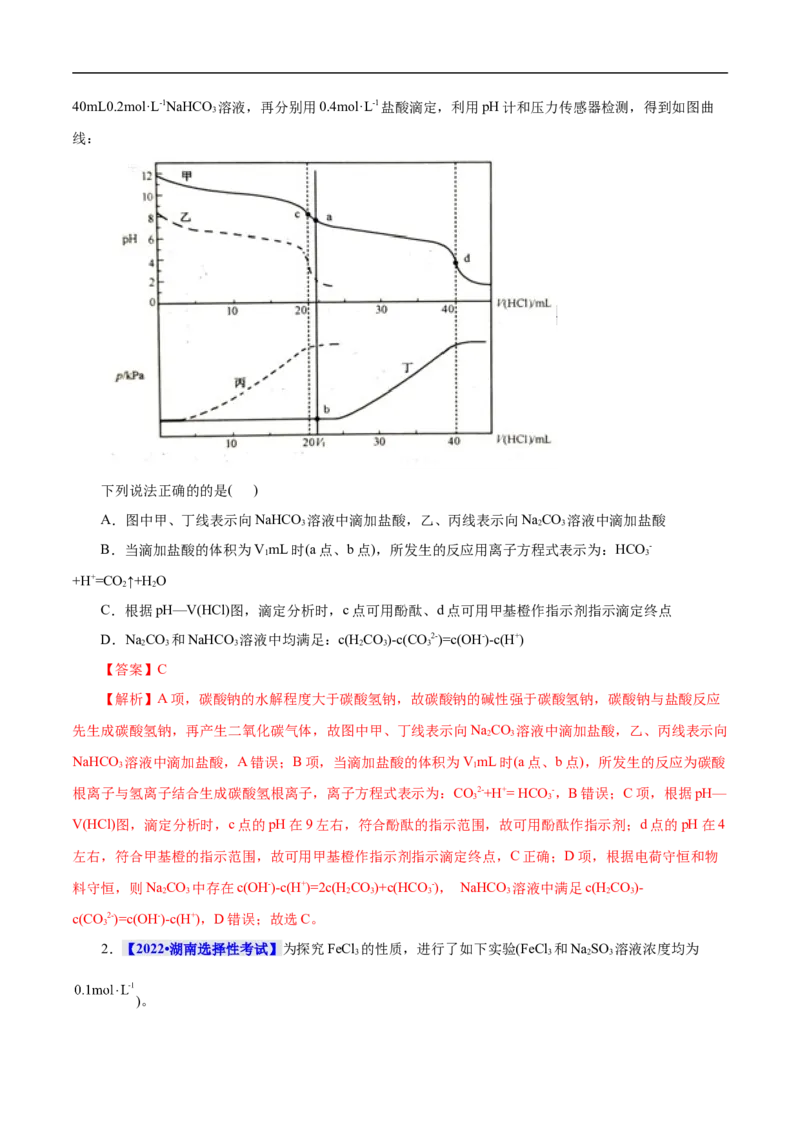
2 340mL0.2mol·L-1NaHCO 溶液,再分别用0.4mol·L-1盐酸滴定,利用pH计和压力传感器检测,得到如图曲
3
线:
下列说法正确的的是( )
A.图中甲、丁线表示向NaHCO 溶液中滴加盐酸,乙、丙线表示向NaCO 溶液中滴加盐酸
3 2 3
B.当滴加盐酸的体积为VmL时(a点、b点),所发生的反应用离子方程式表示为:HCO -
1 3
+H+=CO ↑+H O
2 2
C.根据pH—V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点
D.NaCO 和NaHCO 溶液中均满足:c(HCO)-c(CO2-)=c(OH-)-c(H+)
2 3 3 2 3 3
【答案】C
【解析】A项,碳酸钠的水解程度大于碳酸氢钠,故碳酸钠的碱性强于碳酸氢钠,碳酸钠与盐酸反应
先生成碳酸氢钠,再产生二氧化碳气体,故图中甲、丁线表示向NaCO 溶液中滴加盐酸,乙、丙线表示向
2 3
NaHCO 溶液中滴加盐酸,A错误;B项,当滴加盐酸的体积为VmL时(a点、b点),所发生的反应为碳酸
3 1
根离子与氢离子结合生成碳酸氢根离子,离子方程式表示为:CO2-+H+= HCO -,B错误;C项,根据pH—
3 3
V(HCl)图,滴定分析时,c点的pH在9左右,符合酚酞的指示范围,故可用酚酞作指示剂;d点的pH在4
左右,符合甲基橙的指示范围,故可用甲基橙作指示剂指示滴定终点,C正确;D项,根据电荷守恒和物
料守恒,则NaCO 中存在c(OH-)-c(H+)=2c(H CO)+c(HCO-), NaHCO 溶液中满足c(HCO)-
2 3 2 3 3 3 2 3
c(CO2-)=c(OH-)-c(H+),D错误;故选C。
3
2.【2022•湖南选择性考试】为探究FeCl 的性质,进行了如下实验(FeCl 和NaSO 溶液浓度均为
3 3 2 3
)。实验 操作与现象
① 在 水中滴加2滴FeCl 溶液,呈棕黄色;煮沸,溶液变红褐色。
3
在5mL FeCl 溶液中滴加2滴NaSO 溶液,变红褐色;
3 2 3
②
再滴加K[Fe(CN) ]溶液,产生蓝色沉淀。
3 6
在5mL Na SO 溶液中滴加2滴FeCl 溶液,变红褐色;
2 3 3
将上述混合液分成两份,一份滴加K[Fe(CN) ]溶液,无蓝色沉淀生
③ 3 6
成;
另一份煮沸,产生红褐色沉淀。
依据上述实验现象,结论不合理的是( )
A.实验①说明加热促进Fe3+水解反应
B.实验②说明Fe3+既发生了水解反应,又发生了还原反应
C.实验③说明Fe3+发生了水解反应,但没有发生还原反应
D.整个实验说明SO 2-对Fe3+的水解反应无影响,但对还原反应有影响
3
【答案】D
【解析】铁离子水解显酸性,亚硫酸根离子水解显碱性,两者之间存在相互促进的水解反应,同时铁
离子具有氧化性,亚硫酸根离子具有还原性,两者还会发生氧化还原反应,在同一反应体系中,铁离子的
水解反应与还原反应共存并相互竞争,结合实验分析如下:实验①为对照实验,说明铁离子在水溶液中显
棕黄色,存在水解反应Fe3++3H O Fe(OH) +3H+,煮沸,促进水解平衡正向移动,得到红褐色的氢氧
2 3
化铁胶体;实验②说明少量亚硫酸根离子加入铁离子后,两者发生水解反应得到红褐色的氢氧化铁胶体;
根据铁氰化钾检测结果可知,同时发生氧化还原反应,使铁离子被还原为亚铁离子,而出现特征蓝色沉淀;
实验③通过反滴操作,根据现象描述可知,溶液仍存在铁离子的水解反应,但由于铁离子少量,没检测出
亚铁离子的存在,说明铁离子的水解反应速率快,铁离子的还原反应未来得及发生。A项,铁离子的水解
反应为吸热反应,加热煮沸可促进水解平衡正向移动,使水解程度加深,生成较多的氢氧化铁,从而使溶
液显红褐色,故A正确;B项,在5mLFeCl 溶液中滴加2滴同浓度的NaSO 溶液,根据现象和分析可知,
3 2 3
Fe3+既发生了水解反应,生成红褐色的氢氧化铁,又被亚硫酸根离子还原,得到亚铁离子,加入铁氰化钾
溶液后,出现特征蓝色沉淀,故B正确;C项,实验③中在5mL Na SO 溶液中滴加2滴同浓度少量FeCl
2 3 3
溶液,根据现象和分析可知,仍发生铁离子的水解反应,但未来得及发生铁离子的还原反应,即水解反应
比氧化还原反应速率快,故C正确;D项,结合三组实验,说明铁离子与亚硫酸根离子混合时,铁离子的
水解反应占主导作用,比氧化还原反应的速率快,因证据不足,不能说明亚硫酸离子对铁离子的水解作用
无影响,事实上,亚硫酸根离子水解显碱性,可促进铁离子的水解反应,故D错误。故选D。
3.(2021•天津卷)常温下,下列有关电解质溶液的叙述正确的是( )A.在0.1mol·L-1HPO 溶液中c(H PO )>c(H PO -)>c(HPO 2-)>c(PO 3-)
3 4 3 4 2 4 4 4
B.在0.1mol·L-1NaC O 溶液中c(Na+)+c(H+)= c(OH―)+c(HC O-)+c(C O2-)
2 2 4 2 4 2 4
C.在0.1mol·L-1NaHCO 溶液中c(H CO)+ c(HCO -)=0.1mol·L-1
3 2 3 3
D.氨水和NH Cl溶液混合,形成pH=9的溶液中c(Cl-)>c(NH +)>c(OH―)>c(H+)
4 4
【答案】A
【解析】A项,由于磷酸为多元酸,第一步电离大于第二步电离大于第三步电离,所以在
0.1mol·L-1HPO 溶液中,离子浓度大小为:c(H PO )>c(H PO -)>c(HPO 2-)>c(PO 3-),故A正确;B项,在
3 4 3 4 2 4 4 4
0.1mol·L-1NaC O 溶液中,根据电荷守恒得到c(Na+)+c(H+)= c(OH―)+c(HC O-)+2c(C O2-),故B错误;C
2 2 4 2 4 2 4
项,在0.1mol·L-1NaHCO 溶液中,根据物料守恒得到c(H CO)+ c(HCO -)+ c(CO2-)=0.1mol·L-1,故C错误;
3 2 3 3 3
D项,氨水和NH Cl溶液混合,形成pH=9的溶液,则c(OH―)>c(H+),根据电荷守恒c(Cl-)
4
+c(OH―)=c(NH +)+c(H+),则c(Cl-)<c(NH +),故D错误;故选A。
4 4
4.【2021•广东选择性考试】鸟嘌呤(G)是一种有机弱碱,可与盐酸反应生成盐酸盐(用GHCl表示)。
已知GHCl水溶液呈酸性,下列叙述正确的是( )
A.0.001mol·L-1GHCl水溶液的pH=3
B.0.001mol·L-1GHCl水溶液加水稀释,pH升高
C.GHCl在水中的电离方程式为:GHCl=G+HCl
D.GHCl水溶液中:c(OH-)+c(Cl-)=c(GH+)+c(G)
【答案】B
【解析】A项,GHCl为强酸弱碱盐,电离出的GH+会发生水解,弱离子的水解较为微弱,因此
0.001mol/L GHCl水溶液的pH>3,故A错误;B项,稀释GHCl溶液时,GH+水解程度将增大,根据勒夏
特列原理可知溶液中c(H+)将减小,溶液pH将升高,故B正确;C项,GHCl为强酸弱碱盐,在水中电离
方程式为GHCl=GH++Cl-,故C错误;D项,根据电荷守恒可知,GHCl溶液中c(OH-)+c(Cl-)=c(H+)
+c(GH+),故D错误;故选B。
5.【2021·浙江省6月选考】取两份10mL 0.05mol·Lˉ1的NaHCO 溶液,一份滴加0.05mol·Lˉ1的盐酸,
3
另一份滴加0.05mol·Lˉ1 NaOH溶液,溶液的pH随加入酸(或碱)体积的变化如图。下列说法不正确的是( )
A.由a点可知:NaHCO 溶液中HCO -的水解程度大于电离程度
3 3
B.a→b→c过程中:c(HCO -)+2c(CO2-)+c(OH-)逐渐减小
3 3
C.a→d→e过程中:c(Na+)<c(HCO -)+c(CO2-)+c(H CO)
3 3 2 3
D.令c点的c(Na+)+c(H+)= x,e点的c(Na+)+c(H+)=y,则x>y
【答案】C
【解析】向NaHCO 溶液中滴加盐酸,溶液酸性增强,溶液pH将逐渐减小,向NaHCO 溶液中滴加
3 3
NaOH溶液,溶液碱性增强,溶液pH将逐渐增大,因此abc曲线为向NaHCO 溶液中滴加NaOH溶液,
3
ade曲线为向NaHCO 溶液中滴加盐酸。A项,a点溶质为NaHCO ,此时溶液呈碱性,HCO -在溶液中电离
3 3 3
使溶液呈酸性,HCO -在溶液中水解使溶液呈碱性,由此可知,NaHCO 溶液中HCO -的水解程度大于电离
3 3 3
程度,故A正确;B项,由电荷守恒可知,a→b→c过程溶液中c(HCO -)+2c(CO2-)+c(OH-)= c(Na+)+c(H
3 3
+),滴加NaOH溶液的过程中c(Na+)保持不变,c(H+)逐渐减小,因此c(HCO -)+2c(CO2-)+c(OH-)逐渐减小,
3 3
故B正确;C项,由物料守恒可知,a点溶液中c(Na+)=c(HCO -)+c(CO2-)+c(H CO),向NaHCO 溶液中滴
3 3 2 3 3
加盐酸过程中有CO 逸出,因此a→d→e过程中c(Na+)>c(HCO -)+c(CO2-)+c(H CO),故C错误;D项,
2 3 3 2 3
c点溶液中c(Na+)+c(H+)=(0.05+10-11.3)mol/L,e点溶液体积增大1倍,此时溶液中c(Na+)+c(H+)=(0.025+10-
4)mol/L,因此x>y,故D正确;故选C。
6.(2020•浙江7月选考)下列说法不正确的是( )
A.2.0×10-7 mol/L的盐酸中c(H+)=2.0×10-7 mol/L
B.将KCl溶液从常温加热至800C ,溶液的pH变小但仍保持中性
C.常温下,NaCN溶液呈碱性,说明HCN是弱电解质
D.常温下,pH为3的醋酸溶液中加入醋酸钠固体,溶液pH增大
【答案】A
【解析】A项,盐酸的浓度为2.0×10-7 mol/L,完全电离,接近中性,溶剂水电离出的氢离子浓度的数量级与溶质HCl电离的氢离子浓度相差不大,则计算中氢离子浓度时,不能忽略水中的氢离子浓度,其数
值应大于2.0×10-7 mol/L,故A错误;B项, KCl溶液为中性溶液,常温下pH=7,加热到800C时,水的
离子积K 增大,对应溶液的氢离子浓度随温度升高会增大,pH会减小,但溶液溶质仍为KCl,则仍呈中
w
性,故B正确;C项,NaCN溶液显碱性,说明该溶质为弱酸强碱盐,即CN-对应的酸HCN为弱电解质,
故C正确;D项,醋酸在溶液中会发生电离平衡:CHCOOH CHCOO-+H+,向溶液中加入醋酸钠固
3 3
体,根据同离子效应可知,该平衡会向生成弱电解质的方向(逆向)移动,使溶液中的氢离子浓度减小,pH
增大,故D正确;故选A。
7.(2020•浙江 7 月选考)常温下,用 0.1 mol·L−1氨水滴定 10 mL 浓度均为 0.1 mol·L−1的 HCl 和
CHCOOH的混合液,下列说法不正确的是( )
3
A.在氨水滴定前,HCl和CHCOOH的混合液中c(Cl−)>c(CHCOO−)
3 3
B.当滴入氨水10 mL时,c(NH)+c(NH ·H O)=c(CHCOO−)+c(CHCOOH)
3 2 3 3
C.当滴入氨水20 mL时,c(CHCOOH)+c(H+)=c(NH ·H O)+c(OH−)
3 3 2
D.当溶液呈中性时,氨水滴入量大于20 mL,c(NH)<c(Cl−)
【答案】D
【解析】A项,未滴定时,溶液溶质为HCl和CHCOOH,且浓度均为0.1mol/L,HCl为强电解质,
3
完全电离,CHCOOH为弱电解质,不完全电离,故,c(Cl-)>c(CHCOO-),A正确;B项,当滴入氨水
3 3
10mL时,n(NH ·H O)=n(CHCOOH),则在同一溶液中c(NH +)+ c(NH ·H O)=c(CHCOOH)+ c(CH COO-),
3 2 3 4 3 2 3 3
B正确;C项,当滴入氨水20mL时,溶液溶质为NH Cl和CHCOONH,质子守恒为c(CHCOOH)+c(H+)=
4 3 4 3
c(NH +)+c(OH-),C正确;D项,当溶液为中性时,电荷守恒为:c(NH +)+c(H+)= c(CHCOO-)+c(Cl-)+
4 4 3
c(OH-),因为溶液为中性,则c(H+)=c(OH-),故c(NH +)>c(Cl-),D不正确;故选D。
4
8.(2020•天津卷)常温下,下列有关电解质溶液的说法错误的是( )
A.相同浓度的 HCOONa和NaF两溶液,前者的pH较大,则K(HCOOH)>K(HF)
a a
B.相同浓度的CHCOOH和CHCOONa两溶液等体积混合后pH约为4.7,则溶液中c(CHCOO-)>
3 3 3
c(Na+)>c(H+)>c(OH-)
C.FeS溶于稀硫酸,而CuS不溶于稀硫酸,则K (FeS)>K (CuS)
sp sp
D.在1 mol∙L−1 Na S溶液中,c(S2−)+c(HS-)+c(H S)=1 mol∙L−1
2 2
【答案】A
【解析】A项,HCOONa和NaF的浓度相同,HCOONa溶液的pH较大,说明HCOO-的水解程度较
大,根据越弱越水解,因此甲酸的电离平衡常数较小,即K(HCOOH)<K(HF),故A错误;B项,相同浓
a a
度的CHCOOH和CHCOONa两溶液等体积混合后pH约为4.7,此时溶液呈酸性,氢离子浓度大于氢氧根
3 3
浓度,说明溶液中醋酸电离程度大于水解程度,则醋酸根浓度大于钠离子浓度,则溶液中c(CHCOO-)>
3c(Na+)>c(H+)>c(OH-),故B正确;C项,CuS的溶解度较小,将CuS投入到稀硫酸溶液中,CuS溶解平
衡电离出的S2−不足以与H+发生反应,而将FeS投入到稀硫酸后可以得到HS气体,说明K (FeS)>
2 sp
K (CuS),故C正确;D项,根据溶液中的物料守恒定律,1 mol∙L−1 Na S溶液中所有含S元素的粒子的总
sp 2
物质的量的浓度为1 mol∙L−1,即c(S2−)+c(HS-)+c(H S)=1 mol∙L−1,故D正确;故选A。
2
9.(2020•山东卷)25℃时,某混合溶液中c(CHCOOH)+ c(CHCOO-)=c(CHCOOH)=0.1mol/L,
3 3 3
1gc( CH COOH)、1gc(CHCOO-)、lgc(H+)和1gc(OH-)随pH变化的关系如下图所示。K 为CHCOOH的电离
3 3 a 3
常数,下列说法正确的是( )
A.O点时,c(CHCOOH)=c(CHCOO-)
3 3
B.N点时,
C.该体系中,
D.pH由7到14的变化过程中, CHCOO-的水解程度始终增大
3
【答案】BC
【解析】根据图像分析可知,随着pH的升高,氢氧根离子和醋酸根离子浓度增大,氢离子和醋酸离子
浓度减小,又pH=7的时候,氢氧根离子浓度等于氢离子浓度,故可推知,图中各曲线
代表的浓度分别是:曲线1为lgc(CHCOO-)随pH的变化曲线,曲
3线2为lgc(H+)随pH的变化曲线,曲线3为lgc(OH-)随pH的变化曲线,曲线4为lgc(CHCOOH)随pH的变
3
化曲线。A项,根据上述分析可知,O点为曲线2和曲线3的交点,对应的pH=7,应该得出的结论为:
c(H+)= c(OH-),故A错误;B项,N点为曲线1和曲线4的交点, lgc(CHCOO-)=lgc(CHCOOH),即
3 3
c(CHCOO-)=c(CHCOOH),因Ka= ,代入等量关系并变形可知pH=-lgKa,故B正确;C
3 3
项,c(CHCOO-)+c(CHCOOH)=0.1mol/L,则c(CHCOO-)=0.1mol/L- c(CHCOOH),又Ka=
3 3 3 3
,联立两式消去c(CHCOO-)并化简整理可得出,c(CHCOOH)= mol/L,故C正
3 3
确;D项,醋酸根离子的水解平衡为:CHCOO-+H O CHCOOH +OH-,pH由7到14的变化过程中,
3 2 3
碱性不断增强,c(OH-)不断增大,则使不利于醋酸根离子的水解平衡,会使其水解程度减小,故D错误;
故选BC。
10.【2019•江苏卷】室温下,反应 +H O HCO+OH−的平衡常数K=2.2×10−8。将
2 2 3
NH HCO 溶液和氨水按一定比例混合,可用于浸取废渣中的ZnO。若溶液混合引起的体积变化可忽略,室
4 3
温时下列指定溶液中微粒物质的量浓度关系正确的是( )
A.0.2mol·L−1氨水:c(NH ·H O)>c(NH +)>c(OH−)>c(H+)
3 2 4
B.0.2mol·L−1NH HCO 溶液(pH>7):c(NH +)>c(HCO -)>c(H CO)>c(NH ·H O)
4 3 4 3 2 3 3 2
C.0.2mol·L−1氨水和0.2mol·L−1NH HCO 溶液等体积混合:c(NH +)+c(NH ·H O)=c(H CO)+c(HCO -)
4 3 4 3 2 2 3 3
+c(CO2-)
3
D.0.6mol·L−1氨水和0.2mol·L−1NH HCO 溶液等体积混合:c(NH ·H O)+c(CO2-)
4 3 3 2 3
+c(OH−)=0.3mol·L−1+c(H CO)+c(H+)
2 3
【答案】BD
【解析】A.NH ∙HO 属于弱电解,部分电离,氨水中存在的电离平衡有:NH ∙HO NH +
3 2 3 2 4
+OH-,HO H++OH-,所以c(OH-)>c(NH+),故A错误;B.NH HCO 溶液显碱性,说明HCO -的水
2 4 4 3 3
解程度大于NH +的水解,所以c(NH +)>c(HCO-),HCO -水解:HCO - HCO+OH-,NH +水解:NH +
4 4 3 3 3 2 3 4 4
+H O NH ∙HO+H+,前者水解程度大,则 c(HCO)>c(NH∙HO),故 B 正确;C.由物料守恒,
2 3 2 2 3 3 2
n(N):n(C)=2:1,则有c(NH +)+c(NH∙HO)=2[c(HCO)+c(HCO-)+c(CO 2-)],故C错误;D.由物料守恒,
4 3 2 2 3 3 3
n(N):n(C)=4:1,则有 c(NH +)+c(NH∙HO)=4[c(HCO)+c(HCO-)+c(CO 2-)]①;电荷守恒有:c(NH +)
4 3 2 2 3 3 3 4
+c(H+)=c(HCO-)+2c(CO 2-)+c(OH-)② ; 结 合 ① ② 消 去 c(NH +) 得 : c(NH ∙HO)+c(OH-)=c(H+)
3 3 4 3 2+4c(H CO)+3c(HCO-)+2c(CO 2-)③,0.2mol/LNH HCO 与氨水等体积混合后,c(NH HCO )=0.1mol/L,由碳
2 3 3 3 4 3 4 3
守恒有,c(HCO)+c(HCO-)+c(CO 2-)=0.1mol/L④,将③等式两边各加一个 c(CO2-),则有 c(NH ∙HO)
2 3 3 3 3 3 2
+c(OH-)+c(CO 2-)=c(H+)+c(H CO)+3c(H CO)+3c(HCO-)+3c(CO 2-),将④带入③中得,c(NH ∙HO)+c(OH-)
3 2 3 2 3 3 3 3 2
+c(CO 2-)=c(H+)+3c(H CO)+0.3mol/L,故D正确;故选BD。
3 2 3
11.【2019•浙江4月选考】室温下,取20 mL 0.1 mol·L−1某二元酸HA,滴加0.1 mol·L−1 NaOH溶液。
2
已知:HA H++HA−,HA− H++A2−。下列说法不正确的是( )
2
A.0.1 mol·L−1 HA溶液中⇌有c(H+)-c(OH−)-c(A2−)=0.1 mol·L−1
2
B.当滴加至中性时,溶液中c(Na+)=c(HA−)+2c(A2−),用去NaOH溶液的体积小于10 mL
C.当用去NaOH溶液体积10 mL时,溶液的pH<7,此时溶液中有c(A2−)=c(H+)-c(OH−)
D.当用去NaOH溶液体积20 mL时,此时溶液中有c(Na+)=2c(HA−)+2c(A2−)
【答案】B
【解析】由于该二元酸 HA,第一步电离完全,第二步部分电离,可以把 20 mL 0.1 mol·L−1二元酸
2
HA看做20 mL 0.1 mol·L−1HA-一元弱酸和 0.1mol/LH+溶液,注意该溶液是不存在 HA微粒。A. 0.1
2 2
mol·L−1HA溶液存在电荷守恒,其关系为c(H+)=c(OH−)+2c(A2−)+ c(HA−),因而c(H+)-c(OH−)-c(A2−)= c(A2−)
2
+c(HA−)=0.1mol·L−1,A项正确;B.若NaOH用去10ml,反应得到NaHA溶液,由于HA− H++A2−,溶
液显酸性,因而滴加至中性时,需要加入超过10ml的NaOH溶液,B项错误;C.当用去N⇌aOH溶液体积
10 mL时,得到NaHA溶液,溶液的pH<7,存在质子守恒,其关系为c(A2−)=c(H+)-c(OH−),C项正确;
D.当用去NaOH溶液体积20 mL时,得到NaA溶液,根据物料守恒有:c(Na+)=2c(HA−)+2c(A2−),D项
2
正确。故选B。
12.【2019•上海等级考】常温下0.1mol/L ①CHCOOH、②NaOH、③CHCOONa,下列叙述正确的
3 3
是( )
A.①中c(CHCOOH)> c(CHCOO-)> c(H+)> c(OH-)
3 3
B.①②等体积混合后,醋酸根离子浓度小于③的二分之一
C.①③等体积混合以后,溶液呈酸性,则c(Na+)> c(CHCOO-)> c(H+)
3
D.①②等体积混合以后,水的电离程度比①③等体积混合的电离程度小
【答案】 B
【解析】A.CHCOOH溶液中的H+来自醋酸分子的电离和水的电离,所以 c(CHCOOH)> c(H+)>
3 3
c(CHCOO-)> c(OH-)故A错误;B.①②等体积混合后恰好反应生成CHCOONa,体积大约为原来的2倍,
3 3
如果 CHCOO-不水解,浓度约为原来的 1/2,CHCOONa 为弱酸强碱盐,越稀越水解,CHCOO-
3 3 3
+H O→CH COOH+OH-,水解平衡向正向移动,因此CHCOO-浓度小于原来的1/2.B正确;C.①③等体积
2 3 3
混 合 以 后 , 溶 液 呈 酸 性 , 说 明 CHCOOH 的 电 离 程 度 大 于 CHCOO- 的 水 解 程 度 , 因 此
3 3(CHCOO-)>(Na+)>(H+),C错误;D.①②等体积混合以后恰好反应生成CHCOONa,CHCOO- 的水解促
3 3 3
进水的电离。①③等体积混合,CHCOOH的电离产生H+抑制水的电离。因此总体上看①②等体积混合后
3
水的电离程度比①③等体积混和后水的电离程度大。D错误。
13.【2018•江苏卷】HC O 为二元弱酸,K (H C O ) =5.4×10−2,K (H C O ) =5.4×10−5,设
2 2 4 a1 2 2 4 a2 2 2 4
HC O 溶液中 c(总)=c(H C O) +c(HC O−) +c(C O2−)。室温下用 NaOH 溶液滴定 25.00 mL 0.1000
2 2 4 2 2 4 2 4 2 4
mol·L−1HC O 溶液至终点。滴定过程得到的下列溶液中微粒的物质的量浓度关系一定正确的是( )
2 2 4
A.0.1000 mol·L−1 HC O 溶液:c(H+ ) =0.1000 mol·L−1+c(C O2− )+c(OH−)−c(H C O )
2 2 4 2 4 2 2 4
B.c(Na+ ) =c(总)的溶液:c(Na+ ) >c(H C O ) >c(C O2− ) >c(H+ )
2 2 4 2 4
C.pH = 7的溶液:c(Na+ ) =0.1000 mol·L−1+ c(C O2−) −c(H C O)
2 4 2 2 4
D.c(Na+ ) =2c(总)的溶液:c(OH−) −c(H+) = 2c(H C O) +c(HC O−)
2 2 4 2 4
【答案】AD
【解析】A项,HC O 溶液中的电荷守恒为c(H+)=c(HC O-)+2c(C O2-)+c(OH-),0.1000 mol·L−1HC O
2 2 4 2 4 2 4 2 2 4
溶液中 0.1000mol/L=c(H C O)+ c(HC O-)+ c(C O2-),两式整理得 c(H+)=0.1000mol/L-c(H C O)+c(C O2-)
2 2 4 2 4 2 4 2 2 4 2 4
+c(OH-),A项正确;B项,c(Na+)=c(总)时溶液中溶质为NaHC O ,HC O-既存在电离平衡又存在水解平衡,
2 4 2 4
HC O-水解的离子方程式为HC O-+H O HC O+OH-,HC O-水解常数K= =
2 4 2 4 2 2 2 4 2 4 h
= = =1.85 10-13 K (H C O),HC O-的电离程度
a2 2 2 4 2 4
大于水解程度,则 c(C O2-) c(HC O),B项错误;C项,滴入 NaOH溶液后,溶液中的电荷守恒为
2 4 2 2 4
c(Na+)+c(H+)=c(HC O-)+2c(C O2-)+c(OH-) , 室 温 pH=7 即 c(H+)=c(OH-) , 则 c(Na+)=c(HC O-)
2 4 2 4 2 4
+2c(C O2-)=c(总)+c(C O2-)-c(HC O),由于溶液体积变大,c(总) 0.1000mol/L,c(Na+)=0.1000mol/L
2 4 2 4 2 2 4
+c(C O2-)-c(HC O),C 项错误;D 项,c(Na+)=2c(总)时溶液中溶质为 NaC O ,溶液中的电荷守恒为
2 4 2 2 4 2 2 4
c(Na+)+c(H+)=c(HC O-)+2c(C O2-)+c(OH-),物料守恒为c(Na+)=2[c(H C O) + c(HC O-)+ c(C O2-)],两式整
2 4 2 4 2 2 4 2 4 2 4
理得c(OH-)-c(H+)=2c(H C O)+c(HC O-),D项正确;答案选AD。
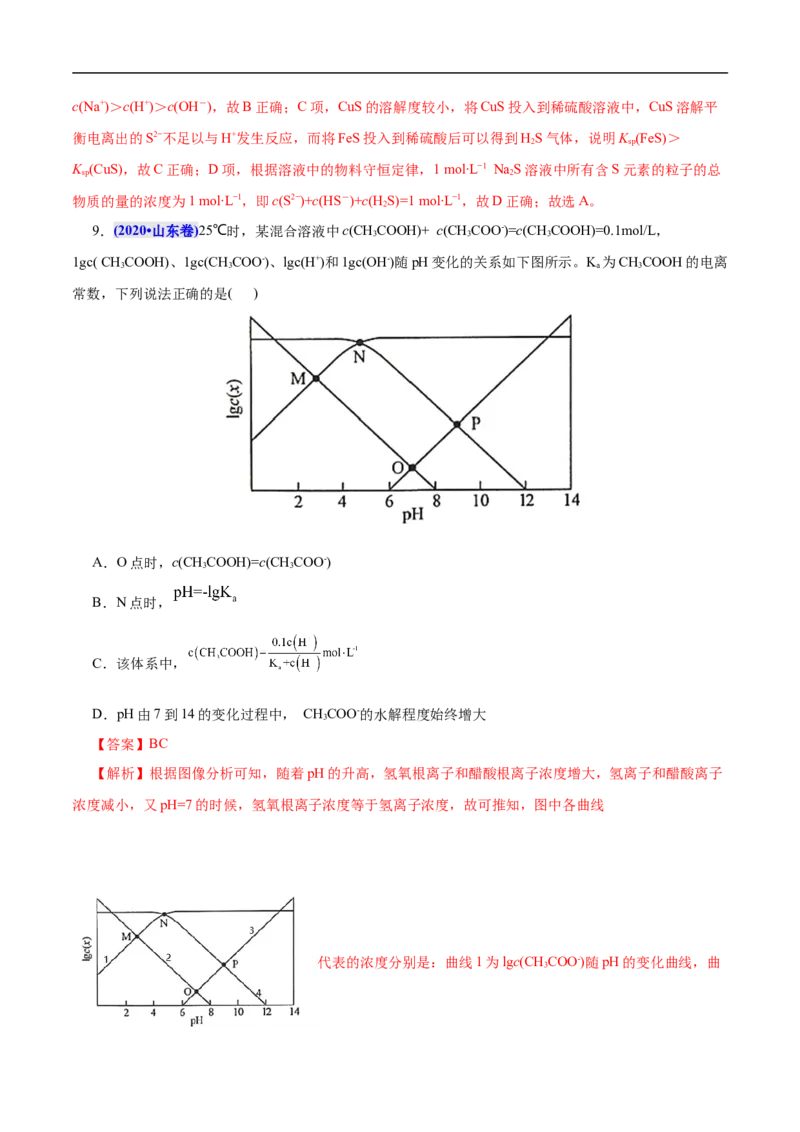
2 2 4 2 4
14.【2017•全国Ⅰ卷】常温下将NaOH溶液滴加到己二酸(H X)溶液中,混合溶液的pH与离子浓度变
2
化的关系如图所示。下列叙述错误的是( )A.K (H X)的数量级为10-6
a2 2
B.曲线N表示pH与lg的变化关系
C.NaHX溶液中c(H+)>c(OH-)
D.当混合溶液呈中性时,c(Na+)>c(HX-)>c(X2-)>c(OH-)=c(H+)
【答案】D
【解析】横坐标取0时,曲线M对应pH约为5.4,曲线N对应pH约为4.4,因为是NaOH滴定HX
2
溶液,所以在酸性较强的溶液中会存在c(HX-)=c(H X),所以曲线N表示pH与lg的变化关系,B正确;
2
=1时,即lg=0,pH=5.4,c(H+)=1×10-5.4 mol·L-1,K =≈1×10-5.4,A正确;NaHX溶液中,c(HX
a2
-)>c(X2-),即<1,lg<0,此时溶液呈酸性,C正确;当溶液呈中性时,由曲线M可知lg>0,>1,即c(X2
-)>c(HX-),D错误。
15.【2016•四川卷】向1 L含0.01 mol NaAlO 和0.02 mol NaOH的溶液中缓慢通入CO ,随n(CO)增
2 2 2
大,先后发生三个不同的反应,当 0.01 molc(AlO)+c(OH-)
B 0.01 c(Na+)>c(AlO)> c(OH-)>c(CO)
C 0.015 c(Na+)>c(HCO)> c(CO)>c(OH-)
D 0.03 c(Na+)>c(HCO)> c(OH-)>c(H+)
【答案】D
【解析】当n(CO)=0 mol时,c(Na+)c(CO)>c(AlO)>c(OH-),B
项错误;当 n(CO)=0.015 mol 时,溶液中的溶质仅为 NaCO ,则溶液中离子浓度关系为 c(Na
2 2 3
+)>c(CO)>c(OH-)>c(HCO),C项错误;当n(CO)=0.03 mol时,溶液中的溶质仅为NaHCO ,则溶液中离
2 3
子浓度关系为c(Na+)>c(HCO)>c(OH-)>c(H+),D项正确。