文档内容
考点巩固卷 13 化学实验基础(二)
考点 题型
考点一 物质的制备 非选择题(10题)
考点二 定量分析与测定 非选择题(10题)
考点三 探究性实验 非选择题(10题)
考点一 物质的制备 分值:100分 建议用时:50分钟
1.(2023·全国甲卷·统考高考真题)钴配合物 溶于热水,在冷水中微溶,可通过如下反应
制备: 。
具体步骤如下:
Ⅰ.称取 ,用 水溶解。
Ⅱ.分批加入 后,将溶液温度降至 以下,加入 活性炭、 浓氨水,搅拌下逐滴
加入 的双氧水。
Ⅲ.加热至 反应 。冷却,过滤。
Ⅳ.将滤得的固体转入含有少量盐酸的 沸水中,趁热过滤。
Ⅴ.滤液转入烧杯,加入 浓盐酸,冷却、过滤、干燥,得到橙黄色晶体。
回答下列问题:
(1)步骤Ⅰ中使用的部分仪器如下。
资料收集整理【淘宝店铺:向阳百分百】仪器a的名称是 。加快NH Cl溶解的操作有 。
4
(2)步骤Ⅱ中,将温度降至10℃以下以避免 、 ;可选用 降低溶液温度。
(3)指出下列过滤操作中不规范之处: 。
(4)步骤Ⅳ中,趁热过滤,除掉的不溶物主要为 。
(5)步骤Ⅴ中加入浓盐酸的目的是 。
2.(2023·云南·校联考二模)阿司匹林( )是被广泛应用的解热镇痛和抗凝药。在实验
室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH CO) O] 为主要原料合成阿司匹林,设计如下实验步骤:
3 2
①取反应物:取适量水杨酸、酷酸酐、浓硫酸加入反应容器,混合摇匀;
②合成:控制温度为85°C ~90°C加热10分钟后,冷却反应液、过滤、洗涤得粗产品;
③提纯。
已知:
名称 相对分子质量 相关性质
水杨酸 138 熔点15°C,微溶于水
醋酸酐 102 沸点139.4°C,与水激烈反应生成醋酸
乙酰水杨酸 180 熔点135°C,128~ 135°C分解,微溶于水
请根据以上信息回答下列问题:
资料收集整理【淘宝店铺:向阳百分百】(1)取反应物前应先向反应容器中加入 。
(2)合成应在 (填“无水”或“有水”)条件下进行,最合适的加热方法是 。
(3)冷却反应液后,发现无晶体析出,此时可采取的措施是 。
(4)I.提纯时,先加入少量的NaHCO 溶液后过滤,再向固体中加盐酸酸化,冷却、过滤、洗涤、干燥后得到
3
较纯的阿司匹林。判断洗涤干净的方法是 。
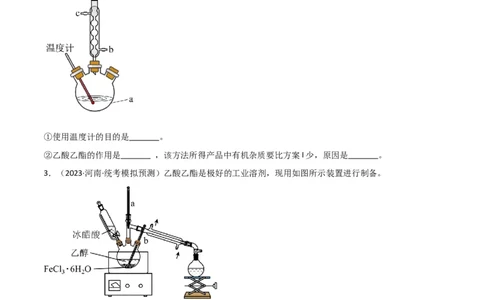
II.另一种提纯方法是将粗产品与乙酸乙酯、沸石混合后加热回流,趁热过滤、冷却过滤、洗涤干燥。其中
回流的装置如图所示:
①使用温度计的目的是 。
②乙酸乙酯的作用是 ,该方法所得产品中有机杂质要比方案I少,原因是 。
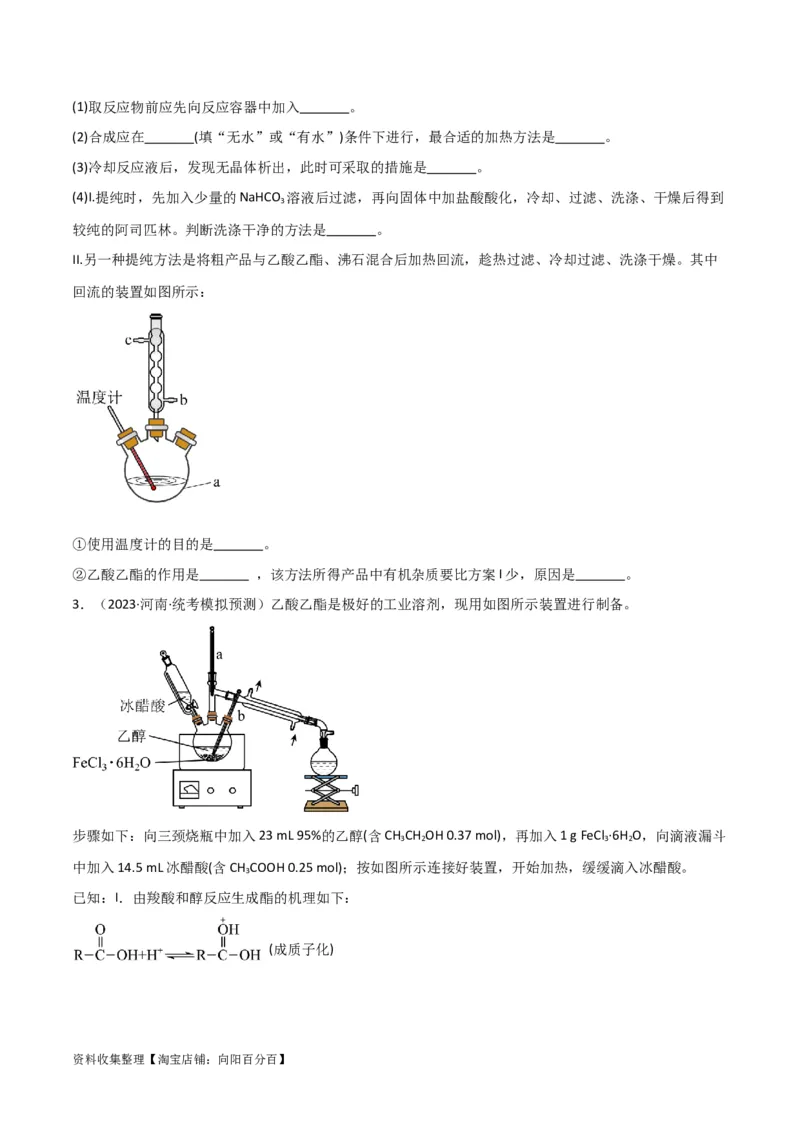
3.(2023·河南·统考模拟预测)乙酸乙酯是极好的工业溶剂,现用如图所示装置进行制备。
步骤如下:向三颈烧瓶中加入23 mL 95%的乙醇(含CH CH OH 0.37 mol),再加入1 g FeCl ·6H O,向滴液漏斗
3 2 3 2
中加入14.5 mL冰醋酸(含CH COOH 0.25 mol);按如图所示连接好装置,开始加热,缓缓滴入冰醋酸。
3
已知:I.由羧酸和醇反应生成酯的机理如下:
(成质子化)
资料收集整理【淘宝店铺:向阳百分百】(脱质子化)
II.乙醇可与CaCl 结合形成CaCl ·6C H OH难溶物。
2 2 2 5
(1)实验中乙醇要过量的目的是 。
(2)实验中三颈烧瓶适合的容积为___________(填字母)。
A.50mL B.100 mL C.250 mL D.500 mL
(3)实验温度为80℃时产率最高,此时需要观察温度计 ( 填“a”或“b”)的读数,另一只温度计
在 操作中使用。
(4)选用FeCl ·6H O作为催化剂,可不加入碎瓷片,原因是 。根据羧酸和醇生成酯的反应机理推
3 2
测,下列物质中可用作制备乙酸乙酯催化剂的是 (填字母)。
A.NaOH B.BaCl C.FeSO D.HIO (固体)
2 4 4
(5)对得到的粗产品提纯:
①向粗产品中加入碳酸钠粉末,至无 气体逸出。
②向其中加入饱和氯化钙溶液,以除去
③向所得有机层中加入无水硫酸钠,以除去 ,过滤后再蒸馏,收集77℃左右的馏分。
4.(2023·湖北武汉·湖北省武昌实验中学校考模拟预测)[Co(NH ) ]Cl (三氯化六氨合钴)属于经典配合物,
3 6 3
实验室以Co为原料制备[Co(NH ) ]Cl 的方法和过程如下:
3 6 3
I.制备CoCl
2
已知:钴单质与氯气在加热条件下反应可制得纯净CoCl ,钴单质在300℃以上易被氧气氧化;CoCl 熔点为
2 2
86℃,易潮解。制备装置如图:
(1)试剂X通常是 (填名称)。
(2)试剂Z的作用为 。
(3)为了获得更纯净的CoCl ,开始点燃N处酒精喷灯的标志是 。
2
资料收集整理【淘宝店铺:向阳百分百】II.制备[Co(NH ) ]Cl ——配合、氧化
3 6 3
已知:①Co2+不易被氧化;[Co(NH ) ]2+具有较强还原性,[Co(NH ) ]3+性质稳定。
3 6 3 6
②[Co(NH ) ]Cl 在水中的溶解度曲线如图所示:
3 6 3
③加入少量浓盐酸有利于[Co(NH ) ]Cl 析出。
3 6 3
(4)按图组装好装置→_______(填序号,下同)→打开磁力搅拌器→控制温度在10℃以下
→_______→_______→加热至60℃左右,恒温20min→在冰水中冷却所得混合物,即有晶体析出(粗产品)。
①缓慢加入H O 溶液
2 2
②滴加稍过量的浓氨水
③向三颈烧瓶中加入活性炭、CoCl 、NH Cl和适量水
2 4
(5)氧化阶段发生反应的离子方程式为 。
(6)粗产品可用重结晶法提纯:向粗产品中加入80℃左右的热水,充分搅拌后, ,冷却后向滤液中加
入少量 ,边加边搅拌,充分静置后过滤,用无水乙醇洗涤晶体2~3次,低温干燥,得纯产品
[Co(NH ) ]Cl 。
3 6 3
5.(2023·辽宁鞍山·鞍山一中校考模拟预测)硫代硫酸钠( )可用作分析试剂及还原剂,受热、遇酸
均易分解。学习小组用如图装置,利用绿矾受热分解生成的 气体制备硫代硫酸钠。
资料收集整理【淘宝店铺:向阳百分百】已知:
①绿矾受热分解反应为: ;
② 的沸点为44.8℃。
回答下列问题:
(1)完成实验操作过程:
连接装置, ,加入药品( 和 混合溶液用煮沸过的蒸馏水配制),使所有活塞处于关
闭状态。开始制备,打开某些活塞,通入一段时间 ;关闭活塞 ,打开活塞 ,加
热绿矾;使用pH传感器始终观测C处溶液的pH,在pH7~8之间时停止加热,同时关闭活塞 ;……将锥
形瓶用热水浴浓缩至水层表面出现结晶为止,经过 、过滤、洗涤、干燥得到 晶体。
(2)写出锥形瓶中发生反应的离子方程式 。
(3)装置B的作用为 。
(4)将锥形瓶中的反应停止在pH传感器的读数为7~8时的原因是 。
(5)该装置存在一个明显的缺点,请提出改进方法 。
6.(2023·天津河东·统考二模)某实验小组拟在实验室模拟工业合成氨,并进行氨的催化氧化。
I.实验室模拟合成氨的流程如下:
资料收集整理【淘宝店铺:向阳百分百】已知实验室可用饱和亚硝酸钠(NaNO )溶液与饱和氯化铵溶液经加热后反应制取氮气。
2
(1)图中制取氮气的装置是 ;制取氢气的装置是 。
(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有 、 。
(3)原料气通入合成装置合成氨的化学反应方程式是 。
Ⅱ.氨的催化氧化
(4)乙装置的名称是 。
(5)氨合成器出来经冷却的气体连续通入乙装置的水中吸收氨, (“会”或“不会”)发生倒吸,原因是
(6)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持
红热的原因是 ,锥形瓶中还可观察到的现象是 。
(7)反应结束后锥形瓶内的溶液中含有 、 、 、 离子。
7.(2023·福建厦门·厦门一中校考三模)在无水三氯化铝的催化作用下,利用乙醇制备乙烯的反应温度是
。某兴趣小组据此设计如下图所示实验,合成无水 并完成乙烯的制备及收集。
Ⅰ.无水 的制备
(1) 中盛装浓盐酸的仪器名称为 。
(2)装置 中发生的化学方程式为 。
资料收集整理【淘宝店铺:向阳百分百】(3)硬质玻璃管直接接入收集器的优点是 。
(4)装置F中的药品名称是 。
Ⅱ.乙烯的制备及收集
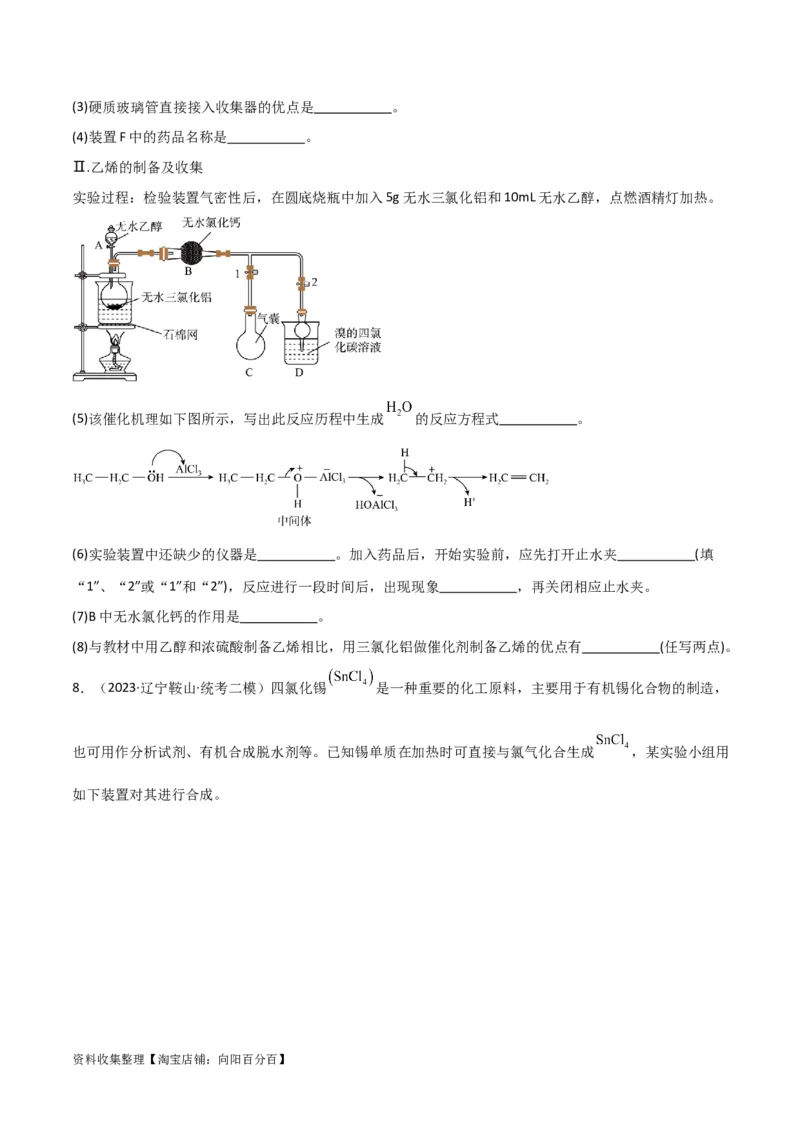
实验过程:检验装置气密性后,在圆底烧瓶中加入5g无水三氯化铝和10mL无水乙醇,点燃酒精灯加热。
(5)该催化机理如下图所示,写出此反应历程中生成 的反应方程式 。
(6)实验装置中还缺少的仪器是 。加入药品后,开始实验前,应先打开止水夹 (填
“1”、“2”或“1”和“2”),反应进行一段时间后,出现现象 ,再关闭相应止水夹。
(7)B中无水氯化钙的作用是 。
(8)与教材中用乙醇和浓硫酸制备乙烯相比,用三氯化铝做催化剂制备乙烯的优点有 (任写两点)。
8.(2023·辽宁鞍山·统考二模)四氯化锡 是一种重要的化工原料,主要用于有机锡化合物的制造,
也可用作分析试剂、有机合成脱水剂等。已知锡单质在加热时可直接与氯气化合生成 ,某实验小组用
如下装置对其进行合成。
资料收集整理【淘宝店铺:向阳百分百】【相关药品性质】
药品 颜色、状态 熔点(℃) 沸点(℃) 其他性质
较活泼金属能与 、 等气体发生反
银白色固体 231 2260
应
无色液体 114 极易水解产生 溶胶
请回答下列问题:
(1)仪器A的名称是 ;
(2)写出 水解的化学方程式 。将少量 置于空气中可观察到的现象是 ;
(3)检验装置气密性后,向A中装入 固体,小试管D内装入 片,恒压滴液漏斗中加入浓盐酸,
(填“操作”及“现象”),点燃酒精灯开始反应;
(4)若无洗气瓶B,可能会导致的问题是 ;洗气瓶C中所盛放的药品是 ;
(5)试验结束后,小试管E内收集到的液体呈淡黄色,其原因是 ;
(6)碳与锡可形成多种氯化物,其沸点如下:
氯化物
沸点(℃) 76 623(分解)* 114
*注: 加热至623℃,未沸腾直接分解
解释表中氯化物沸点差异的原因 。
9.(2023·四川达州·统考二模)某重金属离子处理剂M(Na CS ·xH O)为红色固体,易溶于水,性质与碳酸钠
2 3 2
类似,水溶液显碱性,在空气中易被氧化。
Ⅰ.M的制备:
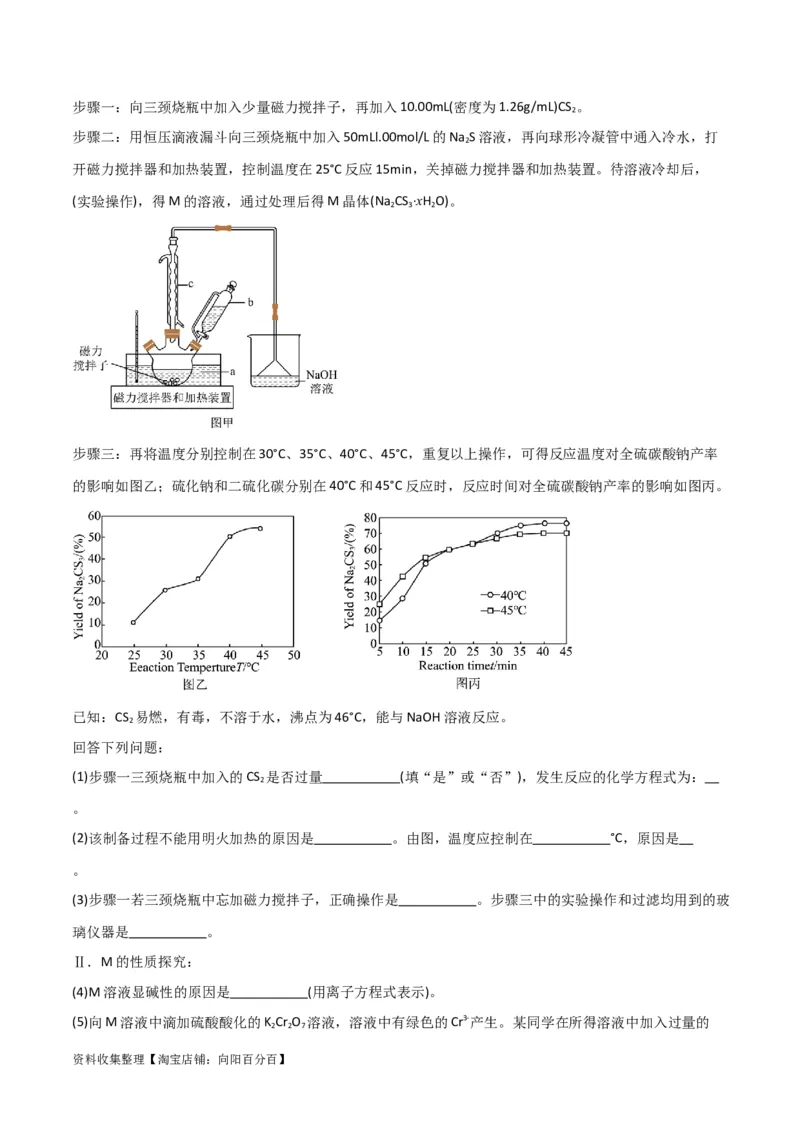
资料收集整理【淘宝店铺:向阳百分百】步骤一:向三颈烧瓶中加入少量磁力搅拌子,再加入10.00mL(密度为1.26g/mL)CS 。
2
步骤二:用恒压滴液漏斗向三颈烧瓶中加入50mLl.00mol/L的Na S溶液,再向球形冷凝管中通入冷水,打
2
开磁力搅拌器和加热装置,控制温度在25°C反应15min,关掉磁力搅拌器和加热装置。待溶液冷却后,
(实验操作),得M的溶液,通过处理后得M晶体(Na CS ·xH O)。
2 3 2
步骤三:再将温度分别控制在30°C、35°C、40°C、45°C,重复以上操作,可得反应温度对全硫碳酸钠产率
的影响如图乙;硫化钠和二硫化碳分别在40°C和45°C反应时,反应时间对全硫碳酸钠产率的影响如图丙。
已知:CS 易燃,有毒,不溶于水,沸点为46°C,能与NaOH溶液反应。
2
回答下列问题:
(1)步骤一三颈烧瓶中加入的CS 是否过量 (填“是”或“否”),发生反应的化学方程式为:
2
。
(2)该制备过程不能用明火加热的原因是 。由图,温度应控制在 °C,原因是
。
(3)步骤一若三颈烧瓶中忘加磁力搅拌子,正确操作是 。步骤三中的实验操作和过滤均用到的玻
璃仪器是 。
Ⅱ.M的性质探究:
(4)M溶液显碱性的原因是 (用离子方程式表示)。
(5)向M溶液中滴加硫酸酸化的K Cr O 溶液,溶液中有绿色的Cr3-产生。某同学在所得溶液中加入过量的
2 2 7
资料收集整理【淘宝店铺:向阳百分百】BaCl 溶液,通过测定产生的白色沉淀的质量来求所用Na CS 质量,你是否同意他的观点 (填
2 2 3
“是”或“否”),理由是 。
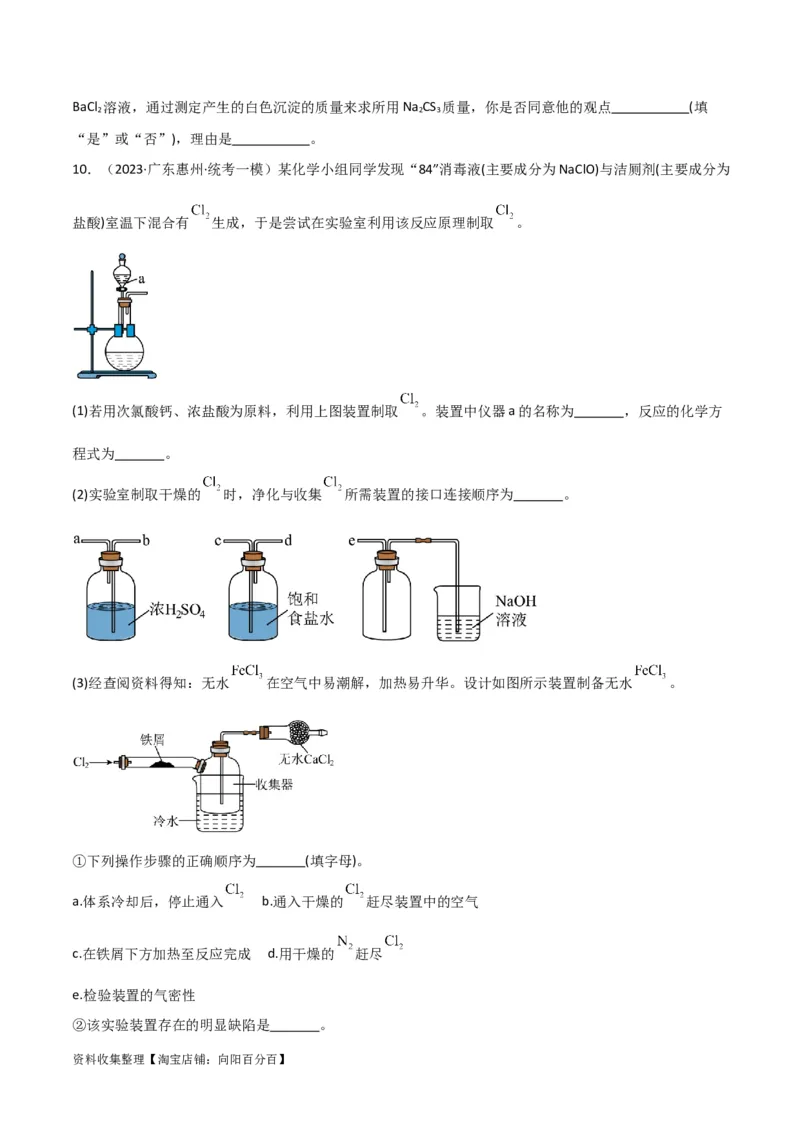
10.(2023·广东惠州·统考一模)某化学小组同学发现“84”消毒液(主要成分为NaClO)与洁厕剂(主要成分为
盐酸)室温下混合有 生成,于是尝试在实验室利用该反应原理制取 。
(1)若用次氯酸钙、浓盐酸为原料,利用上图装置制取 。装置中仪器a的名称为 ,反应的化学方
程式为 。
(2)实验室制取干燥的 时,净化与收集 所需装置的接口连接顺序为 。
(3)经查阅资料得知:无水 在空气中易潮解,加热易升华。设计如图所示装置制备无水 。
①下列操作步骤的正确顺序为 (填字母)。
a.体系冷却后,停止通入 b.通入干燥的 赶尽装置中的空气
c.在铁屑下方加热至反应完成 d.用干燥的 赶尽
e.检验装置的气密性
②该实验装置存在的明显缺陷是 。
资料收集整理【淘宝店铺:向阳百分百】(4)世界环保联盟要求 逐渐取代 作为自来水消毒剂。
已知: , 。
有关物质的熔、沸点如下表:
物质 熔点/℃ 沸点/℃
-59 11
-107 -34.6
的生产流程示意图如下:
该工艺中,需要补充的物质X为 (填化学式,下同),能参与循环的物质是 。从 发生器
中分离出 ,可采用的方法是 。
考点二 定量分析与测定 分值:100分 建议用时:50分钟
1.(2023·山西·校联考模拟预测)氯化亚铜(CuCl)可用作催化剂、杀菌剂和脱色剂,实验室制备CuCl实验
步骤如下:
资料收集整理【淘宝店铺:向阳百分百】回答下列问题:
(1)步骤I中,配制0.50 mol/LCuCl 溶液时,不需要使用下列仪器中的 (填仪器名称)。
2
(2)步骤Ⅱ中,充分反应后铜元素转化为无色的[CuCl ]-,其发生可逆反应的离子方程式为 。在加
2
Cu粉前,通常加一定量的NaCl固体,其目的是 。
(3)在进行制备[CuCl ]- 的实验时,为保持安全的实验环境,可以采取的措施是 。
2
(4)步骤Ⅲ中,用无水乙醇洗涤沉淀的原因是 。
(5)取2.500 g CuCl产品于锥形瓶中,加入稍过量的FeCl 溶液充分反应,再加50 mL水,以邻菲哕啉作指示剂,
3
用1.000 mol/L Ce(SO ) 标准溶液滴定Fe2+,分析样品中CuCl的含量。
4 2
已知:滴定原理: Ce4+ +Fe2+ =Ce3++Fe3+; 邻菲哕啉可分别与Fe3+、Fe2+形成浅蓝色和红色的络离子。
①“再加50mL水”的目的是 。
②滴定终点的现象是 。
③若消耗Ce(SO ) 标准溶液的体积为24.00 mL,该样品中CuCl的质量分数是 。
4 2
2.(2023·山东济南·山东省实验中学校考模拟预测)NaNH 是制取靛青染料的原料,易与水、氧气等反应,
2
在液氨中几乎不溶解。实验室用如图装置(夹持、搅拌、尾气处理装置已省略)制备氨基钠(NaNH ),步骤如
2
下:
Ⅰ.A中加入100mL液氨和0.05gFe(NO ) ·9H O,通入氨气排尽密闭体系中的空气,搅拌。
3 3 2
Ⅱ.加入5g钠粒,反应,得NaNH 小颗粒物。
2
Ⅲ.除去液氨,得产品NaNH
2。
实验过程中可能发生的反应:
2Na+2NH =2NaNH +H ↑
3 2 2
资料收集整理【淘宝店铺:向阳百分百】NaNH +H O=NaOH+NH ↑
2 2 3
4NaNH +3O =2NaOH+2NaNO +2NH ↑
2 2 2 3
回答下列问题:
(1)Fe(NO ) ·9H O的作用是 ;装置B的作用是 。
3 3 2
(2)设计实验方案判断步骤Ⅰ中密闭体系中空气是否排尽: 。
(3)步骤Ⅱ,反应速率应保持在液氨微沸为宜。为防止速率过大,可采取的措施为 (写出一条即
可)。
(4)下列说法错误的是___________(填标号)。
A.步骤Ⅰ中,搅拌的目的是使Fe(NO ) ·9H O均匀地分散在液氨中
3 3 2
B.步骤Ⅱ中,为判断反应是否已完成,可在N处点火,如无火焰,则反应已完成
C.步骤Ⅲ中,为避免污染,应在通风橱内抽滤除去液氨,得到产品NaNH
2
D.产品NaNH 应密封保存于充满干燥氮气的瓶中
2
(5)产品分析:经分析,NaNH 中只含NaOH杂质,可采用如下方法测定产品NaNH 纯度:准确称取产品
2 2
NaNH xg→____→____→____→计算。请选择最佳操作并排序 。
2
a.准确加入过量的水
b.准确加入过量的HCl标准溶液
c.准确加入过量的NH Cl标准溶液
4
d.用NaOH标准溶液滴定
e.用NH Cl标准溶液滴定
4
f.用HCl标准溶液滴定
g.滴加石蕊指示剂
h.滴加酚酞指示剂
i.滴加甲基红指示剂(变色的pH范围4.4~6.2)
3.(2023·辽宁沈阳·辽宁实验中学校考模拟预测)高锰酸钾具有强氧化性,广泛应用于化工、医药、金属
冶炼等领域。实验室可通过固体碱溶氧化法制备高锰酸钾。回答下列问题:
(1)将 和0.09mol KOH置于铁坩埚中并混合均匀,加热混合物至熔融。加热铁坩埚时,图中的
实验仪器还需要 (填仪器名称)。
资料收集整理【淘宝店铺:向阳百分百】(2)将 分多次加入熔融物中,继续加热,反应剧烈,最终得到墨绿色 。该步反应的化学
方程式为 ,分多次加入 的原因是 。
(3)待铁坩埚冷却后,将其置于蒸馏水中共煮至固体全部溶解。趁热向浸取液中通入 ,使 (绿色)
歧化为 与 。用玻璃棒蘸取溶液于滤纸上,观察到只有紫红色没有绿色痕迹时,表明转化已完
全。静置片刻,抽滤。下表是部分化合物溶解度随温度变化的数据, 不宜通入过多,原因是
。
温度/℃ 20 30 40 50
110 114 117 121
33.7 39.9 47.5 65.6
该步骤除了可以用 ,还可以选择哪种酸 。
A.HCl B. C.
(4)水浴加热滤液至出现 晶膜,冷却后抽滤、干燥晶体。利用水浴加热而不采取直接加热滤液的原因
是 。
(5)产品经纯化后称重,质量为3.60g。本实验中 的产率为 %(保留三位有效数字)。
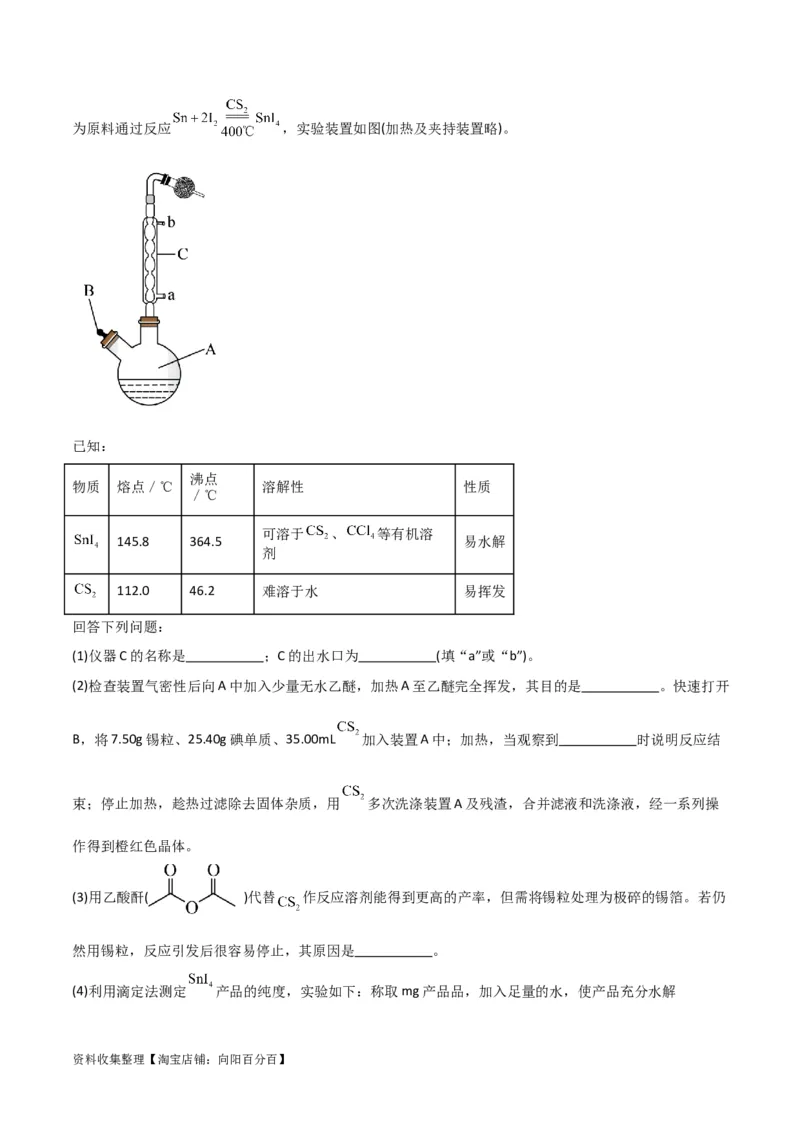
4.(2023·山东烟台·统考二模)四碘化锡为橙红色晶体,广泛应用于黑磷烯材料的制备。实验室常以锡粒
资料收集整理【淘宝店铺:向阳百分百】为原料通过反应 ,实验装置如图(加热及夹持装置略)。
已知:
沸点
物质 熔点/℃ 溶解性 性质
/℃
可溶于 、 等有机溶
145.8 364.5 易水解
剂
112.0 46.2 难溶于水 易挥发
回答下列问题:
(1)仪器C的名称是 ;C的出水口为 (填“a”或“b”)。
(2)检查装置气密性后向A中加入少量无水乙醚,加热A至乙醚完全挥发,其目的是 。快速打开
B,将7.50g锡粒、25.40g碘单质、35.00mL 加入装置A中;加热,当观察到 时说明反应结
束;停止加热,趁热过滤除去固体杂质,用 多次洗涤装置A及残渣,合并滤液和洗涤液,经一系列操
作得到橙红色晶体。
(3)用乙酸酐( )代替 作反应溶剂能得到更高的产率,但需将锡粒处理为极碎的锡箔。若仍
然用锡粒,反应引发后很容易停止,其原因是 。
(4)利用滴定法测定 产品的纯度,实验如下:称取mg产品品,加入足量的水,使产品充分水解
资料收集整理【淘宝店铺:向阳百分百】。将上层清液全部定容于250mL容量瓶中,移取25.00mL于锥形瓶中,
加入少量 和几滴KSCN溶液,用cmol⋅L 的 标准溶液滴定至终点时,消耗 标准溶液VmL。
(已知: )
样品中 的质量分数为 ;若不加 ,则样品中 质量分数的测定值将 (填
“偏大”、“不变”或“偏小”)。
5.(2023·江西·校联考二模)硫脲[CS(NH ) ]在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制
2 2
备Ca(HS) ,再与CaCN 合成CS(NH ) ,实验装置(夹持及加热装置略)如图所示。
2 2 2 2
已知:CS(NH ) 易溶于水,易被氧化,受热(150℃左右)时发生异构化生成NH SCN。
2 2 4
回答下列问题:
(1)仪器M名称 。
(2)实验前先检查装置气密性。检查气密性后加入药品,打开K ,装置B中盛装的试剂为 。反应结束
2
后关闭K ,打开K 通N 一段时间,目的是 。
2 2
(3)撤走搅拌器,打₁开K ,水浴加热D中三颈烧瓶,在80℃时合成硫脲,同时生成一种常见的碱。控制温度
在80℃的原因是 ₃ ,D处合成硫脲的化学方程式为 。判断制备Ca(HS) 反应中H S已过量的方
2 2
法是
(4)将装置D中液体过滤后,结晶得到粗产品。
称取mg产品,加水溶解配成250mL溶液,量取50mL于锥形瓶中,滴加一定量的稀硫酸使溶液显酸性,用
c mol·L-1KMnO 标准溶液滴定,滴定至终点时消耗KMnO 标准溶液V mL。滴定时,硫脲发生反应的离子方程
4 4
式为: 5[CS(NH ) ] +14 +32H+= 14Mn2++5CO +5N +5 + 26H O 。则样品中硫脲的质量分数为
2 2 2 2 2
资料收集整理【淘宝店铺:向阳百分百】(用含“m、c、V”的最简式表示)。
已知:NH SCN、KSCN都易溶于乙醇、水,温度高时容易分解和氧化;常温下KSCN的溶解度为217g。利用
4
硫脲制备KSCN的方法是:取一定量硫脲在隔绝空气的条件下加热至150℃充分反应,将加热后的产物溶于
一定比例的无水乙醇和水中形成溶液, (填写操作过程),得到KSCN晶体。(实验中可选用试剂:
K CO 、无水乙醇。)
2 3
6.(2023·河南·统考模拟预测)草酸是一种重要的化工原料,广泛用于药物生产、稀土元素的提取以及植
物的漂白、高分子合成等化工生产。某化学小组用植物纤维棉籽壳为原料制取草酸,原理是纤维大分子水
解成低聚糖和单糖的混合物,(C H O ) →(C H O ) →nC H O (m< n)然后加入催化剂,用硝酸氧化单糖生成
6 10 5 n 6 10 5 m 6 12 6
草酸,同时促进低聚糖水解为单糖。
I.草酸的制备过程:称取粉碎过筛的棉籽壳50g,用一定浓度硫酸浸泡一段时间,稀释后加入催化剂,移
入右图装置中,用水浴加热至40℃,慢慢滴加65%的硝酸,硝酸滴完后升温并保温反应一定时间,停止反
应趁热抽滤,滤液静置析出晶体,纯化粗品后可得到纯度较高的草酸二水合物。
已知:草酸收率(%)= ×100%
(1)图中A处缺少的仪器为 (填仪器名称)。
(2)硝酸氧化单糖生成NO和NO₂的物质的量之比是1:3的化学方程式为 。
(3)硝酸用量对草酸收率的影响见表:
实验编号 硝酸用量/mL 草酸收率/%
1 60 57.4
2 70 65.2
3 75 66.8
4 80 65.0
5 85 61.5
依据表中数据可知,硝酸的用量为75mL时,草酸的收率最高,分析原因 。
资料收集整理【淘宝店铺:向阳百分百】(4)采用趁热抽滤的原因是 。
(5)利用重结晶法纯化粗品的步骤是加水溶解、 、趁热抽滤、降温结晶。
Ⅱ.草酸晶体纯度的测定
①称取10.00g实验后得到的草酸晶体配成100mL的溶液;
②取20.00mL溶液,加入适量的稀硫酸,用浓度为0.4000 mol/L的KMnO₄溶液滴定,滴定终点消耗KMnO₄
溶液的体积为15.53mL。
(6)滴定时,发现反应速率开始很慢,后来逐渐加快,主要原因是 。
(7)草酸晶体的纯度为 (保留三位有效数字)。
(8)若滴定前滴定管尖嘴处无气泡,滴定后有气泡,则测定的草酸纯度 (填“偏高”“偏低”或
“无影响”)。
7.(2023·福建三明·统考模拟预测)甲醛是有毒气体,某实验小组探究能否用氨水吸收甲醛。
Ⅰ.甲醛溶液的制备与浓度测定
已知制备甲醛的反应原理如下:
①
②
实验室制备甲醛溶液的装置如图所示。(加热装置已略去)
回答下列问题:
(1)装置A中盛放甲醇的仪器名称为 。
(2)从能量利用的角度说明 的作用是 ;为了防止高温下甲醛在催化剂表面吸附太久被 进一
步氧化为甲酸,可采取的措施是 。
(3)实验结束后,取5mL新制 悬浊液,滴入适量的装置D的溶液,加热,有砖红色沉淀生成,反应
的化学方程式为 。
(4)甲醛溶液的浓度测定:装置D的溶液经预处理后,取10.00mL稀释至200mL,移取20.00mL稀释液于碘
资料收集整理【淘宝店铺:向阳百分百】量瓶中,加入 溶液和指示剂,振荡,静置5分钟后用0.1000 标准溶液滴定生成的
NaOH至终点,重复三次实验,平均消耗 标准溶液体积为20.00mL。则所制得的溶液中甲醛浓度为
(计算结果保留四位有效数字)。(已知: )
Ⅱ.甲醛与氨水反应的实验探究
实验探究(ⅰ)
实验编
操作 现象
号
1 取适量D的溶液,用pH计测溶液的pH pH≈7.0
2 取2mL2%氨水(滴有酚酞),逐滴加入3mL10%甲醇溶液 没有明显变化
3 取2mL2%氨水(滴有酚酞),逐滴加入装置D的溶液 红色褪去
(5)实验1的目的是 。
关于实验3褪色的原因,小组成员提出了以下猜想:
猜想①:甲醛与氨水发生反应,溶液碱性减弱,酚酞溶液褪色。
猜想②:甲醛与酚酞溶液发生反应,指示剂失效,溶液褪色。
实验探究(ⅱ)
实验编号 操作 现象
4 取实验3的无色溶液1mL,滴入几滴氨水 溶液变红
5 无明显变化
(6)实验5的操作为 。由实验4、5说明猜想 (填标号)正确。
8.(2023·广西·校联考模拟预测)莫尔盐的化学式为(NH ) SO ·FeSO ·6H O (硫酸亚铁铵),是常见的还原剂。
4 2 4 4 2
设计如下实验来制备莫尔盐并测定硫酸亚铁铵晶体的纯度。
步骤一:铁屑的处理与称量。
在盛有适量铁屑的锥形瓶中加入Na CO 溶液,加热、过滤洗涤、干燥、称量,质量记为m g。
2 3 1
步骤二: FeSO 的制备。
4
将上述铁屑加入到一定量的稀硫酸中,充分反应后过滤并用少量热水洗涤锥形瓶和滤纸。滤液及洗涤液完
全转移至蒸发皿中。滤渣干燥后称重,质量记为m g。
2
步骤三:硫酸亚铁铵晶体的制备。
资料收集整理【淘宝店铺:向阳百分百】准确称取所需质量的(NH ) SO 加入到“步骤二”的蒸发皿中,缓缓加热一段时间后停止,冷却,待硫酸亚
4 2 4
铁铵晶体后过滤。所得晶体用无水乙醇洗涤并自然干燥。
步骤四:硫酸亚铁铵晶体的测定。
称取m g硫酸亚铁铵晶体配置成100 mL溶液。用移液管移取20 mL,上述溶液,用浓度为cmol·L-1的酸性
3
K Cr O 溶液滴定,三次平均消耗K Cr O 标准溶液的体积为V mL。
2 2 7 2 2 7
回答下列问题:
(1)①铁屑用Na CO 溶液处理的目的是 。制备FeSO 溶液时,需用下图中的减压过滤装置进行
2 3 4
趁热过滤,主要有两点原因 、 。
②将(NH ) SO 与FeSO 混合后加热、浓缩,停止加热的时机为 。
4 2 4 4
③步骤三中用乙醇洗涤硫酸亚铁铵结晶的优点是 。
(2)①步骤四中滴定反应的离子方程式为 。
②制备的硫酸亚铁铵晶体(摩尔质量为392 g·mol-1)的纯度为 %。 (列出计算式)
③下述操作对硫酸亚铁铵晶体纯度测定的影响,结果偏小的有 。(填选项标号)
a.待测液在空气中放置时间较长
b.滴定前仰视读取刻度,滴定后俯视读取刻度
c.待测液移入锥形瓶后,加入10 mL蒸馏水
9.(2023·河北·校联考模拟预测)S-蜂斗菜素,具有的解痉作用,强度是罂粟碱的4~5倍,实验室为探究
其元素组成设计如下实验。
I.设计实验证明S-蜂斗菜素中含碳、氢、硫三种元素。
(1)从A~F中选择合适的仪器完成实验,正确的连接顺序是a→ →尾气吸收(按气流方向,用小写字
母表示,仪器不可重复使用)。
资料收集整理【淘宝店铺:向阳百分百】(2)装置F中盛放的试剂为 。
(3)装置E中酸性高锰酸钾溶液足量,所以整个过程中E中现象不太明显,所以实验中能证明药品中含硫元
素的实验现象为 ;E中发生反应的离子方程式为 。
II.测定药品中硫元素的质量分数。
实验步骤:取a g药品,碾碎后,充分燃烧;将产生的 气体全部通过 mL 的碘水;待吸收
完全后,向混合溶液中滴加少量淀粉溶液,再用 硫代硫酸钠标准液滴定,最终消耗硫代硫酸钠溶
液的体积为 mL。已知: 。
(4)滴定时盛放硫代硫酸钠溶液的仪器为 (填仪器名称);该仪器使用前需进行的操作为 。
(5)滴定终点的现象为 。
(6)该药品中的硫元素的质量分数为 (列出表达式即可)。
(7)若 气体中混有少量 ,可能会导致测定结果 (填“偏大”“偏小”或“无影响”)。
10.(2023·湖北·校联考模拟预测)次氯酸钠是家庭洗涤剂中的含“氯”漂白剂。某兴趣小组用如图所示装
置(在冰水浴条件下)制备 溶液并对产品成分含量进行测定。
回答下列问题:
Ⅰ.制备 溶液:
(1)仪器X的名称为 ;按照气流方向,装置正确的连接顺序为a (填小写字母)。
(2)装置A中反应的化学方程式为 。
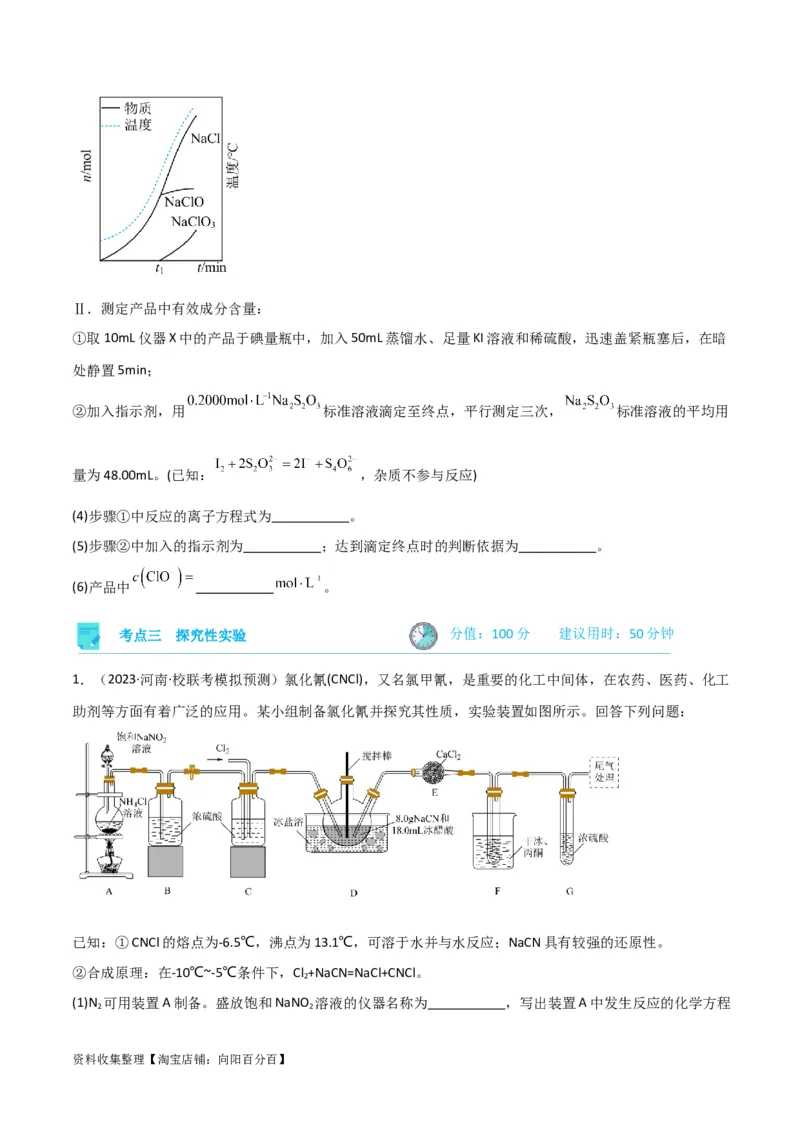
(3)装置E中各生成物的物质的量和溶液的温度随时间的变化如图所示,若发现装置E中温度计的温度上升
过快,可能导致产物中存在杂质,为避免此状况,装置A应进行的操作为 。
资料收集整理【淘宝店铺:向阳百分百】Ⅱ.测定产品中有效成分含量:
①取10mL仪器X中的产品于碘量瓶中,加入50mL蒸馏水、足量KI溶液和稀硫酸,迅速盖紧瓶塞后,在暗
处静置5min;
②加入指示剂,用 标准溶液滴定至终点,平行测定三次, 标准溶液的平均用
量为48.00mL。(已知: ,杂质不参与反应)
(4)步骤①中反应的离子方程式为 。
(5)步骤②中加入的指示剂为 ;达到滴定终点时的判断依据为 。
(6)产品中 。
考点三 探究性实验 分值:100分 建议用时:50分钟
1.(2023·河南·校联考模拟预测)氯化氰(CNCl),又名氯甲氰,是重要的化工中间体,在农药、医药、化工
助剂等方面有着广泛的应用。某小组制备氯化氰并探究其性质,实验装置如图所示。回答下列问题:
已知:①CNCl的熔点为-6.5℃,沸点为13.1℃,可溶于水并与水反应;NaCN具有较强的还原性。
②合成原理:在-10℃~-5℃条件下,Cl +NaCN=NaCl+CNCl。
2
(1)N 可用装置A制备。盛放饱和NaNO 溶液的仪器名称为 ,写出装置A中发生反应的化学方程
2 2
资料收集整理【淘宝店铺:向阳百分百】式: 。
(2)装置F中干冰和丙酮的作用是降低温度,此时干冰 (填“升华”或“凝华”);装置G的作用
是 。
(3)实验中,先向D中通入 (填“N ”或“Cl ”),此操作的目的是 。
2 2
(4)实验中必须保持温度在-10~-5℃,若高于-5℃,CNCl与NaCN反应产生NaCl和与卤素性质相似的气体
(填化学式)。
(5)向盛有少量Na S溶液的试管中通入CNCl,然后向其中滴入一滴FeCl 溶液,溶液显红色,其原因是
2 3
(用离子方程式说明)。
(6)上述实验中,NaCN完全反应时收集到8.5gCNCl,产率为 %(结果保留整数)。
2.(2023·广西玉林·统考模拟预测)KI是中学化学常用的还原剂,某小组设计实验探究I-的性质。回答下列
问题:
实验(一)探究影响氧化剂与KI反应的因素。
FeCl 、CuCl 、AgNO 溶液分别与KI反应,实验及现象如表所示:
3 2 3
实验操作 实验及现象
①X为AgNO 溶液,产生黄色沉淀,溶液不变蓝
3
②X为CuCl 溶液,过滤,得到蓝色溶液和白色沉淀
2
③X为FeCl 溶液,溶液变蓝,没有沉淀产生;再滴加K [Fe(CN) ]溶液,产
3 3 6
生沉淀,过滤,沉淀为蓝色
已知:CuI为难容于水的白色固体。常温下,K (AgI)=8. 5×10-17 ,K (CuI)=1.2×10-12。
sp sp
(1)实验②中的氧化产物为 (填化学式)。
(2)实验③中氧化剂与还原剂的物质的量之比为 。
(3)已知:Ag+的氧化性比Fe3+的强,但氧化剂的氧化性强弱除受本身性质影响外,还与温度、浓度、溶液的
酸碱度等外界条件有关。分析实验①③,试解释实验①中溶液没有变蓝的主要原因可能是 。
实验(二)探究氯气与KI反应的产物。
资料收集整理【淘宝店铺:向阳百分百】资料显示:I 和I-在溶液中会发生反应I +I ,部分离子颜色如表所示。
2 2
离子
颜色 棕黄色,遇淀粉变蓝 红色 黄色 无色
(4)A中发生反应的化学方程式为 。
(5)反应一段时间后,B中溶液颜色变为浅棕色,为了探究B溶液中的含碘物质,设计如下实验:
实验操作 实验现象
I.取反应后B中的溶液10mL,分成两等份,第一份滴入1滴碘水;第 第一份溶液变蓝色;第二份溶液
二份滴入1滴淀粉溶液 颜色没有变化
II.将I 溶于KI溶液中配制得碘总浓度为0.1mol·L-1的溶液,取该溶液 加淀粉后溶液变蓝,通氯气后蓝
2
2mL,向其中滴加1滴淀粉溶液,再通入少量氯气 色褪去,溶液显浅棕色
III.向II反应后的溶液中继续通入氯气 溶液几乎变为无色
①操作I的目的是排除 (填离子符号)的干扰。
②写出 在水溶液中与Cl 反应生成 的离子方程式: 。
2
③由以上实验可推断B中溶液颜色变成浅棕色的原因可能是生成了 (填离子符号),这两种离子混合
后溶液呈浅棕色。
3.(2023·广东汕头·金山中学校考三模)某化学兴趣小组想探究 溶液与 的反应历程。
资料收集整理【淘宝店铺:向阳百分百】Ⅰ.利用如图装置制备
(1)仪器a的名称
(2)b中反应的化学方程式为 ,该反应体现了浓硫酸的 性。
Ⅱ.利用探究 溶液与 的反应
(3)兴趣小组预测, 能使 溶液由黄色变为浅绿色,反应的离子方程式为 。
向 溶液中通入 至饱和后,用橡皮塞封闭试管,观察到溶液由黄色迅速变为血红色,静置
后变回黄色,静置 后,变为浅绿色。
(4)探究血红色物质生成的原因
查阅资料:血红色物质可能与 饱和溶液中的主要微粒: 、 、 、 、 有关。
①取少量上述血红色溶液,立即滴加几滴 溶液A,溶液又褪为黄色。据此推测:红色物质的产生
与 无关。物质A的化学式为 。
②向 溶液中滴加 溶液,溶液变为血红色,滴加几滴 溶液A,
褪成黄色。据此推测:红色物质的产生与 和 无关,主要与 或 有关。推测理由是
。
③利用分光光度仪测定红色物质的浓度(吸光度越高,浓度越大),实验数据如下:
资料收集整理【淘宝店铺:向阳百分百】吸光度
0.5 4.0 0.0 0.412
0.5 3.6 0.4 0.359
0.5 3.2 0.8 0.331
0.5 2.8 1.2 0.297
结论:溶液变血红色的主要原因是 和 发生配合反应。
(5)由以上探究结果说明该条件下, 与 溶液反应的活化能:氧化还原反应 (填“大于”
“小于”“等于”)配合反应。
(6)兴趣小组在某次实验中,通入 后未封闭试管,发现血红色更快变回黄色。其可能原因是 。
4.(2023·湖南长沙·长郡中学校考模拟预测)某中学同学在做铜与浓硫酸(装置如图)的反应实验时,发现有
如下的反应现象:加热初期,铜丝表面变黑;继续加热,有大量气泡产生,品红溶液褪色,溶液变为墨绿
色浊液,试管底部开始有灰白色沉淀生成;再加热,试管中出现“白雾”,浊液逐渐变为澄清,溶液颜色
慢慢变为浅蓝色,试管底部灰白色沉淀增多;冷却,静置,将试管中液体倒入另一支盛水试管中,管壁发
汤,溶液略带蓝色,将灰白色固体倒入水中,形成蓝色溶液。
(1)资料:聚四氯乙烯受热分解产生氯化氢,[CuCl ]2-呈黄色,[Cu(H O) ]2+呈蓝色,两者混合则成绿色,铜的
4 2 4
化合物中CuO、CuS、Cu S都为黑色,其中CuO溶于盐酸;CuS、Cu S不溶于稀盐酸,但溶于浓盐酸。该反
2 2
应中,品红溶液褪色,体现SO 的 性,NaOH溶液的作用是 。
2
该中学同学分成几个小组分别对上述现象探究:
(2)甲组同学查相关文献资料获知:在较低温度(100℃)下,浓硫酸氧化性相对较弱,生成的黑色沉淀为
Cu S,溶液变蓝,但没有气泡产生。请根据文献资料写出反应的化学方程式: 。
2
(3)乙组同学对实验中形成的墨绿色溶液进行探究,特进行下列实验:
资料收集整理【淘宝店铺:向阳百分百】现象
I组 取灼烧后的铜丝 溶液变蓝
Ⅱ
直接取其铜丝(表面有聚四氯乙烯薄膜) 溶液变成墨绿色
组
请解释形成墨绿色的原因: 。
(4)丙组同学对白雾的成分经检验为H SO ,请设计实验证明该白雾为硫酸: 。溶液的蓝色变浅,灰白
2 4
色沉淀增多,这现象体现浓硫酸的 性。
(5)丁组同学进一步对灰白色沉淀通过加水溶解、过滤,最后沉淀为黑色,取其黑色沉淀,进行成分探究:
滴加适量稀盐酸,则发现黑色沉淀几乎不溶解,溶液也不变蓝,则说明黑色沉淀中不含有 。
滴加适量浓盐酸,振荡,加热,观察到黑色沉淀几乎完全溶解,溶液呈略黄色[CuCl ]2-n(n=1~4)。写出CuS
n
与浓盐酸反应的离子方程式: 。
最后,丁组同学经过实验论证证明黑色沉淀中除了有CuS、Cu S,还有S等。
2
5.(2023·北京海淀·清华附中校考三模)某小组同学探究铜和浓硝酸的反应,进行如下实验:
实验1:分别取 浓硝酸与不同质量的铜粉充分反应,铜粉完全溶解,溶液颜色如下表:
编号 ① ② ③ ④ ⑤
铜粉质
0.1 0.2 0.3 0.4 0.5
量/g
草绿
溶液颜色 绿色 蓝绿色偏绿 蓝绿色偏蓝 蓝色
色
(1)写出铜和浓硝酸反应的离子方程式: 。
(2)小组同学认为溶液显绿色的可能原因是:
猜想1:硝酸铜浓度较高,溶液呈绿色;
猜想2: 溶解在混合溶液中,溶液呈绿色。
依据实验1中的现象,判断猜想1是否合理,并说明理由: 。
(3)取⑤中溶液, (填操作和现象),证实猜想2成立。
小组同学进行如下实验也证实了猜想2成立。
实验2:向①中溶液以相同流速分别通入 和空气,观察现象。
通入气体 氮气 空气
现象 液面上方出现明显的红棕色气体 液面上方出现明显的红棕色气体
资料收集整理【淘宝店铺:向阳百分百】后溶液变为蓝色 后溶液变为蓝色
(4)结合上述实验现象,下列推测合理的是 (填字母序号)。
a.①中溶液通入 时, 被缓慢氧化为
b.①中溶液里某还原性微粒与绿色有关,通入空气时较快被氧化
c.空气小的 溶于水显酸性,促进了溶液变蓝色
d.加热溶液①后,可能观察到溶液变蓝的现象
(5)小组同学继续探究实验2中现象的差异,并查阅文献:
ⅰ.“可溶性铜盐中溶解亚硝酸 ”可能是实验①中溶液显绿色的主要原因
ⅱ. 在溶液中存在
反应l: (慢)
反应2: (快)
解释实验2中“通入氮气变蓝慢,通入空气变蓝快”的原因 。
小组同学为确认亚硝酸参与了形成绿色溶液的过程,继续进行实验。
实验3:取3份等体积的①中绿色溶液,分别加入不同物质,观察现象。
加入物
3滴30% 溶液 3滴水
质 固体
现象 溶液绿色变深 溶液迅速变为蓝色 溶液颜色几乎不变
(6)实验中加入的固体物质是 (填化学式)。加入 后溶液迅速变蓝可能的原因是(用化学方程
式表示): , , 。
6.(2023·海南海口·海南中学校考二模)某小组在实验室用NaClO溶液和NH 反应制备N H ,并进行相关
3 2 4
的性质探究实验。
(1)制备N H
2 4
资料收集整理【淘宝店铺:向阳百分百】制备N H 的离子方程式为 。
2 4
Ⅱ.测定产品中水合肼(N H · H O)的含量
2 4 2
称取产品6.0 g,加入适量NaHCO 固体(滴定过程中,调节溶液的pH保持在6.5左右), 加水配成250 mL溶
3
液,移取25.00 mL置于锥形瓶中,并滴加2 ~ 3滴淀粉溶液,用 0.3000 mol • L-1的碘标准溶液滴定(已知:
N H ·H O+2I =N ↑ +4HI+H O)。
2 4 2 2 2 2
(2)滴定到达终点的现象是 。
(3)实验测得消耗碘标准溶液的平均值为20.00 mL,产品中水合肼的质量分数为 。
Ⅲ.探究肼的性质。
(4)写出肼的电子式 ,肼为 分子。(填“极性”或“非极性”)。
(5)预设肼可能具有 (a.氧化性 b.还原性 c.酸性 d.碱性)。
将制得的肼分离提纯后,进行如图实验探究。
【查阅资料]AgOH在溶液中不稳定,易分解生成黑色的Ag O,Ag O可溶于氨水。
2 2
【提出假设】黑色固体可能是Ag、Ag O中的一种或两种。
2
【实验验证】设计如下方案,进行实验。
操作 现象 实验结论
i.取少量黑色固体于试管中,加入适量①___________ 黑色固体部分溶解 黑色固体有Ag O
2
ii.取少量黑色固体于试管中加入足量稀硝酸,振荡 ②___________ 黑色固体是Ag和Ag O
2
(6)请完成表中的空白部分:① ;② 。
(7)实验表明,黑色固体主要成分是Ag,还有少量氧化银,请解释原因: 。
7.(2023·广东惠州·统考一模)铜是生活中常见的金属,以铜为原料进行如下实验
资料收集整理【淘宝店铺:向阳百分百】I. 是常见的化学试剂,利用废铜屑“湿法”制备 。
氯化铜在不同温度下结晶形成的结晶水合物
温度 15℃以下 15~25.7℃ 26~42℃ 42℃以上
结晶水合物
回答下列问题:
(1)“湿法”制备 的离子方程式为 ,水浴加热的温度不宜过高,原因是 。
(2)为得到纯净的 晶体,反应完全后要进行的操作是。除去其他可能的金属离子后,过滤,向滤
液中持续通入 气体,加热蒸发浓缩, ,过滤,洗涤,低温干燥.持续通入 气体的目的是
。
Ⅱ.探究Cu与 溶液的反应。
向 溶液中滴加几滴 溶液,溶液变红;再加入过量Cu粉,溶液红色褪
去,不久有白色沉淀产生。
查阅资料可知: 和 均为难溶于水的白色固体.针对白色沉淀同学们有以下猜想:
猜想1: 与过量的Cu粉反应生成 ,再结合 生成白色沉淀 。
猜想2: 与 发生氧化还原反应生成 ,再结合 生成白色沉淀 。
针对上述猜想,实验小组同学设计了以下实验:
编
操作 现象
号
资料收集整理【淘宝店铺:向阳百分百】实
加入铜粉后无现象
验1
实 溶液很快由蓝色变为绿色,未观察到白色沉淀:2h后溶液为绿色,未观
验2 察到白色沉淀:24h后,溶液绿色变浅,试管底部有白色沉淀
(3)实验结果说明猜想 (填“1”或“2”)不合理。
(4)根据实验2中的现象进一步查阅资料发现:
i. 与 可发生如下两种反应:
反应A: (淡黄色);
反应B: (黄色)。
ⅱ. 与 共存时溶液显绿色。
①由实验2中的现象推测,反应速率:A (填“>”或“<”)B,说明反应B (填“是”或“不
是”)产生 的主要原因。
②进一步查阅资料可知,当反应体系中同时存在 时, 氧化性增强,可将 氧化为
。据此将实验2改进,向 溶液中同时加入 ,立即生成白色沉淀 ,写出该反
应离子方程式 。
8.(2023·山东潍坊·校联考模拟预测)某化学兴趣小组在隔绝空气条件下,向硝酸酸化的0.05mol•L-1硝酸
银溶液(pH≈2)中加入过量铁粉,搅拌后静置,烧杯底部有黑色固体,溶液呈黄色。针对实验现象该小组同
学设计开展了系列实验,具体探究过程如下。
已知:Ag++SCN- AgSCN(白色固体);Fe3++3SCN- Fe(SCN) (红色)
3
回答下列问题:
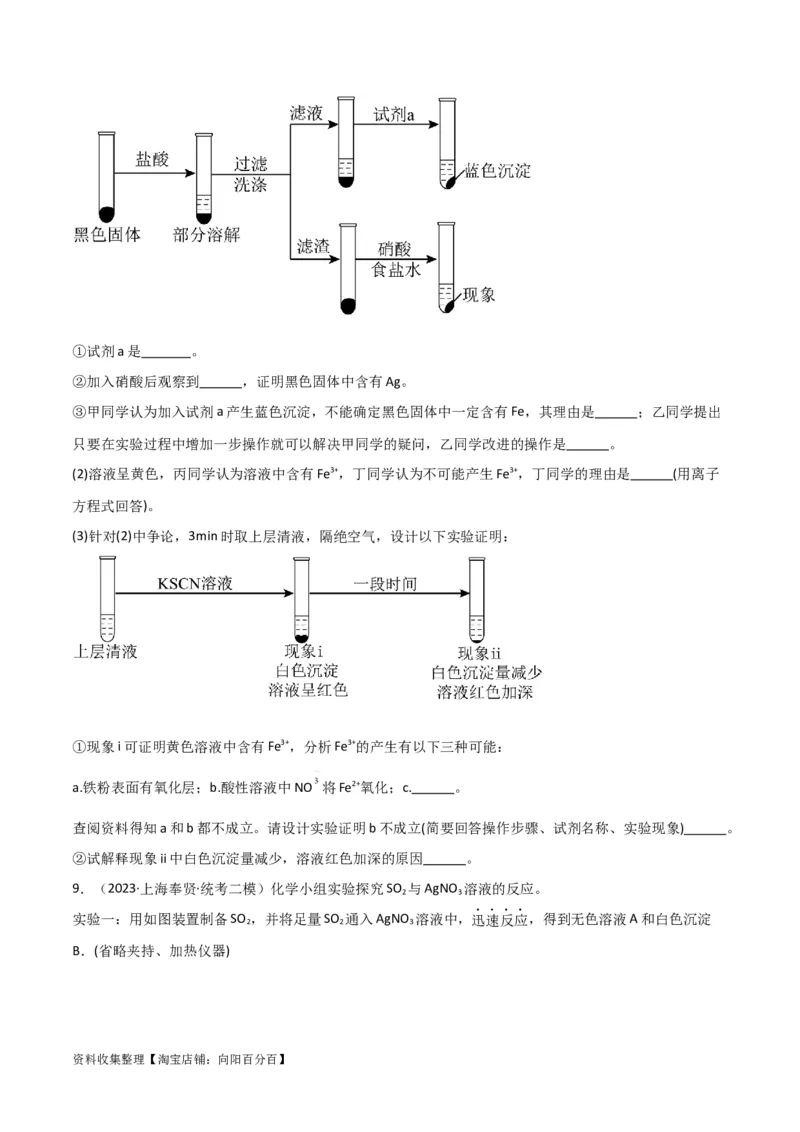
(1)检验黑色产物:取出少量黑色固体,进行如图实验,确认黑色固体中含有Fe和Ag。
资料收集整理【淘宝店铺:向阳百分百】①试剂a是 。
②加入硝酸后观察到 ,证明黑色固体中含有Ag。
③甲同学认为加入试剂a产生蓝色沉淀,不能确定黑色固体中一定含有Fe,其理由是 ;乙同学提出
只要在实验过程中增加一步操作就可以解决甲同学的疑问,乙同学改进的操作是 。
(2)溶液呈黄色,丙同学认为溶液中含有Fe3+,丁同学认为不可能产生Fe3+,丁同学的理由是 (用离子
方程式回答)。
(3)针对(2)中争论,3min时取上层清液,隔绝空气,设计以下实验证明:
①现象i可证明黄色溶液中含有Fe3+,分析Fe3+的产生有以下三种可能:
a.铁粉表面有氧化层;b.酸性溶液中NO 将Fe2+氧化;c. 。
查阅资料得知a和b都不成立。请设计实验证明b不成立(简要回答操作步骤、试剂名称、实验现象) 。
②试解释现象ii中白色沉淀量减少,溶液红色加深的原因 。
9.(2023·上海奉贤·统考二模)化学小组实验探究SO 与AgNO 溶液的反应。
2 3
实验一:用如图装置制备SO ,并将足量SO 通入AgNO 溶液中,迅速反应,得到无色溶液A和白色沉淀
2 2 3
B.(省略夹持、加热仪器)
资料收集整理【淘宝店铺:向阳百分百】(1)制备的SO 中会混有少量的SO ,原因可能为 。为了排除SO 的干扰,试剂a可以为
2 3 3
。
a.浓硫酸 b.饱和Na SO 溶液 c.饱和NaHS溶液 d.饱和NaHSO 溶液
2 3 3
实验二:验证白色沉淀B的成分。
分析:沉淀B可能为Ag SO 、Ag SO 或两者混合物。滴加氨水可释出其阴离子,便于后续检验。
2 3 2 4
相关反应为:①Ag SO +4NH •H O=2 + +4H O;
2 3 3 2 2
②Ag SO +4NH •H O=2 + +4H O。
2 4 3 2 2
流程如下:
(2)欲检验溶液C中加入的Ba(NO ) 是否已经过量,请简述实验方法 。
3 2
(3)沉淀D中主要含BaSO ,理由是 。向滤液E中加入H O 溶液,产生的现象是 ,
3 2 2
可进一步证实B中含Ag SO 。
2 3
实验三:探究 的产生途径。
猜想1:实验一中,SO 在AgNO 溶液中被氧化生成Ag SO ,随沉淀B进入D。
2 3 2 4
猜想2:实验二中, 被氧化为 进入D。
(4)取少量溶液A,滴加过量盐酸,产生白色沉淀。静置后,取上层清液再滴加BaCl 溶液,未出现白色沉淀,
2
可判断猜想1不合理。理由是: 。
(5)不同反应的速率也有所不同。将实验一所得混合物放置一段时间,也会有 生成,同时生成单质Ag。
请从化学反应速率的角度分析原因: 。
(6)实验探究可知, 在 (选填“酸性”“中性”“碱性”)溶液中更易被氧化为 。
资料收集整理【淘宝店铺:向阳百分百】10.(2023·河北保定·统考一模)84消毒液是常用消毒剂,某化学兴趣小组在实验室制备84消毒液并探究
其相关性质。回答下列问题:
Ⅰ.实验室制备84消毒液。
(1)装置甲中盛放高锰酸钾的仪器名称是 ,装置甲中反应的离子方程式为 。
(2)装置乙的作用是 。
(3)装置丙中制备次氯酸钠为放热反应,该反应需要控制温度在40℃以下,写出一种(除搅拌外)控制该反应
温度的操作方法 。
Ⅱ.探究相关性质
为了进一步研究消毒液的性质,兴趣小组向盛有2 mL 84消毒液的试管中,逐滴加入10%的双氧水,发现有
大量的气泡产生,对此作出以下猜测。
猜测1:双氧水与消毒液发生反应产生氧气。猜测2:……
(4)猜测1中反应的化学方程式为 。猜测2可能为 。
(5)为了验证猜想,某探究小组设计用如图装置进行实验,所选药品有:10%的双氧水、一定浓度的84消毒
液、二氧化锰等。该小组通过实验得出猜测1正确,请依据此装置和所给的药品推测该探究小组的实验设
计是 。
资料收集整理【淘宝店铺:向阳百分百】