文档内容
考点巩固卷 06 物质结构与性质
考点一 原子结构与性质 分值:30分 建议用时:15分钟
一、选择题(每小题2分,共30分)
1.(2023·上海·统考模拟预测)2022年6月,由来自德国、日本、美国和中国等国的科学家组成的国际科
研团队在《自然》杂志发表论文证实“四中子态”物质的存在。该物质只由四个中子组成,则其质量数是
A.1 B.2 C.3 D.4
2.(2023·海南海口·统考模拟预测)黑火药是中国古代四大发明之一。爆炸反应为
。下列有关说法不正确的是
A.离子半径: B. 分子的空间结构为直线形
C. 含离子键和共价键 D. 分子中 键与 键的数目比为
3.(2023·海南海口·统考模拟预测)实验室利用CoCl 制备 的原理是
2
。下列有关说法错误的是
A.基态Co3+的价层电子排布式为3d6
B.H O 的电子式为
2 2
C.NH Cl在水中的电离方程式为
4
D.NH 的空间填充模型为
3
4.(2023·山东·沂水县第一中学校联考模拟预测)石灰氮( ,其中 原子间成键方式相同)是一
种氮肥,可与土壤中的 反应生成氰胺( ),氰胺可进一步转化为尿素[CO(NH ) ]。下列说法
2 2
正确的是A. 的电子式为
B. 的空间构型与 的空间构型相同且两者键角相等
C.氰胺分子中氮原子的杂化方式为 和 两种
D. 分子中各元素的电负性大小关系为
5.(2023·重庆·统考三模) (俗称铵铁蓝)是一种蓝色的无机颜料。下列有关该物质说法
错误的是
A.电负性:
B.铵铁蓝中铁元素有两种化合价
C. 中 的键角比 中的 的键角小
D.铵铁蓝中的配体是 ,该配体中的 键与 键之比是1:2
6.(2023·湖北·校联考模拟预测)下列有关化学用语正确的是
A.金刚砂的分子式:
B.基态锗原子的价层电子排布式:
C.邻羟基苯甲醛分子内氢键示意图:
D. 分子的球棍模型:
7.(2023·湖北·校联考模拟预测)硫的下列4种微粒,若失去一个电子所需要能量最多的是
A.[Ne] B.[Ne] C.[Ne] D.[Ne]
8.(2023·天津河北·统考二模)下列化学用语或图示表达正确的是
A.顺-2-丁烯的球棍模型:B. 的空间填充模型:
C. 的电子式:
D.基态氮原子的轨道表示式:
9.(2023·北京东城·统考二模) (镓)的稳定同位素 和 是显示地表风化过程的一种指示剂。下列
说法不正确的是
A. 和 的化学性质不相同
B.可用质谱法区分 和
C. 位于元素周期表中第四周期、第ⅢA族
D. 的第一电离能大于K的第一电离能
10.(2023·江苏连云港·连云港高中校考模拟预测)黑火药爆炸时发生反应
。下列说法正确的是
A.半径大小: B.熔点:
C.电离能大小: D.电负性大小:
11.(2023·江苏连云港·连云港高中校考模拟预测)可以利用反应
得到的 制备活性 催化剂。下列说法正
确的是
A.Fe的外围电子排布式为 B. 中仅含有离子键
C.1mol 中含有3mol 键 D.FeCO 制备 时铁元素被还原
3
σ12.(2023·北京西城·北京四中校考模拟预测)下列事实不能直接从原子结构角度解释的是
A.化合物ICl中I为+1价 B.第一电离能:N>O
C.熔点:纯铁>生铁 D.热稳定性:NH >PH
3 3
13.(2023·江苏扬州·统考三模)软钾镁矾(化学式为 )是一种重要的钾肥。下列说法正
确的是
A.半径大小: B.电负性大小:
C.电离能大小: D.碱性强弱:
14.(2023·江苏扬州·统考三模)检验微量砷的原理为
。 常温下为无色气体。下列说法正确的是
A.As的基态核外电子排布式为 B. 的空间构型为平面三角形
C.固态 属于共价晶体 D. 既含离子键又含共价键
15.(2023·辽宁沈阳·东北育才学校校考模拟预测)下列化学用语表示正确的是
A.乙醚的结构简式:CH OCH B.NaClO的电子式为
3 3
C.苯分子中的大π键: D.基态铍原子最外层的电子云轮廓图:
考点二 分子结构与性质 分值:30分 建议用时:15分钟
一、选择题(每小题2分,共30分)
1.(2023·湖北武汉·统考模拟预测)臭氧是生活中最环保的氧化剂之一,有着重要的应用。下列说法中错
误的是
A.臭氧分子是一种极性分子
B.臭氧可用作自来水消毒剂
C.臭氧在水中的溶解度比在四氯化碳中的高
D.氟利昂的使用对大气臭氧层有着破坏作用2.(2023·浙江温州·乐清市知临中学校考一模)一定条件下,气体 和 都能与 形成笼状
结构的水合物晶体(如图),在深海海底 与 可形成“可燃冰” 和 等
下列说法正确的是
A. 和 ,约78个 包1个
B. 与 形成“可燃冰”的过程发生了化学反应
C.减压和升温,是“可燃冰”开采与利用的重要方法
D. 和 的分子间的作用力小于 与
3.(2023·重庆·重庆南开中学校考三模) 是一种重要的有机溶剂,其工业制备原理为:
,下列说法正确的是
A. 和 中的C原子杂化方式均为
B. 和 分子的空间结构分别是V形和正四面体
C. 为非极性分子, 为极性分子
D.液态 挥发时主要破坏共价键
4.(2023·山西·校联考模拟预测)下列说法正确的是
A.O 为极性分子
3
B.SF 分子的键角为90°
6C.Ge位于元素周期表的d区
D.氢氟酸电离方程式: HF= F-+H+
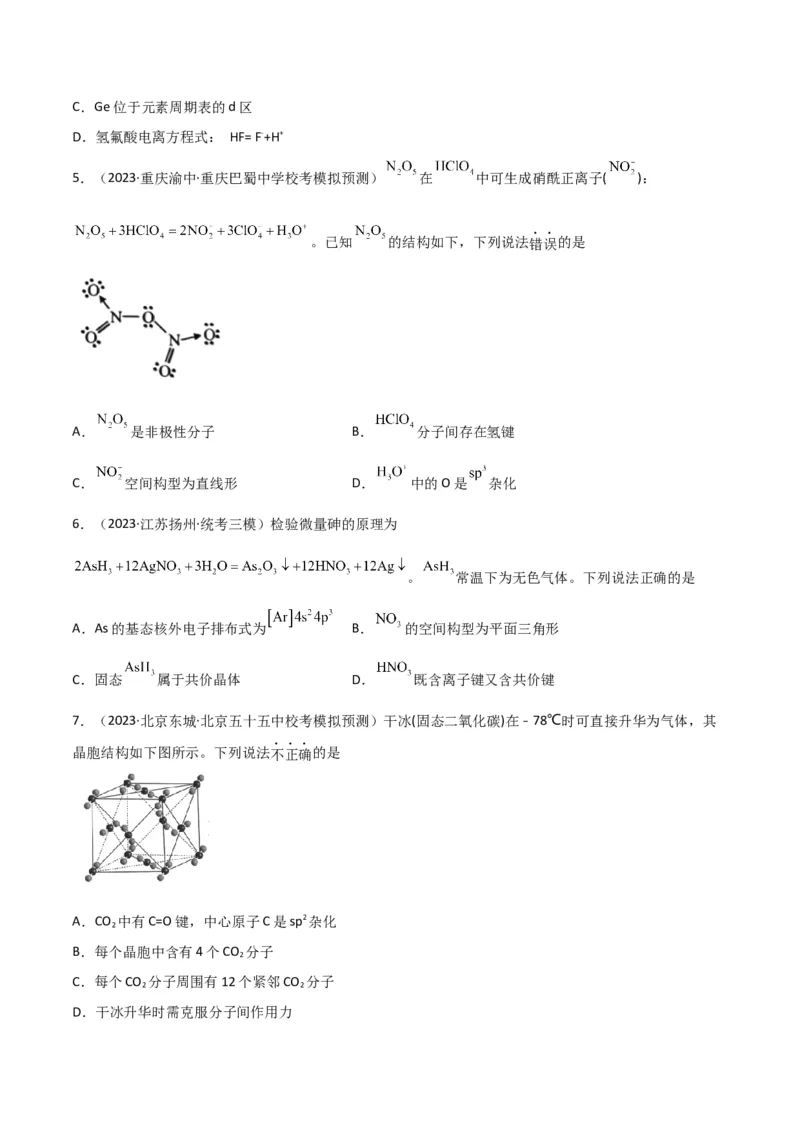
5.(2023·重庆渝中·重庆巴蜀中学校考模拟预测) 在 中可生成硝酰正离子( ):
。已知 的结构如下,下列说法错误的是
A. 是非极性分子 B. 分子间存在氢键
C. 空间构型为直线形 D. 中的O是 杂化
6.(2023·江苏扬州·统考三模)检验微量砷的原理为
。 常温下为无色气体。下列说法正确的是
A.As的基态核外电子排布式为 B. 的空间构型为平面三角形
C.固态 属于共价晶体 D. 既含离子键又含共价键
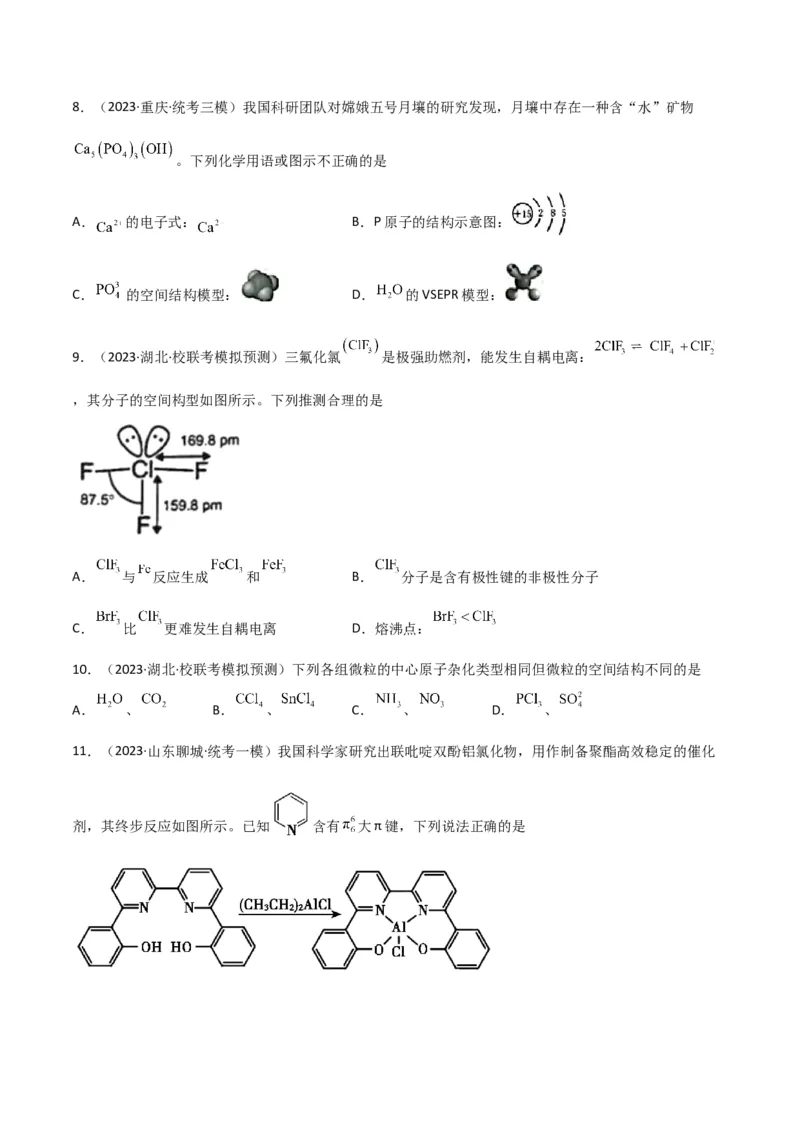
7.(2023·北京东城·北京五十五中校考模拟预测)干冰(固态二氧化碳)在﹣78℃时可直接升华为气体,其
晶胞结构如下图所示。下列说法不正确的是
A.CO 中有C=O键,中心原子C是sp2杂化
2
B.每个晶胞中含有4个CO 分子
2
C.每个CO 分子周围有12个紧邻CO 分子
2 2
D.干冰升华时需克服分子间作用力8.(2023·重庆·统考三模)我国科研团队对嫦娥五号月壤的研究发现,月壤中存在一种含“水”矿物
。下列化学用语或图示不正确的是
A. 的电子式: B.P原子的结构示意图:
C. 的空间结构模型: D. 的VSEPR模型:
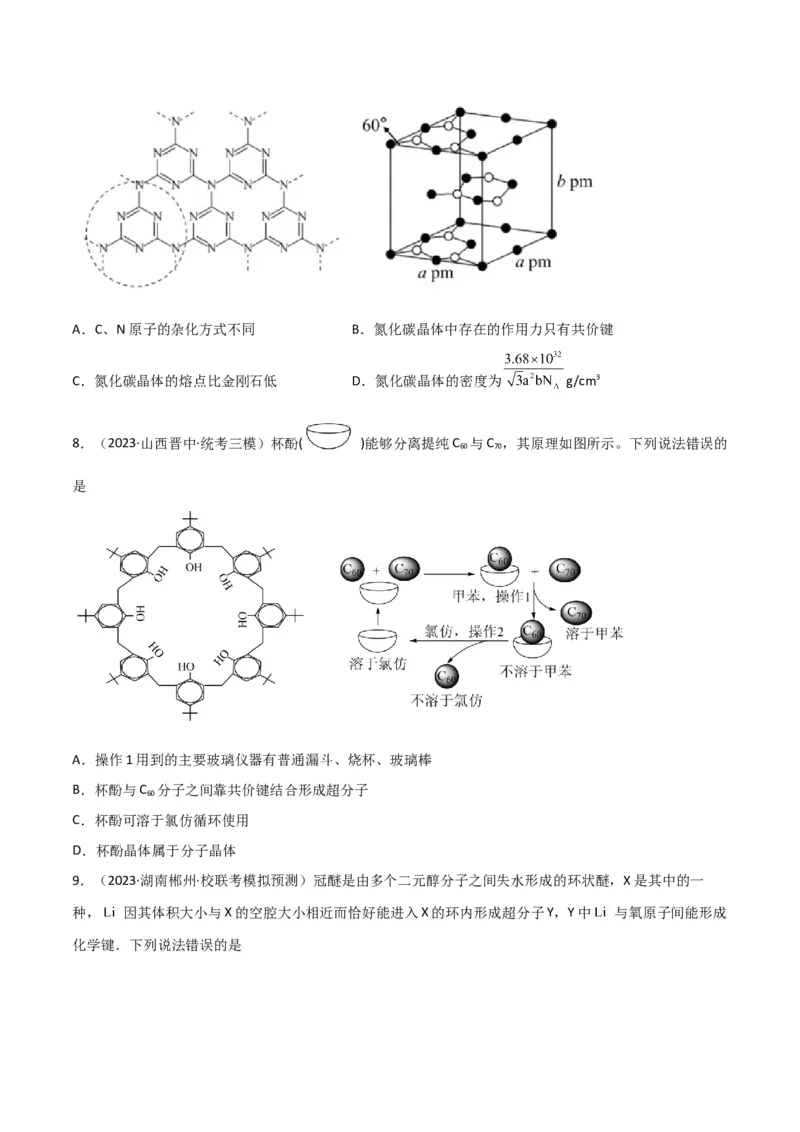
9.(2023·湖北·校联考模拟预测)三氟化氯 是极强助燃剂,能发生自耦电离:
,其分子的空间构型如图所示。下列推测合理的是
A. 与 反应生成 和 B. 分子是含有极性键的非极性分子
C. 比 更难发生自耦电离 D.熔沸点:
10.(2023·湖北·校联考模拟预测)下列各组微粒的中心原子杂化类型相同但微粒的空间结构不同的是
A. 、 B. 、 C. 、 D. 、
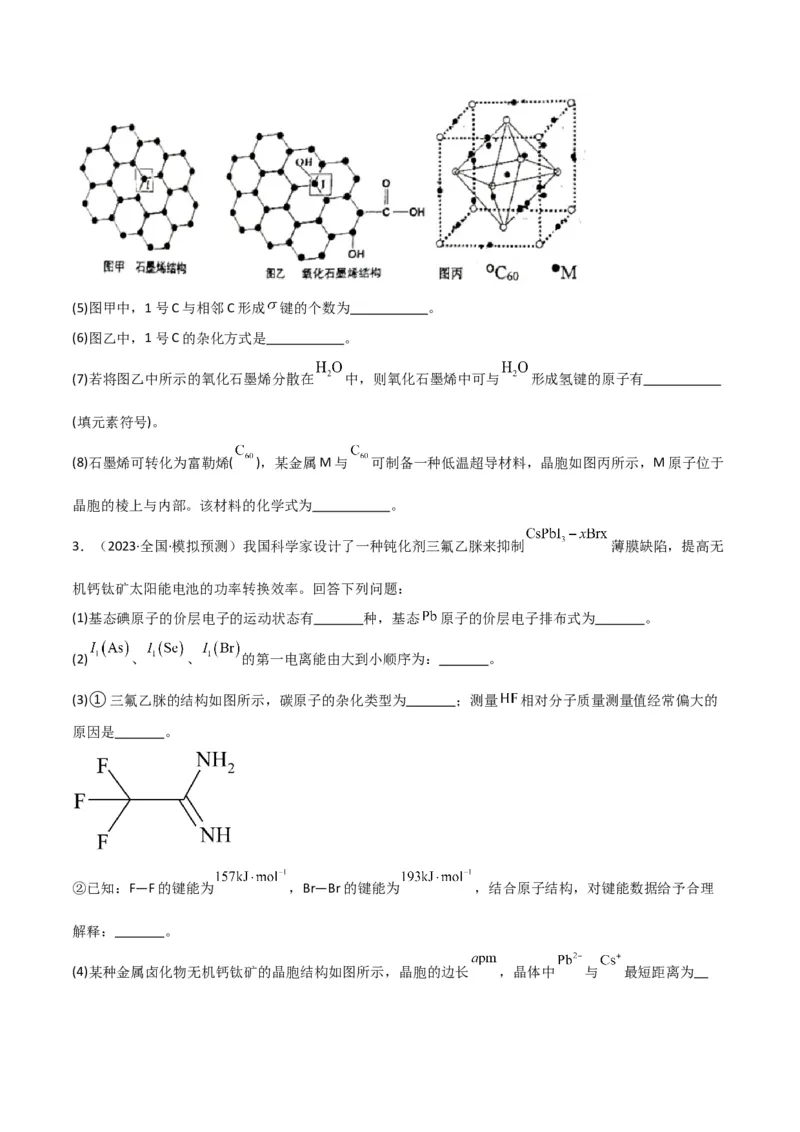
11.(2023·山东聊城·统考一模)我国科学家研究出联吡啶双酚铝氯化物,用作制备聚酯高效稳定的催化
剂,其终步反应如图所示。已知 含有 大π键,下列说法正确的是A.反应物中C、N、O原子均采用 杂化
B. 的熔点比 的高
C.产物中有2个配位键与Al相结合
D.产物中含有离子键和共价键
12.(2023·辽宁·校联考三模)利用生石灰粉可吸收烟气中的 ,其相关反应为:
反应i:
反应ii:
反应iii:
下列叙述正确的是
A. 分子键角大于 分子
B.钙元素的焰色属于吸收光谱
C.基态硫原子核外一定有9个电子自旋状态相同
D.CaS的熔点高于CaO
13.(2023·湖北·校联考模拟预测)科学研究发现新型含碳化合物 和 ,它们的结构类似 ,均
为直线形分子。下列结论中错误的是
A. 是非极性分子, 与 也是非极性分子
B. 、 、 分子中碳原子的杂化方式均为
C. 、 分子中 键与 键的数目之比均为
D. 、 分子中所有原子最外层均满足8电子稳定结构
14.(2023·山东烟台·校联考模拟预测)3-氨基-1-金刚烷醇是一种重要的医药中间体,其分子结构如图。
下列说法正确的是A.分子中H、O之间形成s-pσ键
B.分子间存在4种氢键
C.该物质存在芳香族化合物的同分异构体
D.分子中带有*的碳原子均为手性碳原子
15.(2023·辽宁朝阳·朝阳市第一高级中学校联考二模)“结构决定性质”是化学学科的核心观念,下列
推理不恰当的是
A. 比HF沸点高是由于 氢键O—H…O数目多于1molHF中F—H…F
B. 比苯酚( )的酸性弱,由于前者能形成分子内氢键
C. 的稳定性强于 ,是由于 分子间存在氢键
D.含 溶液中加过量氨水生成 是由于与 的配位能力 大于
考点三 晶体结构与性质 分值:30分 建议用时:15分钟
一、选择题(每小题2分,共30分)
1.(2023·上海崇明·统考一模)下列变化需克服共价键的是
A.金刚石熔化 B.汞变成汞蒸气 C.碘升华 D.食盐溶于水
2.(2023·重庆沙坪坝·重庆南开中学校考模拟预测)X为一种由汞(Hg)、锗(Ge)、锑(Sb)形成的可作潜在拓
扑绝缘体材料的新物质,其晶胞如图所示(底面为正方形)。下列说法错误的是A.X的化学式为
B.与Hg距离最近的Sb的数目为4
C.若晶胞中原子1的坐标为 ,则原子2的坐标为
D.设X的最简式的分子量为 ,则X晶体的密度为
3.(2023·湖北·校联考二模)Fe C是一种纳米材料,熔点高,硬度很大,Fe呈+1价,激光法制备Fe C的
3 3
反应如下:
①Fe(CO) (g)=Fe(s)+5CO(g);②6Fe(s)+C H (g)=2Fe C(s)+2H (g)
5 2 4 3 2
下列说法正确的是
A.Fe(CO) 配合物中与Fe配位的原子是O
5
B.电负性:O>C>Fe
C.Fc C属于分子晶体
3
D.反应②中的还原产物为Fe C,氧化产物为Fe C和H
3 3 2
4.(2023·湖北武汉·统考模拟预测)我国科技工作者利用富勒烯-铜-二氧化硅催化草酸二甲酯合成乙二
醇取得了新进展。下列说法正确的是
A.SiO 属于分子晶体 B.Cu的焰色为砖红色
2
C.乙二醇可用于生产汽车防冻液 D.草酸二甲酯的分子式是C H O
4 8 4
5.(2023·重庆·校联考三模)纳米 可催化 的分解,其晶胞结构如图所示。关于 的说法正确的
是A. 的配位数是4
B. 与 间最短距离为
C.若A离子的坐标为 ,则B原子的坐标为
D.若晶体密度为 ,则晶胞参数
6.(2023·广东广州·统考三模)研究者利用冷冻透射电子显微镜,在石墨烯膜上直接观察到了自然环境下
生成的二维晶体,其结构如图所示。下列说法正确的是
A.石墨烯属于烯烃,可发生加成反应
B.石墨烯中碳原子的杂化轨道类型为sp2
C.二维晶体的化学式为CaCl
2
D.二维晶体中Ca和Cl的配位数均为6
7.(2023·湖北荆门·荆门市龙泉中学校联考二模)石墨相氮化碳是一种光催化剂,类似于石墨层状结构,
其结构单元及晶胞结构如图所示。设N 为阿伏加德罗常数的值,下列说法正确的是
AA.C、N原子的杂化方式不同 B.氮化碳晶体中存在的作用力只有共价键
C.氮化碳晶体的熔点比金刚石低 D.氮化碳晶体的密度为 g/cm3
8.(2023·山西晋中·统考三模)杯酚( )能够分离提纯C 与C ,其原理如图所示。下列说法错误的
60 70
是
A.操作1用到的主要玻璃仪器有普通漏斗、烧杯、玻璃棒
B.杯酚与C 分子之间靠共价键结合形成超分子
60
C.杯酚可溶于氯仿循环使用
D.杯酚晶体属于分子晶体
9.(2023·湖南郴州·校联考模拟预测)冠醚是由多个二元醇分子之间失水形成的环状醚,X是其中的一
种, 因其体积大小与X的空腔大小相近而恰好能进入X的环内形成超分子Y,Y中 与氧原子间能形成
化学键.下列说法错误的是A.X形成的晶体为分子晶体 B.电负性:O>C>H>Li
C. 不能与X形成超分子 D.Y中 与氧原子间形成的是离子键
10.(2023·湖南郴州·校联考模拟预测)某卤化物可用于制作激光基质材料,其立方晶胞结构如图所示,
已知:晶胞参数为 , 为阿伏加德罗常数的值。下列有关该晶体的说法正确的是
A.化学式为 B.K的配位数为6
C.若K位于晶胞的体心,则F位于面心 D.密度为
11.(2023·辽宁·校联考模拟预测)几种晶体的晶胞结构如图所示。已知: 、 均为立方晶胞。
下列说法错误的是
A.相同条件下,熔点:
B.另一种 晶胞结构中,当 处于体心时,则 处于棱心
C. 晶胞中a点原子坐标参数为 ,则b点原子坐标参数为D.三种晶体中,Ca的配位数均为8
12.(2023·湖南长沙·长沙一中校考模拟预测)双钙钛矿型晶体的一种典型结构单元如图所示,真实的晶
体中存在5%的氧原子缺陷,能让 在其中传导,可用作固体电解质材料。已知La为+3价,Ba为+2价。
以下说法错误的是
A.该晶体的一个完整晶胞中含有1个Co原子
B.晶体中与La距离最近的Ba的数目为6
C.+3价Co与+4价Co的原子个数比为4∶1
D.忽略氧原子缺陷,每个Co原子都处于氧原子围成的正八面体空隙的中心
13.(2023·北京朝阳·统考三模)NaCl广泛应用于食品、氯碱工业等领域,其晶胞如下图所示,下列说法
不正确的是
A.a表示的是 ,b表示的是
B.每个晶胞中含有4个 和4个
C.NaCl由固态变成气态,需要吸收能量破坏离子键
D.基态 与 最外层电子排布符合 ,二者位于周期表的p区
14.(2023·湖北武汉·湖北省武昌实验中学校考模拟预测)砷化镓(GaAs)是优良的半导体材料,熔点为
1238℃,用于制作太阳能电池的材料,其结构如图所示,其中以原子1为原点,原子2的坐标为(1,1,1)。下列有关说法中错误的是
A.原子3的坐标为( , , ) B.Ga的配位数为4
C.GaAs为共价晶体 D.若将Ga换成Al,则晶胞参数将变小
15.(2023·山东聊城·校联考三模)BP晶体是一种超硬耐磨的涂层材料,其合成途径之一为
、 。下列说法正确的是
A.BP晶体为离子晶体 B. 的电子式为
C.第一电离能: D. 为正四面体结构,键角为
考点四 物质结构与性质的综合考查 分值:100分 建议用时:50分钟
非选择题(共10题,每题10分,共100分)
1.(2023·海南海口·海南华侨中学校考二模)冰晶石的主要成分为六氟合铝酸钠 。工业上制备
冰晶石的化学方程式为 。
回答下列问题:
(1)Al激发态的电子排布式有 ,其中能量较高的是 。(填字母)
a. b. c. d.
(2)HF的沸点比 的 (填“高”或“低”),其原因是 。
(3)气态氯化铝是以双聚分子 的形式存在的,其结构式为 。(4)冰晶石的结构单元如图所示,该结构单元中 的数目为 ;已知晶胞参数 、
、 、 ,阿伏加德罗常数的值为 ,则 晶体的密度
(列出计算式即可)。
2.(2023·天津河北·统考二模)坐落在河北区的华为天津区域总部项目计划于2023年12月底竣工。石墨
烯液冷散热技术系华为公司首创,所使用材料石墨烯是一种二维碳纳米材料。
I. 、金刚石、石墨的结构模型如图所示(石墨仅表示出其中的一层结构):
(1)金刚石、石墨和 三者互为___________(填序号)。
A.同分异构体 B.同素异形体 C.同系物 D.同位素
(2) 晶体的晶体类型为 。
(3)晶体硅的结构跟金刚石相似,1mol晶体硅中所含有硅硅单键的数目是 。
(4)石墨层状结构中,平均每个正六边形占有的碳原子数是 。
II.石墨烯(图甲)是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面
结构会发生改变,转化为氧化石墨烯(图乙)。(5)图甲中,1号C与相邻C形成 键的个数为 。
(6)图乙中,1号C的杂化方式是 。
(7)若将图乙中所示的氧化石墨烯分散在 中,则氧化石墨烯中可与 形成氢键的原子有
(填元素符号)。
(8)石墨烯可转化为富勒烯( ),某金属M与 可制备一种低温超导材料,晶胞如图丙所示,M原子位于
晶胞的棱上与内部。该材料的化学式为 。
3.(2023·全国·模拟预测)我国科学家设计了一种钝化剂三氟乙脒来抑制 薄膜缺陷,提高无
机钙钛矿太阳能电池的功率转换效率。回答下列问题:
(1)基态碘原子的价层电子的运动状态有 种,基态 原子的价层电子排布式为 。
(2) 、 、 的第一电离能由大到小顺序为: 。
(3)①三氟乙脒的结构如图所示,碳原子的杂化类型为 ;测量 相对分子质量测量值经常偏大的
原因是 。
②已知:F—F的键能为 ,Br—Br的键能为 ,结合原子结构,对键能数据给予合理
解释: 。
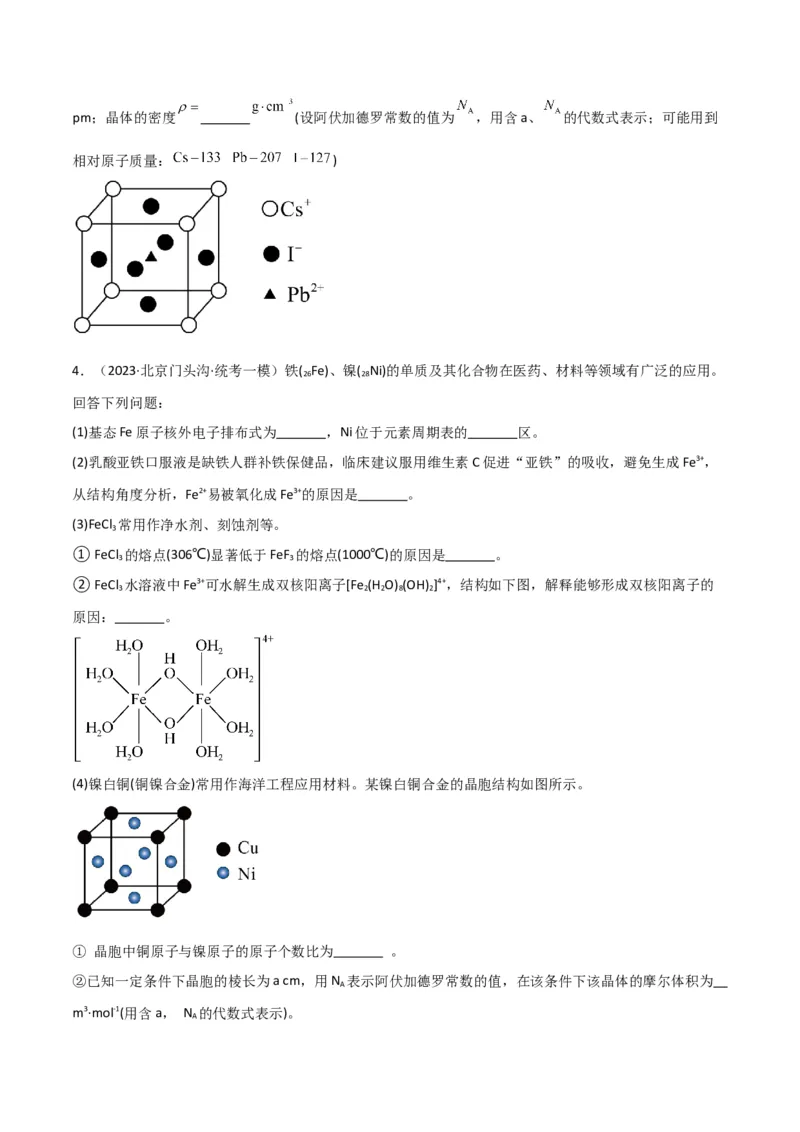
(4)某种金属卤化物无机钙钛矿的晶胞结构如图所示,晶胞的边长 ,晶体中 与 最短距离为pm;晶体的密度 (设阿伏加德罗常数的值为 ,用含a、 的代数式表示;可能用到
相对原子质量: )
4.(2023·北京门头沟·统考一模)铁( Fe)、镍( Ni)的单质及其化合物在医药、材料等领域有广泛的应用。
26 28
回答下列问题:
(1)基态Fe原子核外电子排布式为 ,Ni位于元素周期表的 区。
(2)乳酸亚铁口服液是缺铁人群补铁保健品,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,
从结构角度分析,Fe2+易被氧化成Fe3+的原因是 。
(3)FeCl 常用作净水剂、刻蚀剂等。
3
① FeCl 的熔点(306℃)显著低于FeF 的熔点(1000℃)的原因是 。
3 3
② FeCl 水溶液中Fe3+可水解生成双核阳离子[Fe (H O) (OH) ]4+,结构如下图,解释能够形成双核阳离子的
3 2 2 8 2
原因: 。
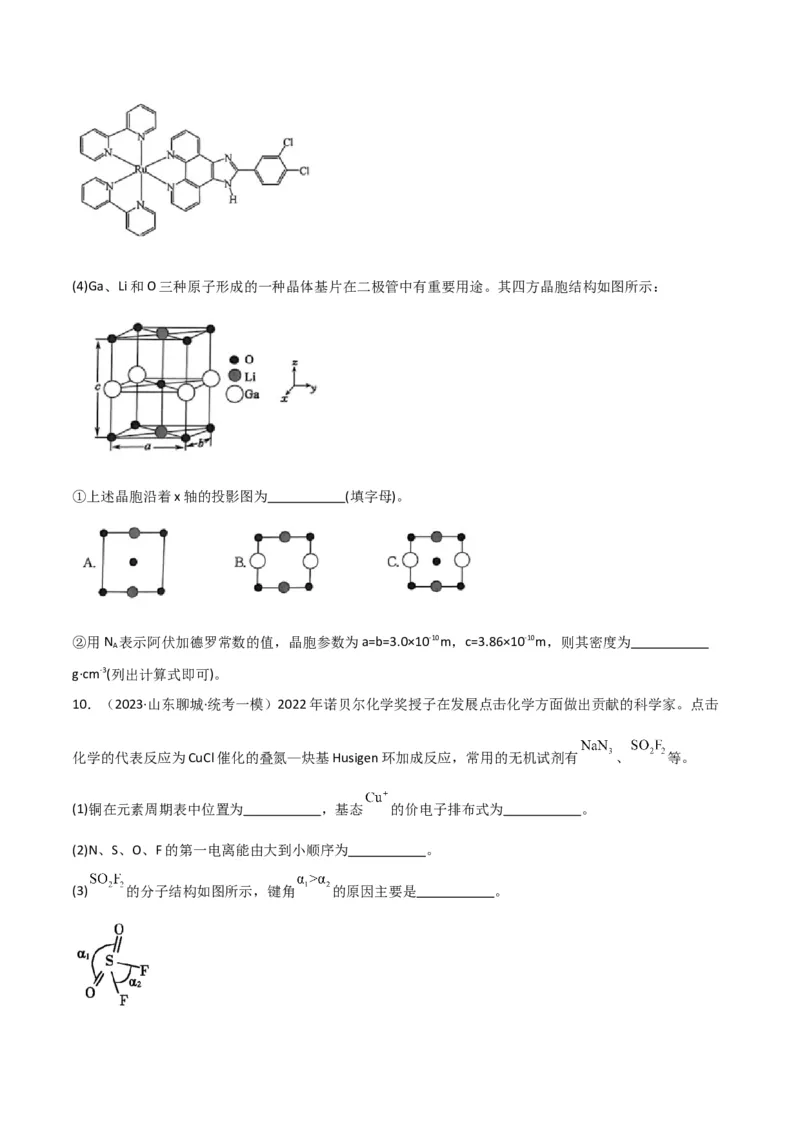
(4)镍白铜(铜镍合金)常用作海洋工程应用材料。某镍白铜合金的晶胞结构如图所示。
① 晶胞中铜原子与镍原子的原子个数比为 。
②已知一定条件下晶胞的棱长为a cm,用N 表示阿伏加德罗常数的值,在该条件下该晶体的摩尔体积为
A
m3·mol-1(用含a, N 的代数式表示)。
A5.(2023·甘肃·统考二模)钴及其化合物具有广泛的用途,我国古代用的陶器釉料中就含有氧化钴。随着
科技的不断发展,钴及其化合物成为制造合金、陶瓷颜料、催化剂、电池的重要原料之一,钴被也称为
“工业味精”和“工业牙齿”,是重要的战略资源之一。回答下列问题。
(1)基态钴原子的价层电子排布式为 ,钴成为阳离子时首先失去 轨道电子。
(2)配合物[Co(NH ) ]2+中的H-N-H的键角比游离的NH 分子 (填“大”“小”或“相同”),其原
3 6 3
因为 。
(3)[Co(NH ) CO ]NO 可用于制备激光起爆器,制取[Co(NH ) CO ]NO 的反应原理为:
3 4 3 3 3 4 3 3
4Co(NO ) +12NH +4(NH ) CO +O =4[Co(NH ) CO ]NO ,+4NH NO +2H O
3 2 3 4 2 3 2 3 4 3 3 4 3 2
① 中N的杂化方式为 。
②[Co(NH ) CO ]NO 中与Co(III)形成配位键的原子是 。
3 4 3 3
③多原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离
城π键”,下列物质中存在“离城π键”的是 (填序号)。
A.NH B. C. D.H O
3 2
(4)Co O 晶体的晶胞如图所示(阳离子略去),O2-围成正四面体空隙(1、3、6、7号O2-围成)和正八面体空隙
3 4
(3、6、7、8、9、12号O2-围成),Co O 中有一半的Co3+填充在正四面体空隙中,Co2+和另一半Co3+填充在正
3 4
八面体空隙中。
①O2-周围紧邻的O2-数目为 ,晶体中正四面体空隙数与正八面体空隙数之比为 。
②已知晶胞参数为apm,阿伏加德罗常数为N ,则晶体密度为 g·cm-3(用含a和N 的代数式表
A A
示)。
6.(2023·四川南充·统考三模)卤素及其化合物在药物中曾占有一定地位,现在临床上仍有使用。回答下
列问题:
(1)基态Br的价电子排布式为 。基态N、O、F第一电离能由大到小的顺序是 。(2)ClO 可用于杀菌消毒。ClO 键角介于ClO 和ClO 之间,ClO 键角 (填字母标号)。
2 2 2
A.>120° B.109°28'~120° C.<109°28'
(3)碘酊是I 和KI在乙醇中的溶液,用于皮肤消毒。I 和KI可形成直线形I 离子,中心I采取的杂化类型为
2 2
(填字母标号)。
A.sp B.sp3 C.sp3d
(4)为提高含氮碱性有机药物的水溶性,常常用它们的盐酸盐。例如盐酸氨溴索(一种止咳药,结构见图)的
阳离子可与水形成氢键,其表示式为O-H…O(H O)、 、 。
2
(5)KBr、NaBr用作镇静剂,NaF可预防龋齿。三者中熔点最高的是 ,原因是 。
(6)氟化物有防治龋齿的作用,氟离子与羟(基)磷灰石[Ca (PO ) OH,M=502g•mol-1]转化成氟磷灰石抵抗酸的
5 4 3
侵蚀。Ca (PO ) OH晶胞结构如图。其中Ca2+、PO 均位于体内,则1个晶胞中含有OH-的数目是 。
5 4 3
晶胞参数分别为apm、apm、cpm,α=β=90°,γ=120°,其密度ρ= g•cm-3(列出计算式,设N 为阿佛
A
伽德罗常数的值)。
7.(2023·广西·统考二模)我国科学家研究发现AgCrS (AMX 家族成员之一,A为一价金属,M为三价金
2 2
属,X为氧族元素)在室温下具有超离子行为。回答下列问题:
(1)基态铬原子M层的电子排布式为 ;基态硫原子核外电子中含有 个未成对电子。
(2)同周期元素Si、P、S的电负性由大到小的顺序为 (用元素符号表示),O、S为同主族元素,H O的
2
键角比H S大的原因是 。
2
(3)硫元素能形成多种微粒如H S、SO 、SO 、SO 、SO 等。SO 的立体构型为 ,SO 的中心原子的
2 2 3 2 3价层电子对数为 。
(4)CrO 中Cr元素化合价为+6价,常温下呈蓝色,则其结构式可能为 (填标号)。
5
A B C
(5)某含铬化合物立方晶胞如图所示。该晶体的化学式为 ;与Cr最近的氧原子的个数为 ;Ca
和Cr的最近距离为anm,设N 为阿伏加德罗常数的值,则该晶体密度为 (填含a、N 的表达
A A
式)g•cm-3。
8.(2023·浙江·校联考模拟预测)分析物质的结构可以解释物质的性质。请回答:
(1)水分子中的共价键,依据原子轨道重叠的方式判断,属于 键,该键是由 杂化轨道和
轨道重叠形成的,水分子的VSEPR模型名称是 。
(2)由铁原子核形成的四种微粒,价电子排布图分别为:① 、②
、③ 、④ ,有关这
些微粒的叙述,不正确的是_______。
A.微粒半径:④>①>②
B.得电子能力:②>①>③
C.电离一个电子所需最低能量:②>①>④
D.微粒③价电子在简并轨道中单独分占,且自旋相同,故不能再继续失去电子
(3)八硝基立方烷结构如图所示,是一种新型高能炸药,其爆炸性强的原因是 。(4)某种冰的晶胞结构如图所示,晶胞参数 , , 。该晶体类型是 ,密度
为 (列出数学表达式,不必计算出结果)。
9.(2023·河南·校联考模拟预测)氟、氮、镓形成的单质及它们形成的化合物有重要的研究和应用价值。
回答下列问题:
(1)下列状态的氟中,能量最高的是 (填字母),其2p电子云轮廓图的形状为 。
(2)在NH H PO 中的N、O两种元素的第一电离能由大到小的顺序是 。N、P原子均能与F形成
4 2 4
稳定的化合物NF 、PF ,试比较键长:N一F P一F(填“>”“<”或“=”)。
3 3
(3)钌-多吡啶配合物具有丰富的光化学和光物理信息,其结构简式如图所示。钌(Ⅱ)的配位数是
,N原子的杂化类型为 。(4)Ga、Li和O三种原子形成的一种晶体基片在二极管中有重要用途。其四方晶胞结构如图所示:
①上述晶胞沿着x轴的投影图为 (填字母)。
②用N 表示阿伏加德罗常数的值,晶胞参数为a=b=3.0×10-10m,c=3.86×10-10m,则其密度为
A
g·cm-3(列出计算式即可)。
10.(2023·山东聊城·统考一模)2022年诺贝尔化学奖授子在发展点击化学方面做出贡献的科学家。点击
化学的代表反应为CuCl催化的叠氮—炔基Husigen环加成反应,常用的无机试剂有 、 等。
(1)铜在元素周期表中位置为 ,基态 的价电子排布式为 。
(2)N、S、O、F的第一电离能由大到小顺序为 。
(3) 的分子结构如图所示,键角 的原因主要是 。(4) 是叠氮酸( )的钠盐, 在常温下是液体,沸点相对较高,为308.8K,主要原因是
。 分子的空间结构如图所示(图中键长单位为 )。 、 和 的共价键键长分别为
、 和 ;试画出 分子的结构式 。
(5)CuCl的晶胞中, 的位置如图所示。 填充于 构成的四面体空隙中,则 的配位数为
;若 为阿伏加德罗常数的值,该晶体的密度为 ,则该晶胞中 之间的距离为
nm(用含ρ、 的代数式表示)。