文档内容
考点巩固卷 06 物质结构与性质 元素周期律(二)
——化学键 分子结构与性质 晶体结构与性质
考法01共价键的分类及键参数的应用
考法02化学键的类型及与物质类别的关系
考点03化学键 分子结构与性质
考法03电子式 化学用语
(限时:25 min)
考法04杂化轨道类型、分子空间结构的判
断
考法05分子结构与物质的性质
考法01晶体及其分类
考点04 晶体结构与性质
考法02 晶胞分析与计算
(限时:25 min)
考法03配位化合物与超分子
考点03 分子结构与性质、化学键
考法01 共价键的分类及键参数的应用
1.下列关于σ键和π键的理解不正确的是( )
A.含有π键的分子在进行化学反应时,分子中的π键比σ键活泼
B.在有些分子中,共价键可能只含有π键而没有σ键
C.有些原子在与其他原子形成分子时只能形成σ键,不能形成π键
D.当原子形成分子时,首先形成σ键,可能形成π键
【答案】B
【解析】同一分子中的π键不如σ键牢固,反应时比较容易断裂,A项正确;在共价单键中只含有σ键,
而含有π键的分子中一定含有σ键,B项错误、D项正确;氢原子、氯原子等跟其他原子形成分子时只能
形成σ键,C项正确。
2.下列物质性质的变化规律,与共价键的键能大小有关的是( )
①F、Cl、Br、I 的熔点、沸点逐渐升高
2 2 2 2
②HF、HCl、HBr、HI的热稳定性依次减弱
③金刚石的硬度、熔点、沸点都高于晶体硅
④HO的沸点高于HS的沸点
2 2
A.①② B.②③ C.①④ D.②④
【答案】B
1
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司【解析】①F 、Cl 、Br 、I 熔沸点与共价键无关,只与分子间作用力有关;④HO的沸点高于HS是因为
2 2 2 2 2 2
HO分子间形成氢键,与共价键无关。
2
3.从实验中测得不同物质中氧氧键的键长和键能的数据:
氧氧键 O2− O− O O+
2 2 2 2
键长/(10−12 m) 149 128 121 112
键能/(kJ⋅mol−1) x y z=494 w=628
其中x、y的键能数据尚未测定,但可根据规律推导键能(单位为kJ⋅mol−1)的大小顺序为w>z>y>x,
该规律是( )
A. 成键时电子数目越多,键能越大 B. 键长越长,键能越小
C. 成键所用电子数目越少,键能越大 D. 成键时电子对越偏移,键能越大
【答案】B
【解析】 和 所含电子数目分别为16、15,但键能分别为 、 ,电子
O O+ 494 kJ⋅mol−1 628 kJ⋅mol−1
2 2
数目越多,键能越小,故A 错误;由题表中数据以及题目所给信息可知,键长越长,键能越小,故B 正
确; 和 成键所用电子数目分别为2和4,键能: ,成键所用电子数目
O2− O z kJ⋅mol−1>x kJ⋅mol−1
2 2
越少,键能越小,故C 错误;电子对偏移程度与键能大小无关,故D 错误。
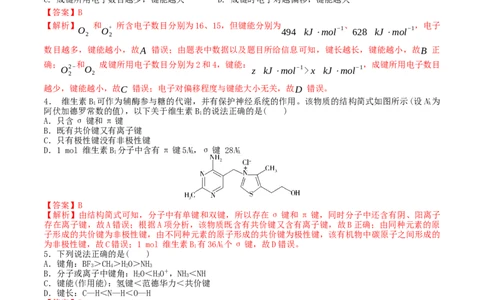
4. 维生素B 可作为辅酶参与糖的代谢,并有保护神经系统的作用。该物质的结构简式如图所示(设N为
1 A
阿伏加德罗常数的值),以下关于维生素B 的说法正确的是( )
1
A.只含σ键和π键
B.既有共价键又有离子键
C.只有极性键没有非极性键
D.1 mol 维生素B 分子中含有π键5N,σ键 28N
1 A A
【答案】B
【解析】由结构简式可知,分子中有单键和双键,所以存在σ键和π键,同时分子中还含有阴、阳离子
存在离子键,故A错误;根据A项分析,该物质既含有共价键又含有离子键,故B正确;由同种元素的原
子形成的共价键为非极性键,由不同种元素的原子形成的共价键为极性键,该有机物中碳原子之间形成的
为非极性键,故C错误;1 mol 维生素B 有36N个σ键,故D错误。
1 A
5.下列说法正确的是( )
A.键角:BF>CH>HO>NH
3 4 2 3
B.分子或离子中键角:HO<HO+,NH<NH
2 3 3
C.键能(作用能):氢键<范德华力<共价键
D.键长:C—H<N—H<O—H
【答案】B
【解析】A.BF 是平面三角形,键角为120°,CH 、HO、NH 的VSEPR模型均为四面体,CH 无孤电子对、
3 4 2 3 4
NH 有1个孤电子对、HO有2个孤电子对,由于孤电子对间排斥力>孤电子对和成键电子对间的排斥力>
3 2
成对电子对间的排斥力,所以键角:BF >CH >NH >HO,故A错误;B.HO、HO+的VSEPR模型均为四面体,
3 4 3 2 2 3
但HO有2个孤电子对、HO+有1个孤电子对,NH 、NH的VSEPR模型为四面体,NH 有1个孤电子对,NH无
2 3 3 3
孤电子对,由于孤电子对间排斥力>孤电子对和成键电子对间的排斥力>成键电子对间的排斥力,所以键
角:HO<HO+,NH<NH,故B正确;C.氢键是特殊的分子间作用力,作用力强弱介于范德华力和共价键之
2 3 3
间,故C错误;D.原子半径:C>N>O,原子半径越大,键长越大,所以键长:C—H>N—H>O—H,故D错
误。
考法02 化学键的类型及与物质类别的关系
6. 下列说法正确的是( )
A.碘晶体受热转变为碘蒸气,吸收的热量用于克服碘原子间的作用力
2
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司B.硫酸钾和硫酸溶于水都电离出硫酸根离子,所以它们在熔融状态下都能导电
C.2NaO +2HO===4NaOH+O↑反应中既有离子键、非极性键、极性键的断裂又有离子键、极性键、
2 2 2 2
非极性键的形成
D.金刚石与NaCl熔化克服相同类型的化学键
【答案】C
【解析】A项,克服I 分子间作用力,错误;B项,HSO 熔融状态不电离,故不能导电,错误;D项,金刚
2 2 4
石熔化克服共价键,NaCl熔化克服离子键,错误。
7.(2023·山东济南联考)过氧化氢 溶液俗称双氧水,医疗上常用溶质质量分数为 的双氧水进
(H O ) 3%
2 2
行伤口消毒。H O 与SO 反应生成H SO ,H O 的分子结构如图所示。下列说法正确的是( )
2 2 2 2 4 2 2
A. 过氧化氢的电子式为H+ [⋅⋅O
B. H O 为含有极性键和非极性键的共价化合物
2 2
C. H O 与SO 反应过程中H O 体现出还原性
2 2 2 2 2
D. H O 与SO 反应过程中有共价键断裂,同时有共价键和离子键形成
2 2 2
【答案】B
【解析】 H 2 O 2 是共价化合物,电子式为 A错误。 H 2 O 2中含有H —O 极性键和O—O 非极
性键,B正确。H O 分子中,O元素的化合价为−1 价,反应后降低为−2 价,H O 表现出氧化性,C
2 2 2 2
错误。H O 与SO 反应过程中有共价键断裂,同时有共价键形成,但没有离子键的形成,D错误。
2 2 2
8.(2024·河北唐山模拟)某电池材料结构如图所示。X、Y、Z、M、W为同周期主族元素。X原子的最外层
电子数是W原子次外层电子数的3倍,下列说法正确的是( )
A.实验室保存M的单质,需使用到Z的多种氢化物形成的混合物
B.该电池材料中存在离子键、极性键、非极性键、配位键、氢键
C.最简单氢化物的沸点为XHF,C错误;O、F、C、Li、B的原子半径的大小为Li>B>C>O>F,D错误。
2
9. (2023·河南开封一模)(1)已知
3(NH)[UO(CO)]=====3UO+10NH↑+9CO↑+N↑+9HO↑。反应中断裂的化学键有__________(填
4 4 2 3 3 2 3 2 2 2
编号)。
a.氢键 b.极性键 c.非极性键 d.离子键 e.配位键
(2)鉴定Ni2+的特征反应如下:
3
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司鲜红色沉淀丁二酮肟镍的晶体中不存在的作用力是__________(填标号)。
a.σ键 b.π键 c.离子键 d.配位键
e.氢键
【答案】(1)bde (2)c
【解析】(1)(NH)[UO(CO)]中不存在非极性键,NH与[UO(CO)]4-之间为离子键,NH中N原子与H原子
4 4 2 3 3 2 3 3
间存在一个配位键和三个极性键,故反应中断裂的化学键有极性键、离子键和配位键。(2)结构中的单键
为σ键,双键中含一个σ键、一个π键,由丁二酮肟镍的结构可知,还含有配位键和氢键,不含有离子
键。
10.Na[Co(NO)]常用作检验 K+的试剂,配体 NO 的中心原子的杂化方式为________,立体构型为
3 2 6
________。大π键可用符号Π表示,其中m代表参与形成大π键的原子数,n为各原子的单电子数(形成
σ键的电子除外)和得电子数的总和(如苯分子中的大π键可表示为Π),则NO中大π键应表示为
________。
【答案】sp2 V形 Π
【解析】配体NO的中心N原子的价层电子对数为2+(6-2×2)=3,且含有一对孤电子对,故NO中N原子
的杂化方式是sp2杂化,立体构型是V形,NO中参与形成大π键的原子数为3,中心原子采取sp2杂化,所
以中心原子中有1对孤电子对没有参与形成大π键,则参与形成大π键的电子数为6×3-2×2-2-4×2
=4,故NO中大π键可表示为Π。
考法03 电子式 化学用语
11.(2024·江苏扬州期末)反应ZnCl ·H O+SOCl ZnCl +SO ↑+2HCl↑可用于
2 2 2 2 2
制备 ZnCl 。下列说法正确的是 ( )
2
A.中子数为37的锌原子:
B.SOCl 中硫元素的化合价:+4
2
C.Cl- 的结构示意图:
D.H O 的电子式:
2
【答案】B
【解析】中子数为37的Zn原子质量数为67,A错误;氧元素和氯元素的化合价分别为-2、-1,则硫元
素的化合价为+4,B正确;Cl-最外层8个电子,C错误;HO分子中氧原子为8电子稳定结构,D错误。
2
12.(2024·广东汕头期末)“宏、微、符”三重表征是重要的化学学科素养。下列相关化学用语正确的
是( )
A. ❑
1H
、❑
2H
互为同位素
2 2
MgCl
B. 用电子式表示 2的形成过程为
4
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司CO
C. 2的电子式为
D. 甲烷分子的球棍模型可以表示为
【答案】C
【解析】❑ 1H 、❑ 2H 是氢元素的不同核素形成的单质,❑ 1H 、❑ 2H 不互为同位素,A错误;用电子
2 2 2 2
MgCl B CO O C
式表示 2 的形成过程为 , 错误; 2的电子式为 , 正
D
确;甲烷分子的球棍模型可以表示为 , 错误。
13.下列表达正确的是( )
A.HClO的电子式为
B.PH 的电子式为
3
C.用电子式表示NaO的形成过程:
2
2Na×+
D.BaCl 的电子式为
2
【答案】B
【解析】HClO分子中,氧原子分别与氢原子和氯原子形成共价键,电子式为 ,故A错误;
用电子式表示NaO的形成过程时,2个Na+不能合并,形成过程为 ,
2
故C错误;BaCl 是离子化合物,电子式为 ,故D错误。
2
14.光气(COCl )是一种重要的有机合成中间体,有剧毒,光气与氨气反应的化学方程式为COCl +4NH
2 2 3
CO(NH)+2NHCl。下列有关说法不正确的是( )
2 2 4
A.NHCl中含有离子键和共价键
4
B.Cl原子的原子结构示意图:
C.CO(NH) 的球棍模型:
2 2
‥ ︰O︰ ‥
‥
D.COCl 2 的电子式为︰Cl︰ C ︰Cl︰
‥ ‥ ‥
5
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司【答案】D
【解析】电子式中的非金属原子(除H原子外)周围应有8个电子,则COCl 的电子式为
2
‥ ︰O︰ ‥
︰Cl︰‥‥
︰Cl︰,D错误。
C
‥ ‥
15.(2024·辽宁卷下列化学用语或表述正确的是
A.中子数为1的氦核素: B. 的晶体类型:分子晶体
C. 的共价键类型: 键 D. 的空间结构:平面三角形
【答案】C
【解析】中子数为1的He核素其质量数为1+2=3,故其表示应为 He,A错误;SiO 晶体中只含有共价键,
2
为共价晶体,B错误;两个F原子的2p轨道单电子相互重叠形成p-p σ键,C正确;PCl 的中心原子存在
3
1对孤电子对,其VSEPR模型为四面体型,PCl 的空间结构为三角锥型,D错误。
3
考法04 杂化轨道类型、分子空间结构的判断
16.氮的最高价氧化物为无色晶体,它由两种离子构成,已知其阴离子的立体构型为平面三角形,则其阳
离子的立体构型和阳离子中氮的杂化方式为( )
A.直线形 sp杂化
B.V形 sp2杂化
C.三角锥形 sp3杂化
D.平面三角形 sp2杂化
【答案】A
【解析】氮的最高价氧化物为NO ,根据N元素的化合价为+5和原子组成,可知阴离子为NO、阳离子为
2 5
NO,NO中N原子形成了2个σ键,孤电子对数目为0,所以杂化类型为sp,阳离子的立体构型为直线形,
故A项正确。
17.(2024·衡水中学测试)用价层电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,有时也
能用来推测键角大小,下列判断正确的是( )
A.SO、CS、HI都是直线形的分子
2 2
B.BF 键角为120°,SnBr 键角大于120°
3 2
C.CHO、BF、SO 都是平面三角形的分子
2 3 3
D.PCl、NH、PCl 都是三角锥形的分子
3 3 5
【答案】C
【解析】SO 是V形分子,A项错误;BF 是平面三角形结构,键角为120°,SnBr 中,Sn原子价电子是4,
2 3 2
与两个Br成键后,还有一对孤对电子,对成键电子有排斥作用,使键角小于 120°,B项错误;CHO、
2
BF、SO 都是平面三角形分子,C项正确;PCl、NH 是三角锥形分子,PCl 是三角双锥形结构,D项错误。
3 3 3 3 5
18.下列关于NH+ 、NH 、NH− 三种微粒的说法不正确的是( )
4 3 2
A. 三种微粒中所含有的电子数相等 B. 三种微粒中氮原子的杂化方式相同
C. 三种微粒的空间结构相同 D.
键角:NH+>NH >NH−
4 3 2
【答案】C
【解析】每个NH+ 、NH 、NH− 中所含有的电子数都为10,故A 正确;NH+ 的中心原子N 原子的价层
4 3 2 4
1
电子对数=4+ ×(5−1−4×1)=4,且孤电子对数为0,采取sp3 杂化,NH 的中心原子N 原子的价层
2 3
6
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司1
电子对数=3+ ×(5−3×1)=4,且孤电子对数为1,采取sp3 杂化,NH− 的中心原子N 原子的价层电子
2 2
1
对数=2+ ×(5+1−1×2)=4,且孤电子对数为2,采取sp3 杂化,故B 正确;根据B 项分析可知,
2
NH+ 的空间结构为正四面体形,NH 的空间结构为三角锥形,NH− 的空间结构为V 形,故C 错误;根据
4 3 2
B 项分析可知,NH+ 、NH 、NH− 中N 原子上的孤电子对数分别为0、1、2,孤电子对数越多键角越小,
4 3 2
所以键角:NH+>NH >NH− ,故D 正确。
4 3 2
19.(2024·河北石家庄期末)VSEPR模型和杂化轨道理论常用于预测和解释分子的空间结构。下列说法
正确的是( )
A. 凡是AB 型的共价化合物,其中心原子A均采取sp2杂化轨道成键
3
B. 凡是中心原子采取sp3杂化的分子,其空间结构都是正四面体形
C. 杂化轨道只用于形成σ 键或用于容纳未参与成键的孤电子对
D. 凡是分子中形成π 键的原子,均采取sp2杂化
【答案】C
【解析】AB 型的共价化合物,其中心原子A 可能采取sp3 杂化也可能采取sp2 杂化,如BF 中B 原子
3 3
采取sp2 杂化,NH 中N 原子采取sp3 杂化,故A 错误;中心原子采取sp3 杂化的分子,其空间结构可
3
能是正四面体形、三角锥形、V形,CCl 、NH 、H O的中心原子都采取sp3 杂化,但是其空间结构分
4 3 2
别是正四面体形、三角锥形、V形,故B 错误;杂化轨道只用于形成σ 键或用于容纳未参与成键的孤电子
对,没有杂化的p 轨道形成π 键,故C 正确;分子中形成π 键的原子,可能采取sp2 杂化,也可能采取
sp 杂化,如HC≡CH 分子中的C 原子形成π 键,采取sp 杂化,故D 错误。
20.(2023·湖北卷)价层电子对互斥理论可以预测某些微粒的空间结构。下列说法正确的是 ( )
A. CH 和H O的VSEPR模型均为四面体
4 2
B.
SO2− 和CO2−
的空间构型均为平面三角形
3 3
C. CF 和SF 均为非极性分子
4 4
D. XeF 与XeO 的键角相等
2 2
【答案】A
【解析】CH 和H O 的中心原子上的价层电子对数均为4,VSEPR模型均为四面体,A正确;SO2− 的
4 2 3
中心原子上的价层电子对数为4,孤电子对数为1,空间构型为三角锥形,CO2−
的中心原子上的价层电子
3
对数为3,孤电子对数为0,空间构型为平面三角形,B错误;CF 的中心原子上的价层电子对数为4,孤
4
电子对数为0,为正四面体结构,CF 为非极性分子,SF 的中心原子上的价层电子对数为5,孤电子对数
4 4
为1,SF 为极性分子,C错误;XeF 的中心原子上的价层电子对数为5,孤电子对数为3,空间构型为直
4 2
线形,XeO 的中心原子上的价层电子对数为4,孤电子对数为2,空间构型为V 形,故二者键角不相等,
2
D错误。
考法05分子结构与物质的性质
21.下列关于范德华力影响物质性质的叙述中,正确的是( )
A. 范德华力是影响由分子构成的物质的熔点、沸点高低的唯一因素
7
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司B. 范德华力与物质的性质没有必然的联系
C. 范德华力能够影响物质的化学性质和物理性质
D. 范德华力仅是影响某些物质部分物理性质的一种因素
【答案】D
【解析】范德华力不能影响物质的化学性质,仅能影响由分子构成的物质的部分物理性质,如熔点、沸点、
溶解性等,且不是唯一的影响因素。
22.下列现象与氢键有关的是( )
①乙醇、乙酸可以和水以任意比互溶
②NH 的熔沸点比PH 的熔、沸点高
3 3
③稳定性:HF>HCl
④冰的密度比液态水的密度小
⑤水分子高温下也很稳定
A.①②③④⑤ B.①②⑤
C.①②④ D.①③④⑤
【答案】C
【解析】①乙醇、乙酸与水分子之间能形成氢键,则可以和水以任意比互溶,故①选;②氨气和磷化氢的
结构相似,但氨气分子中存在氢键,磷化氢中只含分子间作用力,氢键的存在导致物质的熔、沸点升高,
故②选;③HF、HCl的热稳定性依次减弱,是因为H—X共价键稳定性依次减弱,与氢键无关,故③不选;
④冰中存在氢键,其体积变大,则相同质量时冰的密度比液态水的密度小,故④选;⑤水分子高温下也很
稳定,其稳定性与化学键有关,而与氢键无关,故⑤不选。
23.下列物质中既有极性键又有非极性键的极性分子的是( )
A.CS B.CH
2 4
C.HO D.CH===CH
2 2 2 2
【答案】C
【解析】CS 分子结构式为S===C===S,分子中共价键为碳硫极性键,不存在非极性键,故A错误;CH 分子
2 4
中共价键为碳氢极性键,不存在非极性键,故B错误;HO 分子结构式为H—O—O—H,分子中含有氢氧极
2 2
性共价键和氧氧非极性共价键,但是分子结构不对称,属于极性分子,故C正确;CH===CH 中含有碳氢极
2 2
性键和碳碳非极性键,由于CH===CH 分子结构对称,CH===CH 分子为非极性分子,故D错误。
2 2 2 2
24.下列说法错误的是( )
A.甘油和水可以任意比例互溶的原因之一为甘油与水能形成分子间氢键
B.HO的沸点高于HF,是因为前者的氢键作用较大
2
C.氢氟酸水溶液中氢键的类型有 F—H…F、F—H…O、O—H…F、O—H…O
D. 熔点低的原因是前者形成分子内氢键,后者形成分子间
氢键
【答案】B
【解析】甘油为丙三醇,因其能与水形成分子间氢键,故可与水以任意比例互溶,A正确;水的沸点比氢
氟酸高,是因为等物质的量情况下,前者比后者含有的氢键数目多,但氢键作用力氢氟酸比较高,B错误;
氢氟酸水溶液中共有两种不同的氢原子,可以分别与F、O原子形成氢键,故氢氟酸水溶液中氢键类型有四
种,C正确;邻羟基苯甲醛易形成分子内氢键,对羟基苯甲醛易形成分子间氢键,分子内氢键使分子熔点
降低,分子间氢键使分子熔点升高,D正确。
25.下列关于CS、SO、NH 三种物质的说法正确的是( )
2 2 3
A.CS 在水中的溶解度很小,是由于其属于极性分子
2
B.SO 和NH 均易溶于水,原因之一是它们都是极性分子
2 3
8
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司C.CS 为非极性分子,在三种物质中熔沸点最低
2
D.NH 在水中溶解度很大只是因为NH 是极性分子
3 3
【答案】B
【解析】根据“相似相溶”原理,CS 在水中的溶解度很小,水是极性分子,则CS 是非极性分子,故A错
2 2
误;由于SO 和NH 都是极性分子,水也是极性分子,根据“相似相溶”原理,二者均易溶于水,故 B正确;
2 3
由于CS 常温下是液体,SO 和NH 常温下是气体,CS 的熔沸点最高,故C错误;NH 在水中溶解度很大,除
2 2 3 2 3
了由于NH 分子有极性外,还因为NH 分子和HO分子之间可以形成氢键,故D错误。
3 3 2
考点04 晶体结构与性质
考法01 晶体及其分类
1.根据表中给出物质的熔点数据(AlCl 沸点为260 ℃),判断下列说法错误的是( )
3
晶体 NaCl MgO SiCl AlCl 晶体硼
4 3
熔点/ ℃ 801 2 852 -70 180 2 500
A.MgO中的离子键比NaCl中的离子键强
B.SiCl 晶体是分子晶体
4
C.AlCl 晶体是离子晶体
3
D.晶体硼是共价晶体
【答案】C
【解析】NaCl和MgO是离子化合物,形成离子晶体,故熔、沸点越高,说明晶格能越大,离子键越强,A
项正确;SiCl 是共价化合物,熔、沸点较低,为分子晶体,硼为非金属单质,熔、沸点很高,是共价晶体,
4
B、D项正确;AlCl 虽是由活泼金属和活泼非金属形成的化合物,但其晶体熔、沸点较低,应属于分子晶
3
体,C项错误。
2.下列有关晶体类型的判断正确的是( )
A SiI :熔点为120.5 ℃,沸点为287.4 ℃ 共价晶
4
体
B B:熔点为2 300 ℃,沸点为2 550 ℃,硬度大 金属晶
体
C 锑:熔点为630.74 ℃,沸点为1 635 ℃,晶体导电 共价晶
体
D FeCl :熔点为306 ℃,易溶于水,也易溶于有机溶剂 分子晶
3
体
【答案】D
【解析】SiI 的熔、沸点比较低,属于分子晶体,A错误;B的熔、沸点很高,硬度大,属于共价晶体,
4
B错误;Sb是金属,属于金属晶体,C错误;FeCl 的熔点比较低,属于分子晶体,D正确。
3
3.NaF、NaI和MgO均为离子晶体,有关数据如下表:
物质 ①NaF ②NaI ③MgO
离子所带电荷数 1 1 2
键长/(10−10 m) 2.31 3.18 2.10
试判断,这三种化合物熔点的高低顺序是 ( )
A. ①>②>③ B. ③>①>② C. ③>②>① D. ②>①>③
【答案】B
【解析】NaF、NaI、MgO均为离子晶体,它们的熔点高低由离子键的强弱决定,而离子键的强弱与离
9
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司子半径和离子所带电荷数有关,MgO的键长最短,离子所带电荷数最多,故离子键最强,熔点最高;NaI
和NaF 中的离子所带电荷数相同,但NaF 的键长小于NaI 的,故NaF 的熔点高于NaI。
4.AlN、GaN属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在N—Al键、N—Ga 键。
下列说法错误的是( )
A.GaN的熔点高于AlN
B.晶体中所有化学键均为极性键
C.晶体中所有原子均采取sp3杂化
D.晶体中所有原子的配位数均相同
【答案】A
【解析】AlN、GaN为结构相似的共价晶体,由于Al原子的半径小于Ga,N—Al的键长小于N—Ga的,则N
—Al的键能较大,故GaN的熔点低于AlN,A错误;不同种元素的原子之间形成的共价键为极性键,故两
种晶体中所有化学键均为极性键,B正确;由于AlN、GaN与金刚石结构相似,则其晶体中所有原子均采取
sp3杂化,所有原子的配位数也均为4,C、D正确。
5.Al和Si在元素周期表金属和非金属过渡位置上,其单质和化合物在建筑业、电子工业和石油化工等方
面应用广泛。请回答下列问题:
(1)AlCl 是化工生产中的常用催化剂,熔点为192.6 ℃,熔融状态以二聚体AlCl 形式存在,其中铝原子
3 2 6
与氯原子的成键类型是________。
(2)超高导热绝缘耐高温纳米氮化铝(AlN)在绝缘材料中应用广泛,AlN晶体与金刚石类似,每个Al原子与
________个N原子相连,与同一个Al原子相连的N原子构成的空间结构为________。在四大晶体类型中,
AlN属于________晶体。
【答案】(1)共价键(或σ键)
(2)4 正四面体 共价
【解析】(1)AlCl 分子为共价化合物,因此原子间形成的化学键为共价键。(2)AlN晶体与金刚石类似,可
3
以知道AlN为共价晶体,每个Al原子周围有4个N原子,且与同一个Al原子相连的4个N原子构成正四面
体结构。
考法02 晶胞分析与计算
6.某立方卤化物可用于制作光电材料,其晶胞结构如图所示。
下列说法错误的是( )
A.Ca2+的配位数为6
B.与F-距离最近的是K+
C.该物质的化学式为KCaF
3
D.若F-换为Cl-,则晶胞棱长将改变
【答案】B
【解析】Ca2+配位数为与其距离最近且等距离的F-的个数,Ca2+位于体心,F-位于面心,所以Ca2+的配位
数为6,A正确;F-与K+的最近距离为棱长的,F-与Ca2+的最近距离为棱长的,所以与F-距离最近的是
Ca2+,B错误;K+位于顶点,所以K+个数=×8=1,F-位于面心,F-个数=×6=3,Ca2+位于体心,所以
Ca2+个数=1,综上,该物质的化学式为KCaF ,C正确;F-与Cl-半径不同,替换后晶胞棱长将改变,D正
3
确。
7.有关晶体的结构如图所示,下列说法中不正确的是( )
A.在NaCl晶体中,距Na+最近的Cl-有6个
B.在CaF 晶体中,每个晶胞平均占有4个Ca2+
2
C.在金刚石晶体中,最小的环上有6个C原子
D.该气态团簇分子的分子式为EF或FE
10
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司【答案】D
【解析】以顶点Na+研究,与之最近的Cl-处于晶胞棱心且关于Na+对称,即距Na+最近的Cl-有6个,故
A正确;在CaF 晶体中,Ca2+位于晶胞顶点和面心,数目为8×+6×=4,即每个晶胞平均占有4个Ca2+,
2
故B正确;金刚石晶体中,由共价键形成的最小碳环上有6个碳原子,每个碳原子形成四个共价键,从而
形成空间网状结构,由金刚石的晶胞结构图可以看出最小的环上有6个碳原子,故C正确;该气态团簇分
子中含有4个E、4个F原子,分子式应为EF 或FE,故D错误。
4 4 4 4
8.氧化锌常作为金属缓蚀剂,其结构有很多种,其中一种立方晶胞结构如图,晶胞边长为a pm,下列说
法错误的是( )
A.该晶体属于离子晶体
❑√2
B.O原子与O原子的最短距离为 a pm
2
C.Zn原子周围等距且最近的Zn原子数为6
D.该晶胞中含有4个O原子,4个Zn原子
【答案】C
❑√2
【解析】氧化锌晶体属于离子晶体,A正确;O原子与O原子的最短距离为面对角线的一半,即 a pm,B
2
正确;由晶胞示意图,取顶角Zn原子来看,其周围等距且最近的Zn原子为面上的Zn原子,顶角Zn原子
属于12个面,故Zn原子周围等距且最近的Zn原子数为12,C错误;由图可知,该晶胞含4个O原子(晶
1 1
胞内),Zn原子位于晶胞的顶角和面上,故Zn原子的个数为8× +6× =4,D正确。
8 2
9.(2024·北京东城区模拟)干冰(固态二氧化碳)在-78 ℃时可直接升华为气体,其晶胞结构如图所示。
下列说法不正确的是( )
A.CO 中有C===O键,中心原子C是sp2杂化
2
B.每个晶胞中含有4个CO 分子
2
C.每个CO 分子周围有12个紧邻的CO 分子
2 2
D.干冰升华时需克服分子间作用力
【答案】A
【解析】CO 的结构简式为O===C===O,空间构型为直线形,碳原子杂化方式为sp,故A说法错误;每个晶
2
胞中含有CO 个数为8×+6×=4,故B说法正确;根据晶胞图可知,与每个顶点的二氧化碳紧邻的CO 位
2 2
于面心位置,则每个CO 分子周围有12个紧邻的CO 分子,故C说法正确;干冰属于分子晶体,因此干冰
2 2
升华时需要克服分子间作用力,故D说法正确。
10.钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:
11
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司(1)该超导材料的最简化学式为 。
(2)Fe原子的配位数为 。
(3)该晶胞参数 a=b=0.4 nm、c=1.4 nm,阿伏加德罗常数的值为 N,则该晶体的密度为
A
g·cm-3(列出计算式)。
2×(39+56×2+79×2)
【答案】(1)KFeSe (2)4 (3) ×1021
2 2 N ×0.42×1.4
A
【解析】(1)分析晶胞在xz、yz、xy平面的投影图可知,占据顶角和体心位置的为K原子,故K原子个
1 1
数为8× +1=2,每个竖直棱上有2个Se原子,体内有2个Se原子,故Se原子个数为8× +2=4,每
8 4
1
个竖直面上有2个Fe原子,故Fe原子个数为8× =4,该物质的晶胞结构如图所示:
2
其最简化学式为KFeSe 。(2)由题给平面投影图及分析出的晶胞结构图可知,与面上的1号Fe原子在本
2 2
晶胞中距离最近且相等的有2、3、4号Se原子,在共用1号Fe原子的相邻晶胞中也有1个与4号Se原子
对称的 Se 原子与 1 号 Fe 原子距离最近且相等,故 Fe 的配位数为 4。(3)该晶胞的质量为
2×(39+56×2+79×2)
g,体积为0.4×0.4×1.4×10-21 cm3,故该晶体的密度为
N
A
2×(39+56×2+79×2)
×1021 g·cm-3。
N ×0.42×1.4
A
考法06 配位化合物与超分子
11.关于化学式为[TiCl(H O) ]Cl ·H O的配合物,下列说法中正确的是( )
2 5 2 2
A.配体是Cl-和H O,配位数是9
2
B.1 mol [TiCl(H O) ]Cl ·H O含有σ键的数目为12N (设N 为阿伏加德罗常数的值)
2 5 2 2 A A
C.内界和外界中Cl-的数目比是1∶2
D.加入足量AgNO 溶液,所有Cl-均被完全沉淀
3
【答案】C
【解析】在[TiCl(H O) ]Cl ·H O中,中心离子是Ti3+,配体是Cl-、H O,配位数为6,内界
2 5 2 2 2
12
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司和外界的Cl-数目比是1∶2;配合物中,内界Cl-不与Ag+反应,外界中的Cl-与Ag+反应;
1 mol [TiCl(H O) ]Cl ·H O含σ键数目为(6+5×2+2)N =18N ,A、B、D错误。
2 5 2 2 A A
12.将[Co(H O) ]Cl 与过量氨水、氯化铵、双氧水混合,若有活性炭催化时发生反应:
2 6 2
2[Co(H O) ]Cl +10NH ·H O+2NH Cl+H O ===2[Co(NH ) ]Cl +24H O;若没有活性炭催化
2 6 2 3 2 4 2 2 3 6 3 2
则生成[Co(NH ) Cl]Cl 。下列说法正确的是( )
3 5 2
A.基态Co原子核外电子空间运动状态有27种
B.沸点:NH <H O<H O
3 2 2 2
C.常温下,滴加AgNO 溶液可定性鉴别[Co(NH ) ]Cl 与[Co(NH ) Cl]Cl
3 3 6 3 3 5 2
D.1 mol [Co(NH ) Cl]Cl 中含有16 mol σ键
3 5 2
【答案】B
【解析】A项,Co原子的空间运动状态为15种,错误;C项,两种配合物均电离出Cl-,加
AgNO 溶液均有白色沉淀,无法定性鉴别,错误;D项,1 mol [Co(NH ) Cl]Cl 中含有(6+
3 3 5 2
3×5)mol σ键,错误。
13.(2024·甘肃卷)兴趣小组设计了从 中提取 的实验方案,下列说法正确的是
A.还原性:
B.按上述方案消耗 可回收
C.反应①的离子方程式是
D.溶液①中的金属离子是
【答案】C
【解析】金属活动性越强,金属的还原性越强,而且由题中的实验方案能得到证明,还原性从强到弱的顺
序为 Fe > Cu > Ag,A不正确;由电子转移守恒可知,1 mol Fe可以置换1 mol Cu,而1 mol Cu可以置换2
mol Ag,因此,根据按上述方案消耗1 mol Fe可回收2 mol Ag,B不正确;反应①中,氯化四氨合铜溶液与
浓盐酸反应生成氯化铜和氯化铵,该反应的离子方程式是 ,C正确;向
氯化铜和氯化铵的混合液中加入铁,铁置换出铜后生成 ,然后 被通入的氧气氧化为 ,氯化铵
水解使溶液呈酸性,在这个过程中,溶液中的氢离子参与反应,因此氢离子浓度减少促进了铁离子水解生
13
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司成氢氧化铁沉淀,氢氧化铁存在沉淀溶解平衡,因此,溶液①中的金属离子是 ,D不正确。
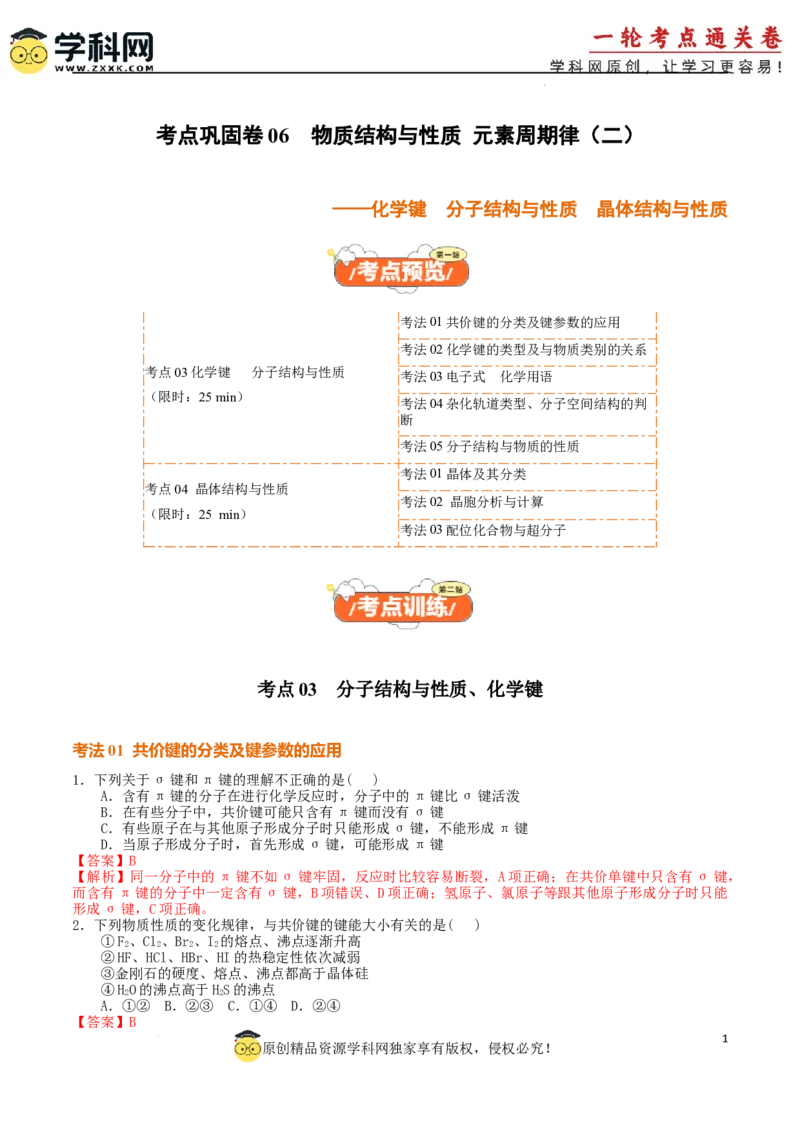
14.冠醚是一种超分子,它是否适配碱金属离子与其空腔直径和离子直径有关。二苯并-18-冠-6与 形成
的整合离子结构如图所示。
冠醚 冠醚空腔直径/pm 适合离子(直径/pm)
15-冠-5 170-220
18-冠-6 260-320
21-冠-7 340-430
下列说法错误的是
A.分子中O原子的杂化形式 B.二苯并-18-冠-6能适配
C.该冠醚分子中碳原子杂化方式有2种 D.该整合离子中配位键数目为6
【答案】B
【解析】分子中O原子形成3个σ键,含有1个孤电子对,价层电子对数为4,杂化形式为 ,A正确;
半径小于 ,二苯并-18-冠-6不能适配 ,B错误;该冠醚分子中,亚甲基中的碳原子杂化方式为
sp3,苯环上碳原子的杂化方式为sp2,故该冠醚分子中碳原子杂化方式有2种,C正确;根据整合离子结构
可知,该整合离子中配位键数目为6,D正确。
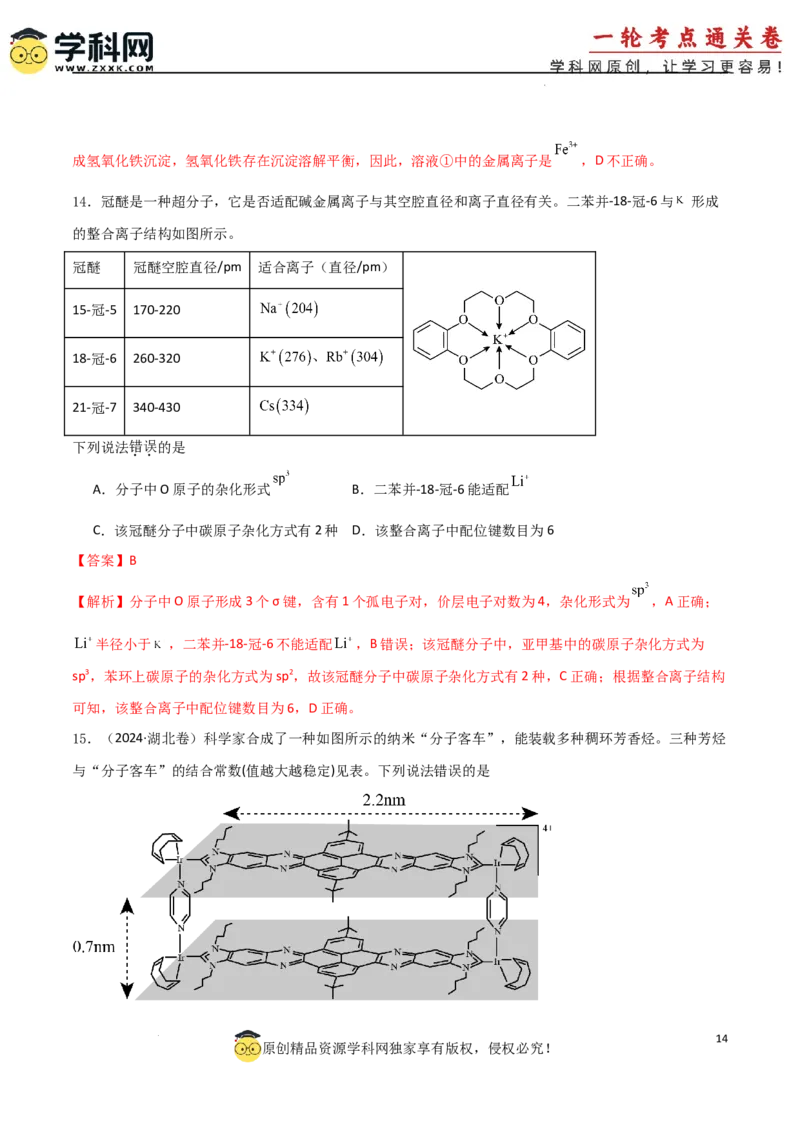
15.(2024·湖北卷)科学家合成了一种如图所示的纳米“分子客车”,能装载多种稠环芳香烃。三种芳烃
与“分子客车”的结合常数(值越大越稳定)见表。下列说法错误的是
14
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司芳烃 芘 并四苯 蒄
结构
结合常
385 3764 176000
数
A.芳烃与“分子客车”可通过分子间相互作用形成超分子
B.并四苯直立装载与平躺装载的稳定性基本相同
C.从分子大小适配看“分子客车”可装载2个芘
D.芳烃π电子数越多越有利于和“分子客车”的结合
【答案】B
【解析】“分子客车”能装载多种稠环芳香烃,故芳烃与“分子客车”通过分子间作用力形成分子聚集体
——超分子,A项正确;“分子客车”的长为2.2nm、高为0.7nm,从长的方向观察,有与并四苯分子适配
的结构,从高的方向观察则缺少合适结构,故平躺装载的稳定性大于直立装载的稳定性,B项错误;芘与
“分子客车”中中间部分结构大小适配,故从分子大小适配看“分子客车”可装载2个芘,C项正确;芘、
并四苯、蒄中碳原子都采取sp2杂化,π电子数依次为16、18、24,π电子数逐渐增多,与“分子客车”的
结合常数逐渐增大,而结合常数越大越稳定,故芳烃π电子数越多越有利于和“分子客车”结合,D项正
确。
15
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司