文档内容
解密 06 化学反应与能量
一、单选题
1.一定温度下反应4A(s)+3B(g)⇌2C(g)+D(g)经2min B的浓度减少0.6mol•L-1,对此反应速
率的表示正确的是
A.用A表示的反应速率是0.4mol•L-1•min-1
B.分别用B、C、D表示反应的速率,其比值是1:2:3
C.2min末的反应速率v(B)=0.3mol•L-1•min-1
D.在2min内用B和C表示的正反应速率的值都是逐渐减小的
2.反应A(g)+3B(g) 2C(g)+2D(g)在四种不同情况下的反应速率分别如下,其中反应速
率最大的是
A.v =0.15 mol·L-1·min-1 B.v =0.6 mol·L-1·min-1
A B
C.v =0.4 mol·L-1·min-1 D.v =0.01 mol·L-1·s-1
C D
3.T℃时在2 L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的物质
的量变化如图1所示;若保持其他条件不变,温度分别为T 和T 时,Y的体积分数与时间
1 2
的关系如图2所示。则下列结论正确的是
A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol/(L·min)
B.容器中发生的反应可表示为3X(g)+Y(g) 2Z(g)
C.保持其他条件不变,升高温度,反应的化学平衡常数K减小
D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强
4.在密闭容器中发生反应2A(g) 2B(g)+C(g),其速率可表示为 。在500℃,实验
测得体系总压强数据如下表:
t/min 0 50 100 150 200
p /kPa 200 250 275 x 293.75
总
下列说法正确的是A.0~50min,生成B的平均速率为1kPa·min−1
B.第80min的瞬时速率小于第120min的瞬时速率
C.推测上表中的x为287.5D.反应到达平衡时2v (A)=v (C)
正 逆
5.某同学为探究浓度对化学反应速率的影响,设计以下实验。
① ② ③ ④
试 1mL0.01mol/L
1mL0.01mol/L酸性 1mL0.01mol/L酸性 1mL0.01mol/L酸性
剂 酸性高锰酸钾水
高锰酸钾水溶液 高锰酸钾水溶液 高锰酸钾水溶液
a 溶液
1mL以浓盐酸为
试
2mL0.1mol/LH C O 2mL0.2mol/LH C O 1mL0.2mol/LH C O 溶剂配制的
2 2 4 2 2 4 2 2 4
剂
水溶液 水溶液 水溶液 0.2mol/LH C O
2 2 4
b
水溶液
褪
色
690s 677s 600s
时
间
下列说法错误的是A.对比实验①、②可知,HC O 水溶液浓度增大,反应速率加快
2 2 4
B.对比实验②、③可知,酸性高锰酸钾水溶液浓度增大,反应速率加快
C.为验证H+浓度对反应速率的影响,设计实验④并与③对照
D.实验③的离子方程式为2 +6H++5H C O=2Mn2++10CO ↑+8H O
2 2 4 2 2
6.如图,反应 可以通过两种不同的进程发生:
(a)反应 直接发生,半衰期与初始浓度无关。在294K时,半衰期为1000min,在
340K时,A浓度降至原始浓度的1/1024所需的时间为0.10min。
(b)反应通过两步进行。
则下面的说法中,错误的是
A.A*是反应的催化剂
B.C比A更稳定
C.(b)的反应方式活化能降低,从而能提高反应速率D.(a)的反应方式中反应速率与A的浓度成正比
7.选择不同的反应探究化学反应速率的影响因素,所用试剂不合理的是
a. (观察气泡产生的快慢)
b. (观察浑浊产生的快慢)
反应 影响因素 所用试剂
块状CaCO 、0.5 mol/L HCl
3
A a 接触面积
粉末状CaCO 、0.5 mol/L HCl
3
块状CaCO 、0.5 mol/L HCl
3
B a H+浓度
块状CaCO 、3.0 mol/LHCl
3
0.1 mol/L Na SO、稀HSO
2 2 3 2 4
C b H+浓度
0.1mol/L Na SO、浓HSO
2 2 3 2 4
0.1 mol/L Na SO、0.1 Na SO HSO 、冷水
2 2 3 2 2 3 2 4
D b 温度
0.1 mol/L Na SO、0.1 Na SO HSO 、热水
2 2 3 2 2 3 2 4
A.A B.B C.C D.D
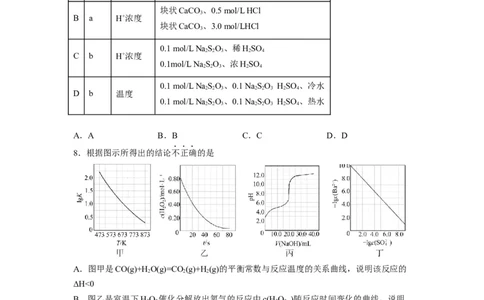
8.根据图示所得出的结论不正确的是
A.图甲是CO(g)+HO(g)=CO(g)+H(g)的平衡常数与反应温度的关系曲线,说明该反应的
2 2 2
ΔH<0
B.图乙是室温下HO 催化分解放出氧气的反应中c(HO )随反应时间变化的曲线,说明
2 2 2 2
随着反应的进行HO 分解速率保持不变
2 2
C.图丙是室温下用0.1000 mol·L-1NaOH溶液滴定20.00 mL 0.1000 mol·L-1某一元酸HX的
滴定曲线,说明HX是弱酸
D.图丁是室温下用NaSO 除去溶液中Ba2+达到沉淀溶解平衡时,溶液中c(Ba2+ )与c(SO
2 4
)的关系曲线,说明溶液中c(SO )越大c(Ba2+ )越小
9.已知 。一定温度下,在体积恒定的密闭容器中,
加入1mol 与1mol ,下列说法正确的是A.充分反应后,放出热量为akJ
B.若增大Y的浓度,正反应速率增大,逆反应速率减小
C.当X的物质的量分数不再改变,表明该反应已达平衡
D.当反应达到平衡状态时,X与W的物质的量浓度之比一定为1:2
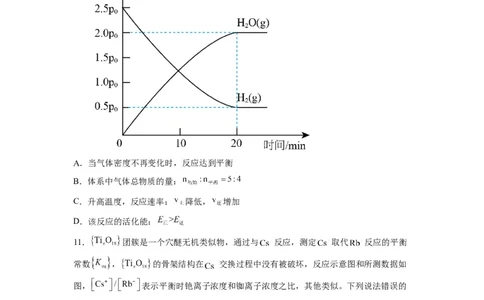
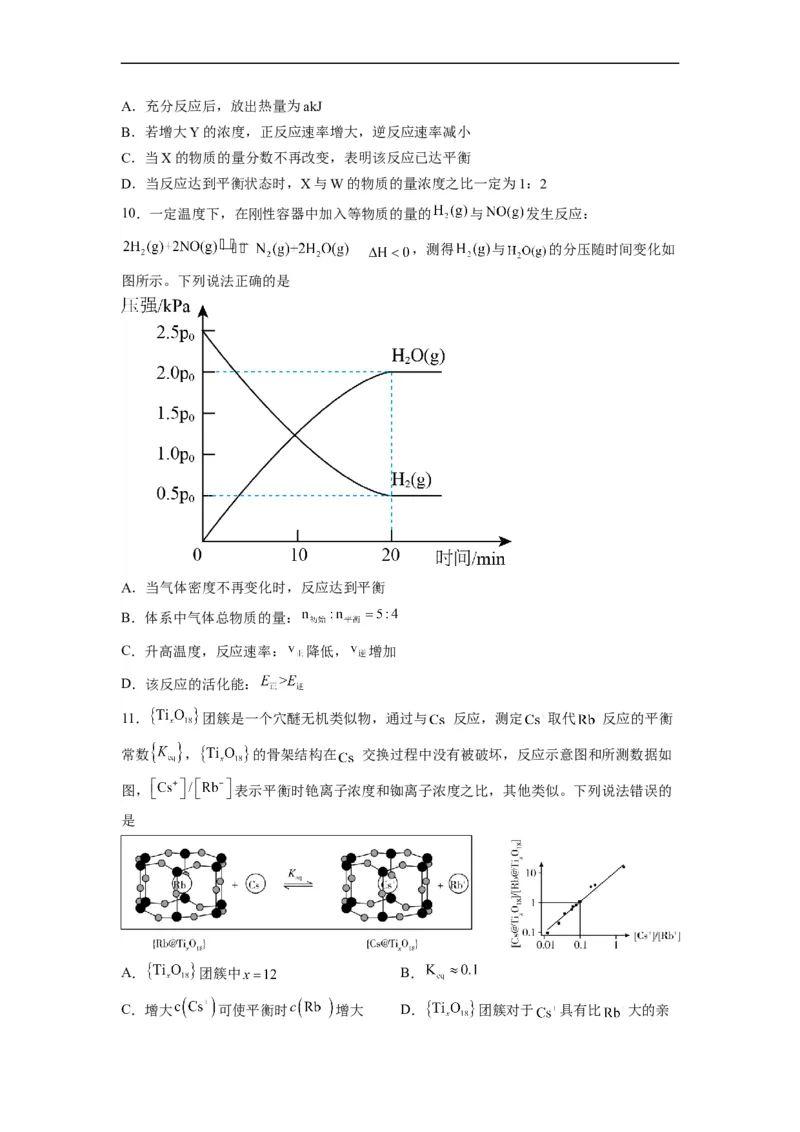
10.一定温度下,在刚性容器中加入等物质的量的 与 发生反应:
,测得 与 的分压随时间变化如
图所示。下列说法正确的是
A.当气体密度不再变化时,反应达到平衡
B.体系中气体总物质的量:
C.升高温度,反应速率: 降低, 增加
D.该反应的活化能:
11. 团簇是一个穴醚无机类似物,通过与 反应,测定 取代 反应的平衡
常数 , 的骨架结构在 交换过程中没有被破坏,反应示意图和所测数据如
图, 表示平衡时铯离子浓度和铷离子浓度之比,其他类似。下列说法错误的
是
A. 团簇中 B.
C.增大 可使平衡时 增大 D. 团簇对于 具有比 大的亲和力
12.某小组同学进行了如下实验:
① 溶液和 溶液各1mL混合得到红色溶液a,均分溶
液a置于b、c两支试管中;
②向b中滴加3滴饱和 溶液,溶液颜色加深;
③再向上述b溶液中滴加3滴 溶液,溶液颜色变浅且出现浑浊;
④向c中逐渐滴加 溶液2mL,过程中溶液颜色先变深后变浅。
下列分析不正确的是
A.实验②中增大 浓度使平衡 正向移动
B.实验③中发生反应:
C.实验③和④中溶液颜色变浅的原因相同
D.实验②、③、④均可说明浓度改变对平衡移动的影响
13.在恒温恒压下,某一体积可变的密闭容器中发生反应 ,
时达到平衡后,在 时改变某一条件,达到新平衡,反应过程v—t如图所示。有关叙述中,
错误的是
A. 时,v >v
正 逆
B. 时向密闭容器中加入物质C
C. 、 两平衡状态中c(C)不相等
D. 时v 先瞬时减小后逐渐增大直至与原平衡相等后保持不变
正
14.某温度下,向密闭容器中充入等物质的量的 和 ,发生反应
。达到平衡后,下列说法正确的是
A.增大压强, ,平衡常数增大
B.加入催化剂,平衡时 的浓度增大
C.恒温下,移走一定量的 , 变大, 变小
D.恒容下,充入一定量的 ,平衡时 的体积分数一定降低
15.一定条件下合成乙烯: 。已知其它条件不变时,温度对 的平衡转化率和催化剂催化效率的影响如图所示。下列说法一定正确的
是
A.平衡常数 B.反应速率:
C.所含总能量: D.经过相同时间后得到乙烯的量:X>Y
16.在298K和100kPa压力下,已知金刚石和石墨的熵、燃烧热和密度分别为:
物质 S/(J·K−1·mol−1) ∆H/(kJ·mol−1) ρ/(kg·m−3)
C(金刚石) 2.4 −395.40 3513
C(石墨) 5.7 −393.51 2260
此条件下,对于反应C(石墨)→C(金刚石),下列说法正确的是A.该反应的∆H<0,∆S<0
B.由公式∆G=∆H−T∆S可知,该反应∆G=985.29kJ·mol−1
C.金刚石比石墨稳定
D.超高压条件下,石墨有可能变为金刚石
二、填空题
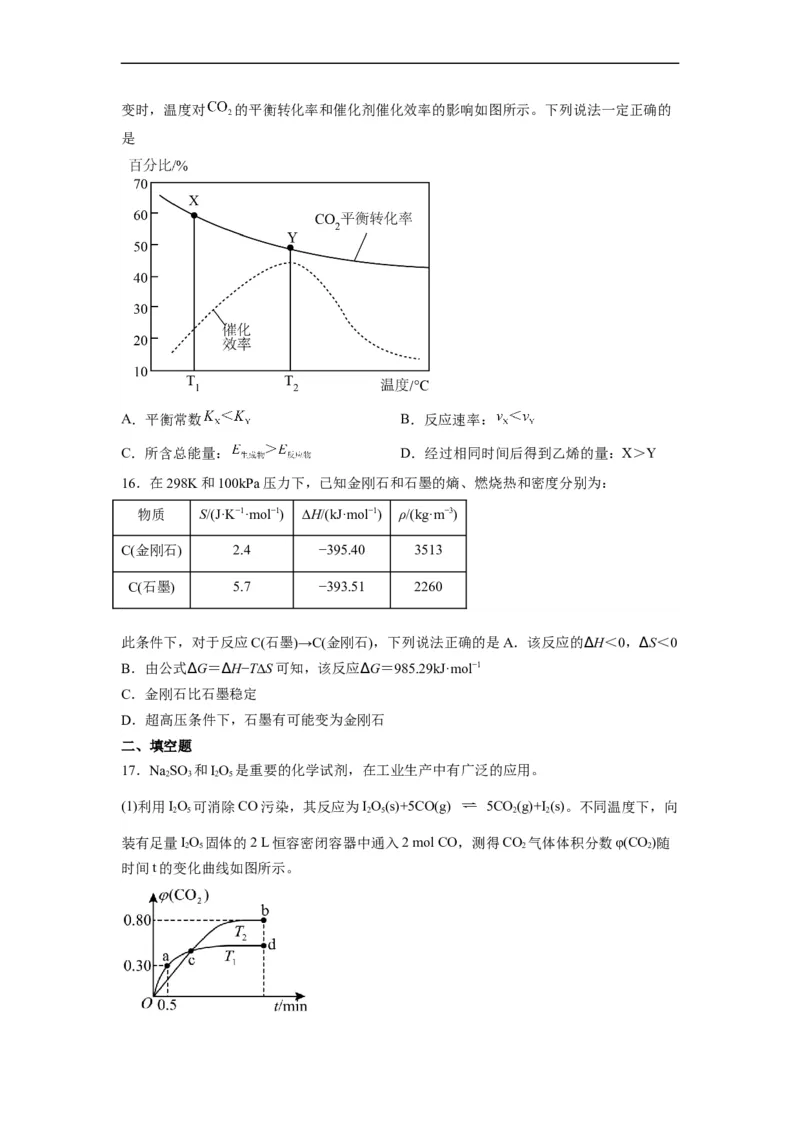
17.NaSO 和IO 是重要的化学试剂,在工业生产中有广泛的应用。
2 3 2 5
(1)利用IO 可消除CO污染,其反应为IO(s)+5CO(g) 5CO(g)+I (s)。不同温度下,向
2 5 2 5 2 2
装有足量IO 固体的2 L恒容密闭容器中通入2 mol CO,测得CO 气体体积分数φ(CO)随
2 5 2 2
时间t的变化曲线如图所示。①T 时,前0.5 min内平均反应速率v(CO)=___________。
1
②b点和d点的化学平衡常数:K___________(填“>”“<”或“=”)K 。
b d
③b点时,CO的转化率为___________。
(2)Na SO 氧化分为富氧区和贫氧区两个阶段,为确定贫氧区速率方程v=k·ca(S )·cb(O )中
2 3 2
a、b的值(取整数),进行实验。
①当溶解氧浓度为4.0 mg·L-1时,c(Na SO )与速率数值关系如下表,则a=___________。
2 3
c(Na SO )/×10-3 3.65 5.65 7.65 11.65
2 3
v/×10-6 10.2 24.4 44.7 103.6
②两个阶段不同温度的速率常数之比如下表。
反应阶段 速率方程
富氧区 v=k·c(S )·c(O) 1.47
2
贫氧区 v=k·c3(S )·c2(O ) 2.59
2
已知,ln =- - ),R为常数,T”或“<”)E(贫
1 2 a a
氧区)。
18.在2020年中央经济工作会议上,我国明确提出“碳达峰”与“碳中和”目标。使利用
CO 合成高价值化学品更突显其重要性。
2
Ⅰ.工业上可以利用CO 和H 合成CHOH:CO(g)+3H(g) CHOH(g)+H O(g)ΔH<0。该反
2 2 3 2 2 3 2
应在起始温度和体积均相同(T℃、1L)的两个密闭容器中分别进行,反应起始物质的量如表:
⇌
反应条件 CO(mol) H(mol) CHOH(mol) HO(mol)
2 2 3 2
①恒温恒容 1 3 0 0
②绝热恒容 0 0 1 1
(1)达到平衡时,CO 的体积分数φ①_____φ②(填“>”“<”或“=”)。
2
(2)当_____= v (H )时,说明反应在条件②达到平衡状态。
逆 2
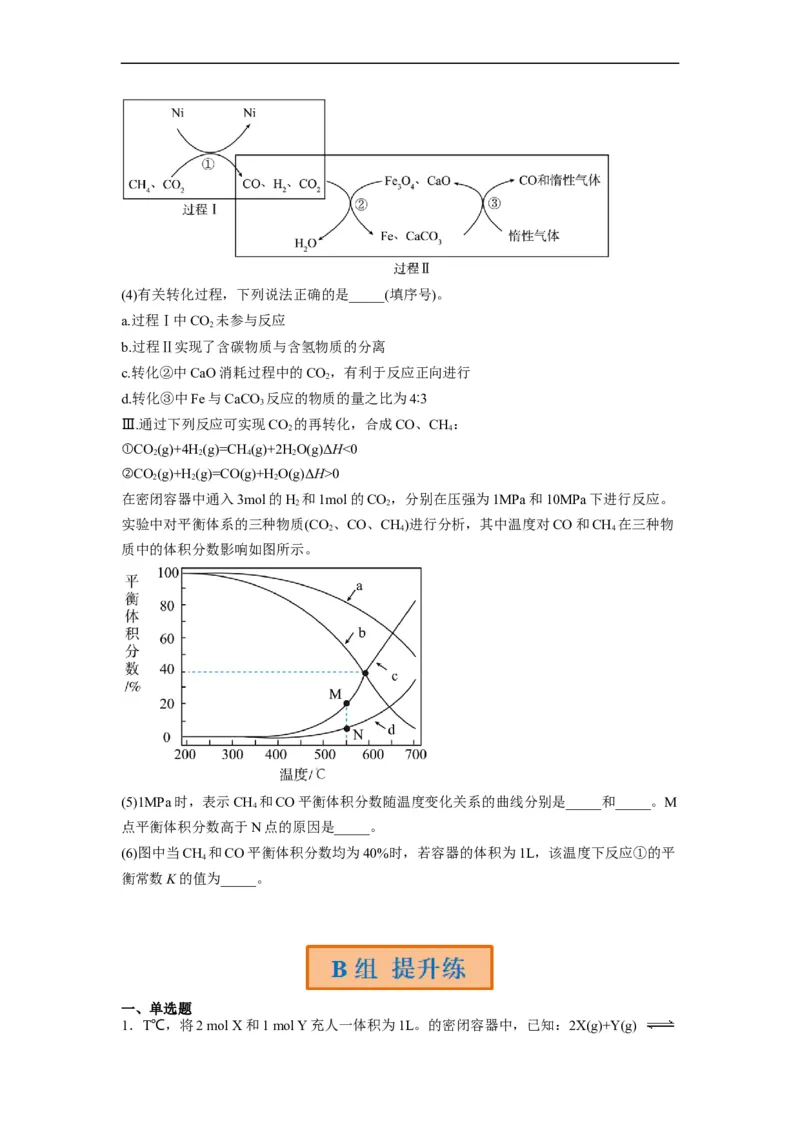
Ⅱ.利用CH 超干重整CO 的催化转化如图所示:
4 2
(3)CH 与CO 超干重整反应的方程式为_____。
4 2(4)有关转化过程,下列说法正确的是_____(填序号)。
a.过程Ⅰ中CO 未参与反应
2
b.过程Ⅱ实现了含碳物质与含氢物质的分离
c.转化②中CaO消耗过程中的CO,有利于反应正向进行
2
d.转化③中Fe与CaCO 反应的物质的量之比为4∶3
3
Ⅲ.通过下列反应可实现CO 的再转化,合成CO、CH:
2 4
①CO(g)+4H(g)=CH (g)+2HO(g)ΔH<0
2 2 4 2
②CO (g)+H(g)=CO(g)+HO(g)ΔH>0
2 2 2
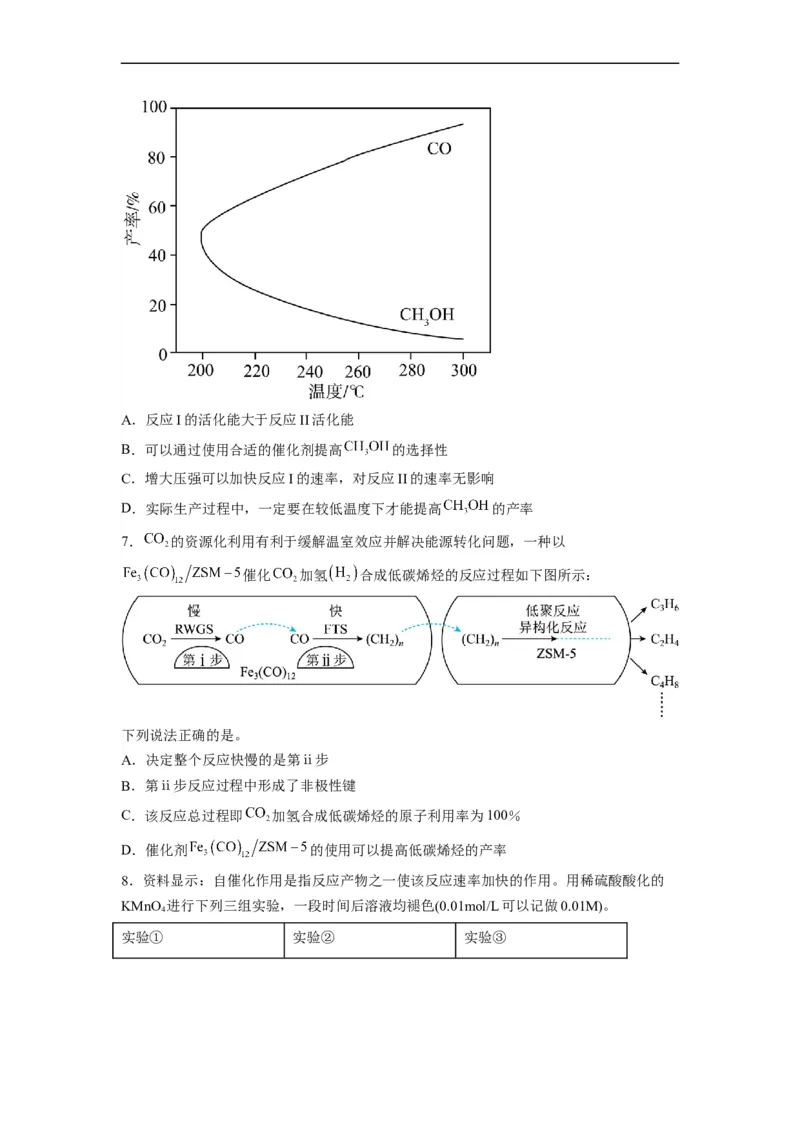
在密闭容器中通入3mol的H 和1mol的CO,分别在压强为1MPa和10MPa下进行反应。
2 2
实验中对平衡体系的三种物质(CO、CO、CH)进行分析,其中温度对CO和CH 在三种物
2 4 4
质中的体积分数影响如图所示。
(5)1MPa时,表示CH 和CO平衡体积分数随温度变化关系的曲线分别是_____和_____。M
4
点平衡体积分数高于N点的原因是_____。
(6)图中当CH 和CO平衡体积分数均为40%时,若容器的体积为1L,该温度下反应①的平
4
衡常数K的值为_____。
一、单选题
1.T℃,将2 mol X和1 mol Y充人一体积为1L。的密闭容器中,已知:2X(g)+Y(g)2Z(s) △H=-M kJ·mol-1。10 min后达到平衡,生成0.2 mol Z,共放出热量N kJ,下列说法
正确的是
A.在10 min时,X的反应速率为0.02 mol·L-1·min-l
B.在0~10 min内,Y的反应速率为 mol·L-1·min-l
C.增加Z的物质的量加快逆反应速率
D.反应达平衡后,保持T℃,通入稀有气体增加压强,则化学反应速率变快
2.高炉炼铁中的一个反应为 ,在1100℃
下,若CO起始浓度为1.2mol/L,10min后达到平衡时 的体积分数为 ,下列说法错误
的是
A.1100℃下,此反应的平衡常数
B.达到平衡过程中,反应的平均速率为
C.达到平衡后,若增大 ,则达到新平衡时, 增大
D.测得某时刻 ,则此时
3.在T℃时,向一个3L的密闭容器中通入4mol 、amol ,发生反应:
。此时 的平衡转化率为60%。下列说法错误
的是
A.当混合气体的平均摩尔质量不变时,反应达到平衡
B.当 时,反应达到平衡
C.反应过程中分离出 ,正反应速率增大
D.平衡时,若 的转化率为60%,则a=5
4.恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应:2NH (g) N(g)
3 2
+3H (g),测得不同起始浓度( )和催化剂表面积下氨浓度随时间的变化,如表
2 ⇌
所示,下列说法不正确的是
编号 0 20 40 60 80
① a 2.40 2.00 1.60 1.20 0.80
② a 1.20 0.80 0.40 x
③ 2a 2.40 1.60 0.80 0.40 0.40A.实验①,0~20min,
B.实验②,60min时处于平衡状态,
C.相同条件下,增加氨气的浓度,反应速率增大
D.相同条件下,增加催化剂的表面积,反应速率增大
5.用下图装置探究原电池中的能量转化。图中注射器用来收集气体并读取气体体积,记录
实验数据如下表:
① ②
气体体积/ 溶液温度/ 气体体积/ 溶液温度/
0 0 22.0 0 22.0
8.5 30 24.8 50 23.8
10.5 50 26.0 — —
下列说法正确的是A.两个装置中 均为负极,发生氧化反应
B. 内,生成气体的平均速率①>②
C.时间相同时,对比两装置的溶液温度,说明反应释放的总能量①>②
D.生成气体体积相同时,对比两装置的溶液温度,说明②中反应的化学能分转化为电能
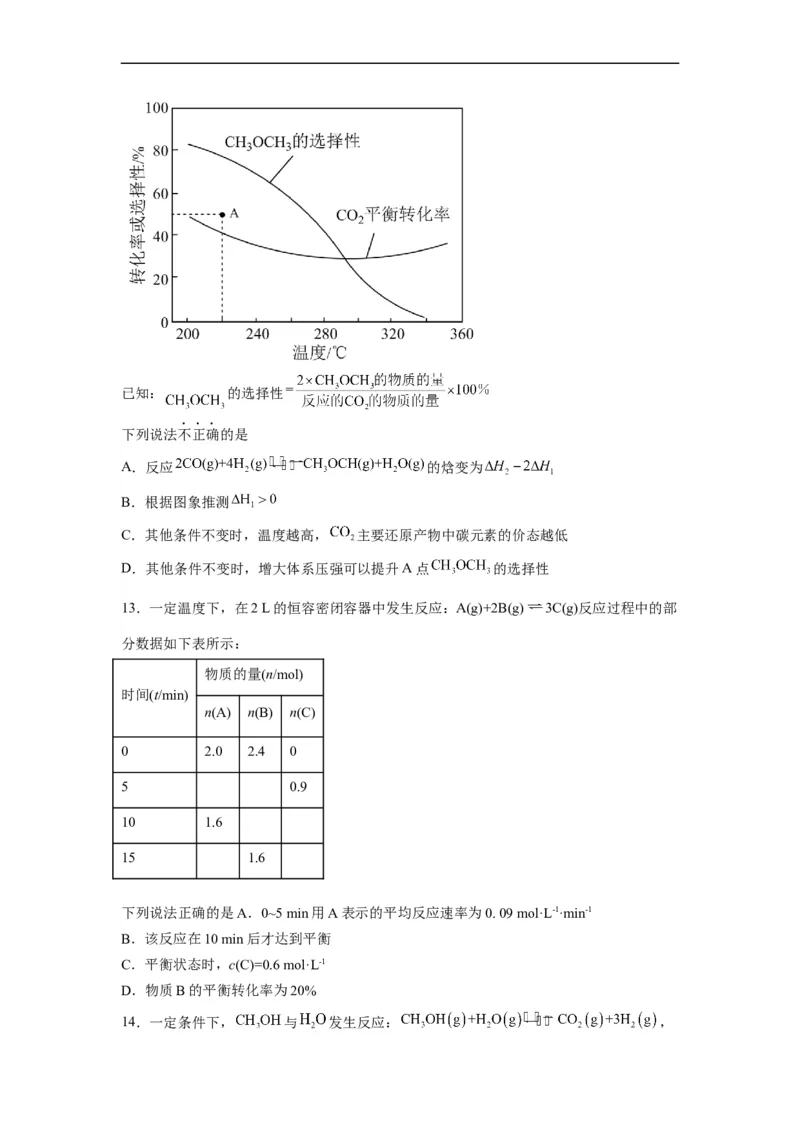
6.为了实现“碳中和”,利用 合成 的反应为:I.
,副反应为:II.
,已知温度对 、CO的平衡产率影响如
下图所示,下列说法中正确的是A.反应I的活化能大于反应II活化能
B.可以通过使用合适的催化剂提高 的选择性
C.增大压强可以加快反应I的速率,对反应II的速率无影响
D.实际生产过程中,一定要在较低温度下才能提高 的产率
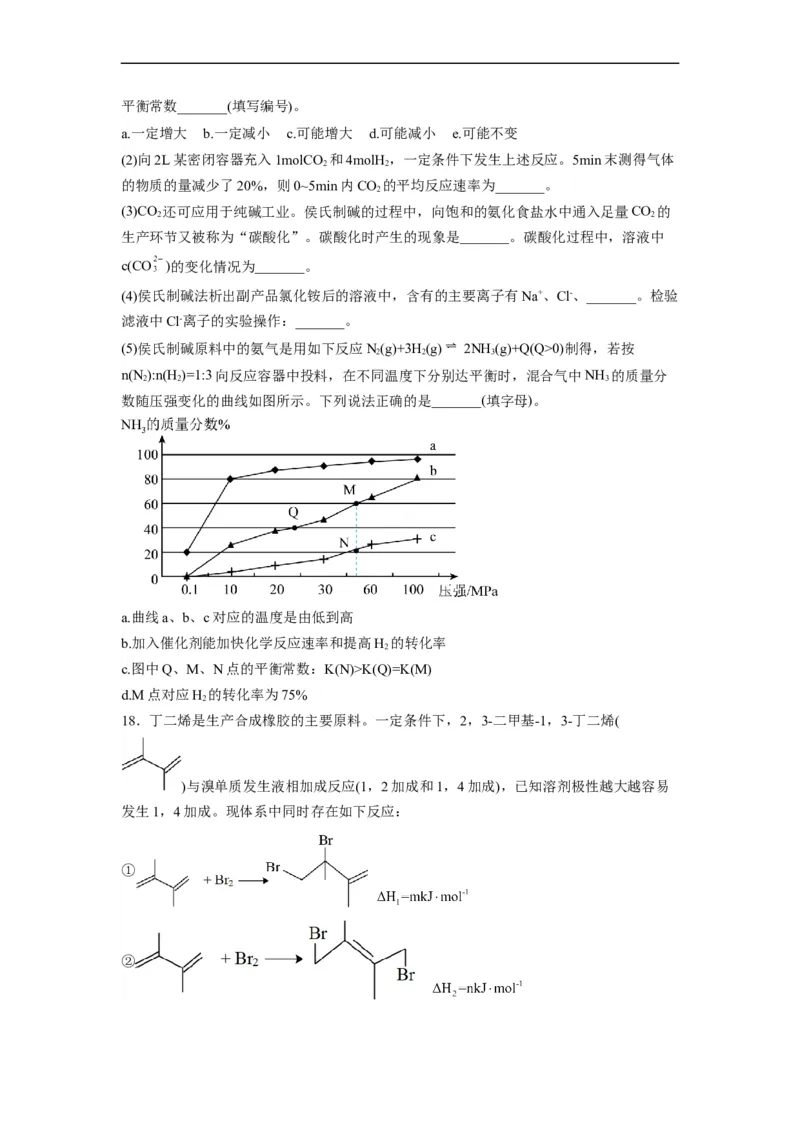
7. 的资源化利用有利于缓解温室效应并解决能源转化问题,一种以
催化 加氢 合成低碳烯烃的反应过程如下图所示:
下列说法正确的是。
A.决定整个反应快慢的是第ⅱ步
B.第ⅱ步反应过程中形成了非极性键
C.该反应总过程即 加氢合成低碳烯烃的原子利用率为100%
D.催化剂 的使用可以提高低碳烯烃的产率
8.资料显示:自催化作用是指反应产物之一使该反应速率加快的作用。用稀硫酸酸化的
KMnO 进行下列三组实验,一段时间后溶液均褪色(0.01mol/L可以记做0.01M)。
4
实验① 实验② 实验③1mL0.01M的KMnO 溶
4
1mL0.01M的KMnO 溶 1mL0.01M的KMnO 溶
液和1mL0.1M的HC O 4 4
2 2 4
液和1mL0.1M的HC O 液和1mL0.1M的HC O
溶液混合 2 2 4 2 2 4
溶液混合 溶液混合
褪色 比实验①褪色快 比实验①褪色快
下列说法不正确的是A.实验①中发生氧化还原反应,HC O 是还原剂,产物MnSO 能起
2 2 4 4
自催化作用
B.实验②褪色比①快,是因为MnSO 的催化作用加快了反应速率
4
C.实验③褪色比①快,是因为Cl-的催化作用加快了反应速率
D.若用1mL0.2M的HC O 做实验①,推测比实验①褪色快
2 2 4
9.对于反应 ,在温度一定时,平衡体系中 的体积分数
随压强的变化情况如图所示。下列说法中,正确的是
A.A、D两点对应状态的正反应速率大小关系:v(A)>v(D)
B.A、B、C、D、E各点对应状态中,v(正)<v(逆)的是E
C.维持 不变,E→A所需时间为 ,维持 不变,D→C所需时间为 ,则
D.欲使C状态沿平衡曲线到达A状态,从理论上,可由 无限缓慢降压至 达成
10.T℃时,降冰片烯在催化剂作用下聚合,反应物浓度与催化剂种类及反应时间的关系如
表所示。下列说法不正确的是
时间/min
编号 浓度/(mol/L) 0 50 100 150 200 250
催化剂种类
1 催化剂I 3.00 2.40 1.80 1.20 0.60 02 催化剂II 3.00 1.80 0.60 0 0 0
3 催化剂III 1.50 0.90 0.30 0 0 0
A.催化效果:催化剂II优于催化剂I
B.编号2和3实验中,反应至125min时,反应物恰好都消耗完
C.编号2实验中,以反应物浓度变化表示的反应速率为0.024mol•L-1•min-1
D.其他条件相同时,反应物浓度越大,反应速率越大
11.将xmolH S气体平均分成两份,分别通入容器A、容器B(容积均为1L),其中一容器
2
为绝热环境,另一容器为25℃恒温环境,在容器内均发生:
(25℃),相关数据如下表:
时间/min 0 10 20 30 40 50 60
容器A 0 0.8 1.5 2 2.3 2.4 2.4
容器B 0 1 1.8 2.5 3 3 3
下列说法正确的是A.根据上表信息,可推算出x=3
B.容器A为25℃恒温环境,容器B为绝热环境
C.1~60min内,25℃恒温环境反应速率可表示为v(H S生成)
2
D.可通过降低容器的温度,从而加快逆反应的速率,达到抑制HS气体分解的目的
2
12. 催化加氢合成二甲醚是一种 资源化利用的方法,其过程中主要发生如下两个
反应:
反应Ⅰ:
反应Ⅱ:
在恒压、 和 的起始量一定的条件下, 平衡转化率和平衡时 的选择性
随温度的变化如下图所示。已知: 的选择性
下列说法不正确的是
A.反应 的焓变为
B.根据图象推测
C.其他条件不变时,温度越高, 主要还原产物中碳元素的价态越低
D.其他条件不变时,增大体系压强可以提升A点 的选择性
13.一定温度下,在2 L的恒容密闭容器中发生反应:A(g)+2B(g) 3C(g)反应过程中的部
分数据如下表所示:
物质的量(n/mol)
时间(t/min)
n(A) n(B) n(C)
0 2.0 2.4 0
5 0.9
10 1.6
15 1.6
下列说法正确的是A.0~5 min用A表示的平均反应速率为0. 09 mol·L-1·min-1
B.该反应在10 min后才达到平衡
C.平衡状态时,c(C)=0.6 mol·L-1
D.物质B的平衡转化率为20%
14.一定条件下, 与 发生反应: ,反应起始时 在恒压条件下,反应达到平衡时 的体积分数
与M和T(温度)的平衡关系如图所示。下列说法正确的是
A.该反应在高温条件下能自发进行
B.图中M的大小关系为
C.图中Q点对应的平衡混合物中
D.温度不变时,增大Q点对应的平衡体系压强,则 减小
15.下列说法正确的是
A.ΔH<0,ΔS >0的反应在任何条件下都可以实际发生
B.O(g) +2SO (g) 2SO (g)在298K时平衡常数K=6.8×1024,说明在该温度下反应速率
2 2 3
很快
C.金属单质导电是物理变化,电解质溶液导电是化学变化
D.可用装置证明元素非金属性:N>C>Si
16.关于可自发反应2SO (g) + O(g) 2SO (g) △H, 下列说法正确的是
2 2 3
A.该反应△S>0
B.使用催化剂不能降低该反应的△H
C.反应中每消耗22.4LO 转移电子数目约等于4×6.02× 1023
2
D.其它条件相同,温度升高或增大压强,可以提高SO 的转化率
2
二、填空题
17.捕集CO 的技术对解决全球温室效应意义重大。目前国际空间站处理CO 的一个重要
2 2
方法是将CO 还原,涉及的化学反应如下:CO(g)+4H(g) CH(g)+2HO(g)+Q(Q>0)
2 2 2 4 2
(1)该反应的平衡常数表达式为_______。如果改变某种条件,平衡向正反应方向移动,则平衡常数_______(填写编号)。
a.一定增大 b.一定减小 c.可能增大 d.可能减小 e.可能不变
(2)向2L某密闭容器充入1molCO 和4molH ,一定条件下发生上述反应。5min末测得气体
2 2
的物质的量减少了20%,则0~5min内CO 的平均反应速率为_______。
2
(3)CO 还可应用于纯碱工业。侯氏制碱的过程中,向饱和的氨化食盐水中通入足量CO 的
2 2
生产环节又被称为“碳酸化”。碳酸化时产生的现象是_______。碳酸化过程中,溶液中
c(CO )的变化情况为_______。
(4)侯氏制碱法析出副产品氯化铵后的溶液中,含有的主要离子有Na+、Cl-、_______。检验
滤液中Cl-离子的实验操作:_______。
(5)侯氏制碱原料中的氨气是用如下反应N(g)+3H(g) 2NH (g)+Q(Q>0)制得,若按
2 2 3
n(N ):n(H)=1:3向反应容器中投料,在不同温度下分别达平衡时,混合气中NH 的质量分
2 2 3
数随压强变化的曲线如图所示。下列说法正确的是_______(填字母)。
a.曲线a、b、c对应的温度是由低到高
b.加入催化剂能加快化学反应速率和提高H 的转化率
2
c.图中Q、M、N点的平衡常数:K(N)>K(Q)=K(M)
d.M点对应H 的转化率为75%
2
18.丁二烯是生产合成橡胶的主要原料。一定条件下,2,3-二甲基-1,3-丁二烯(
)与溴单质发生液相加成反应(1,2加成和1,4加成),已知溶剂极性越大越容易
发生1,4加成。现体系中同时存在如下反应:
①
②③
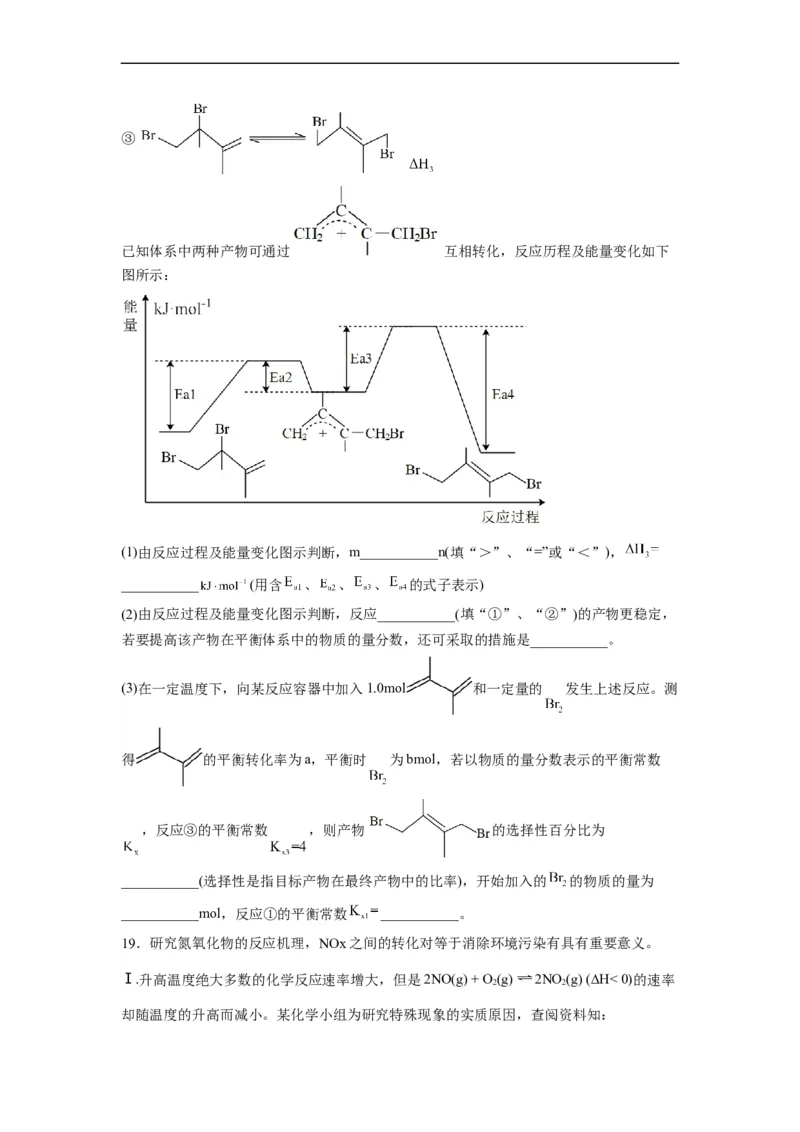
已知体系中两种产物可通过 互相转化,反应历程及能量变化如下
图所示:
(1)由反应过程及能量变化图示判断,m___________n(填“>”、“=”或“<”),
___________ (用含 、 、 、 的式子表示)
(2)由反应过程及能量变化图示判断,反应___________(填“①”、“②”)的产物更稳定,
若要提高该产物在平衡体系中的物质的量分数,还可采取的措施是___________。
(3)在一定温度下,向某反应容器中加入1.0mol 和一定量的 发生上述反应。测
得 的平衡转化率为a,平衡时 为bmol,若以物质的量分数表示的平衡常数
,反应③的平衡常数 ,则产物 的选择性百分比为
___________(选择性是指目标产物在最终产物中的比率),开始加入的 的物质的量为
___________mol,反应①的平衡常数 ___________。
19.研究氮氧化物的反应机理,NOx之间的转化对等于消除环境污染有具有重要意义。
Ⅰ.升高温度绝大多数的化学反应速率增大,但是2NO(g) + O (g) 2NO (g) (∆H< 0)的速率
2 2
却随温度的升高而减小。某化学小组为研究特殊现象的实质原因,查阅资料知:2NO(g)+O (g) 2NO (g)的反应历程分两步:
2 2
①2NO(g) NO(g) (快) v =k c2(NO) v =k c(NO) ∆H < 0
2 2 1正 1正 1逆 1逆 2 2 1
②N O(g)+O(g) 2NO (g) (慢) v =k c(NO) c(O ) v =k c2(NO ) ∆H < 0
2 2 2 2 2正 2正 2 2 2 2逆 2逆 2 2
(1)一定温度下,反应2NO(g)+O (g) 2NO (g)达到平衡状态,请写出用k 、k 、k 、
2 2 1正 1逆 2正
k 表示的平衡常数表达式K=_______,根据速率方程分析,升高温度该反应速率减小的原
2逆
因是_______ (填字母)。
a. k 增大,c(NO)增大 b. k 减小,c(NO)减小 c. k 增大,c(NO)减小 d. k 减小,
2正 2 2 2正 2 2 2正 2 2 2正
c(NO)增大
2 2
(2)由实验数据得到v ~c(O)的关系可用如图表示。当x点升高到某一温度时,反应重新
2正 2
达到平衡,则变为相应的点为_______(填字母)。
Ⅱ.回答下列问题
(3)已知:NO(g) 2NO (g) ∆H> 0,将一定量NO 气体充入恒容的密闭容器中,控制反
2 4 2 2 4
应温度为T
1。
①下列可以作为反应达到平衡的判据是_______。
A.气体的压强不变 B.容器内气体的密度不变 C.K不变 D.v (N O) v
正 2 4 =2 逆
(NO ) E.容器内颜色不变
2
② t 时刻反应达到平衡,混合气体平衡总压强P,NO 气体的平衡转化率为75%,则反应
1 2 4
NO(g) 2NO (g)的平衡常数Kp=_______。[对于气相反应,用某组分B的平衡压强p(B)
2 4 2
代替物质的量浓度c(B)也可表示平衡常数,记作kp,如p(B)=p·x(B),p为平衡总压强,
x(B)为平衡系统中B的物质的量分数]
③反应温度T 时,c(NO)随t(时间)变化曲线如图1,画出0~t 时段,c(NO )随t变化曲线。
1 2 4 2 2
保持其它条件不变,改变反应温度为T(T >T),再次画出0~t 时段,c(NO )随t变化趋势
2 2 1 2 2
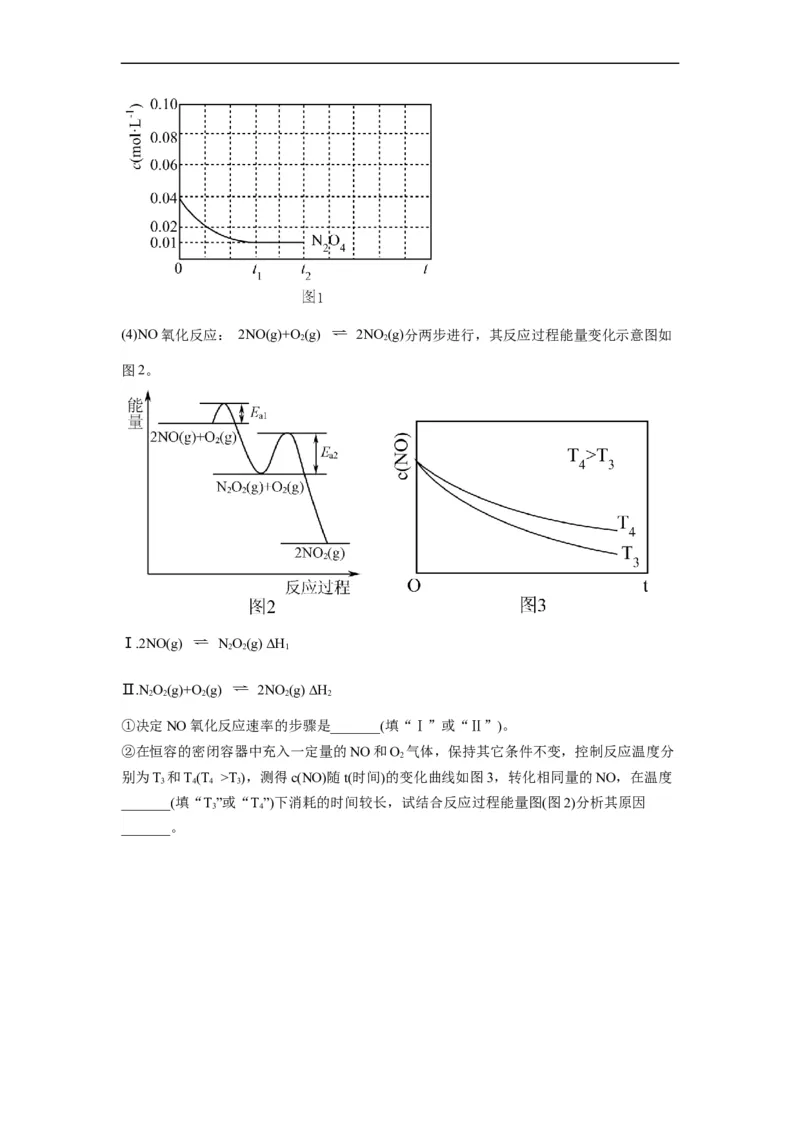
的曲线。_______(4)NO氧化反应: 2NO(g)+O (g) 2NO (g)分两步进行,其反应过程能量变化示意图如
2 2
图2。
Ⅰ.2NO(g) NO(g) ∆H
2 2 1
Ⅱ.N O(g)+O(g) 2NO (g) ∆H
2 2 2 2 2
①决定NO氧化反应速率的步骤是_______(填“Ⅰ”或“Ⅱ”)。
②在恒容的密闭容器中充入一定量的NO和O 气体,保持其它条件不变,控制反应温度分
2
别为T 和T(T >T ),测得c(NO)随t(时间)的变化曲线如图3,转化相同量的NO,在温度
3 4 4 3
_______(填“T”或“T”)下消耗的时间较长,试结合反应过程能量图(图2)分析其原因
3 4
_______。