文档内容
解密 11 化学实验
一、选择题
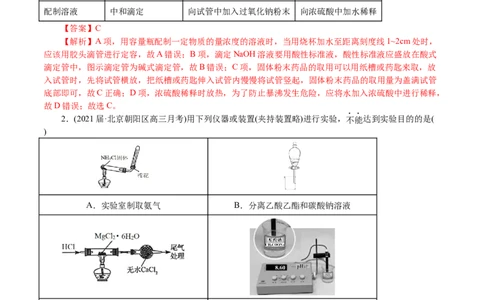
1.(2021届·浙江选考模拟)下列实验操作或装置(略去部分夹持仪器)正确的是( )
A B C D
配制溶液 中和滴定 向试管中加入过氧化钠粉末 向浓硫酸中加水稀释
【答案】C
【解析】A项,用容量瓶配制一定物质的量浓度的溶液时,当用烧杯加水至距离刻度线1~2cm处时,
应该用胶头滴管进行定容,故A错误;B项,滴定NaOH溶液要用酸性标准液,酸性标准液应盛放在酸式
滴定管中,图示滴定管为碱式滴定管,故B错误;C项,固体粉末药品的取用可以用纸槽或药匙来取,放
入试管时,先将试管横放,把纸槽或药匙伸入试管内慢慢将试管竖起,固体粉末药品的取用量为盖满试管
底部即可,故C正确;D项,浓硫酸稀释时放热,为了防止暴沸发生危险,应将水加入浓硫酸中进行稀释,
故D错误;故选C。
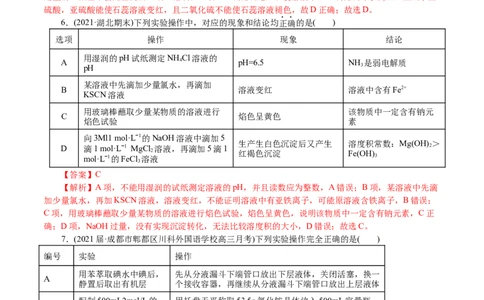
2.(2021届·北京朝阳区高三月考)用下列仪器或装置(夹持装置略)进行实验,不能达到实验目的的是(
)
A.实验室制取氨气 B.分离乙酸乙酯和碳酸钠溶液
C.制备无水氯化镁 D.证明醋酸为弱酸
【答案】A
【解析】A项,实验室制取氨气的药品为氯化铵和氢氧化钙固体,不能直接加热氯化铵,氯化铵受热
分解生成氨气和氯化氢,氯化氢和氨气在试管口反应生成氯化铵,得不到氨气,故A符合题意;B项,乙
酸乙酯不溶于碳酸钠溶液,乙酸乙酯密度比水密度小,用分液漏斗分离乙酸乙酯和碳酸钠溶液,故B不符
合题意;C项,氯化镁属于强酸弱碱盐,能够发生水解,溶液显酸性,加入酸能够抑制氯化镁的水解;在
HCl气流中加热MgCl ∙6H O得到氯化镁,故C不符合题意;D项,醋酸钠溶液的pH为8.6,说明该盐显碱
2 2
性,醋酸钠为强碱弱酸盐,说明醋酸是弱酸,故D不符合题意。故选A。
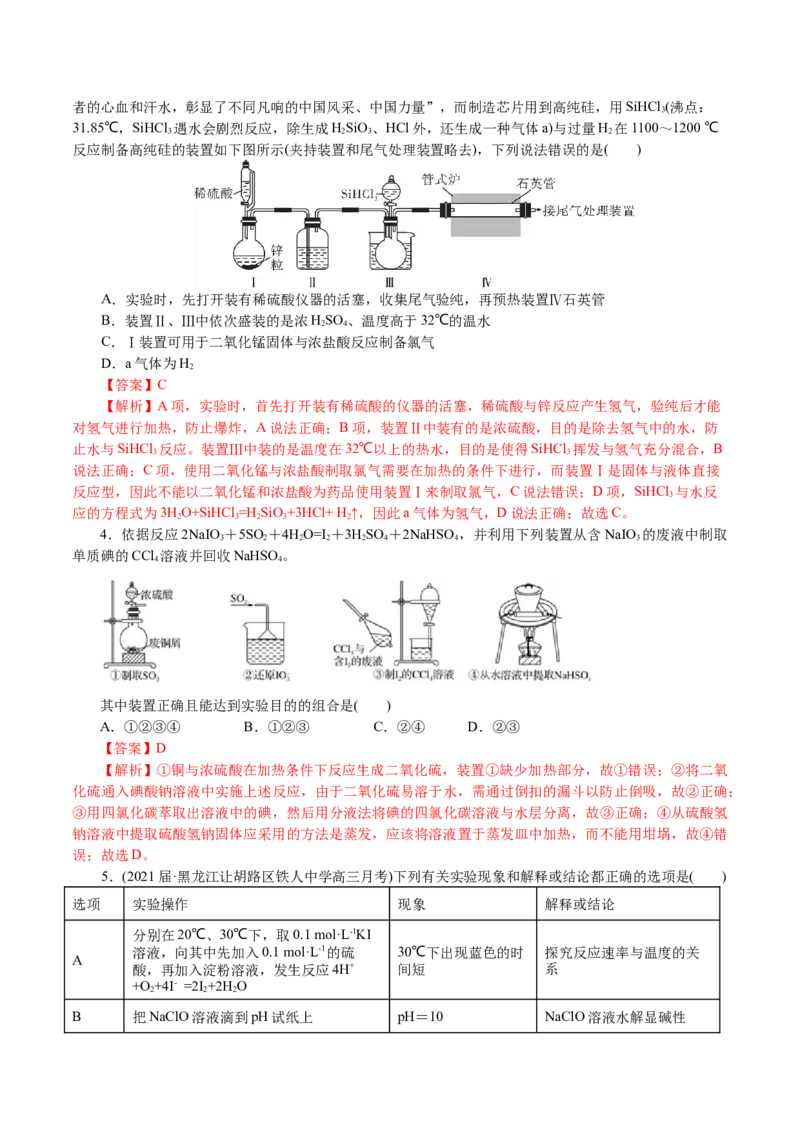
3.(2021届·江西高三月考)习主席在2020年新年贺词中强调“5G商用加速推出,凝结着新时代奋斗者的心血和汗水,彰显了不同凡响的中国风采、中国力量”,而制造芯片用到高纯硅,用SiHCl (沸点:
3
31.85℃,SiHCl 遇水会剧烈反应,除生成HSiO、HCl外,还生成一种气体a)与过量H 在1100~1200 ℃
3 2 3 2
反应制备高纯硅的装置如下图所示(夹持装置和尾气处理装置略去),下列说法错误的是( )
A.实验时,先打开装有稀硫酸仪器的活塞,收集尾气验纯,再预热装置Ⅳ石英管
B.装置Ⅱ、Ⅲ中依次盛装的是浓HSO 、温度高于32℃的温水
2 4
C.Ⅰ装置可用于二氧化锰固体与浓盐酸反应制备氯气
D.a气体为H
2
【答案】C
【解析】A项,实验时,首先打开装有稀硫酸的仪器的活塞,稀硫酸与锌反应产生氢气,验纯后才能
对氢气进行加热,防止爆炸,A说法正确;B项,装置Ⅱ中装有的是浓硫酸,目的是除去氢气中的水,防
止水与SiHCl 反应。装置Ⅲ中装的是温度在32℃以上的热水,目的是使得SiHCl 挥发与氢气充分混合,B
3 3
说法正确;C项,使用二氧化锰与浓盐酸制取氯气需要在加热的条件下进行,而装置Ⅰ是固体与液体直接
反应型,因此不能以二氧化锰和浓盐酸为药品使用装置Ⅰ来制取氯气,C说法错误;D项,SiHCl 与水反
3
应的方程式为3HO+SiHCl =H SiO+3HCl+ H ↑,因此a气体为氢气,D说法正确;故选C。
2 3 2 3 2
4.依据反应2NaIO +5SO +4HO=I +3HSO +2NaHSO ,并利用下列装置从含NaIO 的废液中制取
3 2 2 2 2 4 4 3
单质碘的CCl 溶液并回收NaHSO。
4 4
其中装置正确且能达到实验目的的组合是( )
A.①②③④ B.①②③ C.②④ D.②③
【答案】D
【解析】①铜与浓硫酸在加热条件下反应生成二氧化硫,装置①缺少加热部分,故①错误;②将二氧
化硫通入碘酸钠溶液中实施上述反应,由于二氧化硫易溶于水,需通过倒扣的漏斗以防止倒吸,故②正确;
③用四氯化碳萃取出溶液中的碘,然后用分液法将碘的四氯化碳溶液与水层分离,故③正确;④从硫酸氢
钠溶液中提取硫酸氢钠固体应采用的方法是蒸发,应该将溶液置于蒸发皿中加热,而不能用坩埚,故④错
误;故选D。
5.(2021届·黑龙江让胡路区铁人中学高三月考)下列有关实验现象和解释或结论都正确的选项是( )
选项 实验操作 现象 解释或结论
分别在20℃、30℃下,取0.1 mol·L-1KI
溶液,向其中先加入0.1 mol·L-1的硫 30℃下出现蓝色的时 探究反应速率与温度的关
A
酸,再加入淀粉溶液,发生反应4H+ 间短 系
+O +4I- =2I +2H O
2 2 2
B 把NaClO溶液滴到pH试纸上 pH=10 NaClO溶液水解显碱性两支试管各盛0.1mol/L4mL酸性高锰酸 加入0.2mol/L草酸溶
反应物浓度越大,反应速
C 钾溶液,分别加入0.1mol/L2mL草酸溶 液试管中,高锰酸钾
率越快
液和0.2mol/L2mL草酸溶液 溶液褪色更快
D 把SO 通入紫色石蕊试液中 紫色溶液变红 SO 溶于水显酸性
2 2
【答案】D
【解析】A项,应先加入淀粉溶液,最后加入硫酸,否则可能会先发生反应,观察不到蓝色变化,故
A错误;B项,NaClO溶液具有强氧化性,可使pH试纸褪色,无法测出pH,应用pH计,故B错误;C项,
高锰酸钾与草酸反应,方程式为2KMnO +5H C O+3H SO =2MnSO +K SO +10CO ↑+8H O,两支试管各盛
4 2 2 4 2 4 4 2 4 2 2
0.1mol/L4mL酸性高锰酸钾溶液,分别加入0.1mol/L2mL草酸溶液和0.2mol/L2mL草酸溶液,高锰酸钾是
过量的,颜色不会完全褪去,故C错误;D项,二氧化硫通入石蕊溶液中,二氧化硫与水反应,生成了亚
硫酸,亚硫酸能使石蕊溶液变红,且二氧化硫不能使石蕊溶液褪色,故D正确;故选D。
6.(2021·湖北期末)下列实验操作中,对应的现象和结论均正确的是( )
选项 操作 现象 结论
用湿润的pH试纸测定NH Cl溶液的
A 4 pH=6.5 NH 是弱电解质
pH 3
某溶液中先滴加少量氯水,再滴加
B 溶液变红 溶液中含有Fe2+
KSCN溶液
用玻璃棒蘸取少量某物质的溶液进行 该物质中一定含有钠元
C 焰色呈黄色
焰色试验 素
向3Ml1 mol·Lˉ1的NaOH溶液中滴加5
生产生白色沉淀后又产生 溶度积常数:Mg(OH) >
D 滴1 mol·Lˉ1 MgCl 溶液,再滴加5滴1 2
2 红褐色沉淀 Fe(OH)
mol·Lˉ1的FeCl 溶液 3
3
【答案】C
【解析】A项,不能用湿润的试纸测定溶液的pH,并且读数应为整数,A错误;B项,某溶液中先滴
加少量氯水,再加KSCN溶液,溶液变红,不能证明溶液中有亚铁离子,可能原溶液含铁离子,B错误;
C项,用玻璃棒蘸取少量某物质的溶液进行焰色试验,焰色呈黄色,说明该物质中一定含有钠元素,C正
确;D项,NaOH过量,没有实现沉淀转化,无法比较溶度积的大小,D错误;故选C。
7.(2021届·成都市郫都区川科外国语学校高三月考)下列实验操作完全正确的是( )
编号 实验 操作
用苯萃取碘水中碘后, 先从分液漏斗下端管口放出下层液体,关闭活塞,换一
A
静置后取出有机层 个接收容器,再继续从分液漏斗下端管口放出上层液体
配制500mL2mol/L的 用托盘天平称取53.5g氯化铵晶体放入500mL容量瓶,
B
氯化铵溶液 加少量水,振荡后再加水至刻度线
用玻璃棒蘸取少量溶液滴于pH试纸中央,片刻后与标
C 测定氯水的pH
准比色卡对照
用标准盐酸滴定未知浓
左手控制酸式滴定管活塞使液体滴下,右手不断振荡锥
D 度的NaOH溶液(含酚
形瓶,眼睛要始终观察锥形瓶中溶液颜色变化
酞)
【答案】D
【解析】A项,分液漏斗分液时,先将下层液体从下口放出,上层液体要从上口倒出,故A错误;B
项,不能在容量瓶中进行溶解操作,故B错误;C项,氯水中含有HClO具有漂白性,无法用pH试纸测其pH值,故C错误;D项,用标准盐酸滴定未知浓度的NaOH溶液(含酚酞),操作方法为:左手控制酸式滴
定管活塞使液体滴下,右手不断振荡锥形瓶,为确定滴定终点,眼睛要始终观察锥形瓶中溶液颜色变化,
该操作合理,故D正确;故选D。
8.(2021届·四川射洪县射洪中学高三质检)实验室为了测定复盐KCl·MgCl ·nH O中结晶水的含量,设
2 2
计了如下实验(夹持装置已略去),下列说法正确的是( )
A.反应开始后,圆底烧瓶中生成黄绿色气体
B.装置Ⅱ和装置Ⅳ的位置可以互换
C.装入试剂后,应先点燃酒精灯,再打开分液漏斗活塞
D.已知复盐的质量、实验前后分别称量Ⅳ装置的质量,也无法测定n值
【答案】D
【解析】浓HSO 滴入装置Ⅰ浓HCl中遇水放出大量热量,促使HCl挥发,经过装置Ⅱ得到干燥的
2 4
HCl气体,HCl气体进入装置Ⅲ中可抑制复盐受热时Mg2+的水解,最终装置Ⅳ增加的质量为复盐分解产生
的水蒸气和HCl气体。A项,浓硫酸虽然有强氧化性,但不能将盐酸氧化成氯气,A错误;B项,装置Ⅱ
与装置Ⅳ互换后,则装置Ⅰ中挥发的HCl直接被碱石灰吸收,无法进入装置Ⅲ中抑制Mg2+水解,B错误;
C项,如先点燃酒精灯,会导致部分结晶水被Mg2+水解消耗,产生误差,故应该先打开分液漏斗,一段时
间后再点燃酒精灯,C错误;D项,由于碱石灰增加的质量为复盐分解产生的水蒸气和HCl气体,无法确
定HCl气体质量,故无法确定n值,D正确;故选D。
9.(2021届·江苏省如皋中学高三月考)侯德榜将氨碱法制取碳酸钠和合成氨联合起来,将制碱技术发
展到新的水平。氨碱法的反应原理为NaCl+NH +CO +H O=NaHCO ↓+NHCl,过滤所得NaHCO 可用于制
3 2 2 3 4 3
纯碱。现对过滤所得滤液进行如下实验,所得结论正确的是( )
A.用铂丝蘸取少量滤液进行焰色反应,观察到火焰呈黄色,说明滤液中含有Na+
B.取少量滤液于试管中,加热试管,将湿润的红色石蕊试纸置于试管口,试纸未变蓝,说明滤液中
不含NH +
4
C.取少量滤液,向其中加入足量稀盐酸,再加入硝酸银溶液,观察到有白色沉淀生成,说明滤液中
含有Cl-
D.取少量滤液,向其中加入适量澄清石灰水,观察到有白色沉淀生成,说明滤液中含有
【答案】A
【解析】A项,钠元素的焰色试验是黄色,滤液中钠元素是以钠离子形式存在,A正确;B项,滤液
中含NH Cl,取少量滤液于试管中,直接加热试管,生成的氨气与氯化氢会重新结合生成氯化铵,检验不
4
到氨气,而应取样于试管中加入浓氢氧化钠加热,观察是否产生能使湿润的红色石蕊试纸变蓝的气体判断,
B错误;C项,取少量滤液,向其中加入足量稀盐酸后引入了氯离子,对原滤液中是否含氯离子有干扰,C
错误;D项,若滤液中含碳酸氢根离子,遇澄清石灰水也会出现白色沉淀,则上述操作不能证明是否含碳
酸根离子,D错误;故选A。
10.(2021·沙坪坝区重庆八中高三月考)亚硝酰氯(ClNO)是有机物合成中的重要试剂,遇水反应生成一
种氢化物和两种氧化物。某学习小组用Cl 和NO利用如图所示装置制备亚硝酰氯(ClNO),下列说法正确的
2
是A.X装置可以随开随用,随关随停
B.Y装置中的药品可以换成浓硫酸
C.装入药品打开K 后,应先打开K 再打开K
2 1 3
D.若无装置Y,则Z中可能发生反应的化学方程式为2ClNO+HO=2HCl+NO↑+NO↑
2 2 3
【答案】A
【解析】A项,X装置打开K,铜丝与硝酸接触反应生成的NO被排出。关闭K,NO不溶于稀硝酸,
1 1
将液面压到铜丝下方,反应停止,A项符合题意;B项,Y装置中的药品若换成浓硫酸,则无法除去X中
可能产生的NO 等杂质,且U型管装置承装的干燥剂应为固体,B项不符合题意;C项,实验时应先通入
2
氯气赶走装置内的空气,防止NO被氧化为NO ,C项不符合题意;D项,方程式未配平,N元素不守恒,
2
D项不符合题意;故选A
11.(2021·山东潍坊市期末)为探究铍及其氧化物的性质,进行如下实验(铍片规格相同):
实验操作 实验现象 实验原理
①向盛有铍片的试管中加入足 开始无现象,一段时间后铍片 BeO+2HCl=BeCl +H O
2 2
量6mol•L-1盐酸 逐渐溶解,并有大量气泡产生 Be+2HCl=BeCl +H ↑
2 2
②向盛有铍片的试管中加入足 开始无现象,一段时间后,铍 BeO+H SO =BeSO +H O
2 4 4 2
量3mol•L-1硫酸溶液 片表面缓慢放出少量气泡 Be+H SO =BeSO +H ↑
2 4 4 2
③向盛有铍片的试管中加入足 开始无现象,一段时间后铍片 BeO+2NaOH=Na BeO+H O
2 2 2
量6mol•L-1氢氧化钠溶液 逐渐溶解,并有大量气泡产生 Be+2NaOH=Na BeO+H ↑
2 2 2
下列说法错误的是( )
A.实验开始均无现象原因是:Be在空气中形成氧化膜
B.根据实验可知:BeO既有碱性氧化物的性质,又有酸性氧化物的性质
C.对比实验①、②可知:c(H+)越大,相同时间内产生气泡越多
D.对比实验①、②可知:Cl-对Be与H+的反应可能有促进作用
【答案】C
【解析】A项,Be的化学性质活泼,在空气中,表面容易形成氧化膜,因此实验开始均无气泡放出,
故A正确;B项,对比(1)、(2)、(3)中反应可知,BeO能与酸反应、也能与强碱反应,既有碱性氧化物的
某些性质,又有酸性氧化物的性质,故B正确;C项,实验(1)、(2)中氢离子的浓度相同,不能根据c(H+)
判断相同时间内产生气泡的多少,故C错误;D项,实验(1)、(2)中氢离子浓度相同,阴离子不同,生成氢
气的速率不同,可能是SO 2-对Be与H+的反应可能有阻碍作用,或者Cl-对Be与H+的反应可能有促进作用,
4
故D正确;故选C。
12.(2021·陕西渭南市期末)下列实验装置(夹持装置已省略)进行的相应实验,能达到实验目的的是A.酸性KMnO 溶液的颜色变浅,说明SO 具有漂白性
4 2
B.溶液变为血红色,说明FeCl 已完全变质
2
C.试管中充满溶液,说明通入氧气的体积为NO 体积的
2
D.上下振荡容量瓶,能使配制的NaCl溶液混合均匀
【答案】C
【解析】A项,酸性KMnO 具有强氧化性,通入SO 气体,颜色变浅,发生了氧化还原反应,体现
4 2
SO 的还原性,A错误;B项,向FeCl 溶液中滴加KSCN溶液,溶液变红,说明含有Fe3+,则说明Fe2+被
2 2
氧化,但不能说明已完全变质,要证明是否完全变质,需要检验溶液中是否还有Fe2+,B错误;C项,NO
2
与HO反应生成硝酸和NO,NO又与O 反应生成NO ,总反应可以表示为4NO + O + 2H O = 4HNO ,
2 2 2 2 2 2 3
即按物质的量之比n(NO ):n(O )=4:1时,气体恰好被吸收完全,C正确;D项,操作错误,应用食指按住瓶
2 2
塞,用另一只手的手指托住瓶底,反复上下颠倒,而不是上下振荡,D错误;故选C。
13.(2021·山东济南市高三期末)绿原酸具有抗病毒,降血压,延缓衰老等保健作用.利用乙醚、95%乙
醇浸泡杜仲干叶,得到提取液,进一步提取绿原酸的流程如下:
下列说法错误的是( )
A.从“提取液”获取“有机层”的操作为分液 B.蒸馏时选用球形冷凝管
C.过滤时所需玻璃仪器有烧杯、漏斗、玻璃棒 D.粗产品可通过重结晶的方法提纯
【答案】B
【解析】A项,由流程可知,乙酸乙酯作萃取剂,得到有机层的实验操作为萃取、分液,A正确;B
项,蒸馏时若选用球形冷凝管,会有一部分馏分经冷凝降温后滞留在冷凝管中,而不能进入接收器中,因
此蒸馏时应该选择使用直形冷凝管,B错误;C项,过滤时所需玻璃仪器有烧杯、漏斗、玻璃棒,C正确;
D项,绿原酸难溶于水,易溶于有机溶剂,因此可利用重结晶的方法进一步提纯,D正确;故选B。
14.(2021·辽宁高三零模)下列各实验的现象及结论都正确的是
选
实验 现象 结论
项
浓硫酸滴入蔗糖中,产生的气体导入澄 蔗糖变黑、体积膨胀,澄清石 浓硫酸具有脱水性和
A
清石灰水 灰水变浑浊 强氧化性
铜粉加入稀硫酸中,加热;再加入少量 加热时无明显现象,加入硝酸
B 硝酸钾起催化作用
硝酸钾固体 钾后溶液变蓝
过量铁粉加入稀硝酸中,充分反应后, 有无色气泡产生, 溶液呈血红 稀硝酸能将Fe氧化成
C
滴加KSCN溶液 色 Fe3+D 将Na粒投入MgCl 溶液 析出银白色固体 固体为Mg
2
【答案】A
【解析】A项,蔗糖与浓硫酸反应生成蓬松多孔的黑色物质,浓硫酸先使蔗糖脱水生成C单质,蔗糖
变黑,体现了浓硫酸的脱水性,C单质与浓硫酸反应生成CO,同时生成刺激性气味的气体SO ,使体积
2 2
膨胀,体现了浓硫酸的强氧化性,气体导入澄清石灰水生成固体变浑浊,故A符合题意;B项,铜粉不与
稀硫酸反应,加入硝酸钾,引入NO -,发生反应的离子方程式为:3Cu+2NO -+8H+=3Cu2++2NO↑+4HO,
3 3 2
体现了硝酸根在酸性环境中(HNO 的强氧化性,结论错误,B不符合题意;C项,硝酸具有强氧化性,铁
3)
先被硝酸氧化生成Fe3+再被过量铁粉还原生成Fe2+,滴加KSCN溶液不显红色,现象错误,C不符合题意;
D项,Na粒投入MgCl 溶液,由于Na的还原性极强,Na先与水反应生成NaOH和H,NaOH与MgCl 反
2 2 2
应生成Mg(OH) 白色沉淀,现象、结论错误,D不符合题意;故选A。
2
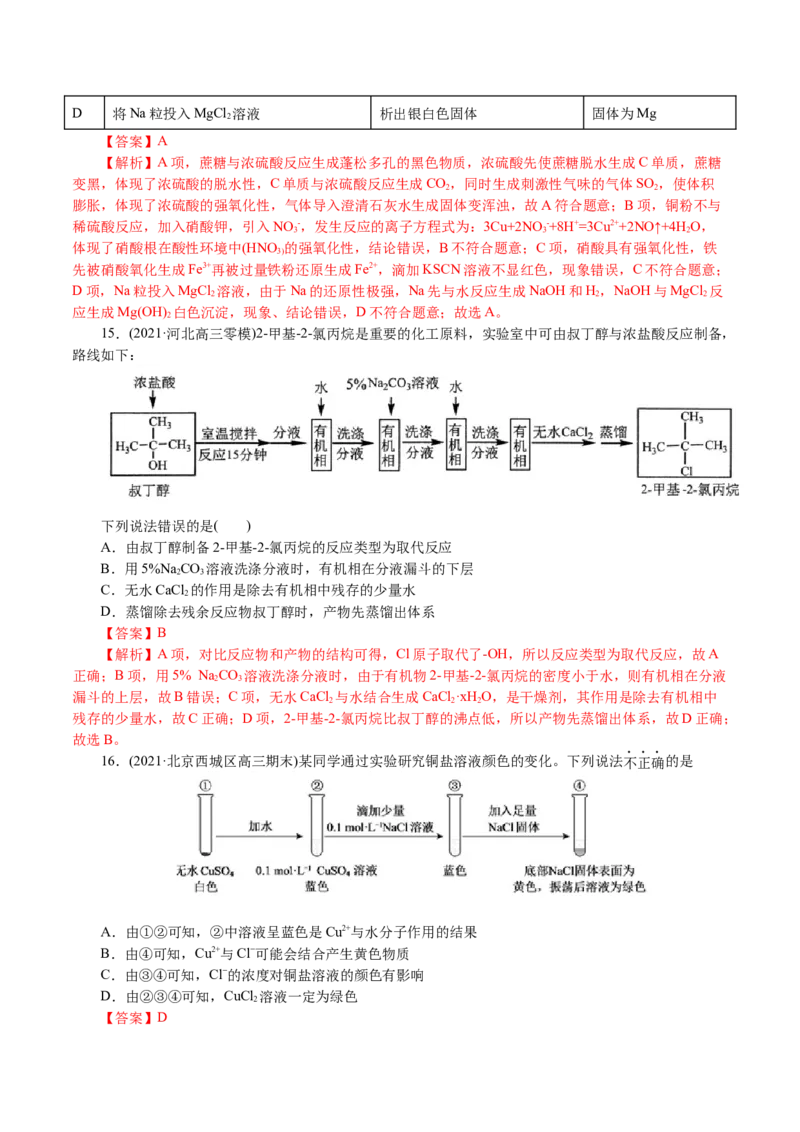
15.(2021·河北高三零模)2-甲基-2-氯丙烷是重要的化工原料,实验室中可由叔丁醇与浓盐酸反应制备,
路线如下:
下列说法错误的是( )
A.由叔丁醇制备2-甲基-2-氯丙烷的反应类型为取代反应
B.用5%NaCO 溶液洗涤分液时,有机相在分液漏斗的下层
2 3
C.无水CaCl 的作用是除去有机相中残存的少量水
2
D.蒸馏除去残余反应物叔丁醇时,产物先蒸馏出体系
【答案】B
【解析】A项,对比反应物和产物的结构可得,Cl原子取代了-OH,所以反应类型为取代反应,故A
正确;B项,用5% Na CO 溶液洗涤分液时,由于有机物2-甲基-2-氯丙烷的密度小于水,则有机相在分液
2 3
漏斗的上层,故B错误;C项,无水CaCl 与水结合生成CaCl·xH O,是干燥剂,其作用是除去有机相中
2 2 2
残存的少量水,故C正确;D项,2-甲基-2-氯丙烷比叔丁醇的沸点低,所以产物先蒸馏出体系,故D正确;
故选B。
16.(2021·北京西城区高三期末)某同学通过实验研究铜盐溶液颜色的变化。下列说法不正确的是
A.由①②可知,②中溶液呈蓝色是Cu2+与水分子作用的结果
B.由④可知,Cu2+与Cl−可能会结合产生黄色物质
C.由③④可知,Cl−的浓度对铜盐溶液的颜色有影响
D.由②③④可知,CuCl 溶液一定为绿色
2
【答案】D【解析】A项,由①②可知,硫酸铜遇水变蓝,所以②中溶液呈蓝色是Cu2+与水分子作用的结果,故
A正确;B项,由④可知,氯化钠固体表面氯离子浓度较大,固体表面为黄色,所以Cu2+与Cl−可能会结合
产生黄色物质,故B正确;C项,③→④增大了氯离子浓度,所以Cl−的浓度对铜盐溶液的颜色有影响,故
C正确;D项,由③溶液为蓝色可知, CuCl 溶液不一定为绿色,故D错误;故选D。
2
17.(2021·北京海淀区高三期末)某小组同学欲通过实验探究影响金属与酸反应速率的因素,进行下列
实验。
实验装置 序号 实验操作 实验现象
钠浮在液面上并来回移动,表面
取下胶塞,放入一 出现有白色固体;白色固体逐渐
实验1 小片金属钠,迅速 沉到烧杯底部,液体不沸腾;气
塞上胶塞 球迅速鼓起,15s时测量气球直径
约为3cm
取下胶塞,放入与 镁条开始时下沉,很快上浮至液
钠表面积基本相同 面,片刻后液体呈沸腾状,同时
实验2
的镁条,迅速塞上 产生大量白雾;气球迅速鼓起,
胶塞 15s时测量气球直径约为5cm
下列说法不正确的是( )
A.实验1获得的白色小颗粒可用焰色反应检验其中的Na元素
B.对比实验1与实验2,不能说明钠比镁的金属活动性强
C.对比实验1与实验2,能说明同温下NaCl的溶解度比MgCl 的小
2
D.金属钠、镁与盐酸反应的速率与生成物状态等因素有关
【答案】B
【解析】通过对比实验1和实验2的操作与现象可知,实验1中钠太活泼,先与水反应生成氢氧化钠,
再与浓盐酸反应生成溶解度不大的氯化钠,附着在还未反应的Na表面,阻碍了Na反应的进行,所以出现
上述现象;对比实验1,实验2中,利用相同表面积的Mg做相同的实验,表面现象看似Mg反应快,是因
为Mg直接与盐酸反应生成氢气,产生的氢气比实验1多。A项,Na元素可用焰色试验来检验,若白色小
颗粒中含Na元素,则焰色反应为黄色,A正确;B项,根据上述分析可知,对比实验1与实验2的操作与
实验现象,能说明钠比镁的金属活动性强,只是因为表面生成的白色固体颗粒阻碍了Na与HCl的反应,
通过表面现象探究实质才是真理,B错误;C项,对比实验1与实验2,实验1中有白色固体,实验2中没
有,则说明同温下NaCl的溶解度比MgCl 的小,C正确;D项,通过上述实验可得出,金属钠、镁与盐酸
2
反应的速率不仅与本身的性质有关,还与生成物状态等因素有关,D正确;故选B。
18.(2021·山东青岛市高三质检)二氧化氯(ClO )是一种黄绿色气体,易溶于水,熔点为﹣59.5℃,沸点
2
为11.0℃,浓度过高时易发生分解引起爆炸,制备二氧化氯溶液的装置如图。下列说法正确的是( )
A.装置A发生的反应中氧化剂与还原剂的物质的量之比为1:2
B.实验中氮气的作用就是将装置内的空气排出
C.装置B可以起到防止倒吸的作用
D.当看到装置C中导管液面上升时应减慢氮气的通入速率
【答案】C【解析】A项,装置A是生成ClO 的装置,Cl元素由NaClO 中的+5价降低到ClO 中的+4价,得到1
2 3 2
个电子,NaClO 是氧化剂,氧元素由HO 中-1价升高到O 中的0价,失去2个电子,HO 是还原剂,根
3 2 2 2 2 2
据得失电子守恒知,NaClO 与HO 的物质的量之比为2:1,A项不符合题意;B项,由题意知,二氧化
3 2 2
氯浓度过高易发生分解引起爆炸,通入氮气主要是为了降低二氧化氯的浓度,B项不符合题意;C项,B
装置中的两根导管都较短,可以起到防倒吸的作用,C项符合题意;D项,装置C中导管液面上升,说明
内部压强偏小,易引起倒吸,此时应加快氮气的通入速率,弥补压强的不足,D项不符合题意;故选C。
19.(2021·北京丰台区高三期末)甲醇可用于合成重要的有机合成中间体3,5—二甲氧基苯酚。
反应结束后,先分离出甲醇,再加入乙醚,将获得的有机层(含少量氯化氢) 进行洗涤,然后分离
提纯得到产物。有关物质的部分物理性质如下:
物质 沸点/℃ 熔点/℃ 溶解性
甲醇 64.7 -97.8 易溶于水
3,5—二甲氧基苯酚 172~175 33~36 易溶于甲醇、乙醚,微溶于水
下列说法不正确的是( )
A.该反应属于取代反应
B.分离出甲醇的操作是蒸馏
C.间苯三酚与3,5—二甲氧基苯酚互为同系物
D.洗涤时,可用NaHCO 溶液除去有机层中的氯化氢
3
【答案】C
【解析】A项,该反应方程式为 ,属于取代反应,
A正确;B项,从该有机混合物中分离出某种有机物(甲醇),常利用沸点的差异,操作方法是蒸馏,B正确;
C项,间苯三酚与3,5—二甲氧基苯酚的官能团种类及数目都不完全相同,二者不互为同系物,C不正确;
D项,洗涤时,往混合液中加入NaHCO 溶液,与HCl反应,生成的NaCl不溶于有机物,便于分离除去,
3
所以可用NaHCO 溶液除去有机层中的氯化氢,D正确;故选C。
3
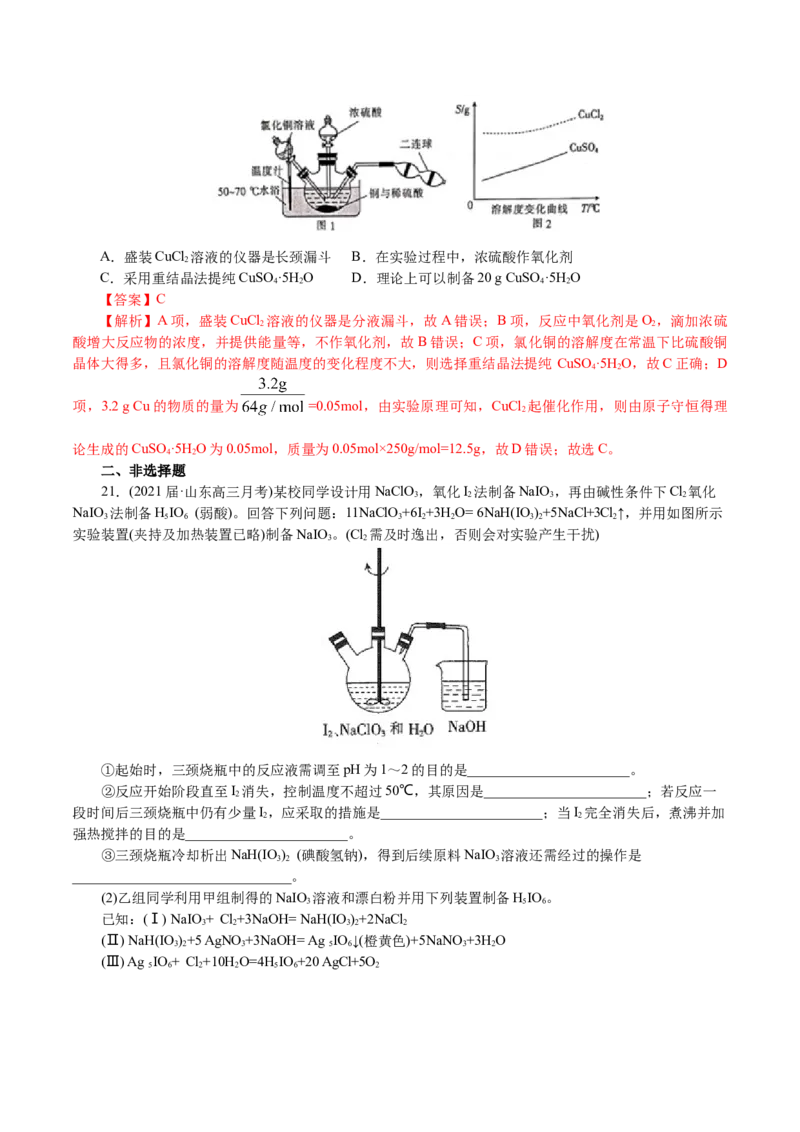
20.蓝矾(CuSO ·5H O)常作杀菌剂。某小组设计如图 1装置制备蓝矾,实验原理: Cu+CuCl =
4 2 2
2CuCl,4CuCl+O+2HO=2[Cu(OH)·CuCl ],[Cu(OH)·CuCl ]+HSO =CuSO +CuCl +2HO。
2 2 2 2 2 2 2 4 4 2 2
操作步骤:向三颈瓶加入3.2 g Cu粉和适量稀硫酸及30 mL 1 mol·L-1 CuCl 溶液,利用二连球向三颈
2
瓶中鼓入空气,铜溶解。当三颈烧瓶中呈乳状浑浊液时,滴加浓硫酸,得到蓝矾(不考虑氯化铜转化成硫酸
铜)。下列说法正确的是( )A.盛装CuCl 溶液的仪器是长颈漏斗 B.在实验过程中,浓硫酸作氧化剂
2
C.采用重结晶法提纯CuSO ·5H O D.理论上可以制备20 g CuSO ·5H O
4 2 4 2
【答案】C
【解析】A项,盛装CuCl 溶液的仪器是分液漏斗,故A错误;B项,反应中氧化剂是O ,滴加浓硫
2 2
酸增大反应物的浓度,并提供能量等,不作氧化剂,故B错误;C项,氯化铜的溶解度在常温下比硫酸铜
晶体大得多,且氯化铜的溶解度随温度的变化程度不大,则选择重结晶法提纯 CuSO ·5H O,故C正确;D
4 2
项,3.2 g Cu的物质的量为 =0.05mol,由实验原理可知,CuCl 起催化作用,则由原子守恒得理
2
论生成的CuSO ·5H O为0.05mol,质量为0.05mol×250g/mol=12.5g,故D错误;故选C。
4 2
二、非选择题
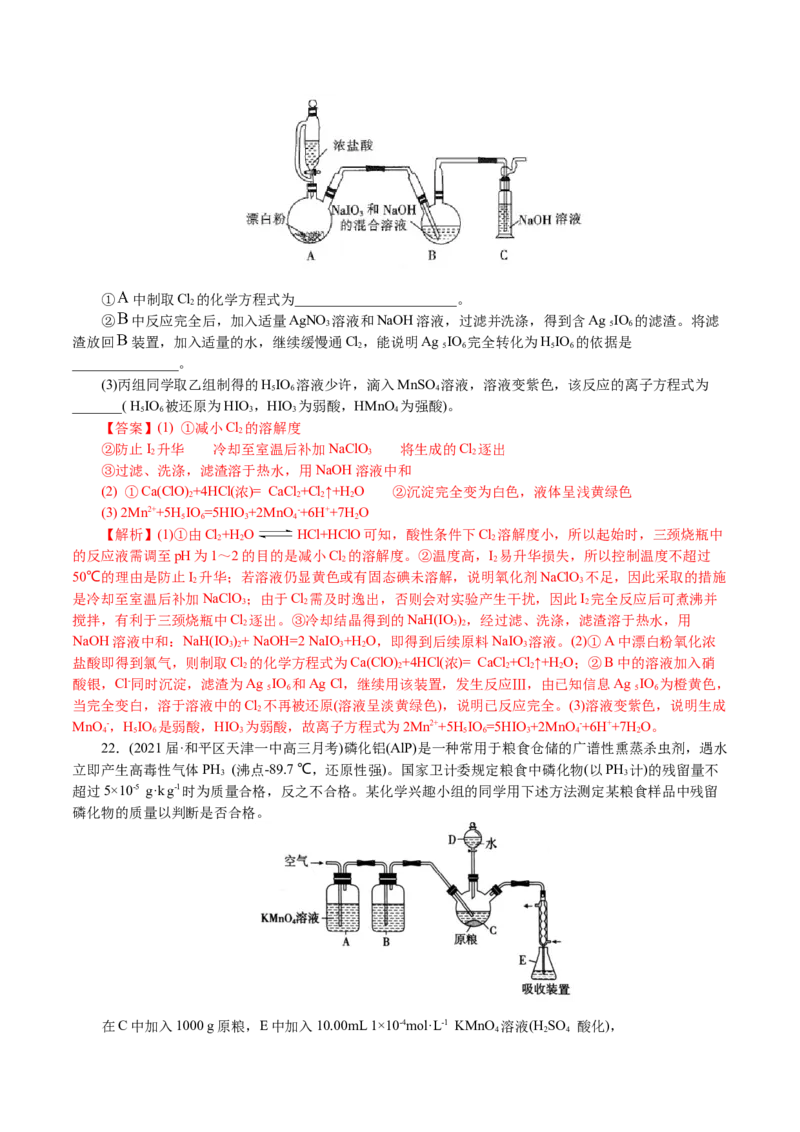
21.(2021届·山东高三月考)某校同学设计用NaClO,氧化I 法制备NaIO ,再由碱性条件下Cl 氧化
3 2 3 2
NaIO 法制备HIO (弱酸)。回答下列问题:11NaClO+6I +3H O= 6NaH(IO)+5NaCl+3Cl ↑,并用如图所示
3 5 6 3 2 2 3 2 2
实验装置(夹持及加热装置已略)制备NaIO 。(Cl 需及时逸出,否则会对实验产生干扰)
3 2
①起始时,三颈烧瓶中的反应液需调至pH为1~2的目的是_______________________。
②反应开始阶段直至I 消失,控制温度不超过50℃,其原因是_______________________;若反应一
2
段时间后三颈烧瓶中仍有少量I,应采取的措施是_______________________;当I 完全消失后,煮沸并加
2 2
强热搅拌的目的是_______________________。
③三颈烧瓶冷却析出NaH(IO) (碘酸氢钠),得到后续原料NaIO 溶液还需经过的操作是
3 2 3
_______________________________。
(2)乙组同学利用甲组制得的NaIO 溶液和漂白粉并用下列装置制备HIO 。
3 5 6
已知:(Ⅰ) NaIO+ Cl+3NaOH= NaH(IO)+2NaCl
3 2 3 2 2
(Ⅱ) NaH(IO)+5 AgNO +3NaOH= Ag IO ↓(橙黄色)+5NaNO +3H O
3 2 3 5 6 3 2
(Ⅲ) Ag IO + Cl+10H O=4HIO +20 AgCl+5O
5 6 2 2 5 6 2① 中制取Cl 的化学方程式为_______________________。
2
② 中反应完全后,加入适量AgNO 溶液和NaOH溶液,过滤并洗涤,得到含Ag IO 的滤渣。将滤
3 5 6
渣放回 装置,加入适量的水,继续缓慢通Cl,能说明Ag IO 完全转化为HIO 的依据是
2 5 6 5 6
_______________。
(3)丙组同学取乙组制得的HIO 溶液少许,滴入MnSO 溶液,溶液变紫色,该反应的离子方程式为
5 6 4
_______( H IO 被还原为HIO ,HIO 为弱酸,HMnO 为强酸)。
5 6 3 3 4
【答案】(1) ①减小Cl 的溶解度
2
②防止I 升华 冷却至室温后补加NaClO 将生成的Cl 逐出
2 3 2
③过滤、洗涤,滤渣溶于热水,用NaOH溶液中和
(2) ①Ca(ClO)+4HCl(浓)= CaCl+Cl↑+H O ②沉淀完全变为白色,液体呈浅黄绿色
2 2 2 2
(3) 2Mn2++5H IO =5HIO+2MnO-+6H++7H O
5 6 3 4 2
【解析】(1)①由Cl+H O HCl+HClO可知,酸性条件下Cl 溶解度小,所以起始时,三颈烧瓶中
2 2 2
的反应液需调至pH为1~2的目的是减小Cl 的溶解度。②温度高,I 易升华损失,所以控制温度不超过
2 2
50℃的理由是防止I 升华;若溶液仍显黄色或有固态碘未溶解,说明氧化剂NaClO 不足,因此采取的措施
2 3
是冷却至室温后补加NaClO;由于Cl 需及时逸出,否则会对实验产生干扰,因此I 完全反应后可煮沸并
3 2 2
搅拌,有利于三颈烧瓶中Cl 逐出。③冷却结晶得到的NaH(IO),经过滤、洗涤,滤渣溶于热水,用
2 3 2
NaOH溶液中和:NaH(IO)+ NaOH=2 NaIO+H O,即得到后续原料NaIO 溶液。(2)①A中漂白粉氧化浓
3 2 3 2 3
盐酸即得到氯气,则制取Cl 的化学方程式为Ca(ClO)+4HCl(浓)= CaCl+Cl↑+H O;②B中的溶液加入硝
2 2 2 2 2
酸银,Cl-同时沉淀,滤渣为Ag IO 和AgCl,继续用该装置,发生反应Ⅲ,由已知信息Ag IO 为橙黄色,
5 6 5 6
当完全变白,溶于溶液中的Cl 不再被还原(溶液呈淡黄绿色),说明已反应完全。(3)溶液变紫色,说明生成
2
MnO -,HIO 是弱酸,HIO 为弱酸,故离子方程式为2Mn2++5H IO =5HIO+2MnO-+6H++7H O。
4 5 6 3 5 6 3 4 2
22.(2021届·和平区天津一中高三月考)磷化铝(AlP)是一种常用于粮食仓储的广谱性熏蒸杀虫剂,遇水
立即产生高毒性气体PH (沸点-89.7 ℃,还原性强)。国家卫计委规定粮食中磷化物(以PH 计)的残留量不
3 3
超过5×10-5 g·k g-1时为质量合格,反之不合格。某化学兴趣小组的同学用下述方法测定某粮食样品中残留
磷化物的质量以判断是否合格。
在C中加入1000 g原粮,E中加入10.00mL 1×10-4mol·L-1 KMnO 溶液(H SO 酸化),
4 2 4往C中加入足量水,充分反应后,用亚硫酸钠标准溶液滴定E中过量的KMnO 溶液。回答下列问题:
4
(1)PH 的电子式为___________。仪器D的名称是___________。
3
(2)装置B中盛装焦性没食子酸的碱性溶液,其作用是吸收空气中的o,若去掉该装置。对实验的影响
2
为___________________________。
(3)实验前、实验结束后均需通入空气,通入空气的作用分别是___________、
(4)装置E中PH 被氧化成磷酸,充分反应后的吸收液,加水稀释至250mL,取25.00mL于锥形瓶中,
3
用2×10-6 mol·L-1的NaSO 标准溶液滴定剩余的KMnO 溶液,消耗NaSO 标准溶液25.00mL,NaSO 与
2 3 4 2 3 2 3
KMnO 溶液反应的离子方程式为SO 2-+MnO-+H+→SO42-+Mn2++H O(未配平),则滴定终点的现象为
4 3 4 2
_____________________。该原粮样品中磷化物(以PH 计)的残留量为___________ g·k g-1。若滴定终点时俯
3
视滴定管刻度,则由此测得的残留量将___________(填“偏大”“偏小”或“不变”)。
(5) PH 也可被NaClO氧化可用于制备NaHPO ,制得的NaHPO 和NiCl 溶液可用于化学镀镍,同时
3 2 2 2 2 2
生成磷酸和氯化物,请写出化学镀镍的化学方程式为___________。
【答案】(1) 分液漏斗 (2)造成测量结果偏低(测得磷化物的含量偏低)
(3)排出装置中空气;保证生成的PH 全部被装置E中的酸性KMnO 溶液吸收
3 4
(4)滴最后一滴标准液时,溶液由浅紫色变为无色,且30秒不变色 1.7×10-5 偏大
(5)NaHPO +2NiCl+2H O=HPO +2Ni+NaCl+3HCl
2 2 2 2 3 4
【解析】(1)PH 中磷原子的三个未成对电子,分别与一个氢原子的电子配对形成一个共价键,磷原子
3
上还有一对没有与其他原子共用的电子,PH 电子式为 ;仪器D的名称是分液漏斗。(2)装置B中盛
3
装焦性没食子酸的碱性溶液,其作用是吸收空气中的O,防止氧气氧化PH ,若去掉该装置,PH 会被氧
2 3 3
化而造成测量结果偏低。(3)实验前通入空气的作用是将装置中的空气排净,实验结束后通入空气是为了把
生成的PH 全部赶入E中被高锰酸钾溶液吸收。 (4)用NaSO 标准溶液滴定剩余的KMnO 溶液,滴定终点
3 2 3 4
的现象为溶液由浅紫色变为无色,且30秒不变色;NaSO 与酸性KMnO 溶液反应的化学方程式为
2 3 4
2KMnO +5Na SO +3H SO =2MnSO +K SO +5Na SO +3H O,得关系式:2KMnO ~5Na SO ,剩余的
4 2 3 2 4 4 2 4 2 4 2 4 2 3
n(KMnO)= ×2×10-6 mol·L-1×0.025 L=2×10-8 mol,则250 mL稀释液中剩余的n(KMnO)= 2×10-8
4 4
mol×10=2×10-7 mol;PH 与KMnO 反应的化学方程式为
3 4
5PH +8KMnO +12H SO =5H PO +8MnSO +4K SO +12H O,得关系式:8KMnO ~5PH ,n(PH )=
3 4 2 4 3 4 4 2 4 2 4 3 3
n(KMnO)= ×(0.01 L ×1×10-4 mol/L-2×10-7 mol )= 5×10-7 mol,m(PH )= 5×10-7 mol×34 g/mol=1.7×10-5 g,
4 3
该原粮样品中磷化物(以PH 计)的残留量为1.7×10-5 g·k g-1;若滴定终点时俯视滴定管刻度,导致滴定液的
3
体积偏大,则由此测得的残留量将偏大。(5) 制得的NaHPO 和NiCl 溶液可用于化学镀镍,生成镍、磷酸
2 2 2
和氯化钠,化学方程式为NaHPO +2NiCl+2H O=HPO +2Ni+NaCl+3HCl。
2 2 2 2 3 4
23.(2021届·陕西西安市西安中学高三月考)2-硝基-1,3-苯二酚由间苯二酚先磺化,再硝化,后去磺
酸基生成。原理如下:部分物质的相关性质如下:
名称 相对分子质量 性状 熔点/℃ 水溶性(常温)
间苯二酚 110 白色针状晶体 110.7 易溶
2-硝基-1,3-苯二酚 155 桔红色针状晶体 87.8 难溶
制备过程如下:
第一步:磺化。称取71.5g间苯二酚,碾成粉末放入烧瓶中,慢慢加入适量浓硫酸并不断搅拌,控制
温度在一定范围内15min(如图1)。
第二步:硝化。待磺化反应结束后将烧瓶置于冷水中,充分冷却后加入“混酸”,控制温度继续搅拌
15min。
第三步:蒸馏。将硝化反应混合物的稀释液转移到圆底烧瓶B中,然后用如图2所示装置进行水蒸气
蒸馏(水蒸气蒸馏可使待提纯的有机物在低于100℃的情况下随水蒸气一起被蒸馏出来,从而达到分离提纯
的目的)。
请回答下列问题:
(1)磺化步骤中控制温度最合适的范围为(填字母)_______。
A.30℃~60℃ B.60℃~65℃ C.65℃~70℃ D.70℃~100℃
(2)图2中的冷凝管是否可以换为图1所用冷凝管_______(填“是”或“否”)。
(3)硝化步骤中制取“混酸”的具体操作是__________________________________。
(4)图2中,烧瓶A中长玻璃管起稳压作用,既能防止装置中压强过大引起事故,又能防止
_________________________;冷凝管C中可能看到的现象是________________。
(5)水蒸气蒸馏是分离和提纯有机物的方法之一,被提纯物质必须具备的条件正确的是
________________。
A.不溶或难溶于水,便于最后分离 B.在沸腾下与水不发生化学反应
C.难挥发性 D.易溶于水
(6)本实验最终获得12.0g桔红色晶体,则2-硝基-1,3-苯二酚的产率约为_______。
【答案】(1)b (2)否
(3)在烧杯中加入适量的浓硝酸,沿杯壁缓慢加入一定量的浓硫酸,边加边搅拌,冷却
(4)压强过小引起倒吸 冷凝管内壁有桔红色晶体析出 (5)ab (6)11.9%【解析】(1)由题中信息可知,在磺化步骤中要控制温度低于65℃。若温度过低,磺化反应的速率过慢;
间苯二酚具有较强的还原性,而浓硫酸具有强氧化性,若温度过高,苯二酚易被浓硫酸氧化,并且酚羟基
的所有邻位均可被磺化,这将影响下一步硝化反应的进行,因此,在磺化步骤中控制温度最合适的范围为
60℃~65℃,故选b。(2) 图1所用冷凝管为球形冷凝管,其常用于有机制备的回流,但不可用于蒸馏装置
中,因为冷凝后的液体凝固后,固体会卡在玻璃球中;图2中的冷凝管为直形冷凝管,其常用于蒸馏装置。
由于2-硝基-1,3-苯二酚的熔点是87.8℃,其蒸气被冷凝结晶为固体,且其难溶于水,因此,图2中的冷
凝管不可以换为图1所用冷凝管,故答案为:否。(3)类比浓硫酸的稀释方法,为了防止液体飞溅和硝酸温
度过高发生分解和挥发过多,要将浓硫酸慢慢加入浓硝酸中,因此,硝化步骤中制取“混酸”的具体操作
是:在烧杯中加入适量的浓硝酸,沿杯壁缓慢加入一定量的浓硫酸,边加边搅拌,冷却。(4)图2中,烧瓶
A中长玻璃管起稳压作用,能使装置中的气体压强维持在一定的安全范围,既能防止装置中压强过大引起
事故,又能防止压强过小引起倒吸;由于2-硝基-1,3-苯二酚的熔点是87.8℃,且其难溶于水,因此,冷
凝管C中有2-硝基-1,3-苯二酚析出,可能看到的现象是冷凝管内壁有桔红色晶体析出。(5)由题中信息可
知,水蒸气蒸馏是分离和提纯有机物的方法之一,在低于100℃的情况下,有机物可以随水蒸气一起被蒸
馏出来,从而达到分离提纯的目的。因此,被提纯物质必须具备的条件是:其在一定的温度范围内有一定
的挥发性,可以随水蒸气一起被蒸馏出来;不溶或难溶于水,便于最后分离;在沸腾条件下不与水发生化
学反应。故答案为ab。(6) 71.5g间苯二酚的物质的量为 ,理论上可以制备出2-硝基--
1,3-苯二酚0.65mol,其质量为0.65mol155g/mol=100.75g。本实验最终获得12.0g桔红色晶体,则2-硝
基-1,3-苯二酚的产率为 。
24.(2021届·江苏高三月考)草酸合铁(Ⅲ) 酸钾晶体,即K[Fe(C O)]·3H O,是制备某些铁触媒的主
3 2 4 3 2
要原料。该配合物易溶于水,难溶于乙醇,对光敏感,光照下即发生分解。可用如下流程来制备。根据题
意完成下列各题:
(1)“溶解”时加入硫酸的目的是_____________________________。
(2)流程的“氧化”这一步,是依次加入一定量的饱和KC O 溶液、HC O 溶液、3%H O 溶液,不断
2 2 4 2 2 4 2 2
搅拌溶液并维持在40 ℃左右。充分反应后,沉淀溶解,溶液的pH保持在4~5,此时溶液呈翠绿色,趁热
将溶液过滤到烧杯中,______________________________(补充必要的步骤),得草酸合铁(Ⅲ) 酸钾晶体。
(3)写出在“氧化”这一步中,使沉淀溶解生成翠绿色溶液的离子方程式:__ __________。
(4)草酸合铁(Ⅲ) 酸钾晶体光照下立即发生分解生成两种草酸盐、CO 等,写出该反应的化学方程式:
2
__ ______________________________________。
(5)某学生想测定草酸合铁(Ⅲ)酸钾晶体{K [Fe(C O)]·cHO}的组成,查阅资料,发现该晶体加热到
a 2 4 b 2
110 ℃时仅完全失去结晶水。在实验室通过下列方法完成了该过程。具体如下:
步骤1:准确称取两份质量均为0.4910 g的草酸合铁(Ⅲ)酸钾样品。
步骤2:一份在N 氛围下保持110 ℃加热至恒重,称得残留固体质量为0.4370 g。
2
步骤3:另一份完全溶于水后,让其通过装有某阴离子交换树脂的交换柱{发生反应:aRCl+
[Fe(C O)]a-=R [Fe(C O)]+aCl-},用蒸馏水冲洗交换柱,收集交换出的Cl-,以KCrO 为指示剂,用0.1500
2 4 b a 2 4 b 2 4
mol·L-1的AgNO 溶液滴定至终点,消耗AgNO 溶液20.00 mL。
3 3
①若步骤3中未用蒸馏水冲洗交换柱,则测得的样品中K+的物质的量____(填“偏大”“偏小”或
“不变”)。②通过计算确定草酸合铁(Ⅲ)酸钾样品的化学式:____________(写出计算过程)。
【答案】(1)抑制Fe2+的水解
(2)降温结晶,过滤,乙醇洗涤干燥(或等滤液降温后加入适量的乙醇,析出晶体,过滤,乙醇洗涤,
干燥)
(3)2FeC O·2H O+HO+H C O+3C O2-=2[Fe(C O)]3- +6H O
2 4 2 2 2 2 2 4 2 4 2 4 3 2
(4)2K [Fe(C O)]·3H O 3KC O+2FeC O+2CO ↑+6H O
3 2 4 3 2 2 2 4 2 4 2 2
(5) ①偏小 ②K[Fe(C O)]·3H O
3 2 4 3 2
【解析】由流程可知,绿矾用稀硫酸溶解,目的是抑制Fe2+水解,加入的草酸与硫酸亚铁反应生成草
酸亚铁沉淀,用过氧化氢将草酸亚铁晶体氧化为k[Fe(C O)],一定条件下结晶得到草酸合铁(Ⅲ)酸钾晶体。
3 2 4 3
(1) H SO 溶液不能与绿矾反应,用硫酸溶解的目的是抑制Fe2+水解;(2) 趁热将溶液过滤到烧杯中,再经
2 4
过蒸发浓缩、冷却结晶、过滤、乙醇洗涤、干燥等操作得草酸合铁(Ⅲ)酸钾晶体;(3) 过氧化氢将
Fe(C O)•2H O氧化为K[Fe(C O)],同时过氧化氢被还原为水,反应离子方程式为:
2 4 2 3 2 4 3
2FeC O·2H O+HO+H C O+3C O2-=2[Fe(C O)]3- +6H O;(4) 草酸合铁(Ⅲ)酸钾晶体光照下立即发生分解
2 4 2 2 2 2 2 4 2 4 2 4 3 2
生成两种草酸盐、CO 等,两种草酸盐为草酸钾、草酸铁,反应方程式为:2K[Fe(C O)]·3H O
2 3 2 4 3 2
3KC O+2FeC O+2CO ↑+6H O; (5)①由电荷守恒可知:n(K+)=n(Cl-),未用蒸馏水冲洗交换柱,收集交
2 2 4 2 4 2 2
换出的Cl-物质的量偏少,则测得的样品中K+的物质的量偏小;②n(H O)=(0.4910-0.4370)g÷18
2
g·mol-1=3×10-3 mol,n(Cl-)=n(Ag+)=0.1500 mol·L-1×20.00×10-3 L=3×10-3 mol;根据离子交换柱中发生的反应:
aRCl+[Fe(C O)]a-=R [Fe(C O)]+aCl-,可得样品中n(K+)=n(Cl-)=3×10-3 mol,n{[Fe(C O)]a-}=
2 4 b a 2 4 b 2 4 b
mol。110 ℃残留固体是晶体失去结晶水后的产物即K+和[Fe(C O)]a-的总质量,为3×10-3 mol×39 g·mol-1+
2 4 b
mol×(56+88b) g·mol-1=0.4370 g;K[Fe(C O)]中根据电荷守恒关系可得:a+3=2b,得a=3,b=3;
a 2 4 b
n{[Fe(C O)]3-}=1×10-3 mol,n(K+)∶n{[Fe(C O)]3-}∶n(H O)=3∶1∶3,则样品的化学式为
2 4 3 2 4 3 2
K[Fe(C O)]·3H O。
3 2 4 3 2
25.(2021届·天津高三模拟)DCCNa(二氯异氰尿酸钠)固体是一种高效、安全的消毒剂,20°C以上易溶
于水。(CNO) H(氰尿酸)为三元弱酸。
3 3
I.制备DCCA(二氯异氰尿酸)装置如图。主要反应有:
碱溶(CNO) H+2NaOH (CNO) NaH+2HO H<0
3 3 3 2 2
氯化(CNO) NaH+2Cl (CNO )Cl H+2NaCl H<0
3 2 2 3 2
⇌ △
⇌ △
回答下列问题:
(1)装置C中的溶液是_________,作用为_________。
(2)装置A中反应的离子方程式为____________。
(3)装置B用冰水浴的原因是___,碱溶时若氢氧化钠过量,(CNO) NaH中可能混有的杂质是__。
3 2
II.制备DCCNa(4)步骤II中“过滤洗盐”洗去的盐是______________________。
(5)“中和”反应的化学方程式为_______________________。
(6)氯元素含量的测定:称取0.1000gDCCNa样品,加入一定量醋酸溶液溶解,样品中的氯元素全部化
成HClO,再加入足量的KI溶液,用淀粉作指示剂,用0.1000mol•L-1NaSO 标准溶液滴定生成的碘,消耗
2 2 3
标准液VmL。已知:I+2S O2-=2I-+ S O2-,样品中氯元素的质量分数=______%。
2 2 3 4 6
(7)下列操作可能使氯元素的质量分数测定结果偏低的是________填字母)。
A.滴定前滴定管未排气泡,滴定后气泡消失 B.滴定后,滴定管尖嘴外还悬着一滴液体
C.锥形瓶内溶液蓝色消失后立即读数 D.读数时,滴定前平视,滴定后仰视
【答案】(1)氢氧化钠溶液 吸收多余氯气,防止污染空气
(2)2 MnO-+10Cl- +16H+ =2Mn2++ 5Cl ↑+8H O
4 2 2
(3)该反应放热, 冰水浴可降温促进反应向正反应方向进行,同时降低产品溶解度 (CNO) Na
3 3
(4)NaCl
(5) (CNO) ClH+ NaOH= (CNO) ClNa +H O (6) 1 .775V (7)cd
3 2 3 2 2
【解析】由图中装置和实验药品可知,A装置为氯气发生装置,B装置发生氯化反应生成DCCA(二氯
异氰尿酸),C装置用于尾气处理,吸收多余的氯气;利用DCCA生产DCCNa,先将B中的产物主要成分
为DCCA和NaCl的混合物进行过滤洗盐,得到DCCA,DCCA与氢氧化钠反应得到DCCNa,再经过冷却
结晶,过滤干燥得到产品DCCNa。Ⅰ.(1)由分析可知,C装置用于尾气处理,吸收多余的氯气,防止污染
环境,试剂为氢氧化钠溶液;(2)A装置为氯气发生装置,离子反应方程式为:2 MnO-+10Cl-+16H+=2Mn2+
4
+5Cl↑+8H O;(3)B装置中的反应为放热反应,冰水浴可降低温度,促进反应正向移动,同时降低温度可
2 2
降低产品溶解度;(CNO) H 为三元弱酸,则碱溶时若氢氧化钠过量,会生成(CNO) Na;Ⅱ.(4)B中产物主
3 3 3 3
要成分为DCCA和NaCl的混合物,则“过滤洗盐”洗去的盐是NaCl;(5) DCCA与氢氧化钠反应得到
DCCNa,其化学反应方程式为:(CNO) ClH+NaOH=(CNO) ClNa+HO;(6) DCCNa样品,加入一定量醋
3 2 3 2 2
酸溶液溶解,样品中的Cl元素全部转化为HClO,再加入足量的KI溶液,用NaSO 标准溶液滴定生成的
2 2 3
碘,则关系式为:DCCNa~2HClO~2I ~ ,则Cl原子的物质的量n(Cl)= n(HClO)= n(SO2-)=
2 2 3
,则样品中氯元素的质量分数:
;(7) a项,滴定前滴定管未排气泡,滴定后气泡消失,消
耗标准液V增大,结果偏高,a不符合题意;b项,滴定后,滴定管尖嘴外还悬着一滴液体,相当于消耗
标准液V增大,结果偏高,b不符合题意;c项,锥形瓶内溶液蓝色消失后立即读数,消耗标准液V减小,
结果偏低,c符合题意;d项,读数时,滴定前平视,滴定后仰视,消耗标准液V减小,结果偏低,d符合
题意;故选cd。