文档内容
“陌生情景下”方程式的书写
目 录
1
【真题研析·规律探寻】 2
【解题技巧】 4
1.陌生化学方程式书写的思路 4
2.陌生氧化还原反应方程式书写的具体步骤 4
【核心提炼·考向探究】 5
1.书写方法 5
2.书写关键——识记常见氧化剂、还原剂及产物预测 5
3.分步法书写非氧化还原方程式 6
【题型特训·命题预测】 6
考点要求 考题统计 考情分析
【命题规律】
2023•全国甲卷,26(5);
陌生方程式的书写是高考题中常见的题型,往往通过陌生情境
2023•辽宁省选择性考
下题干语言或化工流程,给出反应发生的环境,写出反应的化
试,16(5);2023•江苏
学方程式。这就要求通过阅读题干、发现本质、寻求规律,进
化学方程式书写 卷,17(1);2022•河北省
而完成旧知识在新情景中的正确迁移。
或 选择性考试,15(3)(5);
【命题预测】
离子方程式书写 2021·全国甲卷,26(2);
2024年此考点将继续在非选择题呈现。以现代工业生产为基
2021·全国乙卷,26(1);
础,一般简单介绍该工艺生产的原材料和工艺生产的目的(包括
2021·河北,15(4);
副产品),然后用框图形式将原料到产品的主要生产工艺流程表
2021·湖南,17(5) (6)
示出来,根据生产过程中涉及的化学知识设计陌生离子方程式、氧化还原方程式的来进行书写。
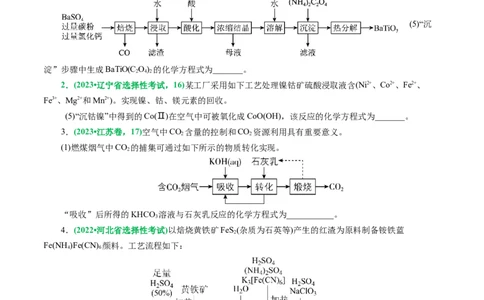
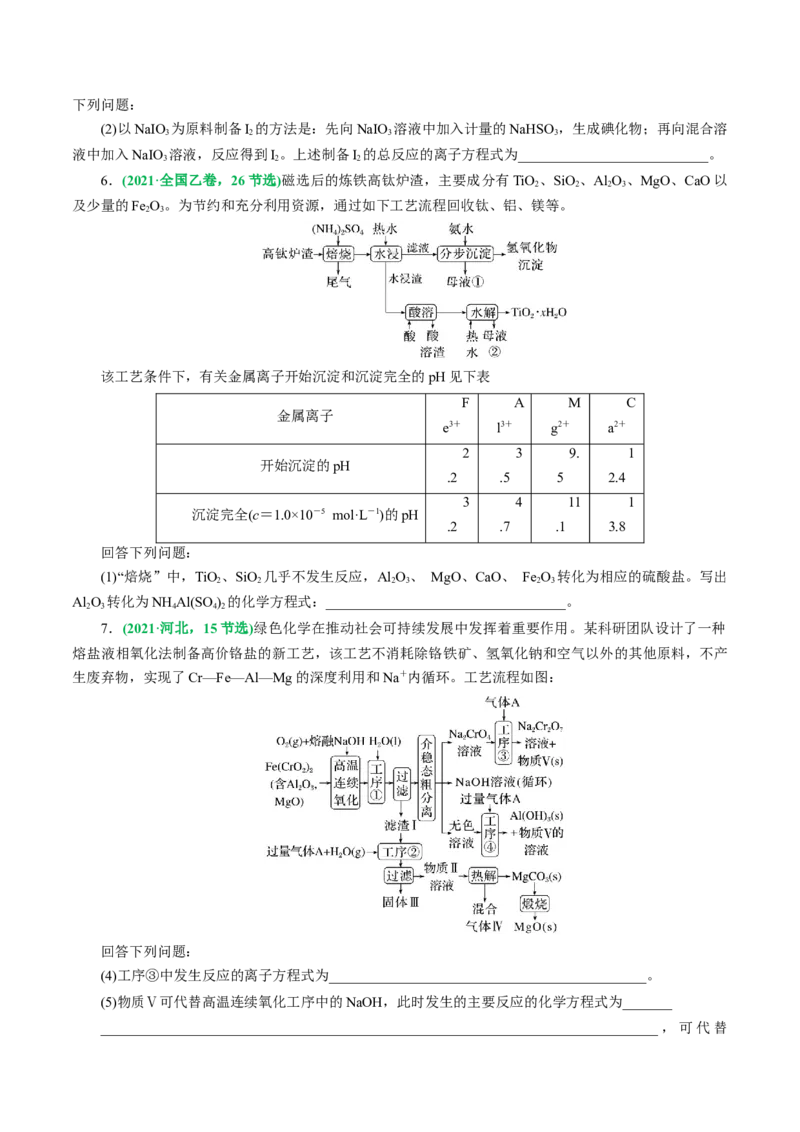
1.(2023•全国甲卷,26)BaTiO 是一种压电材料。以BaSO 为原料,采用下列路线可制备粉状
3 4
BaTiO 。
3
(5)“沉
淀”步骤中生成BaTiO(C O) 的化学方程式为_______。
2 4 2
2.(2023•辽宁省选择性考试,16)某工厂采用如下工艺处理镍钴矿硫酸浸取液含(Ni2+、Co2+、Fe2+、
Fe3+、Mg2+和Mn2+)。实现镍、钴、镁元素的回收。
(5)“沉钴镍”中得到的Co(Ⅱ)在空气中可被氧化成CoO(OH),该反应的化学方程式为_______。
3.(2023•江苏卷,17)空气中CO 含量的控制和CO 资源利用具有重要意义。
2 2
(1)燃煤烟气中CO 的捕集可通过如下所示的物质转化实现。
2
“吸收”后所得的KHCO 溶液与石灰乳反应的化学方程式为___________。
3
4.(2022•河北省选择性考试)以焙烧黄铁矿FeS(杂质为石英等)产生的红渣为原料制备铵铁蓝
2
Fe(NH )Fe(CN) 颜料。工艺流程如下:
4 6
(3)还原工序中,不生成S单质的反应的化学方程式为_______。
(5)沉铁工序产生的白色沉淀Fe(NH )Fe(CN) 中 的化合价为_______,氧化工序发生反应的离子方程
4 2 6
式为_______。
5.(2021·全国甲卷,26节选)碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。回答下列问题:
(2)以NaIO 为原料制备I 的方法是:先向NaIO 溶液中加入计量的NaHSO,生成碘化物;再向混合溶
3 2 3 3
液中加入NaIO 溶液,反应得到I。上述制备I 的总反应的离子方程式为___________________________。
3 2 2
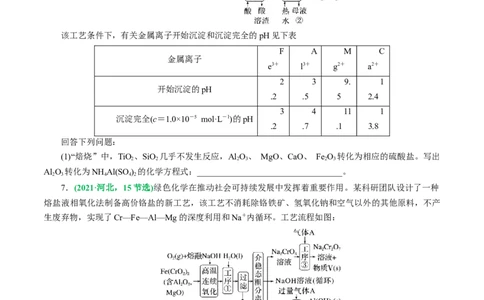
6.(2021·全国乙卷,26节选)磁选后的炼铁高钛炉渣,主要成分有TiO 、SiO 、Al O 、MgO、CaO以
2 2 2 3
及少量的Fe O。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
2 3
该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表
F A M C
金属离子
e3+ l3+ g2+ a2+
2 3 9. 1
开始沉淀的pH
.2 .5 5 2.4
3 4 11 1
沉淀完全(c=1.0×10-5 mol·L-1)的pH
.2 .7 .1 3.8
回答下列问题:
(1)“焙烧”中,TiO 、SiO 几乎不发生反应,Al O 、 MgO、CaO、 Fe O 转化为相应的硫酸盐。写出
2 2 2 3 2 3
Al O 转化为NH Al(SO ) 的化学方程式:__________________________________。
2 3 4 4 2
7.(2021·河北,15节选)绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种
熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产
生废弃物,实现了Cr—Fe—Al—Mg的深度利用和Na+内循环。工艺流程如图:
回答下列问题:
(4)工序③中发生反应的离子方程式为_____________________________________________。
(5)物质Ⅴ可代替高温连续氧化工序中的NaOH,此时发生的主要反应的化学方程式为_______
_______________________________________________________________________________,可代替NaOH的化学试剂还有____________(填化学式)。
8.(2021·湖南,17节选)Ce (CO) 可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要
2 3 3
以CePO 形式存在,还含有SiO 、Al O 、Fe O 、CaF 等物质。以独居石为原料制备Ce (CO)·nHO的工
4 2 2 3 2 3 2 2 3 3 2
艺流程如下:
回答下列问题:
(5)“沉铈”过程中,生成Ce (CO)·nHO的离子方程式为_______________________。
2 3 3 2
(6)滤渣Ⅱ的主要成分为FePO ,在高温条件下,LiCO 、葡萄糖(C H O)和FePO 可制备电极材料
4 2 3 6 12 6 4
LiFePO ,同时生成CO和HO,该反应的化学方程式为________________________。
4 2
1.陌生化学方程式书写的思路
首先根据题给材料中的信息写出部分反应物和生成物的化学式,再根据反应前后元素化合价有无变化
判断反应类型:
(1)元素化合价无变化则为非氧化还原反应,遵循原子守恒定律。
(2)元素化合价有变化则为氧化还原反应,除遵循原子守恒定律外,还要遵循得失电子守恒规律。最后
根据题目要求写出化学方程式或离子方程式(需要遵循电荷守恒规律)即可。
2.陌生氧化还原反应方程式书写的具体步骤1.书写方法
2.书写关键——识记常见氧化剂、还原剂及产物预测
(1)常见的氧化剂及还原产物预测
氧化剂 还原产物预测
Mn2+(酸性);MnO (中性);MnO(碱
2
KMnO
4
性)
KCr O(酸性) Cr3+
2 2 7
浓硝酸 NO
2
稀硝酸 NO
X(卤素单质) X-
2
HO OH-(碱性);HO(酸性)
2 2 2
NaO NaOH(或NaCO)
2 2 2 3
NaClO(或ClO-) Cl-、Cl
2
NaClO Cl、ClO
3 2 2
PbO Pb2+
2
(2)常见的还原剂及氧化产物预测
还原剂 氧化产物预测
Fe2+ Fe3+(酸性);Fe(OH) (碱性)
3
SO (或HSO 、SO) SO
2 2 3
S2-(或HS) S、SO (或SO)、SO
2 2
HC O CO
2 2 4 2HO O
2 2 2
I-(或HI) I、IO
2
CO CO
2
金属单质(Zn、Fe、Cu Zn2+、Fe2+(与强氧化剂反应生成Fe3+)、
等) Cu2+
3.分步法书写非氧化还原方程式
陌生的非氧化还原反应主要为复分解反应,抓住复分解反应条件推断产物,结合盐类水解、酸碱强弱
综合分析。这类复杂的化学反应可以采用分步思考,例如,碳酸钠、氢氟酸和氢氧化铝混合物在高温下反
应 制 备 冰 晶 石 , 可 以 分 三 步 理 解 : Al(OH) +3HF=AlF +3H O , NaCO+2HF=2NaF+CO ↑+H O ,
3 3 2 2 3 2 2
AlF+3NaF=Na AlF 。加合得到总反应式为2Al(OH) +3Na CO+12HF=2Na AlF+3CO ↑+9H O。再如在碳酸
3 3 6 3 2 3 3 6 2 2
氢钠溶液中加入少量硫酸亚铁溶液制备碳酸亚铁:Fe2++HCO-=FeCO ↓+H+,H++ HCO -=CO ↑+H O,加合
3 3 3 2 2
得总反应式为Fe2++2 HCO -=FeCO ↓+CO ↑+H O。
3 3 2 2
1.(2024·辽宁丹东高三阶段性质测试)油画中使用的无机颜料雄黄(As S)在不同空气湿度和光照条件下
2 3
会发生褪色,主要发生以下两种化学反应:
(1)紫外光照射下,被氧化的元素是 (填元素符号),每生成1 mol As O,转移电子的物质的
2 3
量为 mol。
(2)自然光照射下发生反应的化学方程式: 。
(3)氧化等量As S 时,紫外光与自然光照射下消耗O 的物质的量之比为 。
2 3 2
(4) Na S 和NaCO 按物质的量之比为2:1混合后加热,向溶液中通入 即可获得NaSO 和CO,
2 3 2 3 2 2 3 2
该反应的离子方程式: 。上述过程一般在碱性环境下进行,若在酸性条件下由于生成副产物
导致产品会发黄。
(5)芯片制造工业中利用GaAs与HO 反应,将As氧化为+5价,该反应的氧化剂与还原剂物质的量之
2 2
比为 。
2.(2024·山西吕梁高三联考)氧化还原反应在工业生产、环保及科研中有广泛的应用。请根据以下信
息,结合所掌握的化学知识,回答下列问题:
Ⅰ.可以用智利硝石提取硝酸钠后的母液为原料,加入亚硫酸氢钠制取琪,相关反应如下:
___________ NaIO+___________ NaHSO→3NaHSO+___________ Na SO
3 3 4 2 4
+___________I +___________H O(未配平)
2 2(1)配平上述化学方程式,用单线桥标出电子转移的方向和数目。
Ⅱ.钒性能优良,用途广泛,有金属“维生素”之称。
(2) V O 能与盐酸反应生成VO2+和一种黄绿色气体,该黄绿色气体能与NaSO 溶液反应而被吸收,则
2 5 2 3
SO 2-、 、VO2+的还原性由强到弱的顺序是 。
3
(3)V O 在碳高温还原时,在氮气气氛下氮化还原制备VN,还生成一种具有还原性的气体,则该反应
2 5
的化学方程式为 。
VO+5C+N 2VN+5CO
2 5 2
3.(2024·江苏连云港高三统考)根据提供的情境书写指定反应的方程式。
一种以MnCO 为原料制取MnO 的流程如图所示,450℃,MnCO 在空气中灼烧得到三种锰的氧化物,
3 2 3
锰元素所占比例随温度变化的曲线如图所示。
(1)写出450℃,MnCO 在空气中灼烧生成主要产物的化学方程式: 。
3
(2)写出“浸取”时MnO 发生反应的离子方程式: 。
2 3
4.(2024·河南省名校联盟高三联考)硫及其化合物是重要的化学物质。回答下列问题:
(1)二氯化二硫(S Cl,无色液体)常用作贵稀金属的萃取剂,遇水会反应,生成S、SO 和刺鼻的酸雾,
2 2 2
该反应的化学方程式为 ;将干燥的NH 通入SCl 的CCl 溶液中,可发生反应:
3 2 2 4
6SCl+16NH=S N+S +12NHCl (已知S 是硫单质中最稳定的),该反应中,NH 体现的性质有还原性和
2 2 3 4 4 8 4 8 3
。
(2)将SO 通入含有FeCl 和BaCl 的混合溶液中有白色沉淀产生,其原因是 (用离子方程式
2 3 2
解释)。
(3)同种反应物,其反应产物与浓度、温度、反应物相对量等因素有关。影响SO 与NaOH反应产物的
2
因素与下列反应相同的是 (填字母)。
a.Na与O 反应 b.HS与O 反应
2 2 2
c.FeBr 溶液与Cl 反应 d.Fe与稀硝酸反应
2 2
(4)SOCl (遇水产生刺激性气味的气体)是有机合成的氯化剂,与NaOH溶液反应可生成三种钠盐,写出
2
三种钠盐的化学式: 。
(5)造纸、印刷等工业废水中含有大量的硫化物(主要成分为NaS),可用如图所示转化方式除去。
2①当反应I和Ⅱ转移电子数相等时,还原剂的物质的量之比为 。
②已知反应Ⅲ中NaS与NaSO 按等物质的量反应,反应的化学方程式为 (反应物有HO
2 2 3 2
参与)。
5.(2024·浙江绍兴高三选考科目诊断性考试)燃煤火电厂产生的尾气(主要成分为SO 、NO)可以按如下
2
流程脱除或利用。
请回答:
(1)写出途径Ⅰ中SO 转化成CaSO 的总反应化学方程式 。
2 4
(2)下列说法正确的是___________。
A.途径Ⅰ中Cu+的作用是催化剂
B.途径Ⅰ中C H 的作用是还原剂
2 4
C.若用氨水代替石灰乳吸收尾气,则SO 可能最终转化成为NH HSO 或(NH )SO
2 4 4 4 2 4
D.工业制硝酸的第一步是N 与O 反应得到NO
2 2
(3)写出途径Ⅱ中NO与CaCO 、NaClO 混合液反应的化学反应方程式 。
3 2
(4)下列物质有可能代替途径Ⅱ中NaClO 的是___________。
2
A.NaClO B.O C.NH D.NaS
3 3 2
(5)设计实验方案检验途径Ⅱ产物中的含氮阴离子 。
6.(2024·甘肃兰州高三期中)高铁酸钾((K FeO)是一种集氧化、吸附、絮凝于一体的新型多功能水处
2 4
理剂,其生产工艺如图:已知:①Cl 与NaOH溶液反应的产物与反应温度有关,温度较低时产物为NaCl、NaClO、HO;温度
2 2
较高时产物为NaCl、NaClO、HO。
3 2
②同一条件下,溶液的碱性越强,高铁酸盐的稳定性越高。
回答下列问题:
(1)写出此工艺流程中Cl 通入KOH溶液的化学方程式: 。
2
(2)在“反应液I”中加入KOH固体的目的是① ,②提供碱性环境。
(3)写出Fe(NO ) 溶液与碱性KClO浓溶液反应的离子方程式: 。
3 3
(4)从“反应液Ⅱ”中分离出KFeO 后,副产品是 (写化学式)。
2 4
(5)K FeO 可作为新型多功能水处理剂的原因是:① ,② 。
2 4
(6)该工艺每得到1.98kgK FeO,理论上消耗Cl 的物质的量为 mol。
2 4 2
7.(2024·山东枣庄高三期中)钒酸钇(YVO)广泛应用于光纤通信领域,一种用废钒催化剂(含 VO、
4 2 5
KO、SiO 少量Fe O 制取YVO 的工艺流程如下:
2 2 2 3 4
已知:VO(OH) 既能与强酸反应,又能与强碱反应。 回答下列问题:
2 2 4
(1)V O(OH) 中V元素的化合价为 。
2 2 4
(2)“还原酸浸”时,钒以VO2+浸出,“浸出液”中还含有的金属离子是 。VO 被还原的
2 5
离子方程式为 。
(3)常温下,“钒、钾分离”时,pH 对钒的沉淀率的影响如图所示:pH>7时,随pH增大钒的沉淀率
降低的原因可能是 。
(4)结合“碱溶”和“沉钒”可知,ClO -、VO -氧化性更强的是 ,“沉钒”时发生反应的
3 3
化学方程式为 。
(5)某废钒催化剂中VO 的含量为26.0%,某工厂用1吨该废钒催化剂且用该工艺流程生产YVO,整
2 5 4
个流程中V的损耗率为30.0%,则最终得到 YVO 。
4
8.(2024·辽宁沈阳·高三辽宁实验中学校考期中)完成下列填空。(1)已知A、B、C、D为气体,其中A、B为单质,E、F为固体,G是氯化钙,它们之间的转换关系如
下图所示:
请回答下列问题:
①C的化学式是 ,D的电子式为 。
②如何检验E溶液中阳离子? 。
(2)在高压下,NO在 下分解生成两种化合物,体系中各组分的物质的量随时间变化曲线如图甲所
示。NO分解的化学方程式为 。
(3)有色金属提取工艺中会产生大量含氰(CN·)废水,对环境造成了极大的负担。在碱性条件下可用
ClO-将其氧化成 和 写出反应的离子方程式: 。
(4)向酸性废水中加入NaClO,消除 污染。写出相应的离子方程式为 。
(5)将软锰矿与硫铁矿 粉碎混合,用硫酸浸取。研究发现,酸浸时, 和 颗粒构成两个
原电池反应,其原理如图所示(部分产物未标出)。
若 原电池中生成单质S,其反应的离子方程式为 。
9.(2024·安徽合肥十联考高三第一次质量测试)氯的许多化合物在生活中扮演着重要角色,如:亚氯
酸钠(NaClO)和ClO (具有强烈刺激性气味的气体)都是重要的漂白剂。回答下列问题:
2 2
(1) NaClO 中氯元素的化合价为 。
2
(2)草酸(H C O)是一种易溶于水的弱酸,利用硫酸酸化的草酸还原NaClO,可较安全地生成ClO ,反
2 2 4 3 2
应的离子方程式为 。
(3)自来水用ClO 处理后,有少量ClO 残留在水中,可用碘量法做如下检测:
2 2①取500 mL水样,加入一定量的碘化钾,用氢氧化钠溶液调至中性,再加入淀粉溶液,溶液变蓝。
写出ClO 与碘化钾反应的化学方程式: (已知ClO 存在于pH为4~6的溶液中,ClO -存在于
2 2 2
中性溶液中)。
②已知:2NaSO+I = Na SO+2 NaI,向①所得溶液中滴加 的NaSO 溶液,达到滴
2 2 3 2 2 4 6 2 2 3
定终点时,消耗NaSO 溶液的体积为20.00 mL。判断达到滴定终点的方法是 ;该水样中ClO
2 2 3 2
的浓度是 mg· L-1。
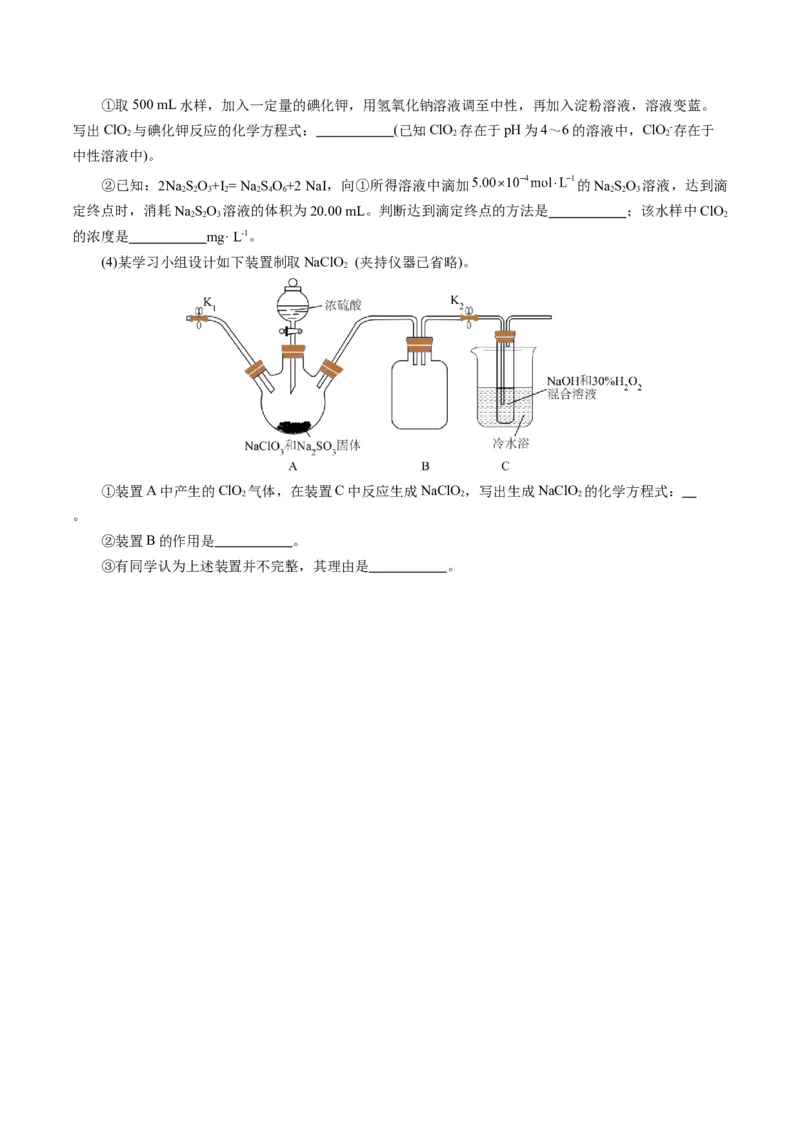
(4)某学习小组设计如下装置制取NaClO (夹持仪器已省略)。
2
①装置A中产生的ClO 气体,在装置C中反应生成NaClO,写出生成NaClO 的化学方程式:
2 2 2
。
②装置B的作用是 。
③有同学认为上述装置并不完整,其理由是 。