文档内容
重难点 17 有机合成与推断综合题
►命题趋势►解题策略►真题回眸►限时检测
“完全推断型”有机合成与推断
有机合成与推断综合题 “结构已知型”有机合成与推断
“半推半知型”有机合成与推断
有机合成与推断综合题通常以药物、材料、新物质的合成为背景,考查有机物结构简式的推断、官能
团的名称、有机物命名、反应类型的判断、有机化学方程式的书写、同分异构体数目的判断、结合核磁共
振氢谱书写指定有机物的结构简式、合成路线设计等。总体来说,命题形式可以大致分为三类:
(1)完全推断型:即在合成路线中各物质的结构简式是未知的,需要结合反应条件、分子式、目标
产物、题给信息等进行推断;
(2)结构已知型:即合成路线中各物质的结构简式是已知的,此类试题中所涉及的有机物大多是陌
生且比较复杂的,需要根据前后的变化来分析其反应特点;
(3)“半推半知“型:即合成路线中部分有机物的结构简式是已知的,部分是未知的,审题时需要
结合条件及已知结构去推断未知有机物的结构。
预计在2024年高考命题中,有机合成与推断向着综合型、信息化、能力型方向发展,仍然以新材
料、新药物、新科技及社会热点为题材来综合考查考生的有机知识。
【策略1】掌握有机合成中碳骨架构建的方法
(1)碳链的增长:
①与HCN的加成反应;
②加聚或缩聚反应;
③酯化反应。
(2)碳链的减短:
①脱羧反应:R—COONa+NaOH――→R—H+NaCO。
2 3
②氧化反应:;
R—CH===CH ―――――――→RCOOH+CO↑。
2 2
③酯类、糖类、蛋白质等的水解反应。
④烃的裂化或裂解反应:C H ――→C H +C H 。
16 34 8 18 8 16
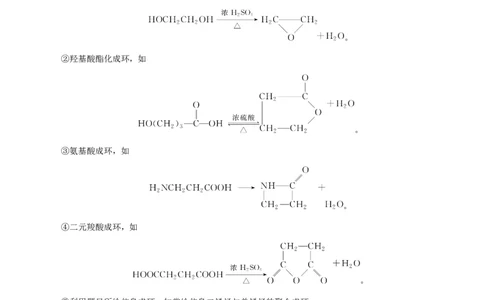
(3)常见碳链成环的方法
①二元醇成环,如
。
②羟基酸酯化成环,如
。
③氨基酸成环,如
。
④二元羧酸成环,如
。
⑤利用题目所给信息成环,如常给信息二烯烃与单烯烃的聚合成环:
【策略2】掌握有机合成中官能团的转化
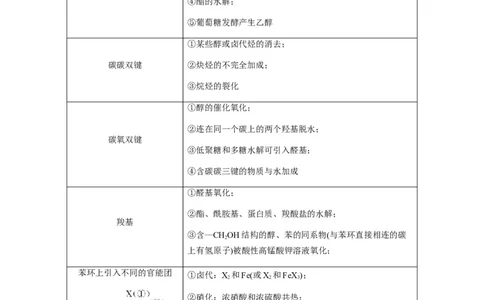
(1)官能团的引入
官能团 引入方法
碳卤键 ①烃、酚的取代;②不饱和烃与HX、X 的加成;
2
③醇与氢卤酸(HX)的取代
①烯烃与水加成;
②醛、酮与氢气加成;
羟基 ③卤代烃在碱性条件下的水解;
④酯的水解;
⑤葡萄糖发酵产生乙醇
①某些醇或卤代烃的消去;
碳碳双键 ②炔烃的不完全加成;
③烷烃的裂化
①醇的催化氧化;
②连在同一个碳上的两个羟基脱水;
碳氧双键
③低聚糖和多糖水解可引入醛基;
④含碳碳三键的物质与水加成
①醛基氧化;
②酯、酰胺基、蛋白质、羧酸盐的水解;
羧基
③含—CHOH结构的醇、苯的同系物(与苯环直接相连的碳
2
上有氢原子)被酸性高锰酸钾溶液氧化;
苯环上引入不同的官能团
①卤代:X 和Fe(或X 和FeX);
2 2 3
②硝化:浓硝酸和浓硫酸共热;
③烃基氧化;
④先卤代后水解
(2)官能团的消除
①通过加成反应消除不饱和键(双键、三键、苯环等)。
②通过消去、氧化或酯化反应等消除羟基。③通过加成或氧化反应消除醛基。
④通过水解反应消除酯基、酰胺基、碳卤键。
(3)官能团的改变
①利用官能团的衍生关系进行衍变,如R—CHOH R—CHO――→R—COOH。
2
②通过某种化学途径使一个官能团变为两个,如
CHCHOH――――――→CH===CH ――――――→X—CH CH—X――→HO—CH CH—OH。
3 2 2 2 2 2 2 2
。
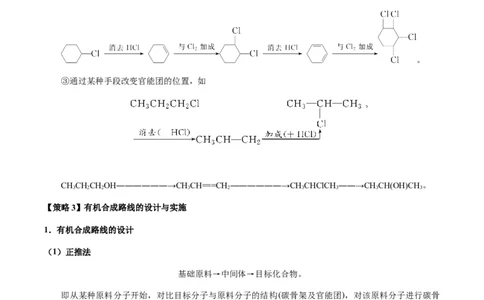
③通过某种手段改变官能团的位置,如
CHCHCHOH――――――→CHCH===CH ――――――→CHCHClCH ――→CHCH(OH)CH 。
3 2 2 3 2 3 3 3 3
【策略3】有机合成路线的设计与实施
1.有机合成路线的设计
(1)正推法
基础原料→中间体→目标化合物。
即从某种原料分子开始,对比目标分子与原料分子的结构(碳骨架及官能团),对该原料分子进行碳骨
架的构建和官能团的引入(或者官能团的转化),从而设计出合理的合成路线。如以乙烯为原料合成乙酸乙
酯,可采用正推法:
(2)逆推法
目标化合物→中间体→基础原料。即从目标分子着手,分析目标分子的结构,然后由目标分子逆推出原料分子,并进行合成路线的设
计。如采用逆推法,通过对苯甲酸苯甲酯( )的结构分析可知合成该有机化合物的是苯
甲酸与苯甲醇,继续逆推可得出原料分子为甲苯,如图所示:
设计合成路线时,要选择反应步骤少,试剂成本低,操作简单,毒性小,污染小,副产物少的路线,
即
2.最佳合成途径的选择
(1)合成基本原则:原理正确,原料价廉,操作简便,步骤简单,条件适宜,易于分离。
具体而言:
①起始原料、溶剂和催化剂要廉价、易得、低毒性、低污染。
②应尽量选择步骤较少的合成路线。为了减少合成步骤,应尽量选择与目标化合物结构相似的原料。
③合成路线要符合“绿色、环保”的要求,高效的有机合成应最大限度地利用原料分子中的每一个原
子,使之转化到目标化合物中。
④有机合成反应要操作简单、条件温和、能耗低、易于实现、不污染环境或污染小。
⑤要按一定的反应顺序和规律引入官能团,不能臆造不存在的反应。综合运用有机反应中官能团的衍
变规律及有关的信息,掌握正确的解题方法,有时则要综合运用顺推和逆推的方法导出最佳的合成路线。
对于多种合理路线的选择,要综合考虑诸多因素:原料的来源和价格、能耗、反应速率、反应物的利
用率、生产设备和技术条件是否具备、是否有污染物产生或排放等。
(2)有机合成路线的选择①一元合成路线
以乙烯为例:② ,
③ ,
⑤ 。
②二元合成路线
以乙烯为例:② ,
④ ,
⑤ 。
③芳香族化合物合成路线
a. 。
b.
。
3.有机合成中常见官能团的保护
如:(1)酚羟基的保护:
因酚羟基易被氧化,所以在氧化其他基团前可以先使其与 NaOH反应,把—OH变为—ONa将其保护
起来,待氧化后再酸化将其转变为—OH。
(2)碳碳双键的保护:
碳碳双键也容易被氧化,在氧化其他基团前可以利用其与 HCl等的加成反应将其保护起来,待氧化后
再利用消去反应转变为碳碳双键。
(3)氨基(—NH)的保护:
2
如在利用对硝基甲苯( )合成对氨基苯甲酸( )的过程中应先把
—CH 氧化成—COOH之后,再把—NO 还原为—NH ,防止当KMnO 氧化—CH 时,—NH (具有还原性)
3 2 2 4 3 2
也被氧化。
【策略4】熟悉有机合成与推断的突破口
1.通过物理特征突破
有机化合物中各类代表物的状态、气味、溶解性、密度、熔点、沸点等往往各有特点,解题时可考虑
通过物理特征找到题眼。
2.根据反应物、产物分子式特征推断有机物结构及反应类型
分析反应物、产物的分子式特征,根据其差异,联想已有有机化学知识,猜想可能的有机反应类型,
由此确定反应物、产物的结构特点,结合框图中的其他物质,确定具体的结构。如:―→:对比F与G的
分子式,G比F的分子式少1个H,多1个NO ,可判断反应类型可能为取代反应,F若为苯酚,则G可能
2
为硝基苯酚。
3.从实验现象突破
反应现象 思考方向
溴水褪色 可能含有碳碳双键、碳碳三键或酚羟基、醛基等
可能含有碳碳双键、碳碳三键、醛基、酚羟基或有机物为
苯的同系物(与苯环直接相连的碳原子上含有H)、醇(含
使酸性KMnO 溶液褪色
4
结构)等
①遇FeCl 溶液显紫色 含有酚羟基
3②与浓溴水反应产生白色沉淀
加入新制Cu(OH) 并加热有砖
2
红色沉淀生成,或加入银氨溶 含有醛基或甲酸酯基或甲酸
液水浴加热有银镜出现
加入Na,有H 产生 可能有—OH或—COOH
2
加入NaHCO 溶液有气体放出 含—COOH
3
4.从反应条件突破
反应条件 可能的有机化合物及反应
①醇的消去反应;
浓硫酸,加热 ②酯化反应;
③苯的硝化反应
浓硝酸、浓硫酸,加热 苯环上的取代
①酯的水解反应;
稀硫酸,加热
②二糖、多糖的水解反应等
氢卤酸(HX),加热 醇的取代
①卤代烃的水解反应;
强碱的水溶液,加热
②酯的水解反应等
强碱的醇溶液,加热 卤代烃的消去反应
新制Cu(OH) 或银氨溶
2
醛基(醛、甲酸、甲酸酯、葡萄糖等)的氧化反应
液,加热
①烯烃、炔烃的氧化反应;
酸性KMnO 溶液或酸 ②某些苯的同系物(与苯环直接相连的碳原子上含有H)的氧化反
4
性重铬酸钾溶液 应;
③醇、醛、苯酚的氧化反应
O、Cu(或Ag),加热 ①醇的催化氧化反应;
2②醛的氧化;
①烯烃、炔烃的加成反应;
②芳香烃的加成反应;
H、催化剂,加热
2
③醛、酮还原为醇
特别注意:羧基、酯基、酰胺基中的碳氧双键不能加成
溴水或溴的CCl 溶液 烯烃、炔烃的加成反应
4
①苯酚的取代反应;
浓溴水 ②碳碳双键和碳碳三键的加成;
③醛的氧化
①烃的取代反应;
Cl,光照
2
② 中侧链的取代反应
铁粉或卤化铁、X 苯环上的卤代反应
2
如:
(1)――――――→:反应类型可能为取代反应(酯化反应),联想乙酸乙酯的制备,则F结构中可能有羧
基,G结构中可能有酯基。
(2)―――――→:反应类型可能为加成反应,通过分子式即可验证,联想乙烯与溴的四氯化碳溶液反
应,则C结构中应该存在一个碳碳双键。
5.根据相关数据确定官能团的数目
(1)烃和卤素单质的取代:取代1 mol 氢原子,消耗1 mol 卤素单质(X )。
2
(2) 的加成:与H、Br 、HCl、HO等加成时按物质的量之比为1∶1反应。
2 2 2
(3)含—OH的有机物与Na反应时:2 mol —OH生成1 mol H 。
2
(4)1 mol —CHO对应2 mol Ag;或1 mol —CHO对应1 mol Cu O(注意:HCHO中相当于有2个—
2
CHO)。
(5)物质转化过程中相对分子质量的变化(关系式中M代表第一种有机化合物的相对分子质量)
6.从转化关系突破
(1)连续氧化关系:
结论Ⅰ A为醇、B为醛、C为羧酸、D为酯
结论Ⅱ A、B、C三种物质中碳原子数相同,碳骨架结构相同
结论Ⅲ A分子结构中与羟基相连的碳原子上至少有2个氢原子,即含—CHOH
2
若D能发生银镜反应,则A为CHOH,B为HCHO,C为HCOOH,D为
3
结论Ⅳ
HCOOCH
3
(2)重要的“三角”转化关系:
①卤代烃在强碱的醇溶液中加热,醇在浓硫酸、加热条件下均发生消去反应生成烯烃。
②烯烃在一定条件下分别与HX(X为卤素原子)、HO发生加成反应生成卤代烃、醇。
2
③卤代烃在强碱的水溶液中加热发生取代反应生成醇,醇与浓HX在加热条件下发生取代反应生成卤
代烃。
在有机推断中灵活运用以上转化关系,并根据题目的限制条件拓展和完善,可起到事半功倍的效果。
(3)有机反应各类物质的转化关系:7.有机推断中常考的“陌生信息”
(1)羟醛缩合:RCHO+R′CHCHO―――――→ +HO(R、R′表示烃基或氢)
2 2
(2)利用格氏试剂发生加成反应
(R代表烃基,R′、R″代表烃基或氢)。
(3)烯烃的氧化:
(4)成环反应:
考向一 “完全推断型”有机合成与推断
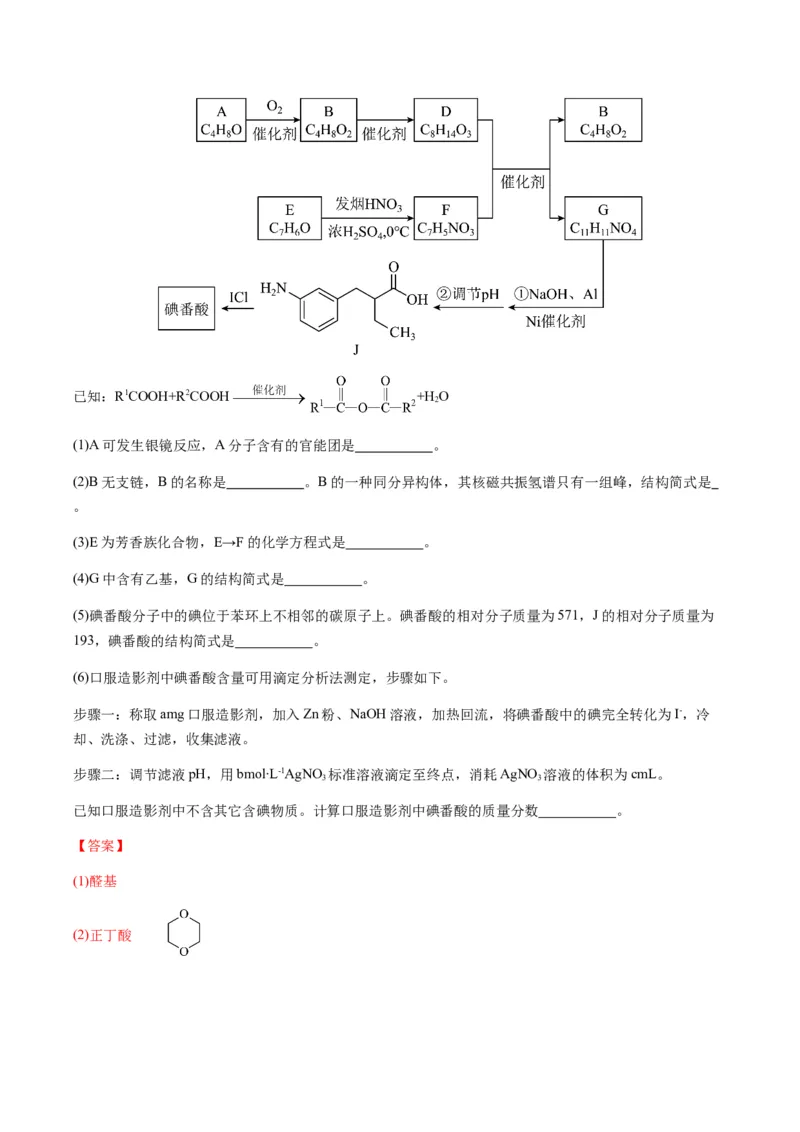
1.(2022·北京·高考真题)碘番酸是一种口服造影剂,用于胆部X—射线检查。其合成路线如下:已知:R1COOH+R2COOH +H O
2
(1)A可发生银镜反应,A分子含有的官能团是 。
(2)B无支链,B的名称是 。B的一种同分异构体,其核磁共振氢谱只有一组峰,结构简式是
。
(3)E为芳香族化合物,E→F的化学方程式是 。
(4)G中含有乙基,G的结构简式是 。
(5)碘番酸分子中的碘位于苯环上不相邻的碳原子上。碘番酸的相对分子质量为571,J的相对分子质量为
193,碘番酸的结构简式是 。
(6)口服造影剂中碘番酸含量可用滴定分析法测定,步骤如下。
步骤一:称取amg口服造影剂,加入Zn粉、NaOH溶液,加热回流,将碘番酸中的碘完全转化为I-,冷
却、洗涤、过滤,收集滤液。
步骤二:调节滤液pH,用bmol∙L-1AgNO 标准溶液滴定至终点,消耗AgNO 溶液的体积为cmL。
3 3
已知口服造影剂中不含其它含碘物质。计算口服造影剂中碘番酸的质量分数 。
【答案】
(1)醛基
(2)正丁酸(3)
(4)
(5)
(6)
【详解】本流程的目的,以A为原料制取碘番酸。由A可发生银镜反应,可确定A为醛,由B无支链,
可确定B为CHCHCHCOOH,则A为CHCHCHO;依据题干信息,可确定D为
3 2 2 3 2
;E为芳香族化合物,则E为 ;由J的结构简式
,可确定F为 。由题给信息,要确定G为
。
(1)由A的分子式C HO及可发生银镜反应,可确定A分子含有的官能团是醛基。答案为:醛基;
4 8
(2)B的分子式为C HO、无支链,由醛氧化生成,则B为CHCHCHCOOH,名称是正丁酸。B的一
4 8 2 3 2 2
种同分异构体,其核磁共振氢谱只有一组峰,则表明分子中8个H原子全部构成-CH-,B的不饱和度为
2
1,则其同分异构体应具有对称的环状结构,从而得出其结构简式是 。答案为:正丁酸; ;
(3)由分析知,E为 ,F为 ,则E→F的化学方程式是。答案为: ;
(4)由分析可知,G的结构简式是 。答案为: ;
(5)碘番酸的相对分子质量为571,J的相对分子质量为193,由相对分子质量差可确定,J生成碘番酸
时,分子中引入3个I原子,而碘番酸分子中的碘位于苯环上不相邻的碳原子上,则碘番酸的结构简式是
。答案为: ;
(6) ——3AgNO,n(AgNO)= bmol∙L-1×c×10-3L=bc×10-3mol,则口服造影剂中碘
3 3
番酸的质量分数为 = 。答案为: 。
考向二 “结构已知型”有机合成与推断
2.(2023·福建·统考高考真题)沙格列汀是治疗糖尿病的常用药物,以下是制备该药物重要中间产物F的
合成路线。
已知: 表示叔丁氧羰基。
(1)A中所含官能团名称 。
(2)判断物质在水中的溶解度:A B(填“>”或“<”)(3)请从物质结构角度分析 能与 反应的原因 。
(4) 的反应类型 。
(5)写出D的结构简式 。
(6)写出 的化学反应方程式 。
(7)A的其中一种同分异构体是丁二酸分子内脱水后的分子上一个H被取代后的烃的衍生物,核磁共振氢谱
图的比例为 ,写出该同分异构体的结构简式 。(只写一种)
【答案】
(1)羧基、酰胺基
(2)>
(3)(C H)N结构中的N原子有孤对电子,分子偏碱性,能和酸性的HCl发生反应
2 5 3
(4)酯化反应或取代反应
(5)
(6) + HCONH +HCOOC H
2 2 5
(7)
【详解】 和C HOH发生酯化反应生成 ,加Boc-OH发生取代反应
2 5
生成 ,加入氢气发生加成反应生成 ,发生消去反应生成
,加入HCONH 发生取代反应生成 。
2(1)A为 ,官能团为羧基、酰胺基;
故答案为:羧基、酰胺基。
(2)A中含有羧基,属于亲水基,B中含有酯基,属于疏水基,故A的溶解度大于B的溶解度;
故答案为:>。
(3)(C H)N结构中的N原子有孤对电子,分子偏碱性,能和酸性的HCl发生反应;
2 5 3
故答案为:(C H)N结构中的N原子有孤对电子,分子偏碱性,能和酸性的HCl发生反应。
2 5 3
(4)根据分析可知,A→B的反应类型为酯化反应或取代反应;
故答案为:酯化反应或取代反应。
(5)根据分析可知D结构简式为为 ;
故答案为: 。
(6)根据分析可知E→F的化学反应方程式为 + HCONH +
2
HCOOC H;
2 5
故答案为: + HCONH +HCOOC H。
2 2 5
(7)丁二酸为 ,分子内脱水时,两个羧基间脱水,脱水产物分子上一个H被取代后的烃的衍
生物是A的同分异构体,核磁共振氢谱图的比例为3:2:1:1,则该同分异构体的结构简式为
;故答案为: 。
3.(2023·江苏·统考高考真题)化合物I是鞘氨醇激酶抑制剂,其合成路线如下:
(1)化合物A的酸性比环己醇的 (填“强”或“弱”或“无差别”)。
(2)B的分子式为 ,可由乙酸与 反应合成,B的结构简式为 。
(3)A→C中加入 是为了消耗反应中产生的 (填化学式)。
(4)写出同时满足下列条件的C的一种同分异构体的结构简式: 。
碱性条件水解后酸化生成两种产物,产物之一的分子中碳原子轨道杂化类型相同且室温下不能使2%酸性
溶液褪色;加热条件下,铜催化另一产物与氧气反应,所得有机产物的核磁共振氢谱中只有1个
峰。
(5)G的分子式为 ,F→H的反应类型为 。
(6)写出以 、 和 为原料制备 的合成路线流图
(须用NBS和AlBN,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
【答案】
(1)强
(2)CH COCl
3
(3)HCl
(4)
(5)取代反应
(6)【详解】 与 发生取代反应生成 ,可推知化学方程式为
+CH COCl→ +HCl,可知B为CHCOCl; 发生水解反应得到F:
3 3
, 与G: 发生取代反应得到 ,可知化学方程式为
+ → +HBr,由此推知G为 。
【详解】
(1)化合物A: 中含有酚羟基,酚羟基酸性强于醇羟基,故化合物A的酸性比环己醇的
强。
(2)由分析可知B的结构简式为CHCOCl。
3
(3)A→C的化学方程式为 +CH COCl→ +HCl, 显碱性可以与HCl
3
发生中和反应促进 +CH COCl→ +HCl平衡正移,提供 的产率,
3
故A→C中加入 是为了消耗反应中产生的HCl。
(4) 的同分异构体碱性条件水解后酸化生成两种产物,产物之一的分子中碳原子轨道杂化
类型相同且室温下不能使2%酸性 溶液褪色,说明其同分异构体为5,且该水解产物为苯甲酸;另
一水解产物为丙醇,且加热条件下,铜催化该产物与氧气反应,所得有机产物的核磁共振氢谱中只有1个峰,由此确定该醇为2-丙醇,由此确定 的同分异构体为 。
(5)由分析可知F→H的反应为 + → +HBr,该
反应为取代反应。
(6)结合F→H可设计以下合成路线:
。
考向三 “半推半知型”有机合成与推断
4.(2023·辽宁·统考高考真题)加兰他敏是一种天然生物碱,可作为阿尔茨海默症的药物,其中间体的合
成路线如下。
回答下列问题:(1)A中与卤代烃成醚活性高的羟基位于酯基的 位(填“间”或“对”)。
(2)C发生酸性水解,新产生的官能团为羟基和 (填名称)。
(3)用O 代替PCC完成D→E的转化,化学方程式为 。
2
(4)F的同分异构体中,红外光谱显示有酚羟基、无N-H键的共有 种。
(5)H→I的反应类型为 。
(6)某药物中间体的合成路线如下(部分反应条件已略去),其中M和N的结构简式分别为 和
。
【答案】
(1)对
(2)羧基
(3)2 +O 2 +2H O
2 2
(4)3
(5)取代
(6)
【详解】根据有机物A的结构和有机物C的结构,有机物A与CH3I反应生成有机物B,根据有机物B的
分子式可以得到有机物B的结构,即 ;有机物与BnCl反应生成有机物C,有机物C
发生还原反应生成有机物D,有机物D与PCC发生氧化反应生成有机物E,根据有机物E的结构和有机物D的分子式可以得到有机物D的结构,即 ;有机物E与有机物有机物F发生已知条
件给的②反应生成有机物G,有机物G发生还原反应生成有机物H,根据有机物H与有机物G的分子式可
以得到有机物G的结构,即 ,同时也可得到有机物
F的结构,即 ;随后有机物H与HCOOCH CH 反应生成有机物I。由此分析
2 3
解题。
【详解】
(1)由有机物A与CHI反应得到有机物B可知,酚与卤代烃反应成醚时,优先与其含有的其他官能团的
3
对位羟基发生反应,即酯基对位的酚羟基活性最高,可以发生成醚反应,故答案为;对位。
(2)有机物C含有酯基,在酸性条件下发生水解生成羧基和羟基,故答案为羧基。
(3)O2与有机物D发生催化氧化反应生成有机物E,反应的化学方程式为2 +O
2
2 +2H O。
2
(4)F的同分异构体中不含有N-H键,说明结构中含有 结构,又因红外中含有酚羟基,说明结
构中含有苯环和羟基,固定羟基的位置 有邻、间、对三种情况,故有3种同分异构体。(5)有机物H与HCOOCH CH 反应生成有机物I,反应时,有机物H中的N-H键发生断裂,与
2 3
HCOOCH CH 中断裂的醛基结合,故反应类型为取代反应。
2 3
(6)根据题目中给的反应条件和已知条件,利用逆合成法分析,有机物N可以与NaBH 反应生成最终产
4
物,类似于题中有机物G与NaBH 反应生成有机物H,作用位置为有机物N的N=C上,故有机物N的结
4
构为 ,有机物M可以发生已知条件所给的反应生成有机物N,说明有机物M中含有
C=O,结合反应原料中含有羟基,说明原料发生反应生成有机物M的反应是羟基的催化氧化,有机物M
的结构为 ,故答案为 、 。
5.(2023·全国·统考高考真题)莫西赛利(化合物K)是一种治疗脑血管疾病的药物,可改善脑梗塞或脑出
血后遗症等症状。以下为其合成路线之一。
回答下列问题:
(1)A的化学名称是 。
(2)C中碳原子的轨道杂化类型有 种。
(3)D中官能团的名称为 、 。
(4)E与F反应生成G的反应类型为 。
(5)F的结构简式为 。(6)I转变为J的化学方程式为 。
(7)在B的同分异构体中,同时满足下列条件的共有 种(不考虑立体异构);
①含有手性碳;②含有三个甲基;③含有苯环。
其中,核磁共振氢谱显示为6组峰,且峰面积比为 的同分异构体的结构简式为 。
【答案】
(1)3-甲基苯酚(间甲基苯酚)
(2)2
(3)氨基 羟基
(4)取代反应
(5)
(6) +H O +HCl+N ↑
2 2
(7) 9
【详解】根据流程,A与2-溴丙烷发生取代反应生成B,B与NaNO 发生反应生成C,C与NH HS反应生
2 4
成D,D与乙酸酐[(CH CO) O]反应生成E,结合E的结构简式和D的分子式可知,D为
3 2
;E与F反应生成G,结合E和G的结构简式和F的分子式可知,F为 ;G发生两步反应生
成H,H再与NaNO /HCl反应生成I,结合I的结构和H的分子式可知,H为
2;I与水反应生成J,J与乙酸酐[(CH CO) O]反应生成K,结合K的结构简式
3 2
和J的分子式可知,J为 ;据此分析解题。
(1)根据有机物A的结构,有机物A的化学名称为3-甲基苯酚(间甲基苯酚)。
(2)有机物C中含有苯环,苯环上的C原子的杂化类型为sp2杂化,还含有甲基和异丙基,甲基和异丙基
上的C原子的杂化类型为sp3杂化,故答案为2种。
(3)根据分析,有机物D的结构为 ,其官能团为氨基和羟基。
(4)有机物E与有机物F发生反应生成有机物G,有机物中的羟基与有机物F中的Cl发生取代反应生成
有机物G,故反应类型为取代反应。
(5)根据分析,有机物F的结构简式为 。
(6)有机物I与水反应生成有机物J,该反应的方程式为 +H O
2
+HCl+N ↑。
2
(7)连有4个不同原子或原子团的碳原子称为手性碳原子。在B的同分异构体中,含有手性碳、含有3个甲基、含有苯环的同分异构体有9种,分别为: 、 、 、 、
、 、 、 、 ;其中,核磁共振氢谱显示
为6组峰,且峰面积比为3:3:3:2:2:1的同分异构体的结构简式为 。
(建议用时:120分钟)
1.(2024·广西·统考模拟预测)英菲替尼(化合物L)是治疗胆管癌的新型药物,其合成路线如下。
回答下列问题:
(1)A的化学名称是 。
(2)由A生成C的反应类型是 。
(3)E的结构简式为 。
(4)由G→J的转化过程可知,G转化为H的目的是(5)符合下列条件的B的同分异构体共有 种,其中一种的结构简式为 。
①分子中含环状结构
②核磁共振氢谱显示2组峰
(6)L中氮原子的杂化方式为 。
(7)1,3-二苯基脲( )是某些药物分子的重要结构单元。参照上述合成路线,写出以苯为
原料制备1,3-二苯基脲的合成路线(无机试剂任选)。
。
【答案】
(1)4-溴硝基苯或对溴硝基苯
(2)取代反应
(3)
(4)保护氨基
(5)4 或 或 或
(6)sp2、sp3
(7)
【详解】由框图可知,A( )与B( )发生取代反应生成C( )和HBr,C与H 发生还原反应,-NO 还原为-NH ,生成D( ),D与E(
2 2 2
)发生取代反应生成F( )和HCl,G( )
与 反应生成H( ),保护-NH ,H与SOCl 发生取代反应生成I(
2 2
),I与KOH反应生成J( ),将-NH 恢复,J与COCl 反应生成K(
2 2
),K与F发生取代反应生成目标产物英菲替尼L( )。
(1)A为 ,名称为4-溴硝基苯或对溴硝基苯;
(2)根据分析,由A生成C的反应类型是取代反应;
(3)根据分析,E的结构简式为 ;(4)根据分析,G转化为H的目的是保护氨基;
(5)B为 ,分子式为C H N,①分子中含环状结构,②核磁共振氢谱显示2组峰说明分子结
6 14 2
构对称性较好,符合条件的同分异构体有 、 、 、 ,共4种;
(6)L中以单键相连的N为sp3杂化,有双键相连的N为sp2杂化;
(7)要合成 ,需要用 和 反应合成, 由
还原得到, 由 与COCl 反应得到,因此合成路线为
2
。
2.(2024·河北·校联考模拟预测)盐酸克林沙星(化合物M)是一种具有杀菌、抑菌作用的药物。M的一种
合成路线如下(部分试剂和条件略去):回答下列问题:
(1)A的化学名称是 。
(2)B→C的反应类型是 。
(3)F中含氧官能团的名称是 。
(4)I的结构简式为 。
(5)K→L的化学方程式为 。
(6)满足下列条件的B的同分异构体有 种;其中核磁共振氢谱显示为三组峰且峰面积比为2:2:1的
同分异构体的结构简式为 。
①具有相同官能团
②苯环上含有三个取代基
(7)4-硝基二苯甲酮( )是一种重要的医药中间体。利用以上合成路线中的相关信息,设计以对硝基甲苯和苯为原料合成 的合成路线 。(用流程图表示,无机试剂任
选)。已知:
【答案】
(1)间氟甲苯
(2)氧化反应
(3)酯基、硝基、酮羰基
(4)
(5) + +HCl
(6)16 、
(7)
【详解】由有机物的转化关系可知,浓硫酸作用下,A( )与浓硝酸发生取代反应生成B(
),B在硫酸作用下与三氧化铬发生氧化反应生成C( ),C与SOCl 发生取代反应生成D( ),D与CH(COOC H) 发生取代反应生成E(
2 2 2 5 2
),E在一定条件下转化为F( ),F在一定条件
下与 反应转化为G( ),G在一定条件下转化为H(
),H在一定条件下发生还原反应生成 ,则I为
;I在一定条件下发生取代反应生成J( ),J在盐
酸溶液中发生水解反应生成K,则K为 ;K与 发生取代反应生成L
( );L经多步转化得到 。
(1)由结构简式可知, 的名称为间氟甲苯;
(2)由分析可知,B→C的反应为 在硫酸作用下与三氧化铬发生氧化反应生成
;(3)由结构简式可知,F的含氧官能团为硝基、酯基和酮羰基;
(4)由分析可知,I的结构简式为 ;
(5)由分析可知,K→L的反应为 与 发生取代反应生成
和HCl,反应的化学方程式为 +
+HCl;
(6)B的同分异构体与B具有相同官能团,苯环上含有三个取代基,说明苯环上的取代基可能为1个-
CHF和2个-NO 或-CHNO 、-F和-NO ,其中取代基为1个-CHF和2个-NO 的结构共有6种,取代基为-
2 2 2 2 2 2 2
CHNO 、-F和-NO 的结构共有10种,则符合条件的结构共有16种;其中核磁共振氢谱显示为三组峰且
2 2 2
峰面积比为2:2:1的同分异构体的结构简式为 、 ;
(7)由有机物的转化关系可知,以对硝基甲苯和苯为原料合成 的合成步骤为
在硫酸作用下与三氧化铬发生氧化反应生成 , 与SOCl 发生取代反应生成
2,氯化铝作用下 与苯发生取代反应生成 ,故合成路线为
。
3.(2024·安徽·统考模拟预测)非天然氨基酸AHPA是一种重要的药物中间体,其合成路线之一如下:
(1)A可由 氧化得到, 的化学名称是 。
(2)C的结构简式为 。
(3)D中手性碳原子数目为 。
(4)E转化为AHPA的反应类型为 。
(5)AHPA中酸性官能团名称为 ,碱性官能团名称为 。
(6)写出同时满足下列条件的AHPA的同分异构体的结构简式 。
①含苯环且苯环只有一个取代基;
②红外光谱显示含氧官能团只有 和 ;
③核磁共振氢谱显示有6组峰,峰面积比为4∶2∶2∶2∶2∶1。(7)参照上述合成路线,设计以苄基氯( )为主要原料制备 的合成路线
(其他原料、试剂任选)。
【答案】
(1)羟基乙酸
(2)
(3)3
(4)加成反应、还原反应
(5)羧基 氨基
(6)
(7)
【详解】
(1) 的化学名称是羟基乙酸。
(2)C的结构简式为 。
(3)D中手性碳原子数目为3,如图 。(4)E转化为AHPA的反应类型为加成反应、还原反应。
(5)AHPA中酸性官能团名称为羧基,碱性官能团名称为氨基。
(6)满足①含苯环且苯环只有一个取代基;
②红外光谱显示含氧官能团只有 和 ;
③核磁共振氢谱显示有6组峰,峰面积比为4∶2∶2∶2∶2∶1,下列条件的AHPA的同分异构体的结构简式
。
(7)苄基氯( )在碱性条件下发生水解反应生成 , 发生催
化氧化生成 , 在碱性条件下和CHON 发生加成反应生成
3 2
, 在碱性条件下加热发生消去反应生成
, 发生加聚反应生成 ,合成路线
。
4.(2024·广西·校联考模拟预测)多环化合物是合成很多药物的中间体,下面是一种多环化合物G的合成
路线:已知:RNH + +2HO
2 2
回答下列问题:
(1)A的分子式为 ,A侧链上的碳原子的杂化类型有 。
(2)由B生成D的反应类型为 。
(3)E中含氧官能团的名称为 ,E→F反应的方程式为 。
(4)C的同分异构体中,同时满足以下两个条件的有 种(考虑碳碳双键的顺反异构)。
ⅰ.除苯环外不含其他的环状结构;
ⅱ.能发生银镜反应。
(5)G的结构简式为 。
(6)结合题中相关信息,设计以 和 为原料制备 的合成路线 (其他无
机试剂任选)。
【答案】
(1)C HON sp、sp2杂化
8 5 2 4
(2)加成反应
(3)酮羰基
(4)6(5)
(6)
【详解】A( )与 在THF、CDI、MgCl 作用下发生取代反应,生成B(
2
)和KHCO ;B与C( )在C HOH/OH-作用下发生加成反应,生成D(
3 2 5
);由D的结构简式、F的分子式,可确定F的结构简式为
;由G的分子式及F的结构简式,可确定G为 。
(1)由分析可知,A的结构简式为 ,则其分子式为:C HON,A侧链上,-CN中的碳原
8 5 2 4
子的价层电子对数为2,发生sp杂化、-COOH中碳原子的价层电子对数为3,发生sp2杂化。
(2)由B( )生成D( )时,B与C( )在
C HOH/OH-作用下发生加成反应。
2 5(3)E的结构简式为 ,含氧官能团的名称为酮羰基。E(
)与H 发生加成反应,生成F( ),反应的方程式为
2
。
(4)C的同分异构体中,同时满足以下两个条件:” i.除苯环外不含其他的环状结构;ii.能发生银镜
反应”的有机物,分子中含有苯环、-CHO、-CH=CH-,可能是苯环上连有1个取代基-CH=CH-CHO(有顺
反异构体,2种)、-C(CHO)=CH ;可能是苯环上连有2个取代基,-CHO、-CH=CH 分别位于苯环的邻、
2 2
间、对位,共3种,所以共有6种(考虑烯烃的立体异构) 。
(5)由分析可知,G的结构简式为 。
(6)以 和 为原料制备 时,需将 转化为
HOCH CH=CHCH OH,也就是应将 与Br 发生1,4-加成,再水解,所以合成路线为
2 2 2
。
5.(2024·贵州·统考模拟预测)化合物J具有多种生物药理活性。某研究小组以植物中提取的对-茴香醛A
和香草醛F为原料合成J,一种合成路线如下(部分反应条件和过程已简化):已知: +
( 为 或烷基)
回答下列问题:
(1)A中的官能团名称是 。
(2) 的结构简式是 。
(3)由 生成 经过①②两步反应,写出第①步反应的化学方程式 。
(4)根据Ⅰ的结构,发生加成反应时,Ⅰ的碳碳双键断裂的是 键(选填“ ”或“ ”)。
(5)根据合成路线,指出 这步反应在合成中的作用是 。
(6)根据化合物 的结构, 不能发生的反应是 (选填“酯化反应”“水解反应”或“消去反应”)。
(7)化合物 有多种同分异构体,满足下列条件的有 种(不考虑立体异构)。
①加入 溶液发生显色反应;
②与 溶液反应有气体放出。
其中,核磁共振氢谱理论上有5组峰,且峰面积之比为 的同分异构体结构简式是 。
【答案】
(1)醚键、醛基(2)
(3) +
(4)
(5)保护酚羟基
(6)水解反应
(7)13
【详解】B与氢气加成反应生成C,结合D的结构,可以判断B中只有碳碳双键与氢气加成,可以得到C
的结构是 ,根据已知信息可以得到G经过①和②生成H的结构为
。
(1)根据A的结构可以得到A中的官能团是醚键、醛基。
(2)结合B与D的结构可以得到B与氢气加成时只有碳碳双键发生加成生成C,所以C的结构是
。
(3)由 生成 经过①②两步反应,根据已知反应可以写出第①步反应的化学方程式为
+ 。(4)由于碳碳双键中的 键不如 稳定,发生加成反应时,Ⅰ的碳碳双键断裂的是 键。
(5)对F、G的结构进行分析, 是F中的酚羟基发生了反应,再结合J的结构左边苯环上原位置的
酚羟基再次出现,所以 这步反应在合成中的作用是保护酚羟基。
(6)根据化合物 的结构,J中含有的官能团是醚键、羰基、酚羟基、醇羟基,所以J可以发生酯化反应
和消去反应,不能发生水解反应。
(7)F的同分异构体满足两个条件:①加入 溶液发生显色反应,说明F中含有酚羟基;②与
溶液反应有气体放出,说明F中含有羧基。F中苯环上可以有两条支链 和 ,两
条支链在苯环上邻、间、对3种结构;F中苯环上还可以有三条支链 、 、 ,苯环上三条
不同支链共有10种结构,所以满足条件的F的同分异构体共有13种。其中,核磁共振氢谱理论上有5组
峰,且峰面积之比为 的同分异构体结构简式是
6.(2024·陕西宝鸡·统考模拟预测)帕罗维德(Paxlovid)是一种有效的新冠病毒抑制剂,可以在病毒感染早
期有效干预抑制病毒复制。下图是合成帕罗韦德的重要中间体之一(I)的合成路线。
请回答下列问题:
(1)A→B的原子利用率100%,A的名称是 ,D的名称是 。
(2)C→D的反应类型 ,E中官能团的名称是 。
(3)F的分子式 。(4)写出G→H转化第一步反应的离子方程式 。
(5)芳香化合物N为I的同分异构体,写出满足下列条件N的结构简式 。
①能与FeCl 溶液发生显色反应;
3
②1mol N最多消耗2mol NaOH;
③磁共振氢谱中有4组峰,其峰面积之比为3:2:2:1;
(6)结合以上流程,设计以乙炔和乙醇为原料制备 的合成路线 (无机试剂任选)。
【答案】
(1)乙炔 2-甲基-1,3-丁二烯
(2)消去反应 碳碳双键、碳氯键
(3)C H O
12 20 2
(4) +2OH- +C HOH+H O
2 5 2
(5)
(6)CH CHOH CHCHO+CH≡CH CHCHOHC≡CCHOHCH
3 2 3 3 3
CHCHOHCH CHCHOHCH
3 2 2 3
【详解】A→B的原子利用率100%,结合B结构可知,A为乙炔CH≡CH,B和氢气加成生成C,结合C
化学式可知,C为 ;C在浓硫酸催化作用下发生消去反应生成D;D和HCl发生加成反应生
成E;E生成F,F被高锰酸钾氧化生成G ;G中酯基水解后酸化得到H,H生成I;
(1)A→B的原子利用率100%,结合B结构可知,A为乙炔CH≡CH;D为 ,名称
是2-甲基-1,3-丁二烯;
(2)C→D的反应类型是消去反应;E中官能团的名称是:碳碳双键、碳氯键;(3)由F结构可知,F分子式为C H O;
12 20 2
(4)G→H转化第一步反应是酯基在碱性溶液中的水解,离子方程式: +2OH-
+C HOH+H O;
2 5 2
(5)I含有7个碳、3个氧,不饱和度为4;芳香化合物N为I的同分异构体,满足下列条件:
①能与 溶液发生显色反应,则含有酚羟基;
②1molN最多消耗 ,则含有2个酚羟基;
③核磁共振氢谱中有4组峰,其峰面积之比为 ,则含有1个甲基且结构对称性较好;其结构可以
为: ;
(6)乙醇氧化为乙醛,乙醛和乙炔发生A生成B的反应得到CHCHOHC≡CCHOHCH ,在和氢气加成得
3 3
到饱和醇CHCHOHCH CHCHOHCH ,故流程为:CHCHOH CHCHO+CH≡CH
3 2 2 3 3 2 3
CHCHOHC≡CCHOHCH CHCHOHCH CHCHOHCH 。
3 3 3 2 2 3
7.(2024·陕西渭南·统考一模)叠氮基和烯烃、炔烃可以在催化剂的作用下发生反应生成杂环,这种反应
广泛应用于药物合成。药物F合成路线如下:
(1)反应①的类型是 ,对有机物A进行系统命名 。流程中有机物 中的官
能团除羟基外,还有 。(2)有机物乙二醇与B能发生缩聚反应得到聚合物M。有关M的说法正确的是___________。
A.蛋白质与M的所含元素相同 B.M与制备PE(聚乙烯)反应类型相同
C.M有固定的熔、沸点 D.M可以被氢气还原
(3)写出有机物C的结构简式 。
(4)写出满足下列条件的化合物B的同分异构体有 种。
a.红外光谱中测出分子中含有一个苯环
b.与碳酸氢钠溶液反应放出二氧化碳
c.能发生银镜反应
(5)写出有机物D与过量NaOH溶液反应的化学方程式 。
(6)THF由C、H、O三种元素组成,称取THF7.200g,使其完全燃烧,将产物依次通过装有无水氯化钙的
干燥管a和装有碱石灰的干燥管b,测得a增重7.200g,b增重17.600g,则THF的最简式为 。
(7)请补充完成以 为原料合成( )的路线 (无机试剂任选)。
(合成路线常用的表示方式为:A B…… 目标产物)
【答案】
(1)加成反应 1,2-二溴乙烷 碳溴键
(2)D
(3)
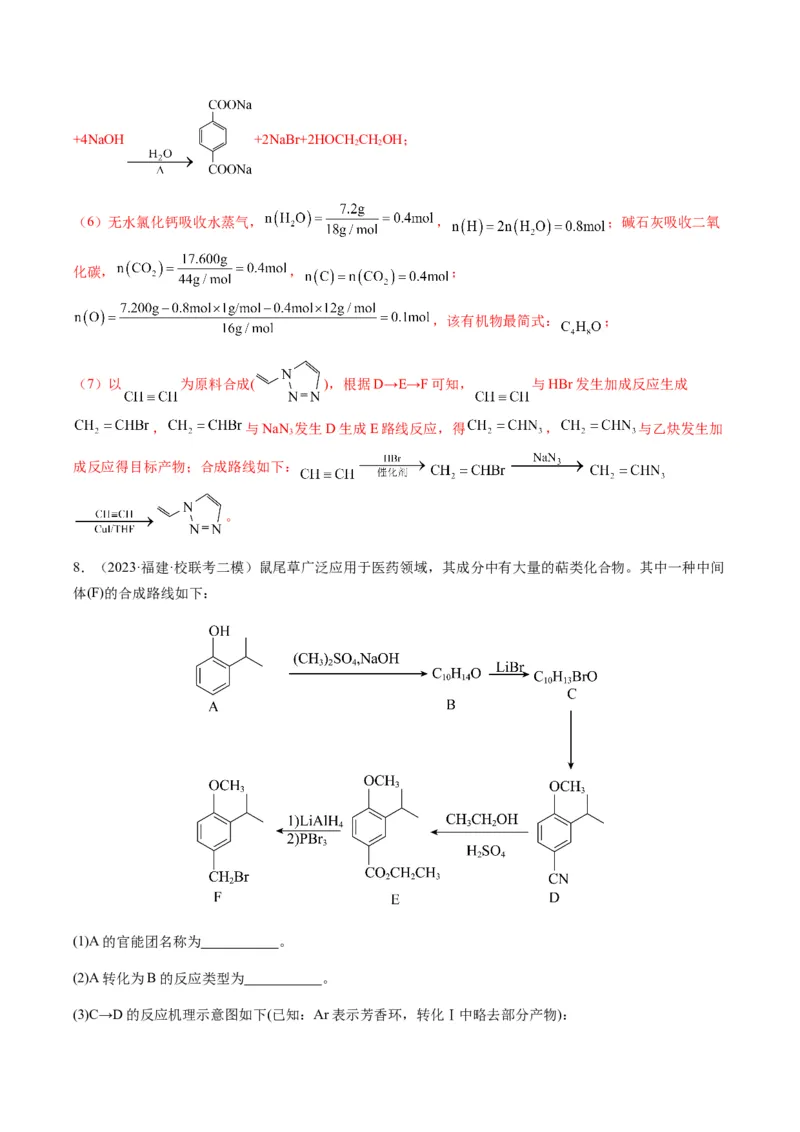
(4)13(5) +4NaOH +2NaBr+2HOCH CHOH;
2 2
(6)
(7)
【详解】
(1)根据分析可知,反应①发生加成反应;物质A结构简式:CHBrCHBr,系统命名:1,2-二溴乙烷;
2 2
有机物 中的官能团除羟基外,还有碳溴键;
(2)A.乙二醇与B能发生缩聚反应得到聚合物M中包含C、H、O元素,而蛋白质中除了C、H、O元
素外还含有N、S等元素,A错误;
B.制备M发生缩聚反应,制备PE(聚乙烯)发生加聚反应,B错误;
C.聚合物M属于混合物,无固定熔沸点,C错误;
D.根据分析可知,聚合物M中含苯环结构,可与氢气发生加成反应,D正确;
答案选D。
(3)根据分析,C为对二苯甲酸甲酯,结构简式: ;
(4)物质B为对二苯甲酸,B的同分异构体满足:
a.红外光谱中测出分子中含有一个苯环;b.与碳酸氢钠溶液反应放出二氧化碳,说明含羧基;c.能发生
银镜反应,说明含醛基或甲酸某酯基;情况如下:①苯环两侧链,一侧链为-COOH,另一侧链为HCOO
-,二者在苯环上具有邻、间、对三种位置关系;②苯环三侧链,一侧链为-COOH,一侧链为-CHO,
一侧链为-OH,苯环上连接3个不同基团,存在10种同分异构体,共计13种;
(5)D中酯基与溴原子均能与NaOH发生反应,则D与过量NaOH反应方程式:+4NaOH +2NaBr+2HOCH CHOH;
2 2
(6)无水氯化钙吸收水蒸气, , ;碱石灰吸收二氧
化碳, , ;
,该有机物最简式: ;
(7)以 为原料合成( ),根据D→E→F可知, 与HBr发生加成反应生成
, 与NaN 发生D生成E路线反应,得 , 与乙炔发生加
3
成反应得目标产物;合成路线如下:
。
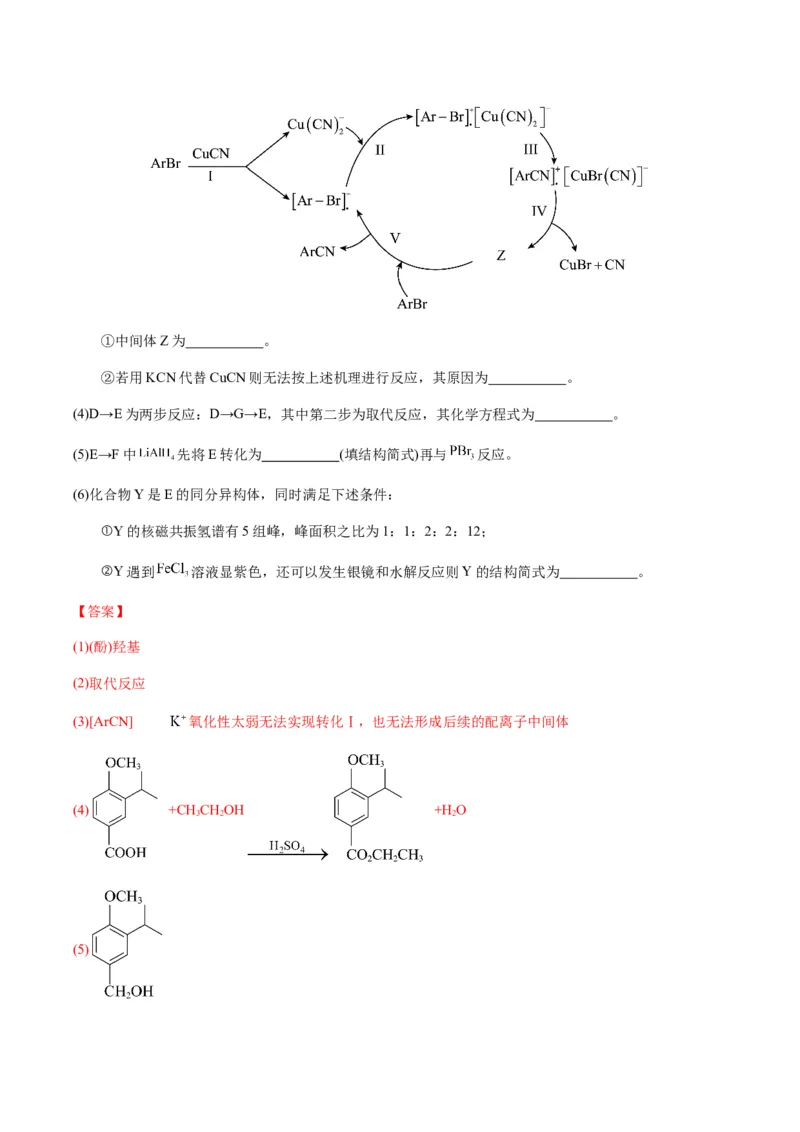
8.(2023·福建·校联考二模)鼠尾草广泛应用于医药领域,其成分中有大量的萜类化合物。其中一种中间
体(F)的合成路线如下:
(1)A的官能团名称为 。
(2)A转化为B的反应类型为 。
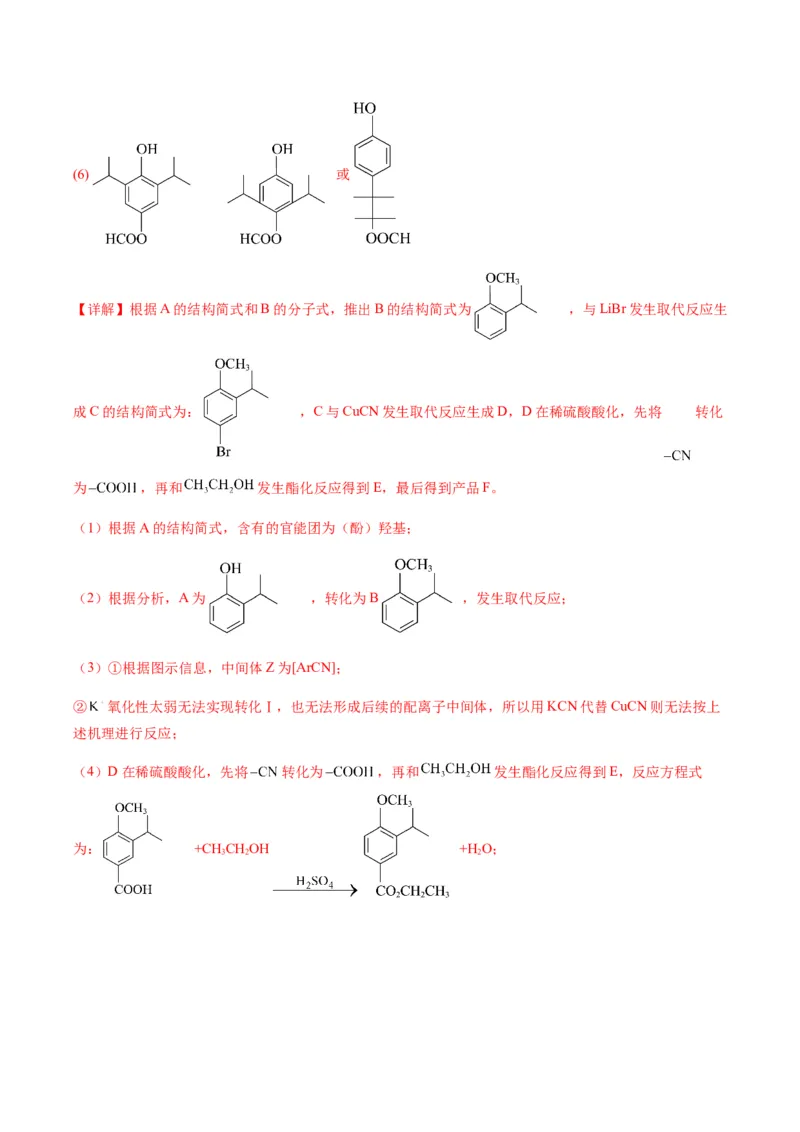
(3)C→D的反应机理示意图如下(已知:Ar表示芳香环,转化Ⅰ中略去部分产物):①中间体Z为 。
②若用KCN代替CuCN则无法按上述机理进行反应,其原因为 。
(4)D→E为两步反应:D→G→E,其中第二步为取代反应,其化学方程式为 。
(5)E→F中 先将E转化为 (填结构简式)再与 反应。
(6)化合物Y是E的同分异构体,同时满足下述条件:
①Y的核磁共振氢谱有5组峰,峰面积之比为1:1:2:2:12;
②Y遇到 溶液显紫色,还可以发生银镜和水解反应则Y的结构简式为 。
【答案】
(1)(酚)羟基
(2)取代反应
(3)[ArCN] 氧化性太弱无法实现转化Ⅰ,也无法形成后续的配离子中间体
(4) +CH CHOH +H O
3 2 2
(5)(6) 或
【详解】根据A的结构简式和B的分子式,推出B的结构简式为 ,与LiBr发生取代反应生
成C的结构简式为: ,C与CuCN发生取代反应生成D,D在稀硫酸酸化,先将 转化
为 ,再和 发生酯化反应得到E,最后得到产品F。
(1)根据A的结构简式,含有的官能团为(酚)羟基;
(2)根据分析,A为 ,转化为B ,发生取代反应;
(3)①根据图示信息,中间体Z为[ArCN];
② 氧化性太弱无法实现转化Ⅰ,也无法形成后续的配离子中间体,所以用KCN代替CuCN则无法按上
述机理进行反应;
(4)D在稀硫酸酸化,先将 转化为 ,再和 发生酯化反应得到E,反应方程式
为: +CH CHOH +H O;
3 2 2(5)E→F中 先将E转化为 ,再与 发生取代反应得到产品F;
(6)Y遇到 溶液显紫色,含有酚羟基,还可以发生银镜和水解反,含有 ,Y的核磁共振氢
谱有5组峰,峰面积之比为1:1:2:2:12,Y的结构简式为:
或 。
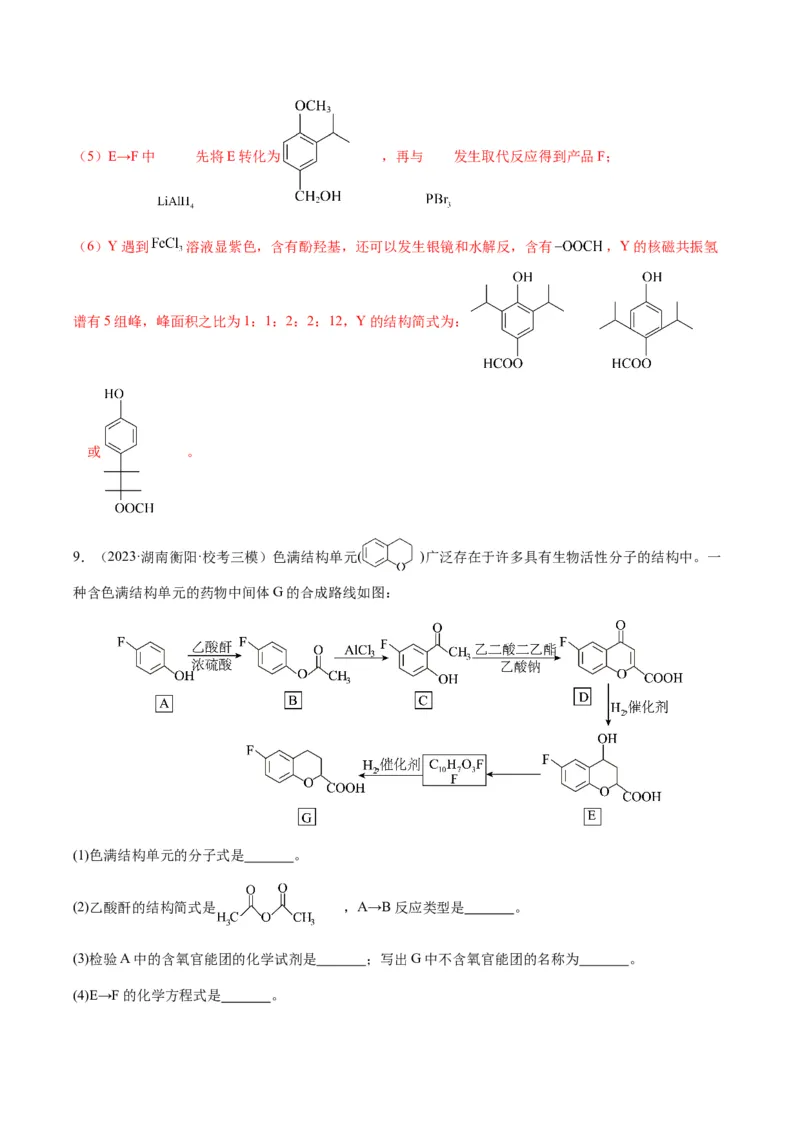
9.(2023·湖南衡阳·校考三模)色满结构单元( )广泛存在于许多具有生物活性分子的结构中。一
种含色满结构单元的药物中间体G的合成路线如图:
(1)色满结构单元的分子式是 。
(2)乙酸酐的结构简式是 ,A→B反应类型是 。
(3)检验A中的含氧官能团的化学试剂是 ;写出G中不含氧官能团的名称为 。
(4)E→F的化学方程式是 。(5)乙二酸二乙酯由乙二酸和乙醇反应制得,乙二酸二乙酯的结构简式是 。M是乙二酸二乙酯的同
分异构体,满足下列两种条件的M的结构简式有 种。
①1 mol M能与足量 反应放出
②含有甲基
(6)设计以 为原料制备 的合成路线 (无机试剂任选)。
【答案】
(1)C H O
9 10
(2)取代反应
(3)FeCl 溶液 碳氟键
3
(4) +H O
2
(5) 8
(6)
【详解】A中酚羟基和乙酸酐发生取代反应生成B和CHCOOH,B发生异构化生成C,C和乙二酸二乙酯
3
发生反应生成D,D与氢气发生加成反应(或还原反应)生成E,对比E、G的结构简式,结合F的分子式
知,E发生消去反应生成F为 ,(6) 发生B→C的转化生成
, 和氢气发生加成反应生成 ,和溴发生取代反应生成 ,据此分析解题。
(1)色满结构单元( )的分子式是C H O,故答案为:C H O;
9 10 9 10
(2)乙酸酐的结构简式是 ,A中酚羟基上的氢原子被 替代生成
B,A→B反应类型是取代反应,故答案为:取代反应;
(3)由题干流程图中A、G的结构简式可知,化合物A中酚羟基与FeCl 溶液作用显紫色,可以检验酚羟
3
基的存在;化合物G中不含氧官能团是碳氟键,故答案为:FeCl 溶液;碳氟键;
3
(4)由题干流程图中E、F的结构简式可知,E→F的化学方程式是
+H O ,故答案为: +H O ;
2 2
(5)乙二酸二乙酯由乙二酸和乙醇反应制得,乙二酸二乙酯的结构简式是 ;M是
乙二酸二乙酯的同分异构体,M的结构简式满足下列条件:①1molM能与足量NaHCO 反应放出
3
2molCO ,说明含有2个-COOH;②含有甲基,符合条件的结构简式有:CHCHCHCH(COOH) 、
2 3 2 2 2
CHCHCH(COOH)CH COOH、CHCH(COOH)CH CHCOOH、(CH)CHCH(COOH) 、
3 2 2 3 2 2 3 2 2
(CH)C(COOH)CH COOH、CHCH(CH COOH)、CHCH(COOH)CH(COOH)CH 、CHCHC(COOH)CH
3 2 2 3 2 2 3 3 3 2 2 3
等8种,故答案为: ;8;
(6) 发生B→C的转化生成 , 和氢气发生加成反
应生成 , 和溴发生取代反应生成 ,合成路线为
,故答案为:
。
10.(2023·江苏南京·校联考一模)化合物F是有机合成的中间体,其合成路线流程图如图:
(1)化合物E中采取sp3和sp2杂化的碳原子个数比为 。
(2)B→C的反应类型为 。
(3)化合物D的分子式为C H O,写出D的结构简式 。
10 14 2
(4)B和乙醇反应的产物为G(C H O),写出满足下列条件G的一种同分异构体的结构简式 。
11 12 3
①不能发生银镜反应,水解产物之一遇FeCl 溶液显紫色
3
②分子中有4种不同化学环境的氢
(5)已知: 。以 和丙二酸
[CH(COOH) ]为原料制备化合物 ,写出相应的合成路线流程图。
2 2
(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
【答案】
(1)3:7(2)还原反应
(3)
(4)
(5)
【详解】A发生取代反应引入支链生成B,B发生还原反应羧基转化为羟基生成C,D发生氧化反应羟基
转化为醛基生成E,根据C、E结构简式,结合化合物D的分子式为C H O,则C中酚羟基发生取代反
10 14 2
应引入甲基生成D,D为 ;E发生一系列反应生成F;
(1)苯环中碳为sp2杂化、醛基碳为sp2杂化,饱和碳原子为sp3杂化,化合物E中采取sp3和sp2杂化的碳
原子个数比为3:7;
(2)B发生还原反应羧基转化为羟基生成C,为还原反应;
(3)由分析可知,D为 ;
(4)B中含有羧基,和乙醇反应的产物为G(C H O),G为酸和醇生成的酯;满足下列条件G的一种同
11 12 3
分异构体:①不能发生银镜反应,水解产物之一遇FeCl 溶液显紫色,则不含醛基,含有酯基且水解能生
3
成酚羟基;②分子中有4种不同化学环境的氢,分子结构较为对称;则可以为:
;
(5) 发生消去反应引入碳碳双键,然后双键发生已知反应氧化为醛基,醛基发
生A生成B的反应引入支链得打羧基,还原羧基为羟基,羟基氧化为醛基:。