文档内容
专项训练 陌生氧化还原反应方程式的书写
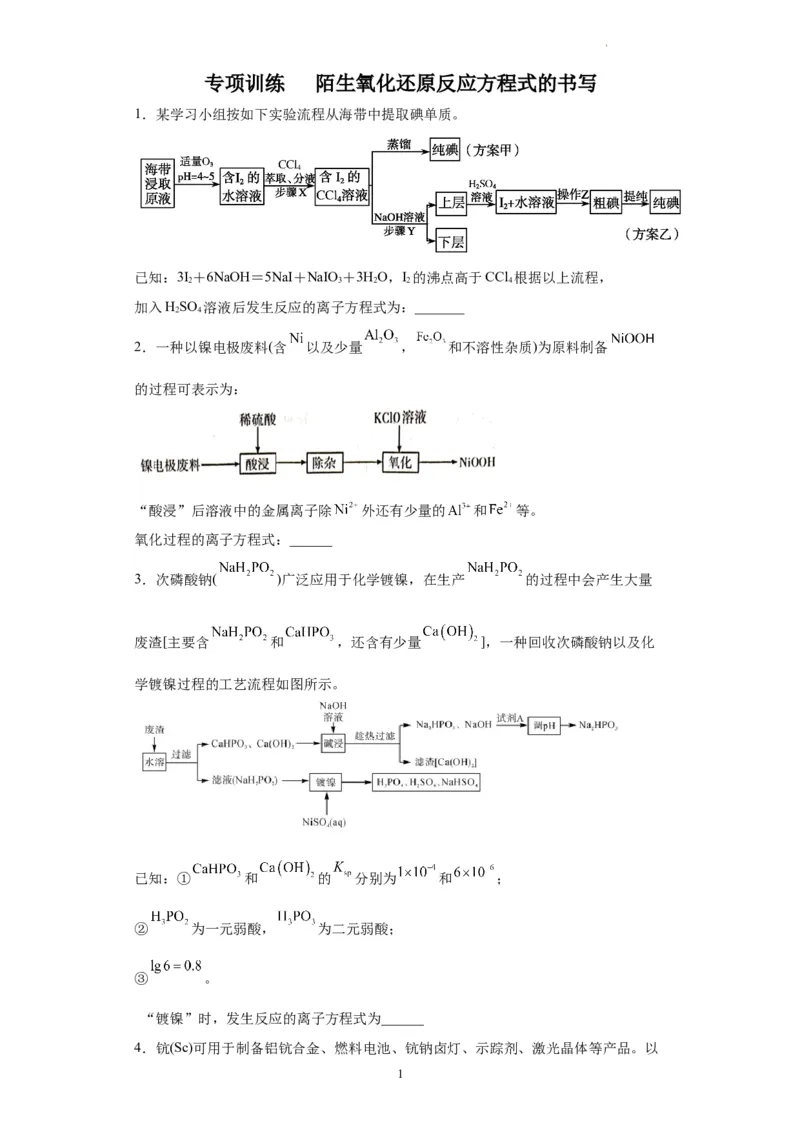
1.某学习小组按如下实验流程从海带中提取碘单质。
已知:3I+6NaOH=5NaI+NaIO +3HO,I 的沸点高于CCl 根据以上流程,
2 3 2 2 4
加入HSO 溶液后发生反应的离子方程式为:_______
2 4
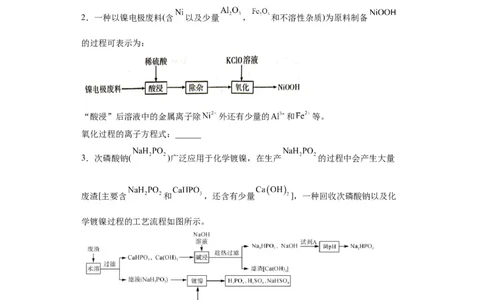
2.一种以镍电极废料(含 以及少量 , 和不溶性杂质)为原料制备
的过程可表示为:
“酸浸”后溶液中的金属离子除 外还有少量的 和 等。
氧化过程的离子方程式:______
3.次磷酸钠( )广泛应用于化学镀镍,在生产 的过程中会产生大量
废渣[主要含 和 ,还含有少量 ],一种回收次磷酸钠以及化
学镀镍过程的工艺流程如图所示。
已知:① 和 的 分别为 和 ;
② 为一元弱酸, 为二元弱酸;
③ 。
“镀镍”时,发生反应的离子方程式为______
4.钪(Sc)可用于制备铝钪合金、燃料电池、钪钠卤灯、示踪剂、激光晶体等产品。以
1
学科网(北京)股份有限公司钛白酸性废水(主要含 、 、 )为原料制备氧化钪( )的工艺流程如下。下
列说法正确的是
草酸钪焙烧时反应的化学方程式:______
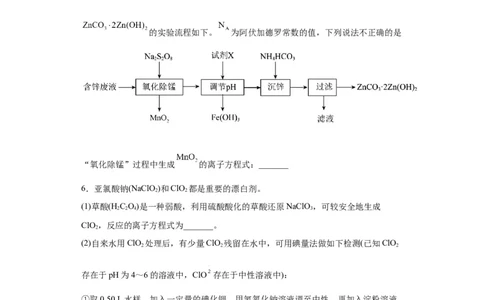
5.以含锌废液(主要成分为 ,含少量的 、 )为原料制备
的实验流程如下。 为阿伏加德罗常数的值,下列说法不正确的是
“氧化除锰”过程中生成 的离子方程式:_______
6.亚氯酸钠(NaClO)和ClO 都是重要的漂白剂。
2 2
(1)草酸(H C O)是一种弱酸,利用硫酸酸化的草酸还原NaClO,可较安全地生成
2 2 4 3
ClO ,反应的离子方程式为_______。
2
(2)自来水用ClO 处理后,有少量ClO 残留在水中,可用碘量法做如下检测(已知ClO
2 2 2
存在于pH为4~6的溶液中,ClO 存在于中性溶液中):
①取0.50 L水样,加入一定量的碘化钾,用氢氧化钠溶液调至中性,再加入淀粉溶液,
溶液变蓝。写出ClO 与碘化钾反应的化学方程式:_______。
2
②已知:2NaSO+I =Na SO+2NaI,向①所得溶液中滴加5.00×10-4 mol·L-1的NaSO
2 2 3 2 2 4 6 2 2 3
溶液至恰好反应,消耗NaSO 溶液20.00 mL。
2 2 3
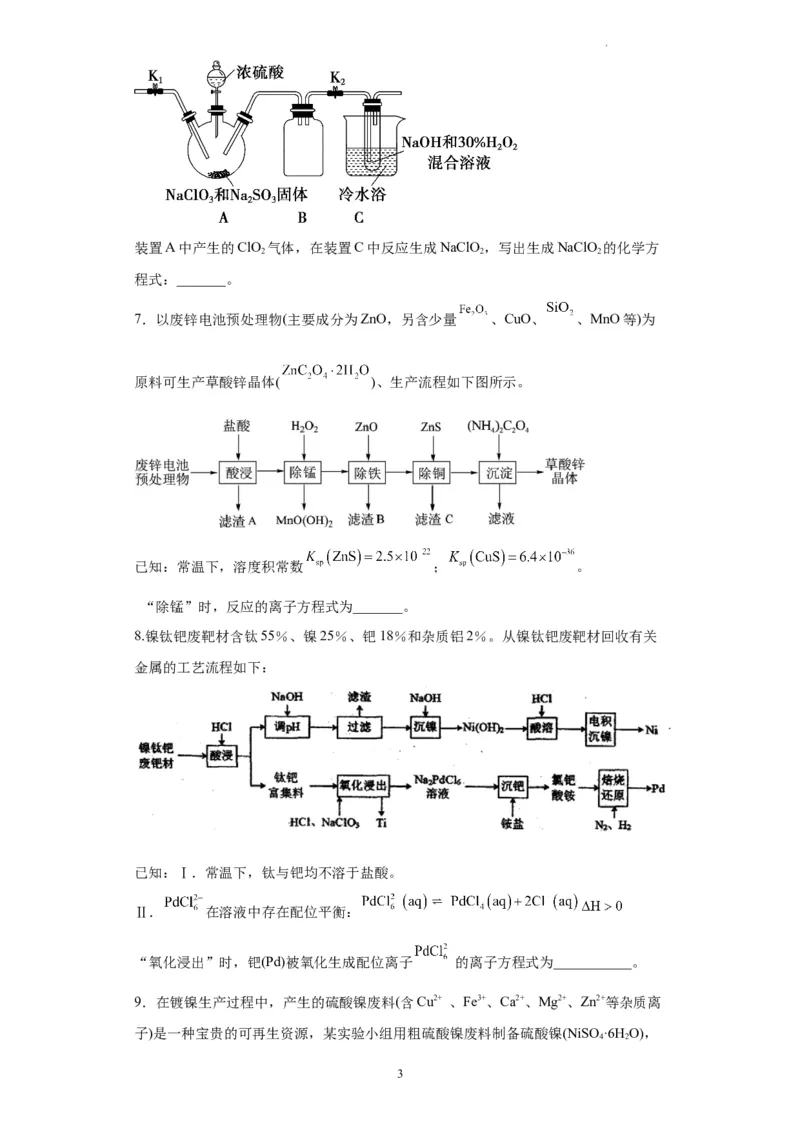
(3)某学习小组设计如下装置制取亚氯酸钠(NaClO)。
2
试卷第2页,共8页装置A中产生的ClO 气体,在装置C中反应生成NaClO,写出生成NaClO 的化学方
2 2 2
程式:_______。
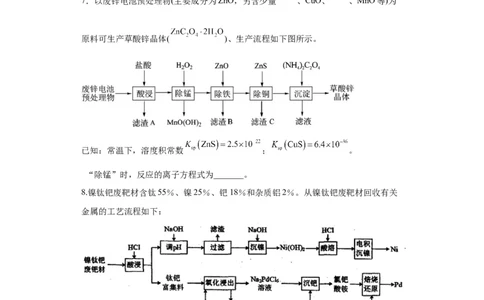
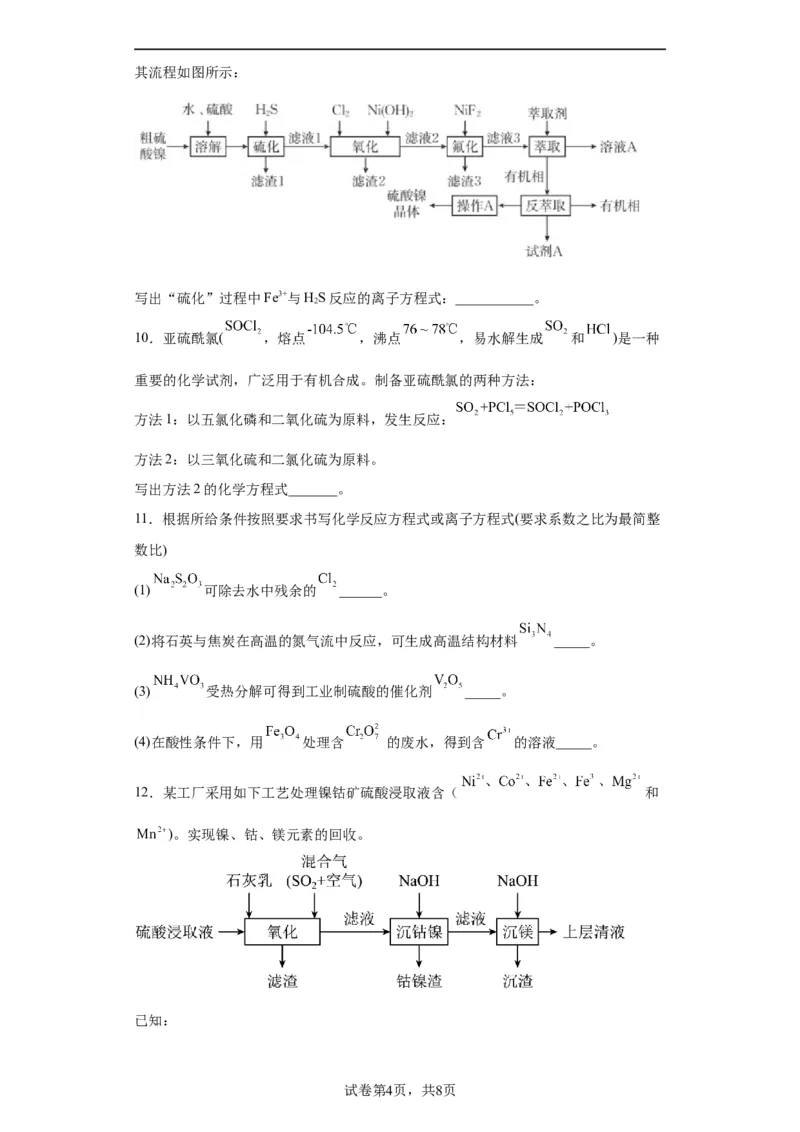
7.以废锌电池预处理物(主要成分为ZnO,另含少量 、CuO、 、MnO等)为
原料可生产草酸锌晶体( )、生产流程如下图所示。
已知:常温下,溶度积常数 ; 。
“除锰”时,反应的离子方程式为_______。
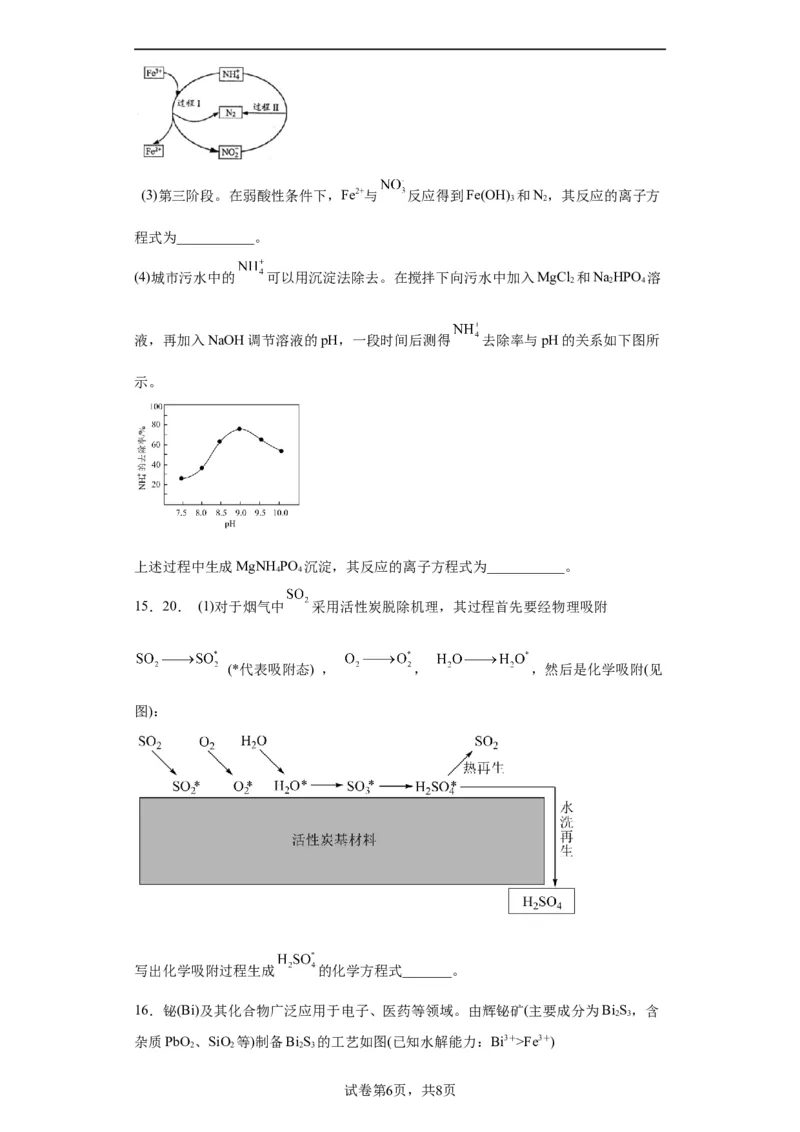
8.镍钛钯废靶材含钛55%、镍25%、钯18%和杂质铝2%。从镍钛钯废靶材回收有关
金属的工艺流程如下:
已知:Ⅰ.常温下,钛与钯均不溶于盐酸。
Ⅱ. 在溶液中存在配位平衡:
“氧化浸出”时,钯(Pd)被氧化生成配位离子 的离子方程式为___________。
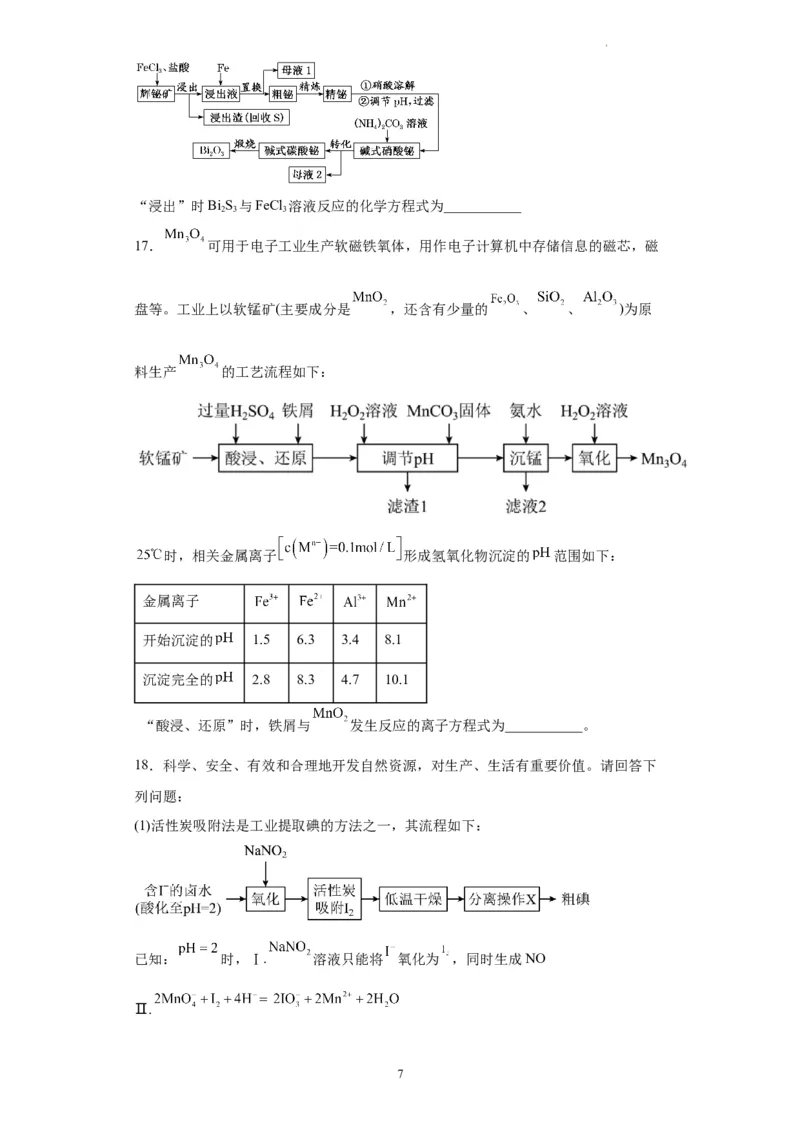
9.在镀镍生产过程中,产生的硫酸镍废料(含Cu2+ 、Fe3+、Ca2+、Mg2+、Zn2+等杂质离
子)是一种宝贵的可再生资源,某实验小组用粗硫酸镍废料制备硫酸镍(NiSO ·6H O),
4 2
3
学科网(北京)股份有限公司其流程如图所示:
写出“硫化”过程中Fe3+与HS反应的离子方程式:___________。
2
10.亚硫酰氯( ,熔点 ,沸点 ,易水解生成 和 )是一种
重要的化学试剂,广泛用于有机合成。制备亚硫酰氯的两种方法:
方法1:以五氯化磷和二氧化硫为原料,发生反应:
方法2:以三氧化硫和二氯化硫为原料。
写出方法2的化学方程式_______。
11.根据所给条件按照要求书写化学反应方程式或离子方程式(要求系数之比为最简整
数比)
(1) 可除去水中残余的 ______。
(2)将石英与焦炭在高温的氮气流中反应,可生成高温结构材料 _____。
(3) 受热分解可得到工业制硫酸的催化剂 _____。
(4)在酸性条件下,用 处理含 的废水,得到含 的溶液_____。
12.某工厂采用如下工艺处理镍钴矿硫酸浸取液含( 和
)。实现镍、钴、镁元素的回收。
已知:
试卷第4页,共8页物质
回答下列问题:
(1)“氧化”中,用石灰乳调节 , 被 氧化为 ,该反应的离子方
程式为_______( 的电离第一步完全,第二步微弱)
(2)“沉钴镍”中得到的 (Ⅱ)在空气中可被氧化成 ,该反应的化学方程式为
_______。
13.铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为
铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:
已知:最高价铬酸根在酸性介质中以Cr O 存在,在碱性介质中以CrO 存在。
2
“还原”步骤中加入焦亚硫酸钠(Na SO)溶液,反应的离子方程式为___________。
2 2 5
14.城市污水中含有一定量的 、 、 等,可以通过如下三个阶段协同作用
实现自养脱氮。
(1)第一阶段。向污水中加入菌体和FeCl 溶液,控制温度和pH,繁殖菌体并进行富集。
3
(2)第二阶段。在菌体的作用下依次发生过程I、过程II,从而实现 、 的脱除,
其过程如下图所示。
5
学科网(北京)股份有限公司(3)第三阶段。在弱酸性条件下,Fe2+与 反应得到Fe(OH) 和N,其反应的离子方
3 2
程式为___________。
(4)城市污水中的 可以用沉淀法除去。在搅拌下向污水中加入MgCl 和NaHPO 溶
2 2 4
液,再加入NaOH调节溶液的pH,一段时间后测得 去除率与pH的关系如下图所
示。
上述过程中生成MgNH PO 沉淀,其反应的离子方程式为___________。
4 4
15.20. (1)对于烟气中 采用活性炭脱除机理,其过程首先要经物理吸附
(*代表吸附态) , , ,然后是化学吸附(见
图):
写出化学吸附过程生成 的化学方程式_______。
16.铋(Bi)及其化合物广泛应用于电子、医药等领域。由辉铋矿(主要成分为BiS,含
2 3
杂质PbO 、SiO 等)制备BiS 的工艺如图(已知水解能力:Bi3+>Fe3+)
2 2 2 3
试卷第6页,共8页“浸出”时BiS 与FeCl 溶液反应的化学方程式为___________
2 3 3
17. 可用于电子工业生产软磁铁氧体,用作电子计算机中存储信息的磁芯,磁
盘等。工业上以软锰矿(主要成分是 ,还含有少量的 、 、 )为原
料生产 的工艺流程如下:
时,相关金属离子 形成氢氧化物沉淀的 范围如下:
金属离子
开始沉淀的 1.5 6.3 3.4 8.1
沉淀完全的 2.8 8.3 4.7 10.1
“酸浸、还原”时,铁屑与 发生反应的离子方程式为___________。
18.科学、安全、有效和合理地开发自然资源,对生产、生活有重要价值。请回答下
列问题:
(1)活性炭吸附法是工业提取碘的方法之一,其流程如下:
已知: 时,Ⅰ. 溶液只能将 氧化为 ,同时生成NO
Ⅱ.
7
学科网(北京)股份有限公司①氧化过程的离子方程式为___________。活性炭上吸附的 还能用浓 溶液吸
收,每吸收 转移5mol电子,该反应的离子方程式是___________。
(2)以金红石(主要成分为 )为原料,制取Ti的工艺流程如图所示:
①Ⅰ在高温条件下进行,产物中有一种可燃性无色气体。Ⅰ中反应的化学方程式为
___________。
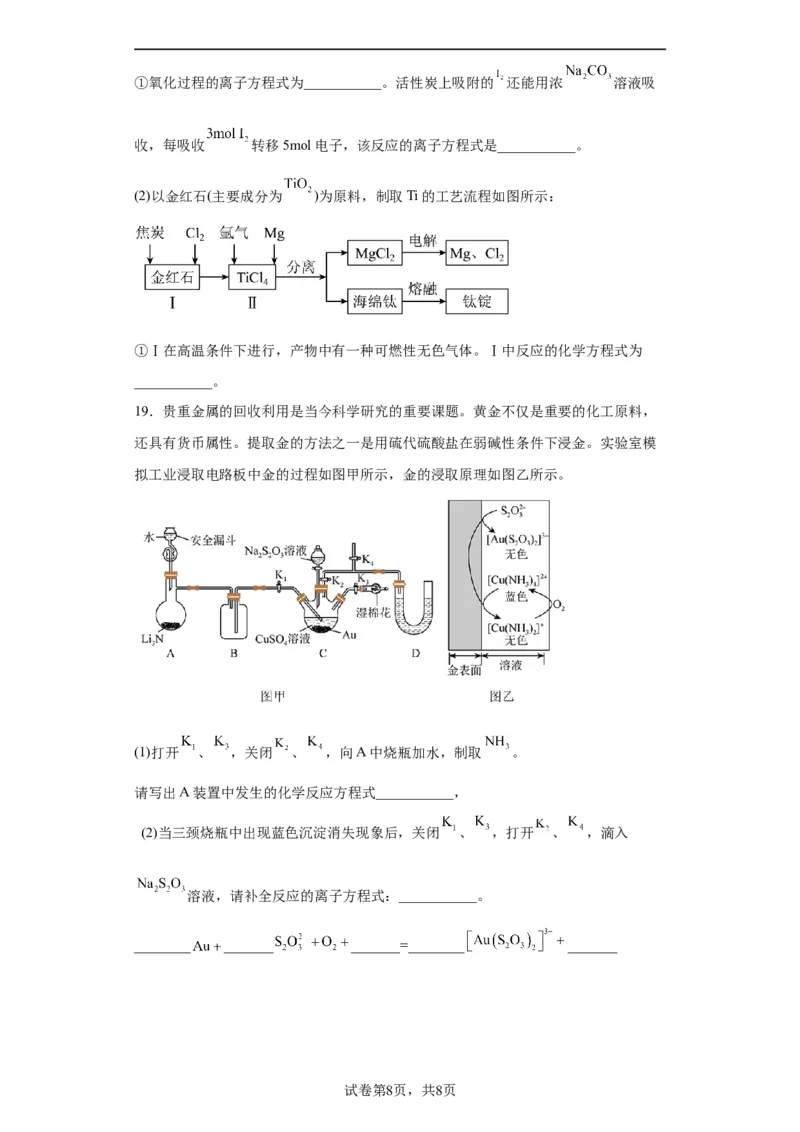
19.贵重金属的回收利用是当今科学研究的重要课题。黄金不仅是重要的化工原料,
还具有货币属性。提取金的方法之一是用硫代硫酸盐在弱碱性条件下浸金。实验室模
拟工业浸取电路板中金的过程如图甲所示,金的浸取原理如图乙所示。
(1)打开 、 ,关闭 、 ,向A中烧瓶加水,制取 。
请写出A装置中发生的化学反应方程式___________,
(2)当三颈烧瓶中出现蓝色沉淀消失现象后,关闭 、 ,打开 、 ,滴入
溶液,请补全反应的离子方程式:___________。
________ _______ _______=________ _______
试卷第8页,共8页