文档内容
高考热点专项 物质能量、能垒变化图像分析
目录
01考情透视·目标导航............................................................................................................................
02知识导图·思维引航............................................................................................................................
03核心精讲·题型突破............................................................................................................................
【真题研析】.............................................................................
【核心精讲】.............................................................................
1.催化机理..............................................................................
2.催化剂的特征..........................................................................
3.过渡态理论............................................................................
4.能垒与决速步..........................................................................
【命题预测】.............................................................................
考向1催化机理能垒图.....................................................................
考向2 能垒与连续反应....................................................................
考点要求 考题统计 考情分析
2024·甘肃卷,10,3分;
采用“图示+文字”形式,一般为能量反应过程的分
2024· 贵州卷,14,3分;
析,通过分析能垒变化图象中的化学键和能量变
2024·河北卷,14,3分;
化,掌握从宏观和微观两个角度进行问题探究的能
能垒变 2023•浙江省1月选考,14,
力,培养宏观辨识与微观探析的核心素养。预计
化图 3分;2022•湖南选择性卷,
2025命题形式比较新颖,以图像为载体,以陌生的
12;2022·浙江省1月卷,
反应历程方程式或示意图为主要信息源,高起点,
18,2分;2022•湖南选择性
低落点,从微观视角来考查能量变化
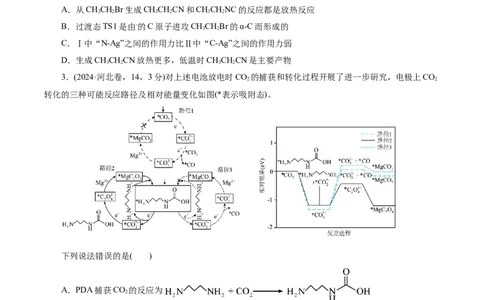
卷,12,3分1.(2024·甘肃卷,10,3分)甲烷在某含Mo催化剂作用下部分反应的能量变化如图所示,下列说法错
误的是( )
A.E=1.41eV B.步骤2逆向反应的ΔH=+0.29eV
2
C.步骤1的反应比步骤2快 D.该过程实现了甲烷的氧化
2.(2024· 贵州卷,14,3分)AgCN与CHCHBr可发生取代反应,反应过程中 的C原子和N原子
3 2
均可进攻CHCHBr,分别生成腈(CHCHCN)和异腈(CHCHNC)两种产物。通过量子化学计算得到的反应
3 2 3 2 3 2
历程及能量变化如图(TS为过渡态,Ⅰ、Ⅱ为后续物)。由图示信息,下列说法错误的是( )
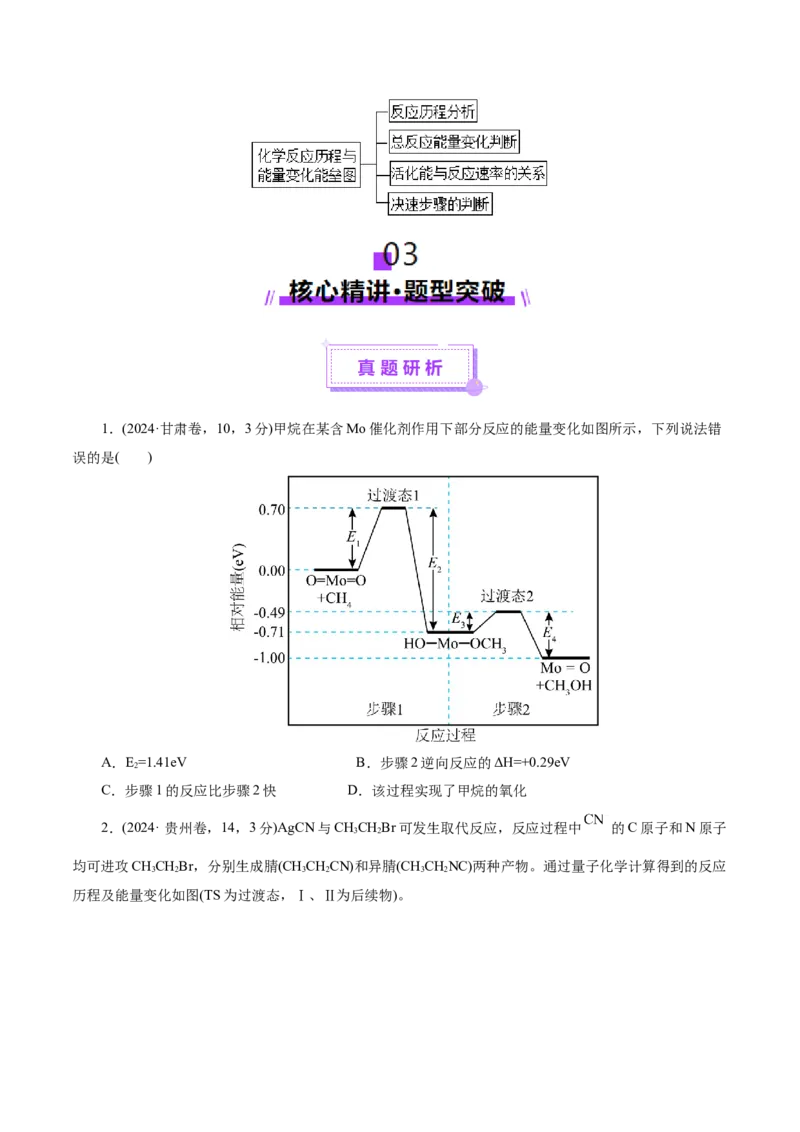
A.从CHCHBr生成CHCHCN和CHCHNC的反应都是放热反应
3 2 3 2 3 2
B.过渡态TS1是由-的C原子进攻CHCHBr的α-C而形成的
3 2
C.Ⅰ中“N-Ag”之间的作用力比Ⅱ中“C-Ag”之间的作用力弱
D.生成CHCHCN放热更多,低温时CHCHCN是主要产物
3 2 3 2
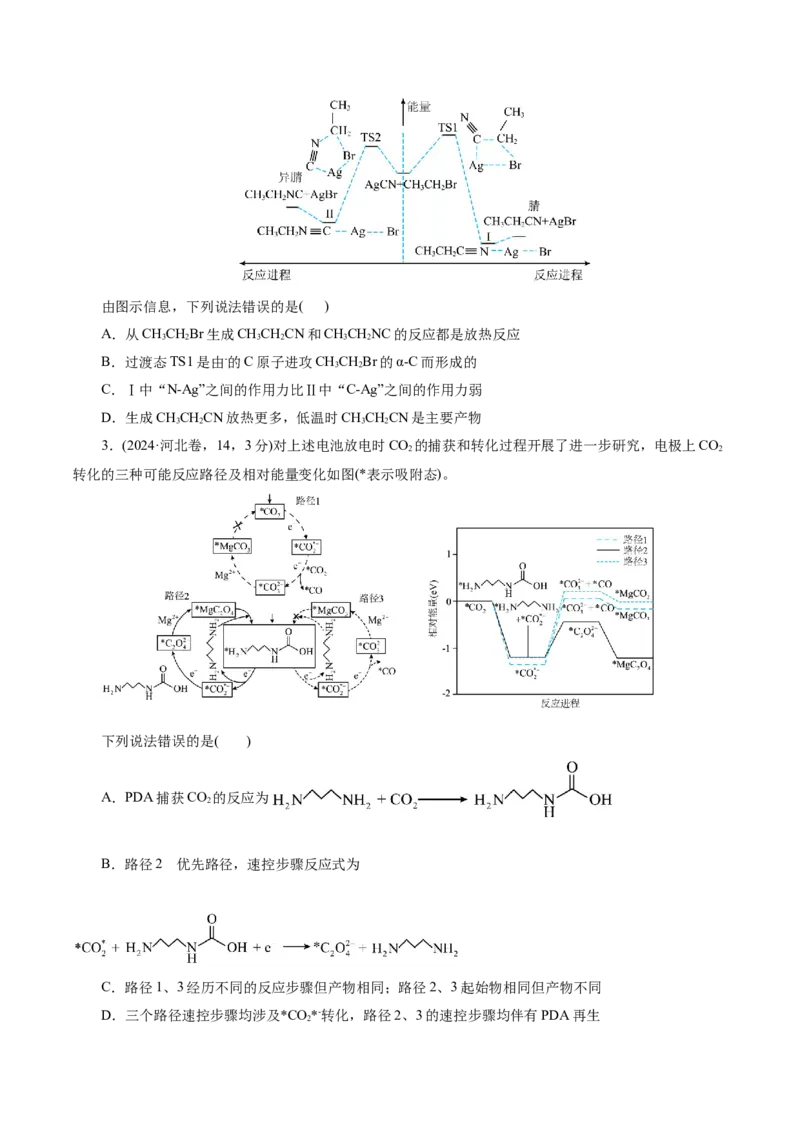
3.(2024·河北卷,14,3分)对上述电池放电时CO 的捕获和转化过程开展了进一步研究,电极上CO
2 2
转化的三种可能反应路径及相对能量变化如图(*表示吸附态)。
下列说法错误的是( )
A.PDA捕获CO 的反应为
2
是
B.路径2 优先路径,速控步骤反应式为
C.路径1、3经历不同的反应步骤但产物相同;路径2、3起始物相同但产物不同
D.三个路径速控步骤均涉及*CO*-转化,路径2、3的速控步骤均伴有PDA再生
24.(2023•浙江省1月选考,14)标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下
[已知O(g)和Cl(g)的相对能量为0],下列说法不正确的是 ( )
2 2
A.E-E=E-E
6 3 5 2
B.可计算Cl-Cl键能为2(E-E)kJ•mol-1
2 3
C.相同条件下,O 的平衡转化率:历程II>历程I
3
D.历程I、历程II中速率最快的一步反应的热化学方程式为:ClO(g)+O(g)=O (g)+Cl(g) ∆H=(E-
2 5
E)kJ•mol-1
4
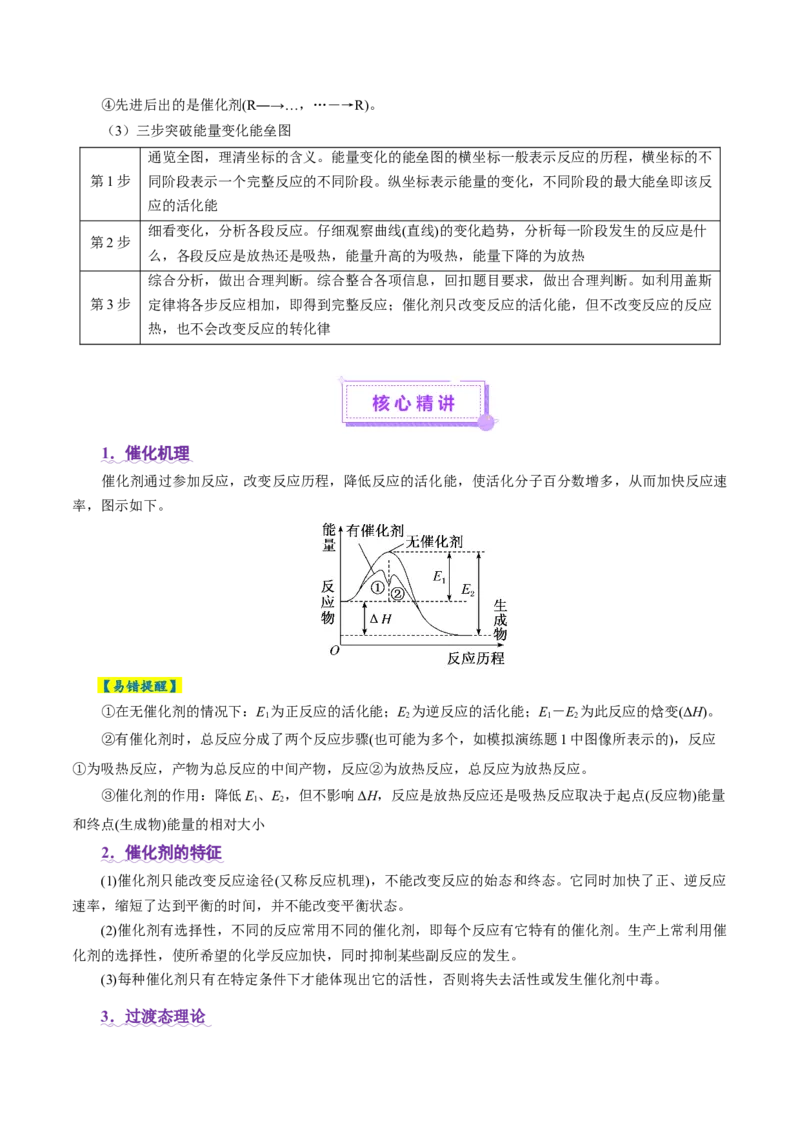
5.(2023·广东卷,15,3分)催化剂Ⅰ和Ⅱ均能催化反应R(g) P(g)。反应历程(下图)中,M为中
间产物。其他条件相同时,下列说法不正确的是( )
A.使用Ⅰ和Ⅱ,反应历程都分4步进行
B.反应达平衡时,升高温度,R的浓度增大
C.使用Ⅱ时,反应体系更快达到平衡
D.使用Ⅰ时,反应过程中M所能达到的最高浓度更大
或
(1)反应历程中化学键的变化
在反应中,旧键断裂与新键形成是同时进行的,形成中间过渡态。
(2)反应历程中物质的变化
①只进不出的是反应物(A―→…);
②只出不进的是产物(…―→M);
③先出后进的是中间体(…―→X,X―→…);④先进后出的是催化剂(R―→…,…―→R)。
(3)三步突破能量变化能垒图
通览全图,理清坐标的含义。能量变化的能垒图的横坐标一般表示反应的历程,横坐标的不
第1步 同阶段表示一个完整反应的不同阶段。纵坐标表示能量的变化,不同阶段的最大能垒即该反
应的活化能
细看变化,分析各段反应。仔细观察曲线(直线)的变化趋势,分析每一阶段发生的反应是什
第2步
么,各段反应是放热还是吸热,能量升高的为吸热,能量下降的为放热
综合分析,做出合理判断。综合整合各项信息,回扣题目要求,做出合理判断。如利用盖斯
第3步 定律将各步反应相加,即得到完整反应;催化剂只改变反应的活化能,但不改变反应的反应
热,也不会改变反应的转化律
1 . 催化机理
催化剂通过参加反应,改变反应历程,降低反应的活化能,使活化分子百分数增多,从而加快反应速
率,图示如下。
【易错提醒】
①在无催化剂的情况下:E 为正反应的活化能;E 为逆反应的活化能;E-E 为此反应的焓变(ΔH)。
1 2 1 2
②有催化剂时,总反应分成了两个反应步骤(也可能为多个,如模拟演练题1中图像所表示的),反应
①为吸热反应,产物为总反应的中间产物,反应②为放热反应,总反应为放热反应。
③催化剂的作用:降低E、E,但不影响ΔH,反应是放热反应还是吸热反应取决于起点(反应物)能量
1 2
和终点(生成物)能量的相对大小
2 . 催化剂的特征
(1)催化剂只能改变反应途径(又称反应机理),不能改变反应的始态和终态。它同时加快了正、逆反应
速率,缩短了达到平衡的时间,并不能改变平衡状态。
(2)催化剂有选择性,不同的反应常用不同的催化剂,即每个反应有它特有的催化剂。生产上常利用催
化剂的选择性,使所希望的化学反应加快,同时抑制某些副反应的发生。
(3)每种催化剂只有在特定条件下才能体现出它的活性,否则将失去活性或发生催化剂中毒。
3 . 过渡态理论【名师提醒】
①该反应的反应物为A、B,中间体为C,生成物为D。
②由A、B生成C的反应为吸热反应,由C生成D的反应为放热反应,总反应为放热反应。
③第一步为慢反应,第二步为快反应,决定总反应快慢的是第一步反应。
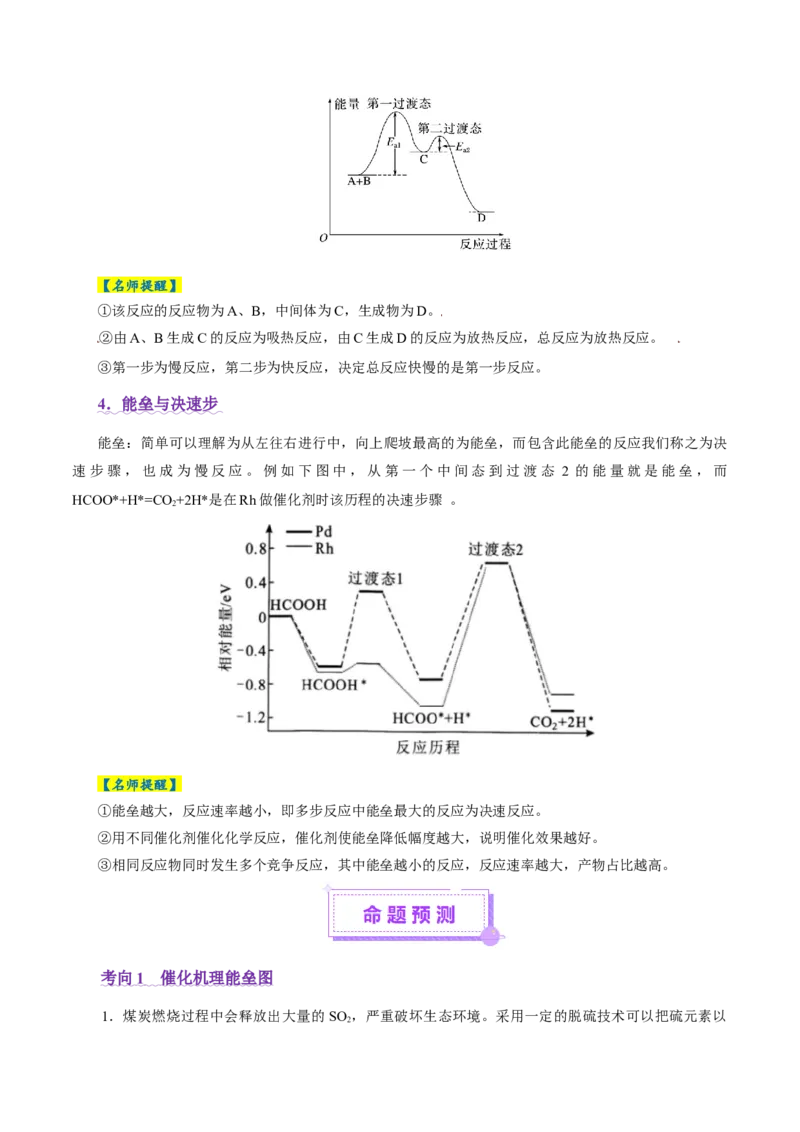
4 .能垒与决速步
能垒:简单可以理解为从左往右进行中,向上爬坡最高的为能垒,而包含此能垒的反应我们称之为决
速步骤,也成为慢反应。例如下图中,从第一个中间态到过渡态 2 的能量就是能垒,而
HCOO*+H*=CO +2H*是在Rh做催化剂时该历程的决速步骤 。
2
【名师提醒】
①能垒越大,反应速率越小,即多步反应中能垒最大的反应为决速反应。
②用不同催化剂催化化学反应,催化剂使能垒降低幅度越大,说明催化效果越好。
③相同反应物同时发生多个竞争反应,其中能垒越小的反应,反应速率越大,产物占比越高。
考向 1 催化机理能垒图
1.煤炭燃烧过程中会释放出大量的SO ,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以
2CaSO 的形式固定,从而降低SO 的排放。但是煤炭燃烧过程中产生的CO又会与CaSO 发生化学反应,降
4 2 4
低了脱硫效率。相关反应的热化学方程式如下:
CaSO(s)+CO(g) CaO(s)+SO (g)+CO(g) ΔH=218.4 kJ·mol-1(反应Ⅰ)
4 2 2 1
CaSO(s)+4CO(g) CaS(s)+4CO(g) ΔH=-175.6 kJ·mol-1(反应Ⅱ)
4 2 2
假设某温度下,反应Ⅰ的速率(v)大于反应Ⅱ的速率(v),则下列反应过程能量变化示意图正确的是(
1 2
)
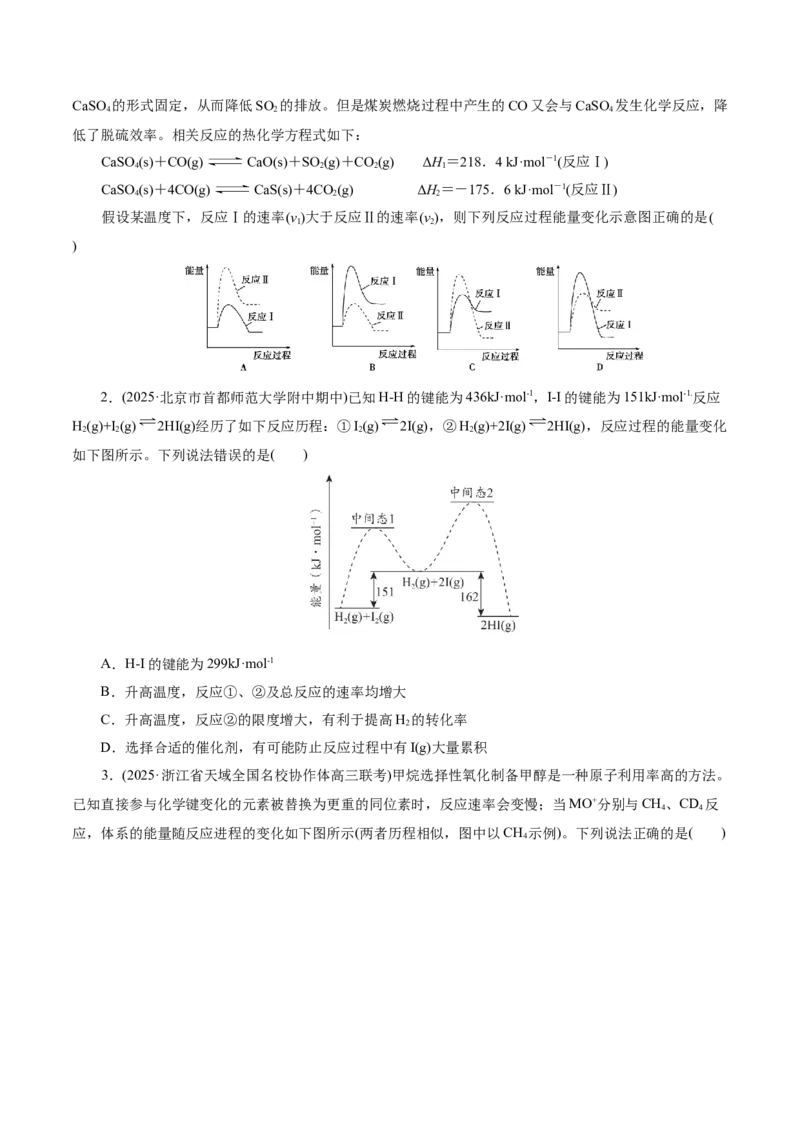
2.(2025·北京市首都师范大学附中期中)已知H-H的键能为436kJ·mol-1,I-I的键能为151kJ·mol-1.反应
H(g)+I (g) 2HI(g)经历了如下反应历程:①I(g) 2I(g),②H(g)+2I(g) 2HI(g),反应过程的能量变化
2 2 2 2
如下图所示。下列说法错误的是( )
A.H-I的键能为299kJ·mol-1
B.升高温度,反应①、②及总反应的速率均增大
C.升高温度,反应②的限度增大,有利于提高H 的转化率
2
D.选择合适的催化剂,有可能防止反应过程中有I(g)大量累积
3.(2025·浙江省天域全国名校协作体高三联考)甲烷选择性氧化制备甲醇是一种原子利用率高的方法。
已知直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢;当MO+分别与CH、CD 反
4 4
应,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以CH 示例)。下列说法正确的是( )
4A.步骤Ⅱ中涉及氢原子成键变化
B.若MO+与CHD 反应,生成的氘代甲醇有2种
3
C.c为MO+与CH 反应的曲线,而d为MO+与CD 反应的曲线
4 4
D.MO+与CHD 反应,相同时间内氘代甲醇的产量:CHDOD>CHD OH
2 2 2 2
4.(2025·浙江省Z20名校联盟高三考试)苯在浓HNO 和浓HSO 作用下,反应过程中能量变化示意图
3 2 4
如下。下列说法不正确的是( )
A.对比进程图,苯更易生成硝基苯的主要原因是该反应速率更快、产物更稳定
B.反应过程中碳原子的杂化方式发生了改变
C.经两步反应生成产物Ⅰ的反应热ΔH=E-E
1 2
D.加入选择性高的催化剂,短时间内可以提高单位时间内产物Ⅰ的产率
5.(2025·浙江省名校协作体高三联考)现以掺氮碳(NC)、氯化镍为原料在恒温条件下合成超高密度单
原子催化剂(UHD-SAC),常温常压下,其机理如图所示。已知基元反应Ⅰ需在高压环境下进行,基元反应
Ⅱ在任何条件下均可自发进行。下列说法中正确的是( )A.基元反应Ⅰ需在高压环境下进行的原因可能是高压环境对其做功,使ΔG<0,从而使反应可以进
行
B.基元反应Ⅱ的过程中反应体系的熵呈减少趋势
C.从总反应来看,决定该过程反应快慢的是基元反应Ⅰ
D.由于总反应ΔH<0,故在工业生产中,反应温度越低越好
6.HBr对CHCH=CH 亲电加成分两步:HBr首先对CHCH=CH 质子化形成CHCHCH+、
3 2 3 2 3 2 2
(CH)CH+两种中间体和Br-,然后中间体分别与Br-结合生成CHCHCHBr、(CH)CHBr两种产物。这两
3 2 3 2 2 3 2
种竞争反应路径的能量(G)变化如图所示。
下列说法不正确的是( )
A.两种路径中的第一步质子化均是整个反应的决速步
B.加成产物主要以1-溴丙烷为主,这是动力学与热力学共同控制的结果
C.(CH)CH+比CHCHCH+更稳定,并且相应的质子化的活化能也更低
3 2 3 2 2
D.温度升高时,该反应的正反应速率增大程度小于逆反应速率增大程度
8.CH 和Cl 反应生成CHCl和HCl的反应进程如图所示。
4 2 3已知总反应分3步进行:
(1)Cl-Cl(g)→2Cl•(g) H=+242.7 kJ∙mol−1
1
(2)CH
4
(g)+•Cl(g)→•CH△3 (g)+HCl(g) H
2
(3)•CH (g)+Cl-Cl(g)→CH Cl(g)+•Cl(g) H
3 3 △ 3
下列有关说法正确的是( ) △
A.△H<0
2
B.第2步的反应速率小于第3步的反应速率
C.根据上述信息,反应中只有C-H键的断裂和C-Cl键的形成
D.CH(g)+Cl (g)→CH Cl(g)+HCl(g) H=−112.9 kJ∙mol−1
4 2 3
9.已知A转化为C和D分步进行:①A△(g) B(g)+2D(g);②B(g) C(g)+D(g),其反应过程能量如图所
示,下列说法正确的是( ) ⇌ ⇌
A.1molA(g)的能量低于1molB(g)的能量
B.B(g) C(g)+D(g) ΔH=(Ea -Ea )kJ/mol
4 3
C.断裂⇌1molA(g)化学键吸收的热量小于形成1molC(g)和3molD(g)化学键所放出的热量
D.反应过程中,由于Ea<Ea,反应②速率大于反应①,气体B很难大量积累
3 1
10.H(g)+2ICl(g)→2HCl(g)+I (g)能量曲线如图。描述正确的是( )
2 2
A.反应①为放热反应,反应②为吸热反应
B.若加入催化剂可降低反应热
C.热化学方程式为H(g)+2ICl(g)→2HCl(g)+I (g)-218kJ
2 2D.若反应的生成物为2HCl(g)+I (s),则反应热数值将变大
2
11.图1表示1mol正丁烷脱氢得到有机物的能量变化图,图2表示1, 丁二烯与 加成的两种
反应历程下列说法正确的是( )
A.对比 丁烯与正丁烷可知碳碳单键比碳碳双键更稳定
B. ,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比
C.相同条件下,1, 丁二烯与 发生加成反应,1, 加成反应速率更快
D.高温条件下,1, 丁二烯与 更容易发生1, 加成
12.苯与Br 的催化反应历程如下图所示。下列说法正确的是( )
2
A.苯与Br 生成 的反应为吸热反应
2
B.上图中,苯与Br 的催化反应生成了溴苯、邻二溴苯
2
C.从图中第III步反应所给信息看,生成 为主要反应D.由 转化为 的过程中有极性键的断裂与形成
考向 2 能垒与连续反应
13.Cu–Ce-O 固溶体作为金属催化剂,能有效促进电化学还原,反应产生CH 和C H 的共同中间体
x 4 2 4
*CO在催化剂表面的反应机理如图所示。下列说法错误的是
A.Cu–Ce-O 固溶体催化剂对生成CH 有较高选择性
x 4
B.制约CO 还原为C H 反应速率的是*CH-CHO→*C-COH
2 2 4
C.由*CO生成*OH的反应为*CO+5H++5e-=CH +*OH
4
D.*CHO→*CH O只有化学键的形成
3
14.一种双功能结构催化剂能同时活化水和甲醇,用以解决氢气的高效存储和安全运输。下图是甲醇
脱氢转化的反应历程( 表示过渡态)
下列说法不正确的是( )
A.CHOH的脱氢反应是分步进行的
3
B.甲醇脱氢反应历程的最大能垒(活化能)是0.95eVC.甲醇脱氢反应中断裂了极性键和非极性键
D.该催化剂的研发为醇类重整产氢的工业应用提供了新思路
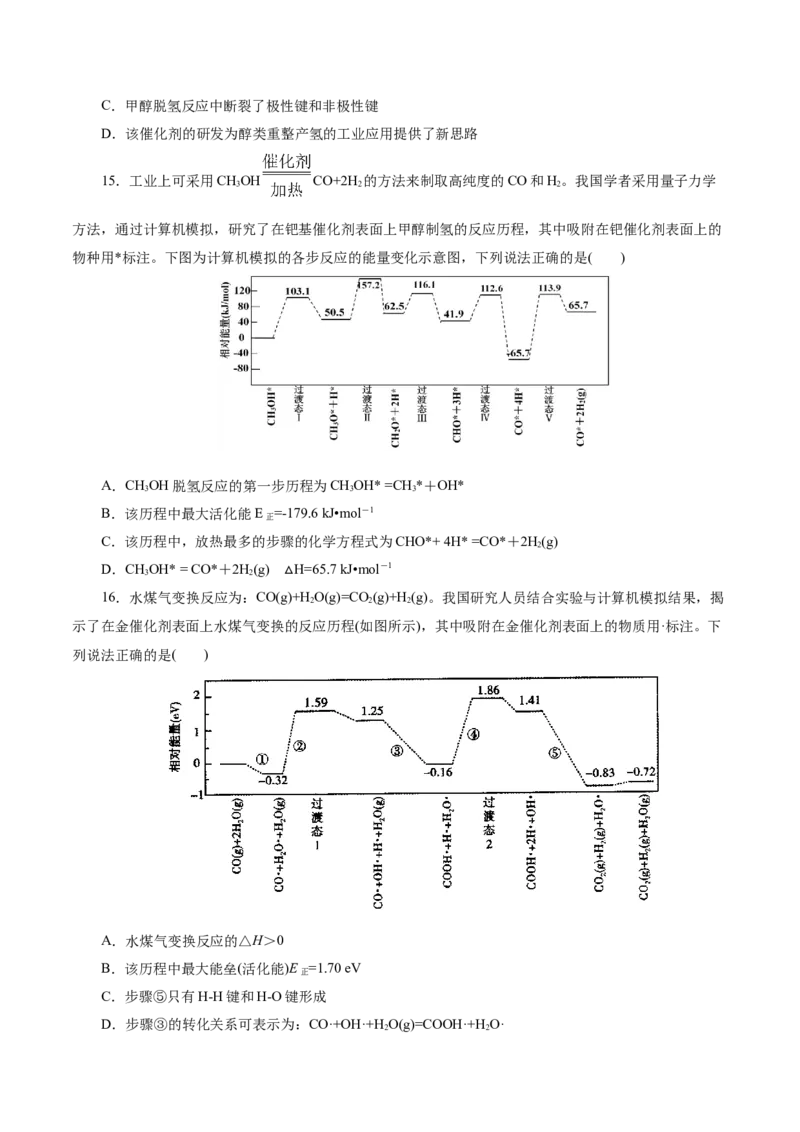
15.工业上可采用CHOH CO+2H 的方法来制取高纯度的CO和H。我国学者采用量子力学
3 2 2
方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的
物种用*标注。下图为计算机模拟的各步反应的能量变化示意图,下列说法正确的是( )
A.CHOH脱氢反应的第一步历程为CHOH* =CH*+OH*
3 3 3
B.该历程中最大活化能E =-179.6 kJ•mol-1
正
C.该历程中,放热最多的步骤的化学方程式为CHO*+ 4H* =CO*+2H(g)
2
D.CHOH* = CO*+2H(g) H=65.7 kJ•mol-1
3 2
16.水煤气变换反应为:CO(g△)+H
2
O(g)=CO
2
(g)+H
2
(g)。我国研究人员结合实验与计算机模拟结果,揭
示了在金催化剂表面上水煤气变换的反应历程(如图所示),其中吸附在金催化剂表面上的物质用·标注。下
列说法正确的是( )
A.水煤气变换反应的△H>0
B.该历程中最大能垒(活化能)E =1.70 eV
正
C.步骤⑤只有H-H键和H-O键形成
D.步骤③的转化关系可表示为:CO·+OH·+H O(g)=COOH·+H O·
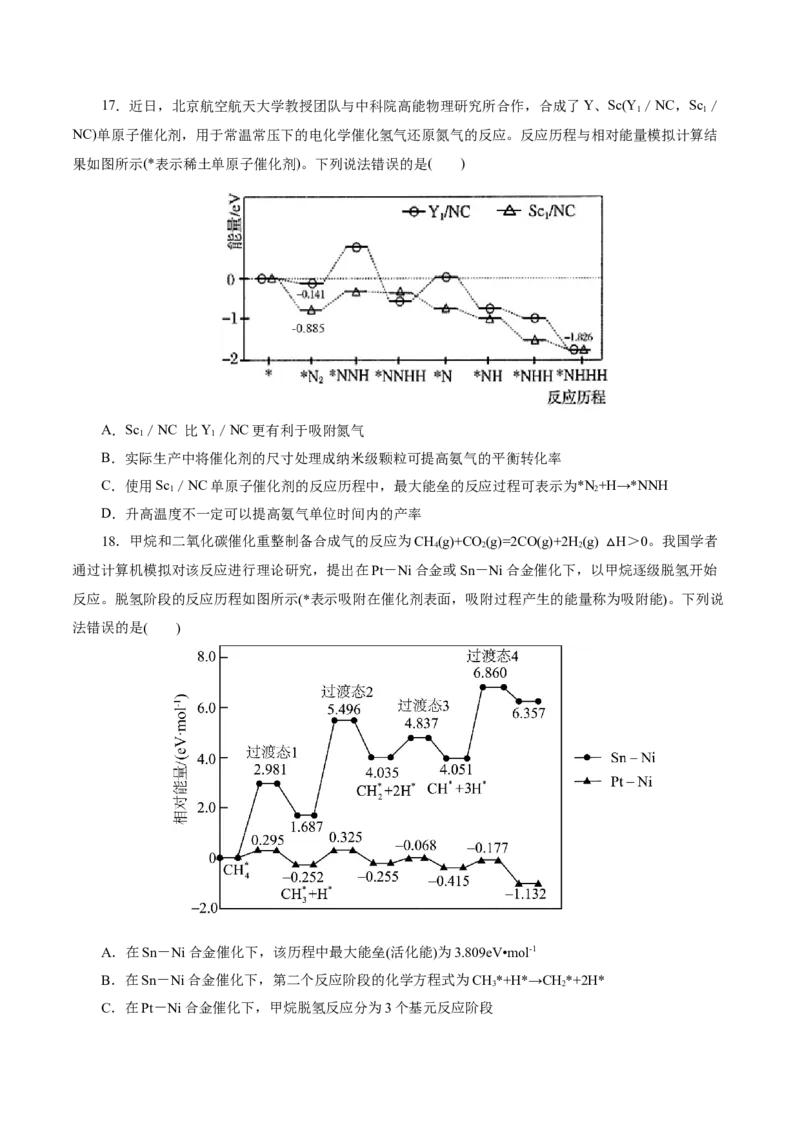
2 217.近日,北京航空航天大学教授团队与中科院高能物理研究所合作,合成了Y、Sc(Y /NC,Sc /
1 1
NC)单原子催化剂,用于常温常压下的电化学催化氢气还原氮气的反应。反应历程与相对能量模拟计算结
果如图所示(*表示稀土单原子催化剂)。下列说法错误的是( )
A.Sc /NC 比Y/NC更有利于吸附氮气
1 1
B.实际生产中将催化剂的尺寸处理成纳米级颗粒可提高氨气的平衡转化率
C.使用Sc /NC单原子催化剂的反应历程中,最大能垒的反应过程可表示为*N+H→*NNH
1 2
D.升高温度不一定可以提高氨气单位时间内的产率
18.甲烷和二氧化碳催化重整制备合成气的反应为CH(g)+CO (g)=2CO(g)+2H(g) H>0。我国学者
4 2 2
通过计算机模拟对该反应进行理论研究,提出在Pt-Ni合金或Sn-Ni合金催化下,以甲△烷逐级脱氢开始
反应。脱氢阶段的反应历程如图所示(*表示吸附在催化剂表面,吸附过程产生的能量称为吸附能)。下列说
法错误的是( )
A.在Sn-Ni合金催化下,该历程中最大能垒(活化能)为3.809eV•mol-1
B.在Sn-Ni合金催化下,第二个反应阶段的化学方程式为CH*+H*→CH*+2H*
3 2
C.在Pt-Ni合金催化下,甲烷脱氢反应分为3个基元反应阶段D.两种催化剂比较,脱氢反应阶段催化效果更好的是Pt-Ni合金
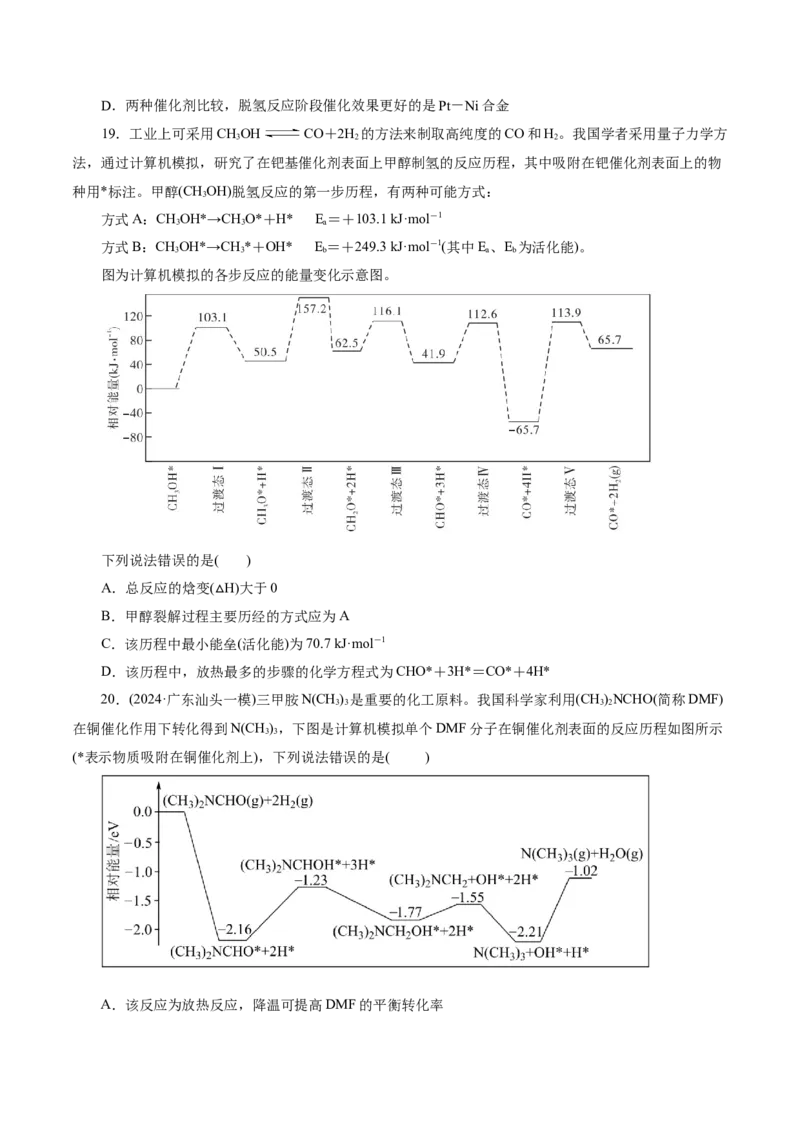
19.工业上可采用CHOH CO+2H 的方法来制取高纯度的CO和H。我国学者采用量子力学方
3 2 2
法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物
种用*标注。甲醇(CHOH)脱氢反应的第一步历程,有两种可能方式:
3
方式A:CHOH*→CH O*+H* E=+103.1 kJ·mol-1
3 3 a
方式B:CHOH*→CH *+OH* E =+249.3 kJ·mol-1(其中E、E 为活化能)。
3 3 b a b
图为计算机模拟的各步反应的能量变化示意图。
下列说法错误的是( )
A.总反应的焓变( H)大于0
B.甲醇裂解过程主△要历经的方式应为A
C.该历程中最小能垒(活化能)为70.7 kJ·mol-1
D.该历程中,放热最多的步骤的化学方程式为CHO*+3H*=CO*+4H*
20.(2024·广东汕头一模)三甲胺N(CH ) 是重要的化工原料。我国科学家利用(CH)NCHO(简称DMF)
3 3 3 2
在铜催化作用下转化得到N(CH ),下图是计算机模拟单个DMF分子在铜催化剂表面的反应历程如图所示
3 3
(*表示物质吸附在铜催化剂上),下列说法错误的是( )
A.该反应为放热反应,降温可提高DMF的平衡转化率B.该历程包含6个基元反应,最大能垒(活化能)为1.19eV
C.设法提高 的速率可以提高总反应速率
D.若1molDMF完全转化为三甲胺,则会吸收1.02eV·N 的能量
A