文档内容
高考热点专项 关系式法与热重分析在化学计算中的应用
目录
01 模拟基础练
【题型一】关系式法
【题型二】热重曲线分析
02 重难创新练
03 真题实战练
题型一 关系式法
1.(2025·江苏省苏州南京航空航天大学附中月考)我国科学家屠呦呦因成功提取青蒿素而获得2015年
诺贝尔医学奖。青蒿素是一种无色针状晶体,其相对分子质量为282,在乙醇、乙醚、石油醚中可溶解,
在水中几乎不溶,熔点为156~157℃,热稳定性差。某兴趣小组取青蒿素样品8.0g配制成 溶液,取
25.00mL加入锥形瓶中,加入足量的KI溶液生成I,生成的I 与0.004molNa SO 恰好完全反应。已知:
2 2 2 2 3
① 1mol青蒿素与足量KI反应只生成1 molI 。②I+2S O2-=S O2-+2I-。计算该青蒿素样品的纯度
2 2 2 3 4 6
(写出计算过程)。
【答案】根据已知条件得到关系式:1青蒿素~2NaI~I~2NaSO,则25.00mL溶液中n(青蒿素)=
2 2 2 3
n(Na SO)= ×0.004mol=0.002mol,样品中m(青蒿素)=nM=0.002mol×282g/mol× =5.64g,可知青蒿
2 2 3
素的纯度= ×100%=70.5%
【解析】已知1 mol青蒿素与足量KI反应只生成1molI ,结合I+2S O2-=S O2-+2I-可得关系式:1青蒿
2 2 2 3 4 6
素~2NaI~I~2NaSO,则25.00mL溶液中n(青蒿素)= n(Na SO)= ×0.004mol=0.002mol,样品中
2 2 2 3 2 2 3
m(青蒿素)=nM=0.002mol×282g/mol× =5.64g,可知青蒿素的纯度= ×100%=70.5%。
2.测定NaSO 样品的纯度:称取0.2500g样品,用蒸馏水溶解,加入20.00mL0.4000mol/LFeSO 溶
2 2 8 4液(过量),加热,再加入20.00mL硫磷混合酸,滴入二苯胺磺酸钠指示剂5~6滴,用0.1000mol/LK Cr O
2 2 7
标准溶液滴定过量的FeSO 至溶液呈紫色(终点),消耗KCr O 标准溶液10.00mL。计算NaSO 样品的纯
4 2 2 7 2 2 8
度 (写出计算过程)。
【答案】95.20%
【解析】该滴定原理为:先加入过量的Fe2+将SO2-还原: SO2-+2Fe2+=2Fe3++2SO 2-,然后利用
2 8 2 8 4
KCr O 标准滴定剩余的Fe2+的量:Cr O2-+6Fe2++14H+=2Cr3++6 Fe3++7HO,从而间接确定SO2-的量;根据
2 2 7 2 7 2 2 8
电子守恒有数量关系:n(Fe2+)=2n(SO2-),n (Fe2+)=6n(K Cr O);n(K Cr O)= 0.1000×10.00 ×10-
2 8 剩 2 2 7 2 2 7
3mol=1.000×10-3mol,即n (Fe2+)=6.000×10-3mol,所以与SO2-反应的n(Fe2+)= 20.00×0.4000×10-
剩 2 8
1
3mol-6.000×10-3mol=2.000×10-3mol,则n(SO2-)= n(Fe2+)= 1.000×10-3mol,NaSO 样品的纯度为
2 8 2 2 2 8
。
3.(2025·重庆市名校联盟高三第一次联考节选)铋酸钠(NaBiO)是一种新型有效的光催化剂,也被广泛
3
应用于制药业。某兴趣小组设计实验制取铋酸钠并测定产品的纯度。
(7)取上面制取的NaBiO 产品xg,加入足量稀硫酸和MnSO 稀溶液使其完全反应,再用0.1mol·L-1的
3 4
HC O 标准溶液滴定生成的MnO -,当达到滴定终点时,消耗ymL。(已知:NaBiO+2Mn2++14H+=5Bi3+
2 2 4 4 3
+2MnO -+5Na++7H O;5HC O+2MnO-+6H+=10CO ↑+2Mn2++8H O)。则滴定终点的现象为 该
4 2 2 2 4 4 2 2
产品的纯度为 。
【答案】(7) 当滴入最后半滴草酸标准溶液,溶液紫红色恰好褪去,且半分钟内不再恢复
【解析】(7)当滴入最后半滴草酸标准溶液,溶液紫红色恰好褪去,且半分钟内不再恢复即达到滴定终
点;根据得失电子守恒建立关系式:5 NaBiO ~2MnO -~5H C O,当达到滴定终点时,消耗0.1mol/L的草
3 4 2 2 4
酸标准溶液ymL,则n(NaBiO)=n(HC O)=0.1mol/L×y×10-3L=y×10-4mol,该产品的纯度为
3 2 2 4
。
题型二 热重曲线分析
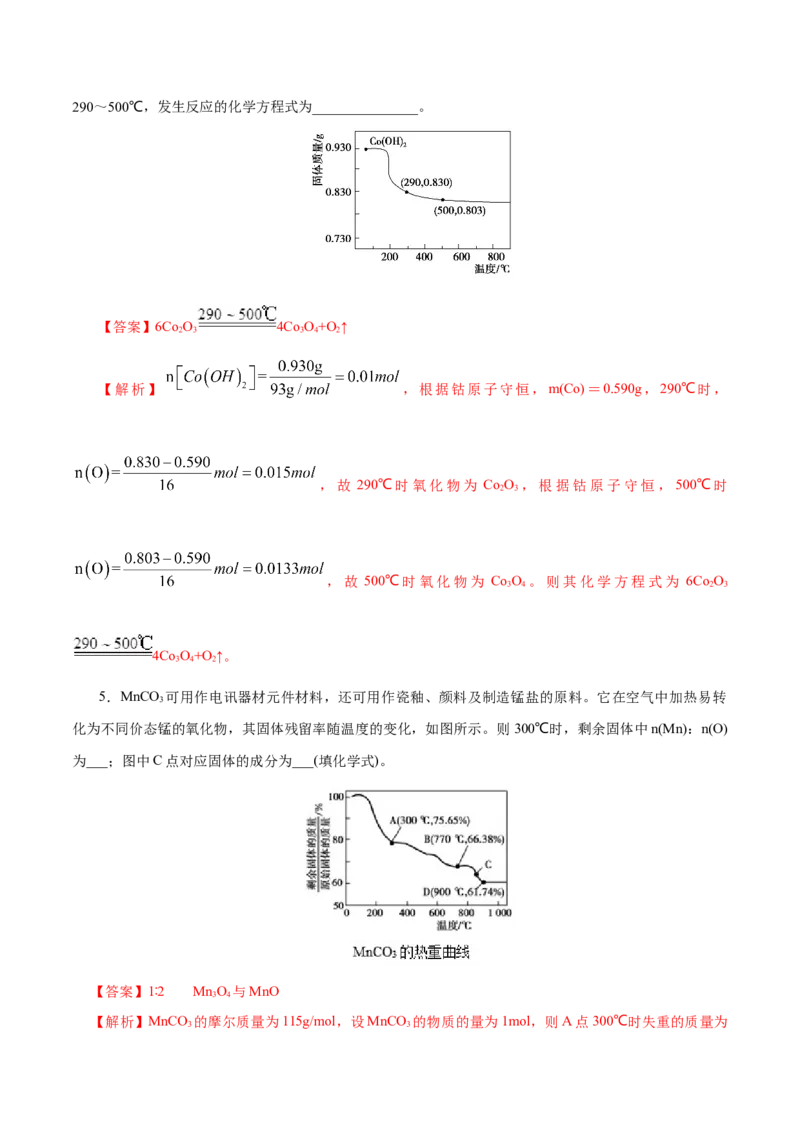
4.在空气中加热Co(OH) ,使其转化为钴的氧化物。加热过程中,固体质量与温度的关系如图所示。
2290~500℃,发生反应的化学方程式为_______________。
【答案】6Co O 4Co O+O ↑
2 3 3 4 2
【解析】 ,根据钴原子守恒,m(Co)=0.590g,290℃时,
,故 290℃时氧化物为 Co O ,根据钴原子守恒,500℃时
2 3
,故 500℃时氧化物为 Co O 。则其化学方程式为 6Co O
3 4 2 3
4Co O+O ↑。
3 4 2
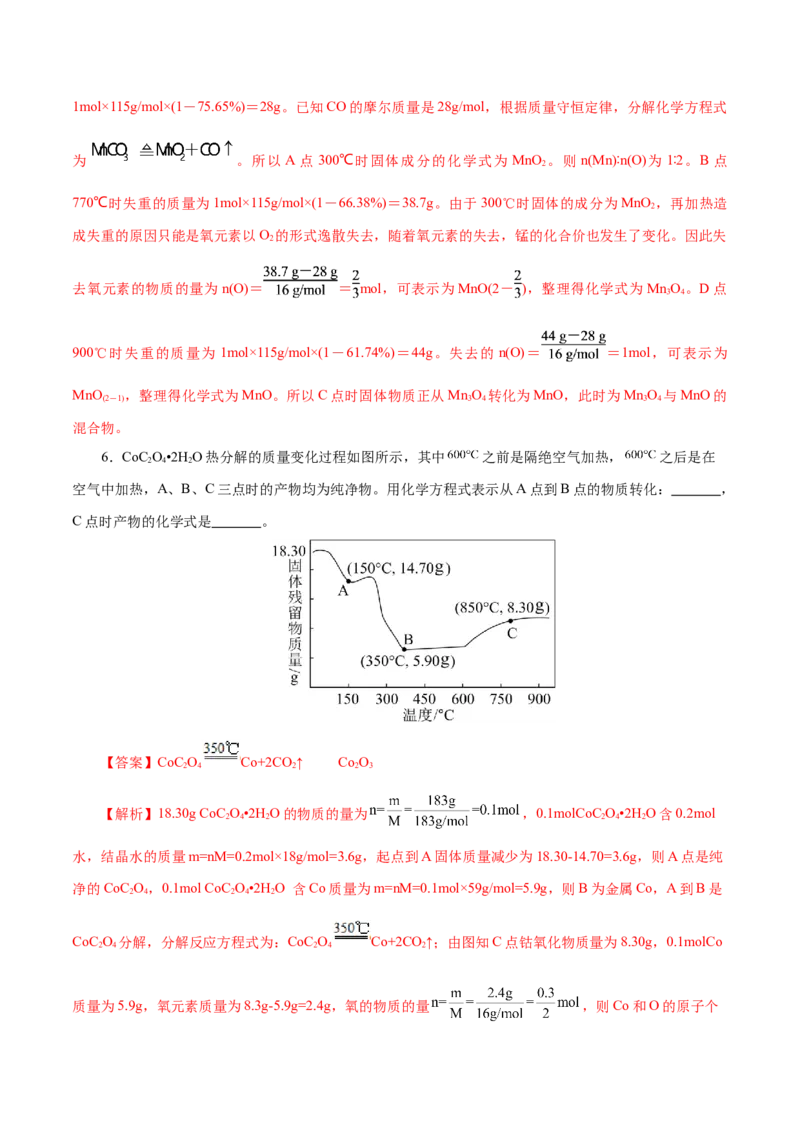
5.MnCO 可用作电讯器材元件材料,还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转
3
化为不同价态锰的氧化物,其固体残留率随温度的变化,如图所示。则300℃时,剩余固体中n(Mn):n(O)
为___;图中C点对应固体的成分为___(填化学式)。
【答案】1∶2 Mn O 与MnO
3 4
【解析】MnCO 的摩尔质量为115g/mol,设MnCO 的物质的量为1mol,则A点300℃时失重的质量为
3 31mol×115g/mol×(1-75.65%)=28g。已知CO的摩尔质量是28g/mol,根据质量守恒定律,分解化学方程式
为 。所以 A 点 300℃时固体成分的化学式为 MnO 。则 n(Mn)∶n(O)为 1∶2。B 点
2
770℃时失重的质量为1mol×115g/mol×(1-66.38%)=38.7g。由于300℃时固体的成分为MnO ,再加热造
2
成失重的原因只能是氧元素以O 的形式逸散失去,随着氧元素的失去,锰的化合价也发生了变化。因此失
2
去氧元素的物质的量为n(O)= = mol,可表示为MnO(2- ),整理得化学式为MnO 。D点
3 4
900℃时失重的质量为 1mol×115g/mol×(1-61.74%)=44g。失去的 n(O)= =1mol,可表示为
MnO ,整理得化学式为MnO。所以C点时固体物质正从MnO 转化为MnO,此时为MnO 与MnO的
(2-1) 3 4 3 4
混合物。
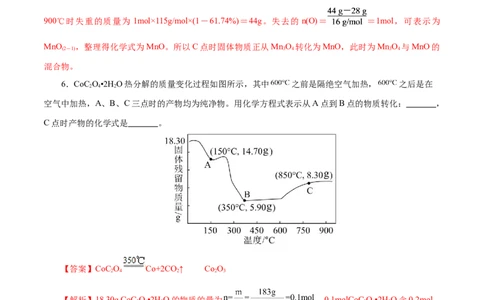
6.CoC O•2H O热分解的质量变化过程如图所示,其中 之前是隔绝空气加热, 之后是在
2 4 2
空气中加热,A、B、C三点时的产物均为纯净物。用化学方程式表示从A点到B点的物质转化: ,
C点时产物的化学式是 。
【答案】CoC O Co+2CO ↑ Co O
2 4 2 2 3
【解析】18.30g CoC O•2H O的物质的量为 ,0.1molCoC O•2H O含0.2mol
2 4 2 2 4 2
水,结晶水的质量m=nM=0.2mol×18g/mol=3.6g,起点到A固体质量减少为18.30-14.70=3.6g,则A点是纯
净的CoC O,0.1mol CoC O•2H O 含Co质量为m=nM=0.1mol×59g/mol=5.9g,则B为金属Co,A到B是
2 4 2 4 2
CoC O 分解,分解反应方程式为:CoC O Co+2CO ↑;由图知C点钴氧化物质量为8.30g,0.1molCo
2 4 2 4 2
质量为5.9g,氧元素质量为8.3g-5.9g=2.4g,氧的物质的量 ,则Co和O的原子个数比为0.1: =2:3,C点产物化学式是Co O。
2 3
7.如图是1.00gMgC O•nH O晶体放在坩埚里从25℃徐徐加热至700℃分解时,所得固体产物的质量
2 4 2
(m)随温度(t)变化的关系曲线。(已知100℃以上才会逐渐失去结晶水,并约在230℃时完全失去结晶水)
试回答下列问题:
(1)MgC O•nH O中n=___。
2 4 2
(2)通过计算确定C点固体物质的化学式___(要求写出推断过程);
(3)通过计算确定从E点到F点过程中的化学方程式___(要求写出推断过程)。
【答案】(1)2 (2)MgC O•H O (3)MgC O MgO+CO↑+CO ↑
2 4 2 2 4 2
【解析】(1)根据图像中的数据,由B到D反应是结晶水合物受热分解失去全部结晶水,则:
= ,根据计算,n=2;(2)根据图像中的数据,由B到C反应是结晶水合物受
热分解失去部分结晶水,设C物质化学式中结晶水系数为x,= ,解得x=1,B点固体的化学式为MgC O•H O;(3)草酸镁受热分解,设最
2 4 2
终存留固体为X,利用反应前后Mg元素的质量守恒, = = ,
M(X) =40g•mol-1,可推测出X即为MgO,根据原子个数守恒和质量守恒,再考虑草酸镁中C元素化合价
为+3价,逸散气体不会只有CO,应该还有CO,所以最终化学方程式为:,MgC O
2 2 4
MgO+CO↑+CO ↑。
2
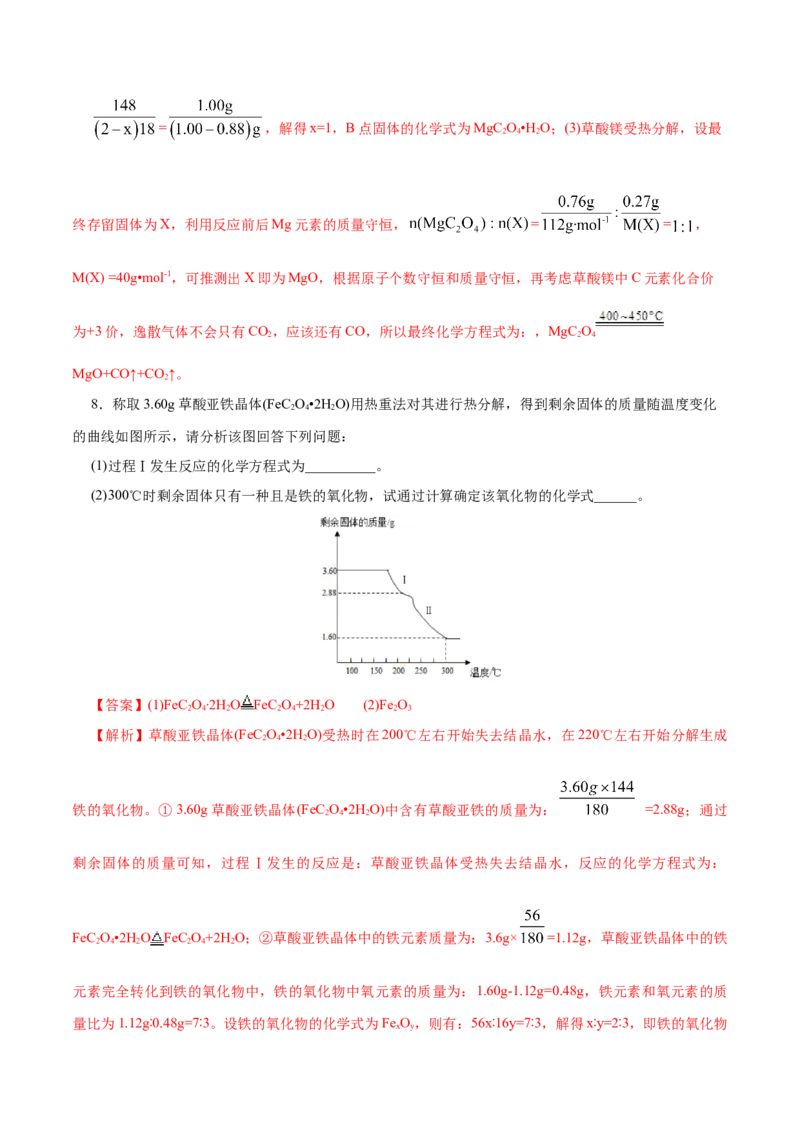
8.称取3.60g草酸亚铁晶体(FeC O•2H O)用热重法对其进行热分解,得到剩余固体的质量随温度变化
2 4 2
的曲线如图所示,请分析该图回答下列问题:
(1)过程Ⅰ发生反应的化学方程式为__________。
(2)300℃时剩余固体只有一种且是铁的氧化物,试通过计算确定该氧化物的化学式______。
【答案】(1)FeC O∙2HO FeC O+2H O (2)Fe O
2 4 2 2 4 2 2 3
【解析】草酸亚铁晶体(FeC O•2H O)受热时在200℃左右开始失去结晶水,在220℃左右开始分解生成
2 4 2
铁的氧化物。①3.60g草酸亚铁晶体(FeC O•2H O)中含有草酸亚铁的质量为: =2.88g;通过
2 4 2
剩余固体的质量可知,过程Ⅰ发生的反应是:草酸亚铁晶体受热失去结晶水,反应的化学方程式为:
FeC O•2H O FeC O+2H O;②草酸亚铁晶体中的铁元素质量为:3.6g× =1.12g,草酸亚铁晶体中的铁
2 4 2 2 4 2
元素完全转化到铁的氧化物中,铁的氧化物中氧元素的质量为:1.60g-1.12g=0.48g,铁元素和氧元素的质
量比为1.12g∶0.48g=7∶3。设铁的氧化物的化学式为Fe O,则有:56x∶16y=7∶3,解得x∶y=2∶3,即铁的氧化物
x y为Fe O。
2 3
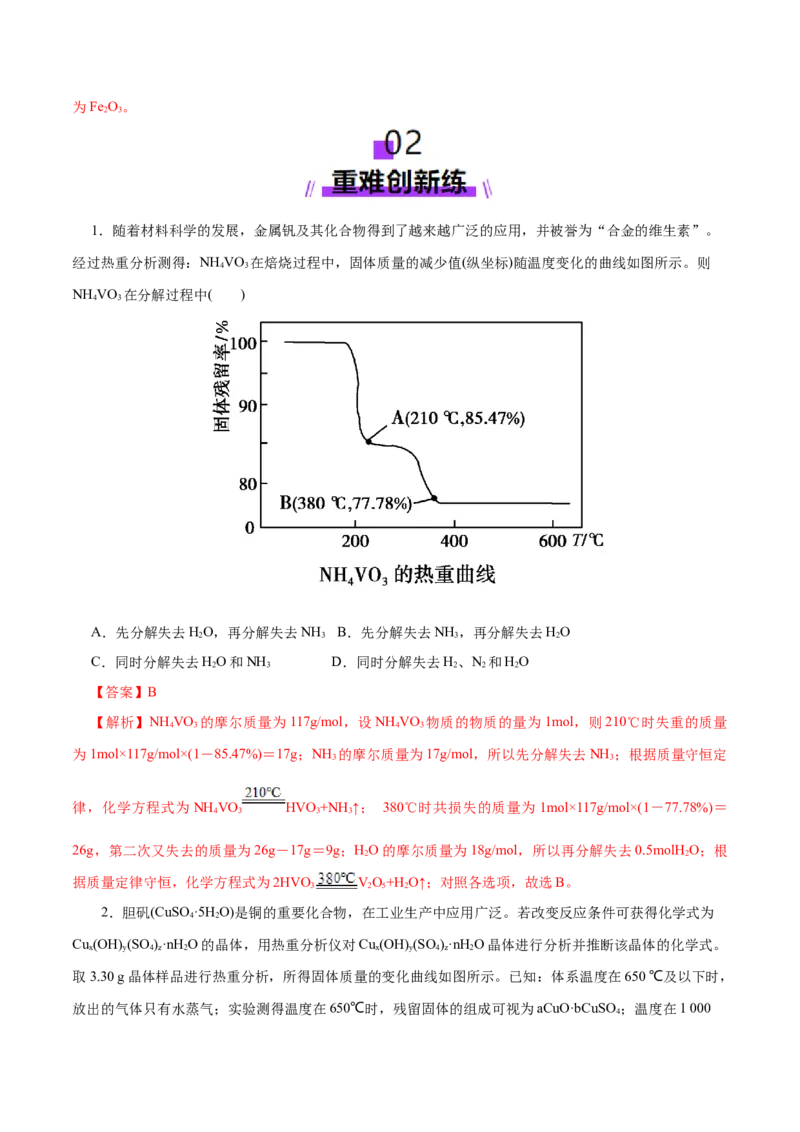
1.随着材料科学的发展,金属钒及其化合物得到了越来越广泛的应用,并被誉为“合金的维生素”。
经过热重分析测得:NH VO 在焙烧过程中,固体质量的减少值(纵坐标)随温度变化的曲线如图所示。则
4 3
NH VO 在分解过程中( )
4 3
A.先分解失去HO,再分解失去NH B.先分解失去NH ,再分解失去HO
2 3 3 2
C.同时分解失去HO和NH D.同时分解失去H、N 和HO
2 3 2 2 2
【答案】B
【解析】NH VO 的摩尔质量为117g/mol,设NH VO 物质的物质的量为1mol,则210℃时失重的质量
4 3 4 3
为1mol×117g/mol×(1-85.47%)=17g;NH 的摩尔质量为17g/mol,所以先分解失去NH ;根据质量守恒定
3 3
律,化学方程式为NH VO HVO+NH↑; 380℃时共损失的质量为1mol×117g/mol×(1-77.78%)=
4 3 3 3
26g,第二次又失去的质量为26g-17g=9g;HO的摩尔质量为18g/mol,所以再分解失去0.5molHO;根
2 2
据质量定律守恒,化学方程式为2HVO VO+H O↑;对照各选项,故选B。
3 2 5 2
2.胆矾(CuSO ·5H O)是铜的重要化合物,在工业生产中应用广泛。若改变反应条件可获得化学式为
4 2
Cu (OH) (SO )·nH O的晶体,用热重分析仪对Cu (OH) (SO )·nH O晶体进行分析并推断该晶体的化学式。
x y 4 z 2 x y 4 z 2
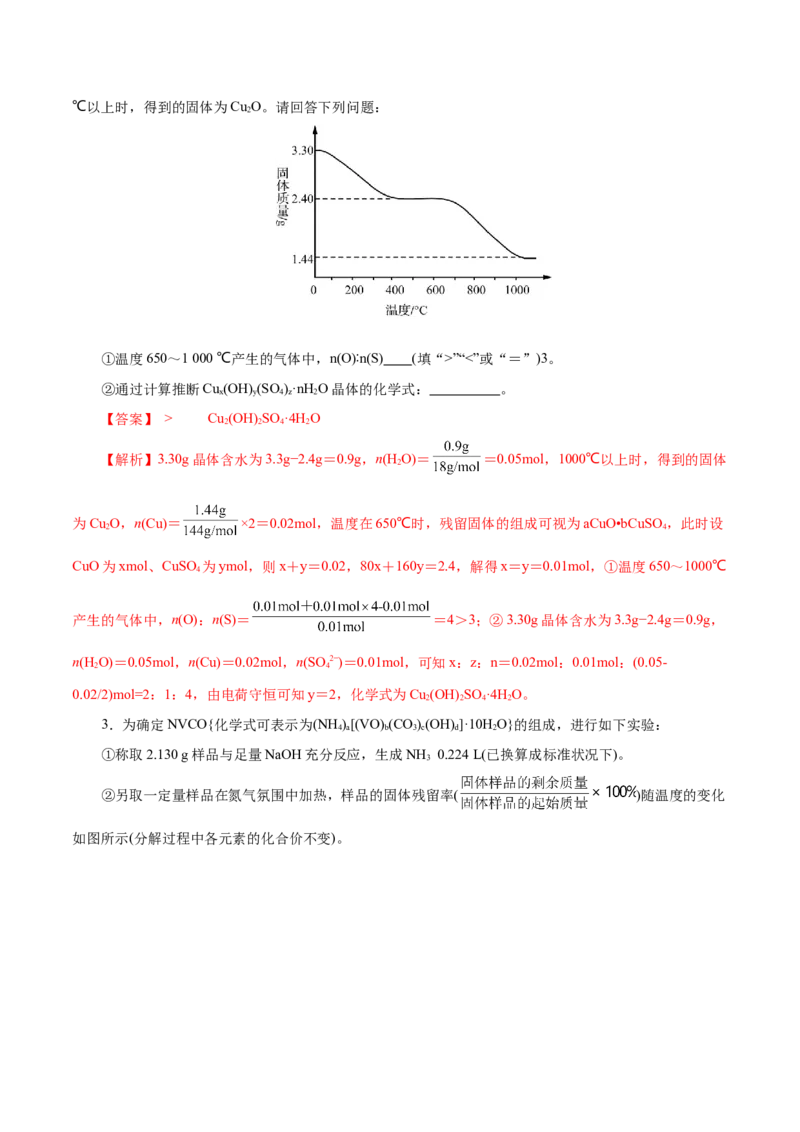
取3.30 g晶体样品进行热重分析,所得固体质量的变化曲线如图所示。已知:体系温度在650 ℃及以下时,
放出的气体只有水蒸气;实验测得温度在650℃时,残留固体的组成可视为aCuO·bCuSO ;温度在1 000
4℃以上时,得到的固体为Cu O。请回答下列问题:
2
①温度650~1 000 ℃产生的气体中,n(O)∶n(S) (填“>”“<”或“=”)3。
②通过计算推断Cu (OH) (SO )·nH O晶体的化学式: 。
x y 4 z 2
【答案】 > Cu (OH) SO ·4H O
2 2 4 2
【解析】3.30g晶体含水为3.3g−2.4g=0.9g,n(H O)= =0.05mol,1000℃以上时,得到的固体
2
为Cu O,n(Cu)= ×2=0.02mol,温度在650℃时,残留固体的组成可视为aCuO•bCuSO ,此时设
2 4
CuO为xmol、CuSO 为ymol,则x+y=0.02,80x+160y=2.4,解得x=y=0.01mol,①温度650~1000℃
4
产生的气体中,n(O):n(S)= =4>3;②3.30g晶体含水为3.3g−2.4g=0.9g,
n(H O)=0.05mol,n(Cu)=0.02mol,n(SO 2−)=0.01mol,可知x:z:n=0.02mol:0.01mol:(0.05-
2 4
0.02/2)mol=2:1:4,由电荷守恒可知y=2,化学式为Cu (OH) SO ·4H O。
2 2 4 2
3.为确定NVCO{化学式可表示为(NH )[(VO) (CO)(OH) ]·10H O}的组成,进行如下实验:
4 a b 3 c d 2
①称取2.130 g样品与足量NaOH充分反应,生成NH 0.224 L(已换算成标准状况下)。
3
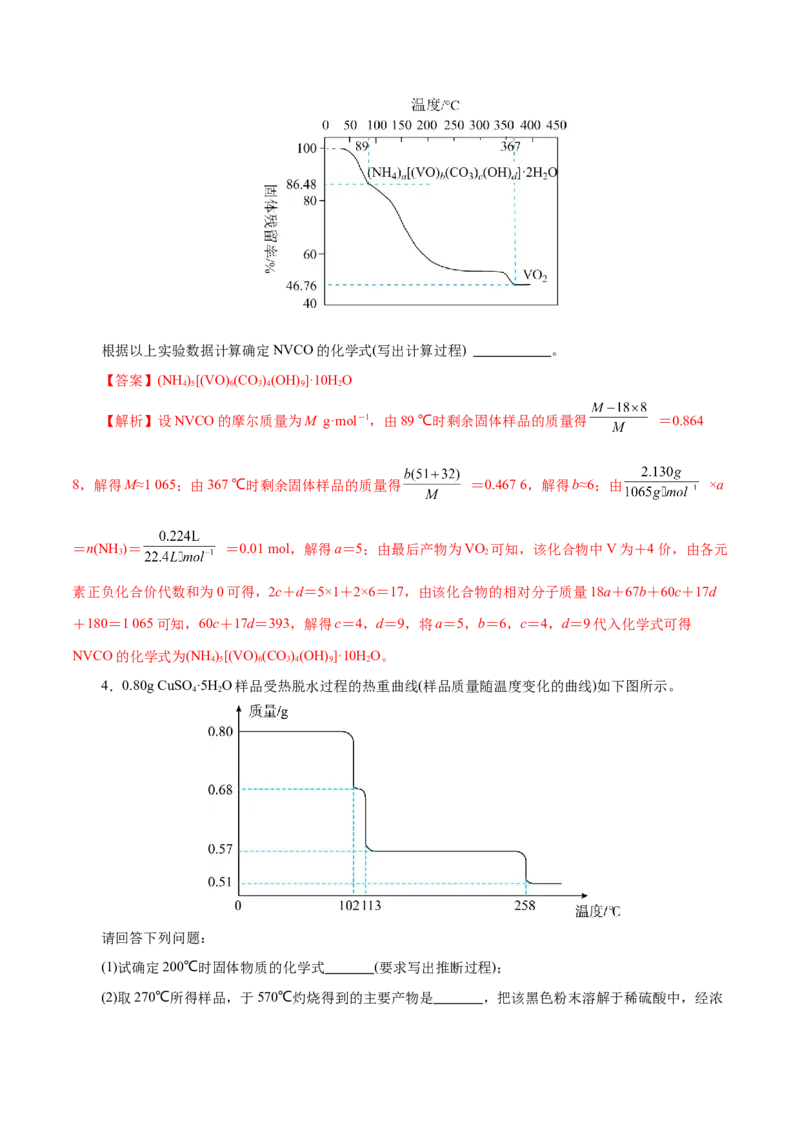
②另取一定量样品在氮气氛围中加热,样品的固体残留率( )随温度的变化
如图所示(分解过程中各元素的化合价不变)。根据以上实验数据计算确定NVCO的化学式(写出计算过程) 。
【答案】(NH )[(VO) (CO)(OH) ]·10H O
4 5 6 3 4 9 2
【解析】设NVCO的摩尔质量为M g·mol-1,由89 ℃时剩余固体样品的质量得 =0.864
8,解得M≈1 065;由367 ℃时剩余固体样品的质量得 =0.467 6,解得b≈6;由 ×a
=n(NH )= =0.01 mol,解得a=5;由最后产物为VO 可知,该化合物中V为+4价,由各元
3 2
素正负化合价代数和为0可得,2c+d=5×1+2×6=17,由该化合物的相对分子质量18a+67b+60c+17d
+180=1 065可知,60c+17d=393,解得c=4,d=9,将a=5,b=6,c=4,d=9代入化学式可得
NVCO的化学式为(NH )[(VO) (CO)(OH) ]·10H O。
4 5 6 3 4 9 2
4.0.80g CuSO ·5H O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示。
4 2
请回答下列问题:
(1)试确定200℃时固体物质的化学式 (要求写出推断过程);
(2)取270℃所得样品,于570℃灼烧得到的主要产物是 ,把该黑色粉末溶解于稀硫酸中,经浓缩、冷却,有晶体析出,该晶体的化学式为 ,其存在的最高温度是 ;
(3)上述氧化性气体与水反应生成一种化合物,该化合物的浓溶液与Cu在加热时发生反应的化学方程
式为 。
(4)在0.10mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的
pH=8时,c(Cu2+)= mol·L-1(K [Cu(OH) ]=2.2×10-20)。若在0.1mol·L-1 硫酸铜溶液中通入过量 HS气
sp 2 2
体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是 mol·L-1。
【答案】(1)CuSO ·H O
4 2
(2)黑色粉末和一种氧化性气体 CuSO ·5H O 102℃
4 2
(3)2H SO (浓)+ Cu CuSO +SO↑+ 2H O
2 4 4 2 2
(4) 2.2×10-8 0.2
【解析】(1)由图分析可知,CuSO ·5H O受热到102℃时开始脱水分解,113℃时可得到较稳定的一种
4 2
中间物,到258℃时才会继续分解。在200℃时固体的质量为0.57g,可能是失去了部分结晶水,用差量法
可以计算:
,解n=4,由此可以确定在200℃时固体物质的化学式为CuSO ·H O。(2)570℃灼烧得到
4 2
的主要产物是氧化铜和三氧化硫,因此得到的产物是黑色粉末和一种氧化性气体; CuO与稀硫酸反应的
产物是硫酸铜和水,蒸发浓缩、冷却结晶所得的晶体为CuSO ·5H O,由图中信息可知,其存在的最高温
4 2
度为102℃。(3)SO 与水反应生成硫酸,与铜加热反应:2HSO (浓)+ Cu CuSO +SO↑+2H O。(4)根据溶
3 2 4 4 2 2
度积的概念可以直接计算。pH=8时,c(OH-)=10-6mol·L-1,由c(Cu2+)·c2(OH-)=Ksp[Cu(OH) ]可得,c(Cu2+)=
2
=2.2×10-8 mol·L-1 在0.1mol·L-1硫酸铜溶液中通入过量HS气体,使Cu2+完全沉淀为
。 2
CuS,则溶液中溶质为硫酸,由硫酸根守恒可知,c(SO 2-)不变,为0.1mol·L-1 ,则c(H+)为0.2mol·L-1。
4