文档内容
高考热点专项 物质能量、能垒变化图像分析
目录
01考情透视·目标导航............................................................................................................................
02知识导图·思维引航............................................................................................................................
03核心精讲·题型突破............................................................................................................................
【真题研析】.............................................................................
【核心精讲】.............................................................................
1.催化机理..............................................................................
2.催化剂的特征..........................................................................
3.过渡态理论............................................................................
4.能垒与决速步..........................................................................
【命题预测】.............................................................................
考向1催化机理能垒图.....................................................................
考向2 能垒与连续反应....................................................................
考点要求 考题统计 考情分析
2024·甘肃卷,10,3
分;2024· 贵州卷,14, 采用“图示+文字”形式,一般为能量反应过程的分
3分;2024·河北卷, 析,通过分析能垒变化图象中的化学键和能量变
14,3分;2023•浙江省1 化,掌握从宏观和微观两个角度进行问题探究的能
能垒变化
月选考,14,3分; 力,培养宏观辨识与微观探析的核心素养。预计
图
2022•湖南选择性卷, 2025命题形式比较新颖,以图像为载体,以陌生的
12;2022·浙江省1月 反应历程方程式或示意图为主要信息源,高起点,
卷,18,2分;2022•湖 低落点,从微观视角来考查能量变化
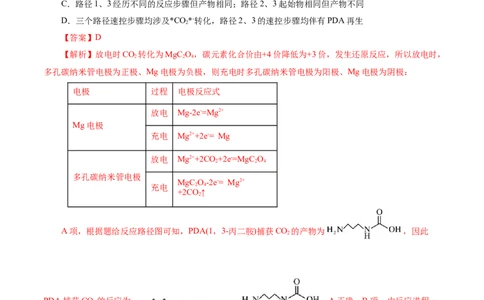
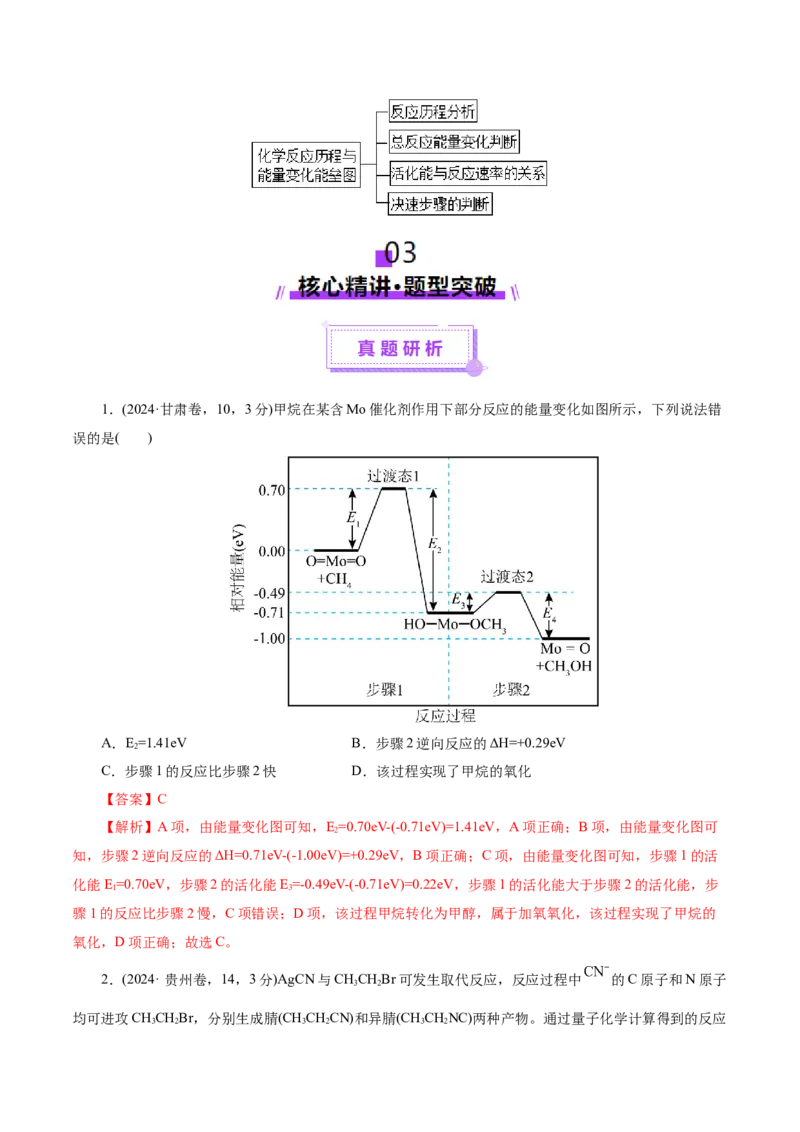
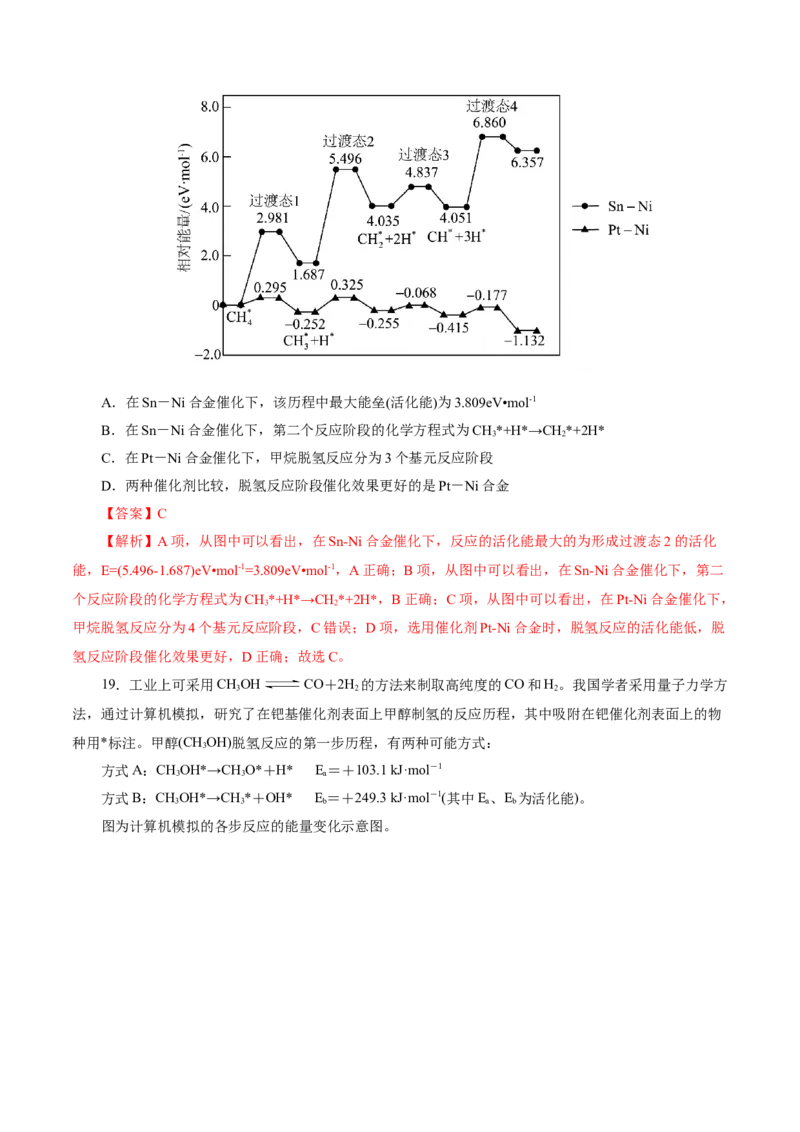
南选择性卷,12,3分1.(2024·甘肃卷,10,3分)甲烷在某含Mo催化剂作用下部分反应的能量变化如图所示,下列说法错
误的是( )
A.E=1.41eV B.步骤2逆向反应的ΔH=+0.29eV
2
C.步骤1的反应比步骤2快 D.该过程实现了甲烷的氧化
【答案】C
【解析】A项,由能量变化图可知,E=0.70eV-(-0.71eV)=1.41eV,A项正确;B项,由能量变化图可
2
知,步骤2逆向反应的ΔH=0.71eV-(-1.00eV)=+0.29eV,B项正确;C项,由能量变化图可知,步骤1的活
化能E=0.70eV,步骤2的活化能E=-0.49eV-(-0.71eV)=0.22eV,步骤1的活化能大于步骤2的活化能,步
1 3
骤1的反应比步骤2慢,C项错误;D项,该过程甲烷转化为甲醇,属于加氧氧化,该过程实现了甲烷的
氧化,D项正确;故选C。
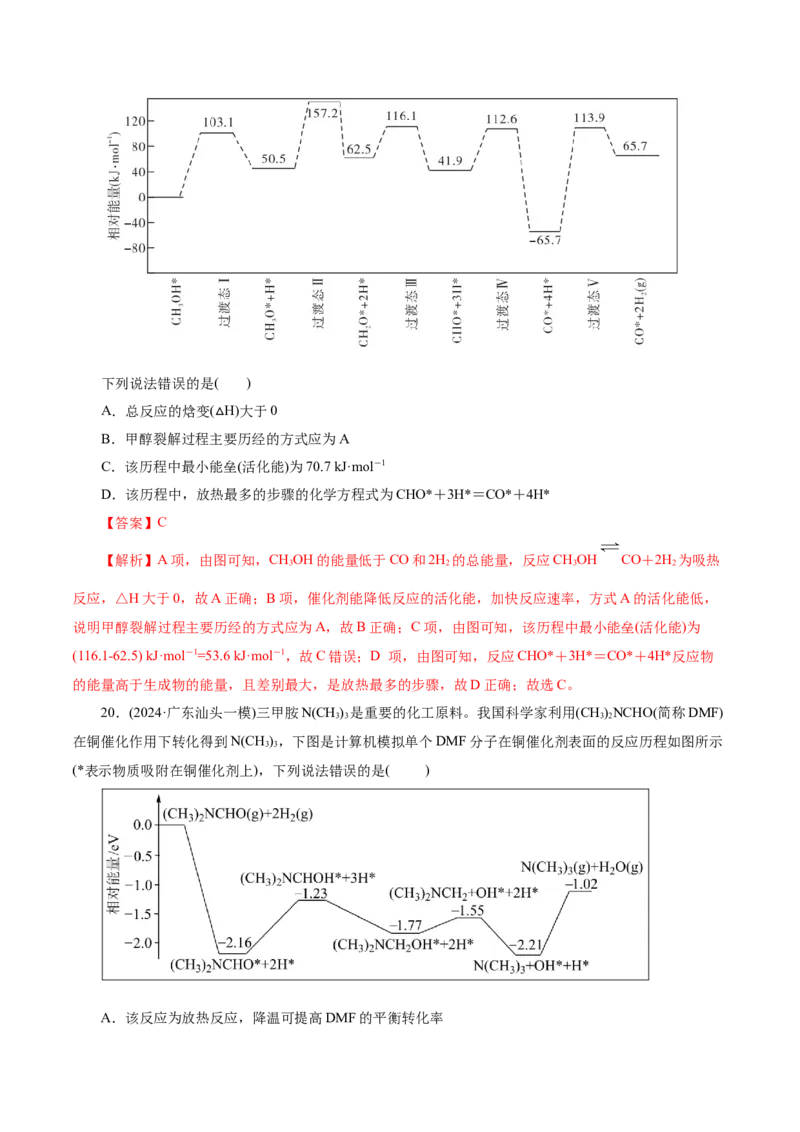
2.(2024· 贵州卷,14,3分)AgCN与CHCHBr可发生取代反应,反应过程中 的C原子和N原子
3 2
均可进攻CHCHBr,分别生成腈(CHCHCN)和异腈(CHCHNC)两种产物。通过量子化学计算得到的反应
3 2 3 2 3 2历程及能量变化如图(TS为过渡态,Ⅰ、Ⅱ为后续物)。
由图示信息,下列说法错误的是( )
A.从CHCHBr生成CHCHCN和CHCHNC的反应都是放热反应
3 2 3 2 3 2
B.过渡态TS1是由-的C原子进攻CHCHBr的α-C而形成的
3 2
C.Ⅰ中“N-Ag”之间的作用力比Ⅱ中“C-Ag”之间的作用力弱
D.生成CHCHCN放热更多,低温时CHCHCN是主要产物
3 2 3 2
【答案】D
【解析】A项,由反应历程及能量变化图可知,两种路径生成的产物的总能量均低于反应物,故从
CHCHBr生成CHCHCN和CHCHNC的反应都是放热反应,A项正确;B项,与Br原子相连的C原子
3 2 3 2 3 2
为α-C,由反应历程及能量变化图可知,过渡态 TS1是由CN-的C原子进攻CHCHBr的α-C,形成碳碳键,
3 2
B项正确;C项,由反应历程及能量变化图可知,后续物Ⅰ、Ⅱ转化为产物,分别断开的是N-Ag和C-
Ag,且后者吸收更多的能量,故Ⅰ中“N-Ag”之间的作用力比Ⅱ中“C-Ag”之间的作用力弱,C项正确;D
项,由于生成CHCHCN所需要的活化能高,反应速率慢,故低温时更容易生成CHCHNC,为主要产物,
3 2 3 2
D项错误;故选D。
3.(2024·河北卷,14,3分)对上述电池放电时CO 的捕获和转化过程开展了进一步研究,电极上CO
2 2
转化的三种可能反应路径及相对能量变化如图(*表示吸附态)。
下列说法错误的是( )A.PDA捕获CO 的反应为
2
是
B.路径2 优先路径,速控步骤反应式为
C.路径1、3经历不同的反应步骤但产物相同;路径2、3起始物相同但产物不同
D.三个路径速控步骤均涉及*CO*-转化,路径2、3的速控步骤均伴有PDA再生
2
【答案】D
【解析】放电时CO 转化为MgC O,碳元素化合价由+4价降低为+3价,发生还原反应,所以放电时,
2 2 4
多孔碳纳米管电极为正极、Mg电极为负极,则充电时多孔碳纳米管电极为阳极、Mg电极为阴极:
电极 过程 电极反应式
放电 Mg-2e-=Mg2+
Mg电极
充电 Mg2++2e-= Mg
放电 Mg2++2CO+2e-=MgC O
2 2 4
多孔碳纳米管电极
MgC O-2e-= Mg2+
充电 2 4
+2CO ↑
2
A项,根据题给反应路径图可知,PDA(1,3-丙二胺)捕获CO 的产物为 ,因此
2
PDA捕获CO 的反应为 ,A正确;B项,由反应进程-
2
相对能量图可知,路径2的最大能垒最小,因此与路径1和路径3相比,路径2是优先路径,且路径2的
最大能垒为*CO*-→*C O2-的步骤,据反应路径2的图示可知,该步骤有 参与反
2 2 4应,因此速控步骤反应式为 ,B正确;C
项,根据反应路径图可知,路径1、3的中间产物不同,即经历了不同的反应步骤,但产物均为*MgCO ,
3
而路径2、3的起始物均为 ,产物分别为*MgC O 和*MgCO ,C正确;D项,根据反
2 4 3
应路径与相对能量的图像可知,三个路径的速控步骤中*CO*-都参与了反应,且由B项分析可知,路径2
2
的速控步骤伴有PDA再生,但路径3的速控步骤为*CO*-得电子转化为*CO和*CO2-,没有PDA的生成,
2 3
D错误;故选D。
4.(2023•浙江省1月选考,14)标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下
[已知O(g)和Cl(g)的相对能量为0],下列说法不正确的是 ( )
2 2
A.E-E=E-E
6 3 5 2
B.可计算Cl-Cl键能为2(E-E)kJ•mol-1
2 3
C.相同条件下,O 的平衡转化率:历程II>历程I
3
D.历程I、历程II中速率最快的一步反应的热化学方程式为:ClO(g)+O(g)=O (g)+Cl(g) ∆H=(E-
2 5
E)kJ•mol-1
4
【答案】C
【解析】对比两个历程可知,历程Ⅱ中增加了催化剂,降低了反应的活化能,加快了反应速率。A项,
催化剂能降低活化能,但是不能改变反应的焓变,因此E-E=E-E,A正确;B项,已知Cl(g)的相对能量
6 3 5 2 2
为0,对比两个历程可知,Cl(g)的相对能量为(E-E)kJ•mol-1,则Cl-Cl键能为2(E-E)kJ•mol-1,B正确;C
2 3 2 3
项,催化剂不能改变反应的平衡转化率,因此相同条件下,O 的平衡转化率:历程Ⅱ=历程Ⅰ,C错误;D
3
项,活化能越低,反应速率越快,由图像可知,历程Ⅱ中第二步反应的活化能最低,所以速率最快的一步
反应的热化学方程式为:ClO(g)+O(g)=O (g)+Cl(g) ∆H=(E-E)kJ•mol-1,D正确;故选C。
2 5 4
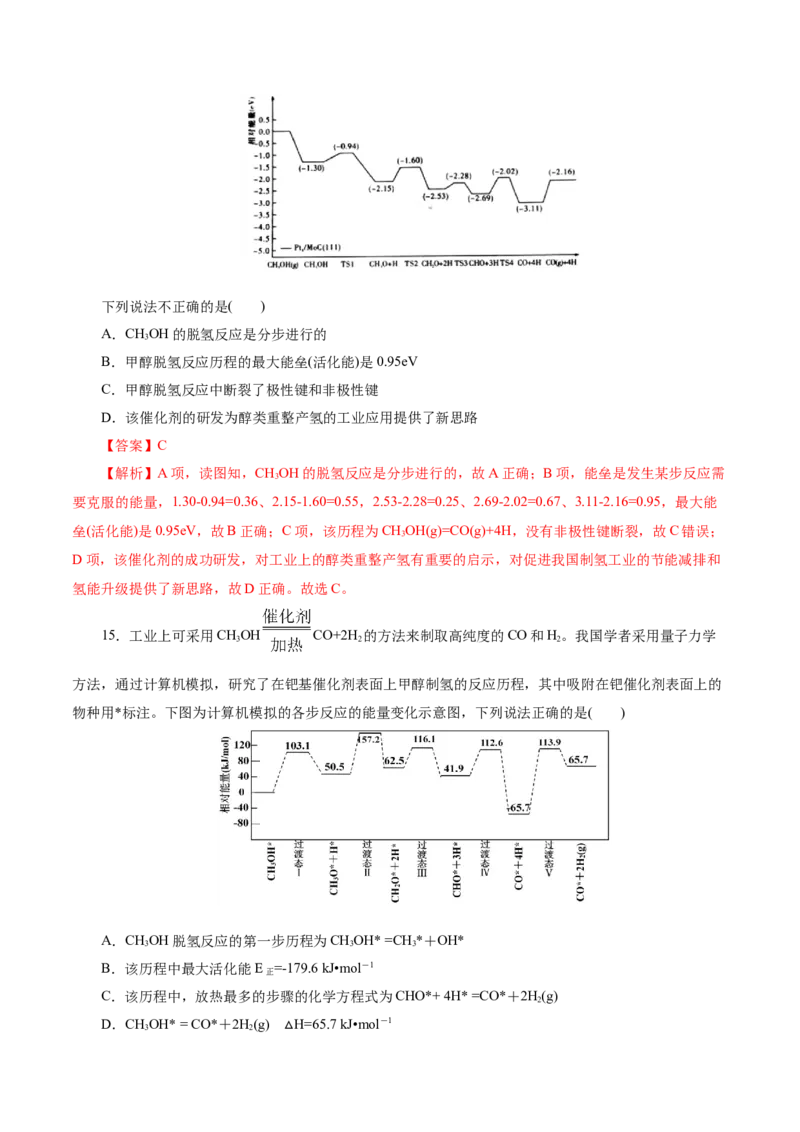
5.(2023·广东卷,15,3分)催化剂Ⅰ和Ⅱ均能催化反应R(g) P(g)。反应历程(下图)中,M为中间产物。其他条件相同时,下列说法不正确的是( )
A.使用Ⅰ和Ⅱ,反应历程都分4步进行
B.反应达平衡时,升高温度,R的浓度增大
C.使用Ⅱ时,反应体系更快达到平衡
D.使用Ⅰ时,反应过程中M所能达到的最高浓度更大
【答案】C
【解析】由图可知两种催化剂均出现四个波峰,所以使用Ⅰ和Ⅱ,反应历程都分4步进行,A正确;
该反应是放热反应,升高温度平衡向左移动,R的浓度增大,B正确;由图可知Ⅰ的最高活化能小于Ⅱ的
最高活化能,所以使用Ⅰ时反应速率更快,反应体系更快达到平衡,C错误;在前两个历程中使用Ⅰ活化
能较低反应速率较快,后两个历程中使用Ⅰ活化能较高反应速率较慢,所以使用Ⅰ时,反应过程中M所能
达到的最高浓度更大,D正确。
(1)反应历程中化学键的变化
在反应中,旧键断裂与新键形成是同时进行的,形成中间过渡态。
(2)反应历程中物质的变化
①只进不出的是反应物(A―→…);
②只出不进的是产物(…―→M);
③先出后进的是中间体(…―→X,X―→…);
④先进后出的是催化剂(R―→…,…―→R)。
(3)三步突破能量变化能垒图
通览全图,理清坐标的含义。能量变化的能垒图的横坐标一般表示反应的历程,横坐标的不
第1步 同阶段表示一个完整反应的不同阶段。纵坐标表示能量的变化,不同阶段的最大能垒即该反
应的活化能
细看变化,分析各段反应。仔细观察曲线(直线)的变化趋势,分析每一阶段发生的反应是什
第2步
么,各段反应是放热还是吸热,能量升高的为吸热,能量下降的为放热
综合分析,做出合理判断。综合整合各项信息,回扣题目要求,做出合理判断。如利用盖斯
第3步 定律将各步反应相加,即得到完整反应;催化剂只改变反应的活化能,但不改变反应的反应
热,也不会改变反应的转化律1 . 催化机理
催化剂通过参加反应,改变反应历程,降低反应的活化能,使活化分子百分数增多,从而加快反应速
率,图示如下。
【易错提醒】
①在无催化剂的情况下:E 为正反应的活化能;E 为逆反应的活化能;E-E 为此反应的焓变(ΔH)。
1 2 1 2
②有催化剂时,总反应分成了两个反应步骤(也可能为多个,如模拟演练题1中图像所表示的),反应
①为吸热反应,产物为总反应的中间产物,反应②为放热反应,总反应为放热反应。
③催化剂的作用:降低E、E,但不影响ΔH,反应是放热反应还是吸热反应取决于起点(反应物)能量
1 2
和终点(生成物)能量的相对大小
2 . 催化剂的特征
(1)催化剂只能改变反应途径(又称反应机理),不能改变反应的始态和终态。它同时加快了正、逆反应
速率,缩短了达到平衡的时间,并不能改变平衡状态。
(2)催化剂有选择性,不同的反应常用不同的催化剂,即每个反应有它特有的催化剂。生产上常利用催
化剂的选择性,使所希望的化学反应加快,同时抑制某些副反应的发生。
(3)每种催化剂只有在特定条件下才能体现出它的活性,否则将失去活性或发生催化剂中毒。
3 . 过渡态理论
【名师提醒】
①该反应的反应物为A、B,中间体为C,生成物为D。
②由A、B生成C的反应为吸热反应,由C生成D的反应为放热反应,总反应为放热反应。③第一步为慢反应,第二步为快反应,决定总反应快慢的是第一步反应。
4 .能垒与决速步
能垒:简单可以理解为从左往右进行中,向上爬坡最高的为能垒,而包含此能垒的反应我们称之为决
速步骤,也成为慢反应。例如下图中,从第一个中间态到过渡态 2 的能量就是能垒,而
HCOO*+H*=CO +2H*是在Rh做催化剂时该历程的决速步骤 。
2
【名师提醒】
①能垒越大,反应速率越小,即多步反应中能垒最大的反应为决速反应。
②用不同催化剂催化化学反应,催化剂使能垒降低幅度越大,说明催化效果越好。
③相同反应物同时发生多个竞争反应,其中能垒越小的反应,反应速率越大,产物占比越高。
考向 1 催化机理能垒图
1.煤炭燃烧过程中会释放出大量的SO ,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以
2
CaSO 的形式固定,从而降低SO 的排放。但是煤炭燃烧过程中产生的CO又会与CaSO 发生化学反应,降
4 2 4
低了脱硫效率。相关反应的热化学方程式如下:
CaSO(s)+CO(g) CaO(s)+SO (g)+CO(g) ΔH=218.4 kJ·mol-1(反应Ⅰ)
4 2 2 1
CaSO(s)+4CO(g) CaS(s)+4CO(g) ΔH=-175.6 kJ·mol-1(反应Ⅱ)
4 2 2
假设某温度下,反应Ⅰ的速率(v)大于反应Ⅱ的速率(v),则下列反应过程能量变化示意图正确的是(
1 2
)【答案】C
【解析】相同温度下,因两个反应的反应物完全相同,反应速率越大,则反应的活化能越小,因此反
应Ⅰ的活化能小于反应Ⅱ的活化能;反应Ⅰ的 ΔH>0,生成物的能量高于反应物的能量,反应Ⅱ的 ΔH<0,
生成物的能量低于反应物的能量,故C项正确。
2.(2025·北京市首都师范大学附中期中)已知H-H的键能为436kJ·mol-1,I-I的键能为151kJ·mol-1.反应
H(g)+I (g) 2HI(g)经历了如下反应历程:①I(g) 2I(g),②H(g)+2I(g) 2HI(g),反应过程的能量变化
2 2 2 2
如下图所示。下列说法错误的是( )
A.H-I的键能为299kJ·mol-1
B.升高温度,反应①、②及总反应的速率均增大
C.升高温度,反应②的限度增大,有利于提高H 的转化率
2
D.选择合适的催化剂,有可能防止反应过程中有I(g)大量累积
【答案】C
【解析】A项,由图可知, ,设H-I
的键能为x,则 ,可得, ,故A正确;B
项,升高温度,反应速率加快,正反应①、反应②反应速率都加快,故B正确;C项,由图可知,反应②
为放热反应,升高温度,反应②速率增大,平衡逆向移动,H 的转化率降低,故C错误;D项,选择合适
2
的催化剂降低反应②的活化能,加快反应,能防止反应过程中有I(g)大量累积,故D正确;故选C。
3.(2025·浙江省天域全国名校协作体高三联考)甲烷选择性氧化制备甲醇是一种原子利用率高的方法。
已知直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢;当MO+分别与CH、CD 反
4 4
应,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以CH 示例)。下列说法正确的是( )
4A.步骤Ⅱ中涉及氢原子成键变化
B.若MO+与CHD 反应,生成的氘代甲醇有2种
3
C.c为MO+与CH 反应的曲线,而d为MO+与CD 反应的曲线
4 4
D.MO+与CHD 反应,相同时间内氘代甲醇的产量:CHDOD>CHD OH
2 2 2 2
【答案】B
【解析】A项,由图可知,步骤Ⅰ涉及碳氢键的断裂和氢氧键的形成,步骤Ⅱ中涉及碳氧键形成,所
以涉及氢原子成键变化的是步骤Ⅰ,A错误;B项,根据反应机理可知,若MO+与CHD 反应,生成的氘
3
代甲醇可能为CHD OD或CDOH,共2种,B正确;C项,直接参与化学键变化的元素被替换为更重的同
2 3
位素时,反应速率会变慢,说明正反应活化能会增大,则MO+与CD 反应的能量变化应为图中曲线c,d
4
为MO+与CH 反应的曲线,C错误;D项,直接参与化学键变化的元素被替换为更重的同位素时,反应速
4
率会变慢,则氧更容易和H而不是和D生成羟基,故氘代甲醇的产量CHDOD