文档内容
高考解密08 水溶液中的离子反应与平衡
考点热度 ★★★★★
考点1、弱电解质(包括水)的电离平衡
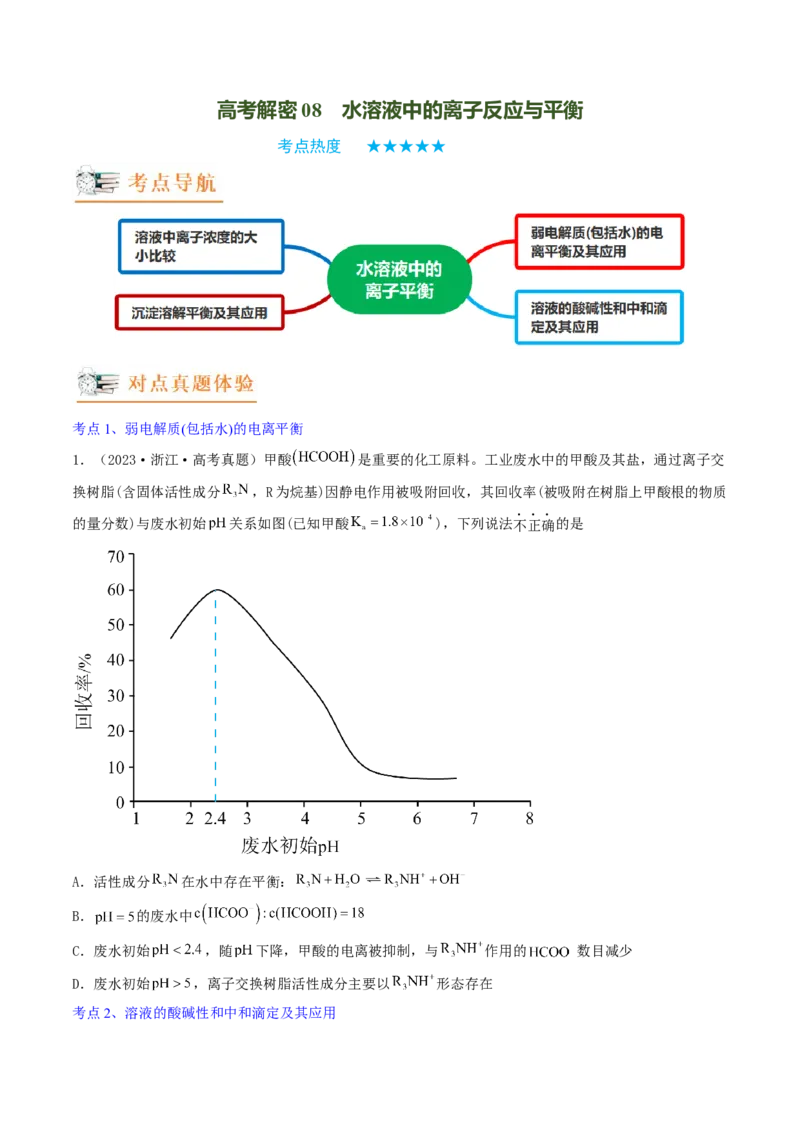
1.(2023·浙江·高考真题)甲酸 是重要的化工原料。工业废水中的甲酸及其盐,通过离子交
换树脂(含固体活性成分 ,R为烷基)因静电作用被吸附回收,其回收率(被吸附在树脂上甲酸根的物质
的量分数)与废水初始 关系如图(已知甲酸 ),下列说法不正确的是
A.活性成分 在水中存在平衡:
B. 的废水中
C.废水初始 ,随 下降,甲酸的电离被抑制,与 作用的 数目减少
D.废水初始 ,离子交换树脂活性成分主要以 形态存在
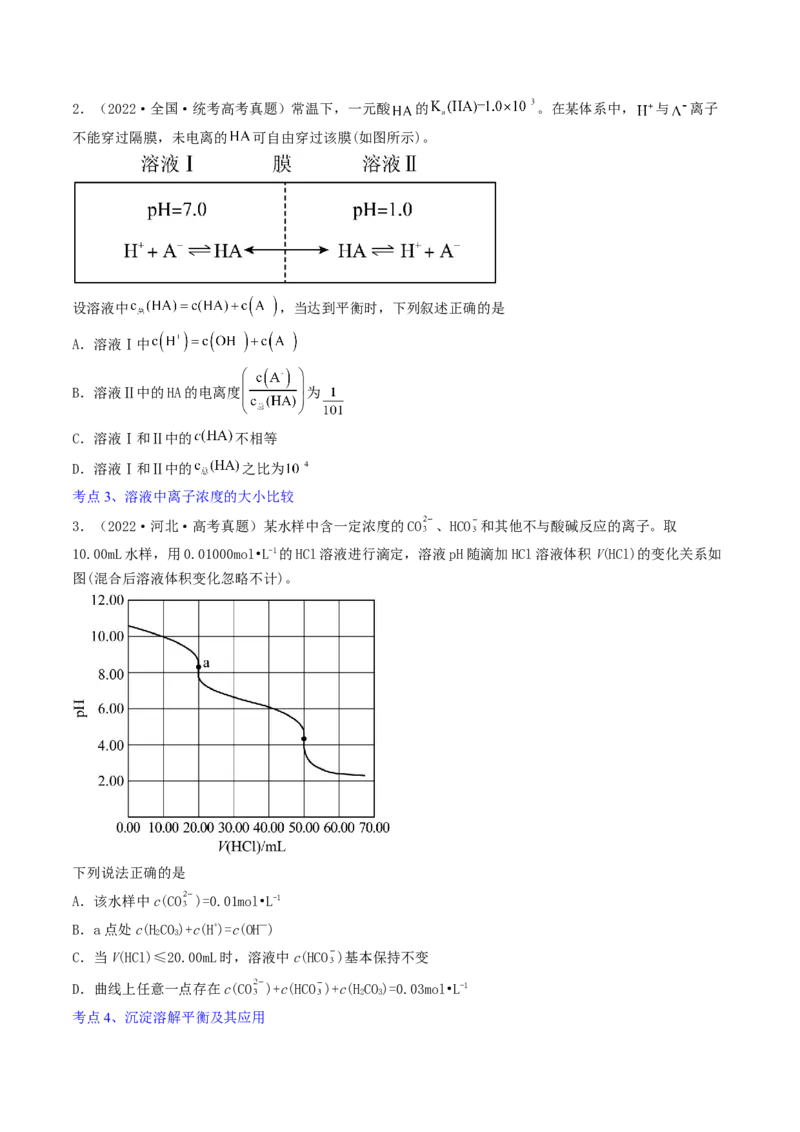
考点2、溶液的酸碱性和中和滴定及其应用2.(2022·全国·统考高考真题)常温下,一元酸 的 。在某体系中, 与 离子
不能穿过隔膜,未电离的 可自由穿过该膜(如图所示)。
设溶液中 ,当达到平衡时,下列叙述正确的是
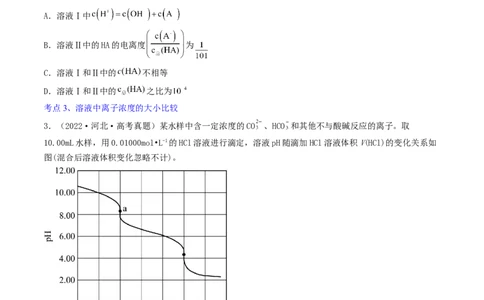
A.溶液Ⅰ中
B.溶液Ⅱ中的HA的电离度 为
C.溶液Ⅰ和Ⅱ中的 不相等
D.溶液Ⅰ和Ⅱ中的 之比为
考点3、溶液中离子浓度的大小比较
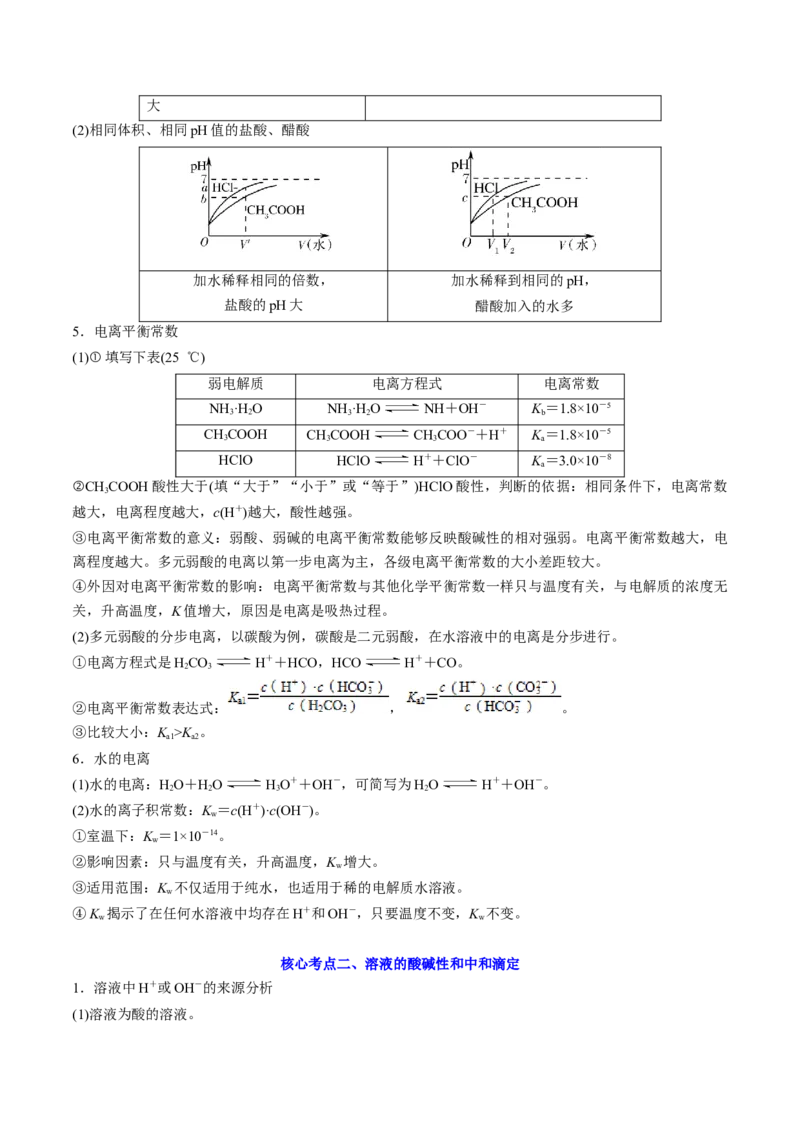
3.(2022·河北·高考真题)某水样中含一定浓度的CO 、HCO 和其他不与酸碱反应的离子。取
10.00mL水样,用0.01000mol•L-1的HCl溶液进行滴定,溶液pH随滴加HCl溶液体积V(HCl)的变化关系如
图(混合后溶液体积变化忽略不计)。
下列说法正确的是
A.该水样中c(CO )=0.01mol•L-1
B.a点处c(HCO)+c(H+)=c(OH—)
2 3
C.当V(HCl)≤20.00mL时,溶液中c(HCO )基本保持不变
D.曲线上任意一点存在c(CO )+c(HCO )+c(HCO)=0.03mol•L-1
2 3
考点4、沉淀溶解平衡及其应用4.(2023·浙江·高考真题)碳酸钙是常见难溶物,将过量碳酸钙粉末置于水中达到溶解平衡:
[已知 , , 的电离常
数 ],下列有关说法正确的是
A.上层清液中存在
B.上层清液中含碳微粒最主要以 形式存在
C.向体系中通入 气体,溶液中 保持不变
D.通过加 溶液可实现 向 的有效转化
1、对点核心素养
(1)变化观念和平衡思想:能以变化观念和平衡思想认识电解质在水溶液中的离子平衡,能运用电离度、电
离平衡常数、水解常数、溶度积常数等,多角度、动态地分析弱电解质的电离平衡、盐类水解平衡和沉淀
溶解平衡,并会用相关原理解决实际问题。
(2)证据推理与模型认知:能运用电离平衡模型、水解平衡、沉淀溶解平衡模型解释化学现象,揭示现象的
本质与规律,培养证据推理与模型认知的核心素养。
(3)科学态度与社会责任感:培养严谨求实的科学态度和探索未知、崇尚真理的意识,能对与盐类水解的应
用,沉淀溶解平衡的应用有关的社会热点问题做出正确的解释和判断,培养科学态度与社会责任感。
2、对点命题分析
水溶液中的离子平衡是历年高考考查的重点和热点,考查方式常以选择题形式呈现。从高考命题的变
化趋势来看,溶液中离子浓度的大小比较及沉淀的溶解平衡和转化是主流试题。试题注重知识的应用,多
以图象、图表的形式,利用平衡移动原理分析外界条件改变对溶液中电离平衡、水解平衡、难溶电解质的
溶解平衡的分析考查,偏重考查粒子浓度大小顺序和溶液中各种守恒关系,使题目具有一定的综合性、灵
活性和技巧性。能较好地考查对知识的迁移能力、灵活应用能力和运用化学用语的能力。溶液中离子浓度
的比较涉及的问题很复杂,其中主要涉及溶液的酸碱性、弱电解质的电离平衡、盐的水解、电离平衡和水
解平衡的移动等。沉淀溶解平衡主要考查沉淀溶解平衡的移动、浓度积的表达式及计算、沉淀的生成与转
化等。
核心考点一、弱电解质的电离平衡
1.正确理解弱酸、弱碱的稀释规律2.一元强酸和一元弱酸的比较
3.弱电解质平衡移动的“三个不一定”
(1)稀醋酸加水稀释时,溶液中不一定所有的离子浓度都减小。因为温度不变,K =c(H+)·c(OH-)是定值,
w
稀醋酸加水稀释时,溶液中的c(H+)减小,故c(OH-)增大。
(2)电离平衡右移,电解质分子的浓度不一定减小,离子的浓度不一定增大,电离程度也不一定增大。
(3)对于浓的弱电解质溶液加HO稀释的过程,弱电解质的电离程度逐渐增大,但离子浓度不一定减小,可
2
能先增大后减小。
4.一元强酸(HCl)与一元弱酸(CHCOOH)稀释图像比较
3
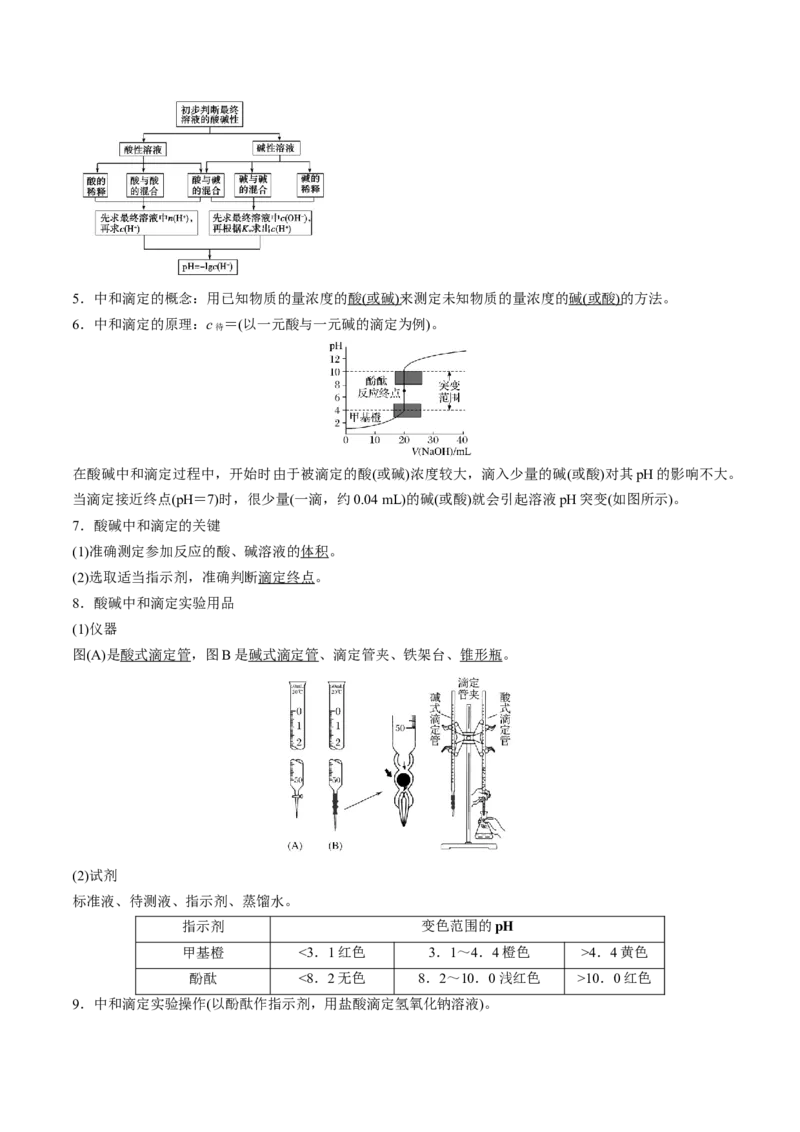
(1)相同体积、相同浓度的盐酸、醋酸
加水稀释相同的倍数,醋酸的pH 加水稀释到相同的pH,盐酸加入的水多大
(2)相同体积、相同pH值的盐酸、醋酸
加水稀释相同的倍数, 加水稀释到相同的pH,
盐酸的pH大 醋酸加入的水多
5.电离平衡常数
(1)①填写下表(25 ℃)
弱电解质 电离方程式 电离常数
NH ·H O NH ·H O NH+OH- K =1.8×10-5
3 2 3 2 b
CHCOOH CHCOOH CHCOO-+H+ K=1.8×10-5
3 3 3 a
HClO HClO H++ClO- K=3.0×10-8
a
②CHCOOH酸性大于(填“大于”“小于”或“等于”)HClO酸性,判断的依据:相同条件下,电离常数
3
越大,电离程度越大,c(H+)越大,酸性越强。
③电离平衡常数的意义:弱酸、弱碱的电离平衡常数能够反映酸碱性的相对强弱。电离平衡常数越大,电
离程度越大。多元弱酸的电离以第一步电离为主,各级电离平衡常数的大小差距较大。
④外因对电离平衡常数的影响:电离平衡常数与其他化学平衡常数一样只与温度有关,与电解质的浓度无
关,升高温度,K值增大,原因是电离是吸热过程。
(2)多元弱酸的分步电离,以碳酸为例,碳酸是二元弱酸,在水溶液中的电离是分步进行。
①电离方程式是HCO H++HCO,HCO H++CO。
2 3
②电离平衡常数表达式: , 。
③比较大小:K >K 。
a1 a2
6.水的电离
(1)水的电离:HO+HO HO++OH-,可简写为HO H++OH-。
2 2 3 2
(2)水的离子积常数:K =c(H+)·c(OH-)。
w
①室温下:K =1×10-14。
w
②影响因素:只与温度有关,升高温度,K 增大。
w
③适用范围:K 不仅适用于纯水,也适用于稀的电解质水溶液。
w
④K 揭示了在任何水溶液中均存在H+和OH-,只要温度不变,K 不变。
w w
核心考点二、溶液的酸碱性和中和滴定
1.溶液中H+或OH-的来源分析
(1)溶液为酸的溶液。溶液中的OH-全部来自水的电离,水电离产生的c(H+)=c(OH-)。如pH=2的盐酸中,溶液中的c(OH-)=
(K /10-2) mol·L-1=10-12 mol·L-1,即由水电离出的c(H+)=c(OH-)=10-12 mol·L-1。
w
(2)溶质为碱的溶液。
溶液中的H+全部来自水的电离,水电离产生的 c(OH-)=c(H+)。如pH=12的NaOH溶液中,溶液中的
c(H+)=10-12 mol·L-1,即由水电离出的c(OH-)=c(H+)=10-12 mol·L-1。
(3)水解呈酸性或碱性的盐溶液。
①pH=5的NH Cl溶液中,H+全部来自水的电离,由水电离的c(H+)=10-5 mol·L-1,因为部分OH-与部
4
分NH结合,溶液中c(OH-)=10-9 mol·L-1。
②pH=12的NaCO 溶液中,OH-全部来自水的电离,由水电离出的c(OH-)=10-2 mol·L-1。
2 3
2.突破溶液酸、碱性判断的四条规律
(1)正盐溶液。
强酸强碱盐溶液显中性,强酸弱碱盐(如NH4Cl)溶液显酸性,强碱弱酸盐(如CH3COONa)溶液显碱性。
(2)酸式盐溶液。
NaHSO (NaHSO=Na++H++SO2-)NaHSO 、NaHCO 、NaHPO 水溶液显酸性(酸式酸根离子的电离程度大于水
4 4 4 3 2 4 2 4
解程度),NaHCO、NaHS、NaHPO 水溶液显碱性(酸式酸根离子的水解程度大于电离程度)。
3 2 4
注意:因为浓度相同的CHCOO-与NH+的水解程度相同,所以CHCOONH 溶液显中性,而NHHCO 溶液略显碱性。
3 4 3 4 4 3
(3)弱酸(或弱碱)及其盐1∶1混合的溶液。
①CHCOOH和CHCOONa混合液呈酸性(等浓度的CHCOOH与CHCOO-,CHCOOH的电离程度大于CHCOO-的水解
3 3 3 3 3 3
程度)。
②NH·HO和NHCl混合溶液呈碱性。
3 2 4
(4)酸碱pH之和等于14等体积混合溶液。
pH之和等于14的意义:酸溶液中的氢离子浓度等于碱溶液中的氢氧根离子的浓度。
已知酸、碱溶液的pH之和为14,则等体积混合时:
强酸、强碱,混合后溶液pH=7,
强酸、弱碱,混合后溶液pH>7,
弱酸、强碱,混合后溶液pH<7。
3.溶液酸碱性判断中的常见误区
(1)误认为溶液的酸碱性取决于pH。如pH=7的溶液在温度不同时,可能呈酸性或碱性,也可能呈中性。
(2)误认为酸碱恰好中和时溶液一定显中性。如强酸和弱碱恰好中和时,溶液显酸性;强碱和弱酸恰好中和
时,溶液显碱性,强酸和强碱恰好中和时,溶液显中性。
(3)使用pH试纸测溶液酸碱性时,若先用蒸馏水润湿,测量结果不一定偏小。先用蒸馏水润湿,相当于将
待测液稀释,若待测液为碱性溶液,则所测结果偏小;若待测液为酸性溶液,则所测液为中性溶液,则所
测结果没有误差。
4.有关pH计算的一般思维模型5.中和滴定的概念:用已知物质的量浓度的 酸 ( 或碱 )来测定未知物质的量浓度的 碱 ( 或酸 )的方法。
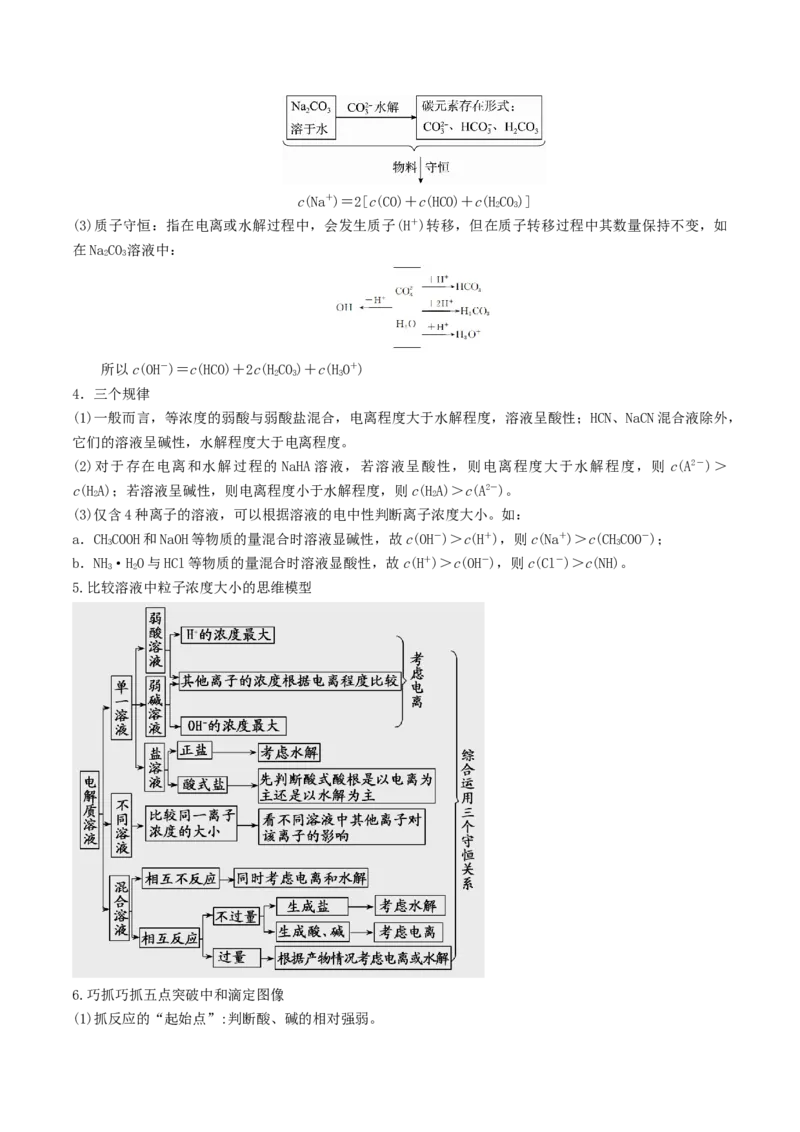
6.中和滴定的原理:c =(以一元酸与一元碱的滴定为例)。
待
在酸碱中和滴定过程中,开始时由于被滴定的酸(或碱)浓度较大,滴入少量的碱(或酸)对其pH的影响不大。
当滴定接近终点(pH=7)时,很少量(一滴,约0.04 mL)的碱(或酸)就会引起溶液pH突变(如图所示)。
7.酸碱中和滴定的关键
(1)准确测定参加反应的酸、碱溶液的体积。
(2)选取适当指示剂,准确判断滴定终点。
8.酸碱中和滴定实验用品
(1)仪器
图(A)是酸式滴定管,图B是碱式滴定管、滴定管夹、铁架台、锥形瓶。
(2)试剂
标准液、待测液、指示剂、蒸馏水。
指示剂 变色范围的pH
甲基橙 <3.1红色 3.1~4.4橙色 >4.4黄色
酚酞 <8.2无色 8.2~10.0浅红色 >10.0红色
9.中和滴定实验操作(以酚酞作指示剂,用盐酸滴定氢氧化钠溶液)。(1)滴定前的准备。
(2)滴定。
(3)终点判断:等到滴入最后一滴反应液,指示剂变色,且在半分钟内不能恢复原来的颜色,视为滴定终点,
并记录标准液的体积。
(4)数据处理:按上述操作重复2~3次,求出用去标准盐酸体积的平均值,根据原理计算。
c(NaOH)=
10.氧化还原滴定的原理及指示剂的选择:
(1)原理:以氧化剂或还原剂为滴定剂,直接滴定一些具有还原性或氧化性的物质,或者间接滴定一些本身
并没有还原性或氧化性,但能与某些还原剂或氧化剂反应的物质。
(2)试剂:常见用于滴定的氧化剂有KMnO 、KCr O 等;常见用于滴定的还原剂有亚铁盐、草酸、维生素
4 2 2 7
C等。
(3)指示剂:氧化还原滴定的指示剂有三类:
①氧化还原指示剂;
②专用指示剂,如在碘量法滴定中,可溶性淀粉溶液遇碘标准溶液变蓝;
③自身指示剂,如高锰酸钾标准溶液滴定草酸时,滴定终点为溶液由无色变为浅红色。
11.沉淀滴定:
(1)概念:沉淀滴定是利用沉淀反应进行滴定、测量分析的方法。生成沉淀的反应很多,但符合条件的却很
少,实际上应用最多的是银量法,即利用Ag+与卤素离子的反应来测定Cl-、Br-、I-浓度。
(2)原理:沉淀滴定所用的指示剂本身就是一种沉淀剂,滴定剂与被滴定物反应的生成物的溶解度要比滴定
剂与指示剂反应的生成物的溶解度小,否则不能用这种指示剂。如用AgNO 溶液测定溶液中Cl-的含量时
3
常以CrO为指示剂,这是因为AgCl比AgCrO 更难溶。
4
12.中和滴定考点归纳
(1)“考”实验仪器。
酸式滴定管、碱式滴定管、滴定管夹(带铁架台)、锥形瓶。其中常考的是滴定管,如正确选择滴定管(包括量
程),滴定管的检漏、洗涤和润洗,滴定管的正确读数方法等。(2)“考”操作步骤。
①滴定前的准备:检漏、洗涤、润洗、充液(赶气泡)、调液面、读数。
②滴定:移液、滴加指示剂、滴定至终点、读数。
③计算。
(3)“考”指示剂的选择。
①强酸强碱相互滴定,可选用甲基橙或酚酞。
②若反应生成强酸弱碱盐,溶液呈酸性,则选用酸性变色范围的指示剂(甲基橙),若反应生成强碱弱酸盐,溶液
呈碱性,则选用碱性变色范围的指示剂(酚酞)。
③石蕊溶液因颜色变化不明显,且变色范围过宽,一般不用作指示剂。
(4)“考”误差分析。
写出计算式,分析操作对V标的影响,由计算式得出对最终测定结果的影响,切忌死记硬背结论。此外对读数
时视线(俯视、仰视)问题的判断要学会画图分析。
(5)“考”数据处理。
正确“取舍”数据,计算“平均”体积,根据反应式确定标准液与待测液浓度和体积的关系,从而列出公式进
行计算。
核心考点三、溶液中离子浓度大小比较
1.同一溶液中,不同粒子浓度大小比较的方法
(1)正盐溶液:基本遵循c(不水解离子)>c(水解离子)>c(显性离子),当水解离子浓度是不水解离子浓度的
数倍时,顺序提前。例如在浓度为c mol·L-1的醋酸钠溶液中,有c(Na+)>c(CHCOO-)>c(OH-)>c(H+);
3
在浓度为c mol·L-1的硫酸铵溶液中,有c(NH)>c(SO)>c(H+)>c(OH-)。
(2)酸式盐溶液:对于电离为主的,如 NaHSO ,遵循c(自身)>c(电离产物)>c(水解产物),即c(Na
3
+)>c(HSO)>c(H+)>c(SO)>c(OH-)>c(HSO);对于水解为主的,如 NaHCO ,遵循 c(自身)>c(水解产
2 3 3
物)>c(电离产物),即c(Na+)>c(HCO)>c(OH-)>c(HCO)>c(H+)>c(CO)。
2 3
(3)缓冲溶液:例如0.2 mol·L-1氨水与0.2 mol·L-1氯化铵溶液等体积混合后,溶液以电离为主,显碱
性(常见物质中除了氢氰酸和氰化物,都以电离为主),所以氢氧根离子浓度大于氢离子浓度,再根据电荷
守恒可知,铵根离子浓度大于氯离子浓度,即c(NH)>c(Cl-)>c(OH-)>c(H+)。
2.弱酸弱碱盐溶液的酸碱性
弱酸弱碱盐双水解,其溶液的酸碱性取决于弱酸和弱碱的相对强弱。当 K=K时,溶液显中性,如
a b
CHCOONH;当K>K时,溶液显酸性,如HCOONH;当KK。
c sp
(3)曲线下方区域的点均为不饱和溶液,此时Qc(MOH)(3)水的电离程度:d>c>a=b (3)水的电离程度:a>b
二、K和K 图像
W sp
1.曲线型
不同温度下水溶液中c(H+)与c(OH-)的变 常温下,CaSO 在水中的沉淀溶解平衡曲线
4
化曲线 [K=9×10-6]
sp
(1)A、C、B三点均为中性,温度依次升高,K
W (1)a、c点在曲线上,a→c的变化为增大c(SO2−
),如加
4
依次增大
入NaSO 固体,但K 不变
(2)D点为酸性溶液,E点为碱性溶液,K=1×10- 2 4 sp
W
(2)b点在曲线的上方,Q>K,将会有沉淀生成
14 c sp
(3)d点在曲线的下方,QCaCO>MnCO。
4 3 3
③X点对CaSO 要析出沉淀,对CaCO 是不饱和溶液,能继续溶解CaCO。
4 3 3
④Y点:c(SO2− )>c(Ca2+),二者的浓度积等于10-5;Z点:c(CO2− )7,强酸与
弱碱反应终点是pH<7
考点一、弱电解质(包括水)的电离平衡
【高考解密】本考点主要考查强弱电解质的判断与比较、弱电解质溶液中离子浓度大小比较、电离常数的
应用,是高考新增热点,一般以选择题的形式出现。解题的关键是明确强、弱电解质的概念、电离平衡及
其影响因素。
例1.(2022·浙江·模拟预测)下列说法不正确的是
A.将纯水加热, 增大, 不变,仍为中性
B.常温下,向 的 溶液中加入少量 固体,溶液的 增大,说明溶液存在电离平衡
C.常温下,酸式盐 的 ,则 一定是弱酸
D.常温下,等 的盐酸和醋酸溶液加水稀释10倍后,
【变式训练1】(考查判断电解质强弱)(2022·浙江·模拟预测)下列物质属于强电解质的是
A. B. C. D.
【变式训练2】(考查影响电离平衡的因素)(2022·浙江·模拟预测) 水溶液中存在电离平衡:
, 。下列说法正确的是
A.若向 溶液中加水,平衡向右移动,溶液中氢离子浓度增大
B.若向 溶液中滴加少量新制氯水,平衡向左移动,溶液pH减小
C.若向 溶液中通入过量 气体,平衡向左移动,溶液pH增大
D.若向 溶液中加入少量硫酸铜固体(忽略溶液体积变化),溶液中所有离子浓度都减小
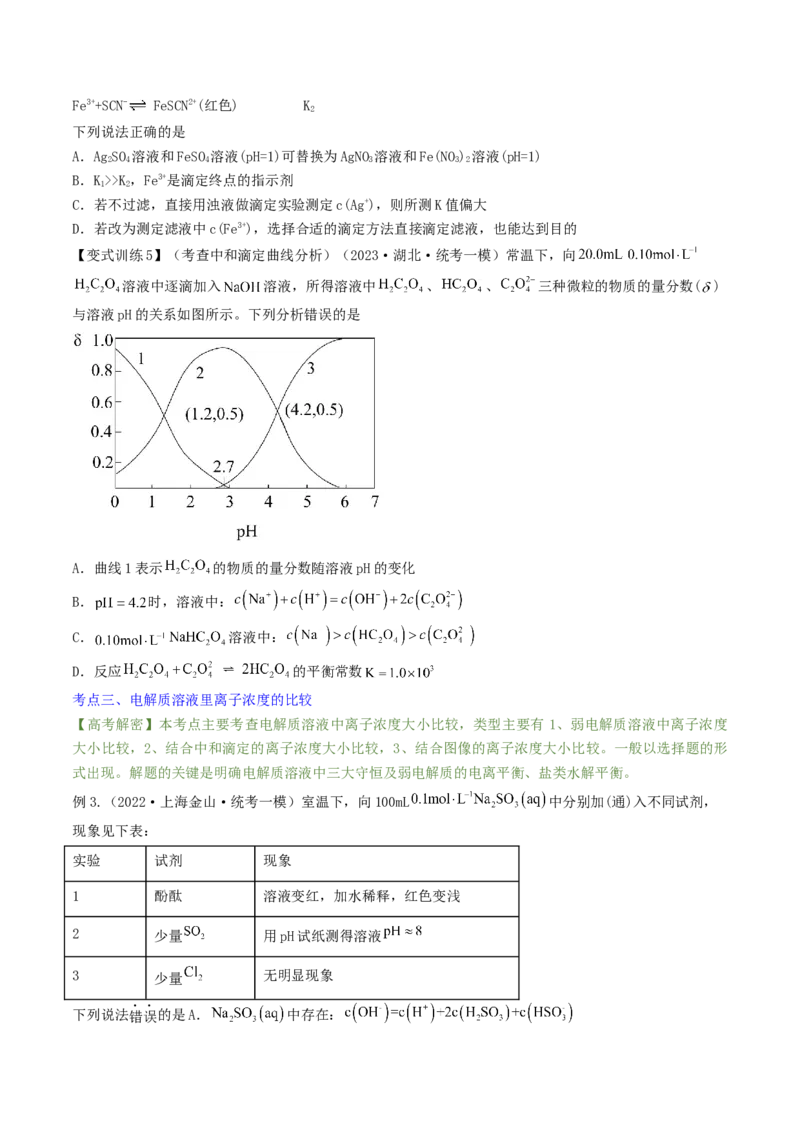
【变式训练3】(考查电解质溶液稀释图象)(2021·浙江绍兴·校考模拟预测)T℃,分别向10mL浓度
均为1mol/L的两种弱酸HA、HB中不断加水稀释,并用pH传感器测定溶液pH。所得溶液pH的两倍(2pH)与
溶液浓度的常用对数(lgc)的关系如图所示。下列叙述正确的是
A.弱酸HB的K = 1×10-5
a
B.a点对应的溶液中c(HA) = 0.1mol/L,pH = 4
C.将1mol/L的HA和HB溶液等体积混合,所得溶液pH为2
D.将pH相同的HA和HB溶液稀释相同倍数,HB稀溶液的pH更大
【变式训练4】(考查电离平衡常数及其应用)(2022·浙江·模拟预测)常温下,
, , ,下列说法正确的是
A.浓度均为 的 和 溶液中阳离子的物质的量浓度之和:前者小于后者
B.用相同浓度的 溶液分别滴定等体积 均为3的 和 溶液至终点,消耗
溶液的体积相等
C. 溶液与 溶液等体积混合后的溶液中:
D. 与 盐酸等体积混合后的溶液 中:考点二、溶液的酸碱性和中和滴定
【高考解密】本考点主要考查溶液酸碱性的判断和酸碱中和滴定及其应用,一般以选择题和填空题的形式
出现。解题的关键是明确溶液酸碱性的判断方法及中和滴定原理及其操作。
例2.(2022·浙江·模拟预测) 时,下列说法正确的是
A. 为5的氯水和 为5的 溶液混合, 仍为5
B.物质的量浓度相同的 溶液和 溶液, 的数值前者大
C. 相同的醋酸和盐酸,分别与足量的锌粒反应,前者产生的氢气一定大于后者
D.某溶液中水电离出的 ,则该溶液中的溶质可能为酸、碱或盐
【变式训练1】(考查溶液酸碱性判断)(2022·上海黄浦·统考二模)下列溶液一定呈中性的是
A. 的溶液 B.等物质的量的强酸和强碱反应得到的溶液
C.c(H+)=c(OH—)的溶液 D.紫色石蕊试液不变色的溶液
【变式训练2】(考查滴定实验仪器的使用及酸碱中和滴定)(2022·云南昆明·昆明一中校考模拟预
测)测定某氢氧化钠样品中NaOH的含量,主要操作步骤为:①称取一定质量的样品溶于水中;②转移、定
容得待测液;③取20.00 mL待测液,用HCl标准溶液滴定。完成上述操作,下列仪器中不需要用到的有
A.1种 B.2种 C.3种 D.4种
【变式训练3】(考查酸碱中和滴定误差分析)(2022·上海虹口·统考模拟预测)用已知浓度盐酸滴定
未知浓度 溶液,甲基橙作指示剂。若测定结果偏低,可能原因是
A.滴定管用蒸馏水洗净后未用盐酸润洗
B.盛装待测液的锥形瓶水洗后未烘干
C.滴定过程中振荡锥形瓶时不慎有少量液体溅出
D.滴定至锥形瓶中溶液颜色由橙变红,且 内不改变时停止
【变式训练4】(考查酸碱中和滴定原理的应用——氧化还原滴定和沉淀滴定)(2022·北京海淀·北大
附中校考三模)某同学设计实验方案,利用沉淀滴定法测定“Ag++Fe2+ Fe3++Ag↓”的平衡常数K。一定
温度下,先将0.0100mol·L-1AgSO 溶液与0.0400mol·L-1FeSO 溶液(pH=1)等体积混合,待反应达到平衡
2 4 4
时,过滤,取vmL滤液用cmol·L-1KSCN标准溶液滴定Ag+,至出现稳定的浅红色时消耗KSCN标准溶液
1
vmL。
1
已知:Ag++SCN- AgSCN↓(白色) K
1Fe3++SCN- FeSCN2+(红色) K
2
下列说法正确的是
A.AgSO 溶液和FeSO 溶液(pH=1)可替换为AgNO 溶液和Fe(NO) 溶液(pH=1)
2 4 4 3 3 2
B.K>>K,Fe3+是滴定终点的指示剂
1 2
C.若不过滤,直接用浊液做滴定实验测定c(Ag+),则所测K值偏大
D.若改为测定滤液中c(Fe3+),选择合适的滴定方法直接滴定滤液,也能达到目的
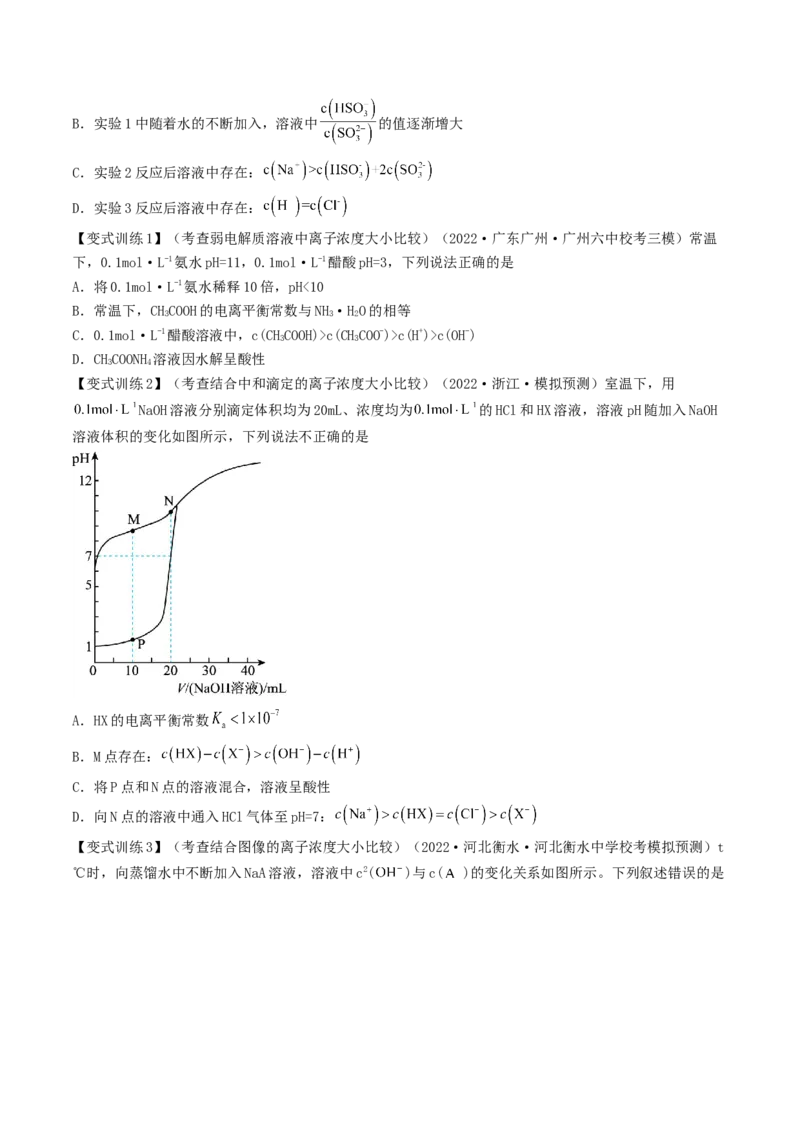
【变式训练5】(考查中和滴定曲线分析)(2023·湖北·统考一模)常温下,向
溶液中逐滴加入 溶液,所得溶液中 、 、 三种微粒的物质的量分数( )
与溶液pH的关系如图所示。下列分析错误的是
A.曲线1表示 的物质的量分数随溶液pH的变化
B. 时,溶液中:
C. 溶液中:
D.反应 的平衡常数
考点三、电解质溶液里离子浓度的比较
【高考解密】本考点主要考查电解质溶液中离子浓度大小比较,类型主要有 1、弱电解质溶液中离子浓度
大小比较,2、结合中和滴定的离子浓度大小比较,3、结合图像的离子浓度大小比较。一般以选择题的形
式出现。解题的关键是明确电解质溶液中三大守恒及弱电解质的电离平衡、盐类水解平衡。
例3.(2022·上海金山·统考一模)室温下,向100mL 中分别加(通)入不同试剂,
现象见下表:
实验 试剂 现象
1 酚酞 溶液变红,加水稀释,红色变浅
2 少量 用pH试纸测得溶液
3 少量 无明显现象
下列说法错误的是A. 中存在:B.实验1中随着水的不断加入,溶液中 的值逐渐增大
C.实验2反应后溶液中存在:
D.实验3反应后溶液中存在:
【变式训练1】(考查弱电解质溶液中离子浓度大小比较)(2022·广东广州·广州六中校考三模)常温
下,0.1mol·L-1氨水pH=11,0.1mol·L-1醋酸pH=3,下列说法正确的是
A.将0.1mol·L-1氨水稀释10倍,pH<10
B.常温下,CHCOOH的电离平衡常数与NH·HO的相等
3 3 2
C.0.1mol·L-1醋酸溶液中,c(CHCOOH)>c(CHCOO-)>c(H+)>c(OH-)
3 3
D.CHCOONH 溶液因水解呈酸性
3 4
【变式训练2】(考查结合中和滴定的离子浓度大小比较)(2022·浙江·模拟预测)室温下,用
NaOH溶液分别滴定体积均为20mL、浓度均为 的HCl和HX溶液,溶液pH随加入NaOH
溶液体积的变化如图所示,下列说法不正确的是
A.HX的电离平衡常数
B.M点存在:
C.将P点和N点的溶液混合,溶液呈酸性
D.向N点的溶液中通入HCl气体至pH=7:
【变式训练3】(考查结合图像的离子浓度大小比较)(2022·河北衡水·河北衡水中学校考模拟预测)t
℃时,向蒸馏水中不断加入NaA溶液,溶液中c2( )与c( )的变化关系如图所示。下列叙述错误的是A.当溶液中c( )=2× mol/L时,有c( ) > 5× mol/L
B.该温度下, 的水解常数K 的数量级为
h
C.溶液中:c(HA)+c( ) = c( )
D.x点溶液中:c( ) > c( ) > c(HA) > c( )
考点四、沉淀的溶解平衡
【高考解密】本考点主要考查高考考查的重点与热点,沉淀溶解平衡主要考点有三个:一是考查溶解平衡
的移动及平衡的建立;二是结合图象,考查溶度积的应用及影响因素;三是沉淀反应在生产、科研、环保
中的应用。难溶电解质的溶解平衡在近几年来一直是考查的重点,预计今后这部分知识可能和元素化合物、
工艺流程、实验等相关知识点组成综合性比较强的题目。解题的关键是理解难溶电解质的溶解平衡及影响
因素、溶度积及其应用。
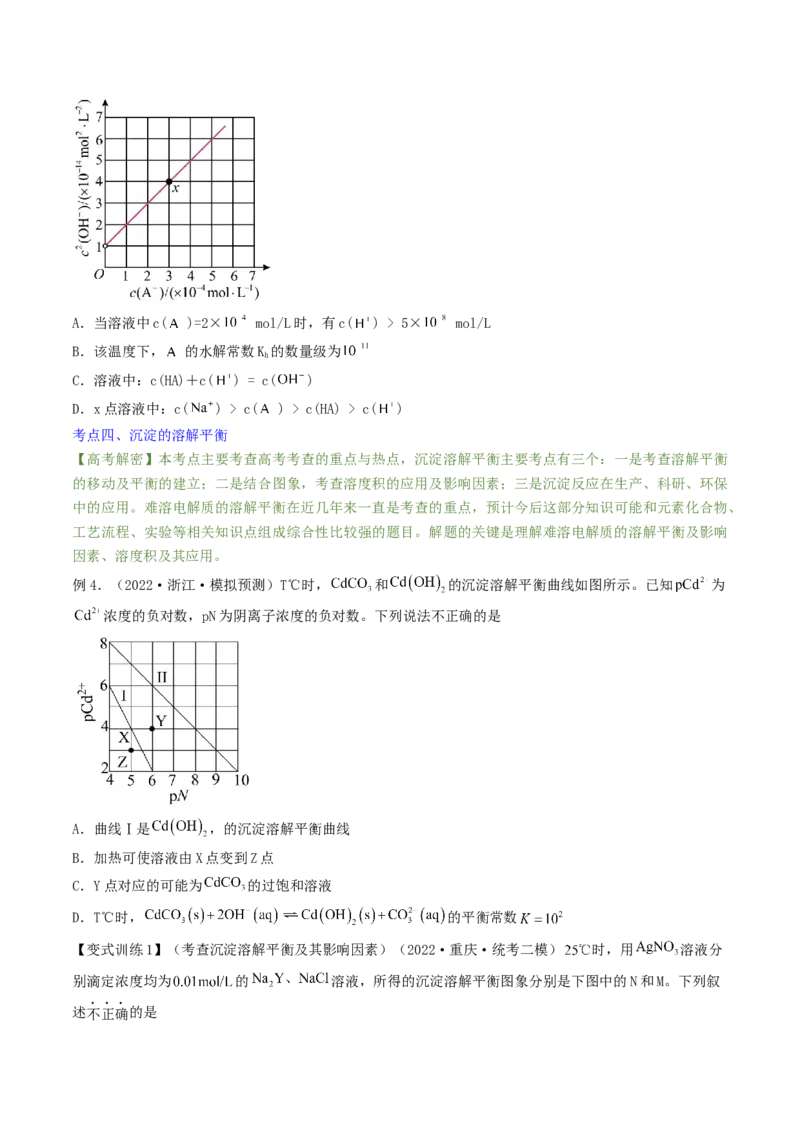
例4.(2022·浙江·模拟预测)T℃时, 和 的沉淀溶解平衡曲线如图所示。已知 为
浓度的负对数,pN为阴离子浓度的负对数。下列说法不正确的是
A.曲线Ⅰ是 ,的沉淀溶解平衡曲线
B.加热可使溶液由X点变到Z点
C.Y点对应的可能为 的过饱和溶液
D.T℃时, 的平衡常数
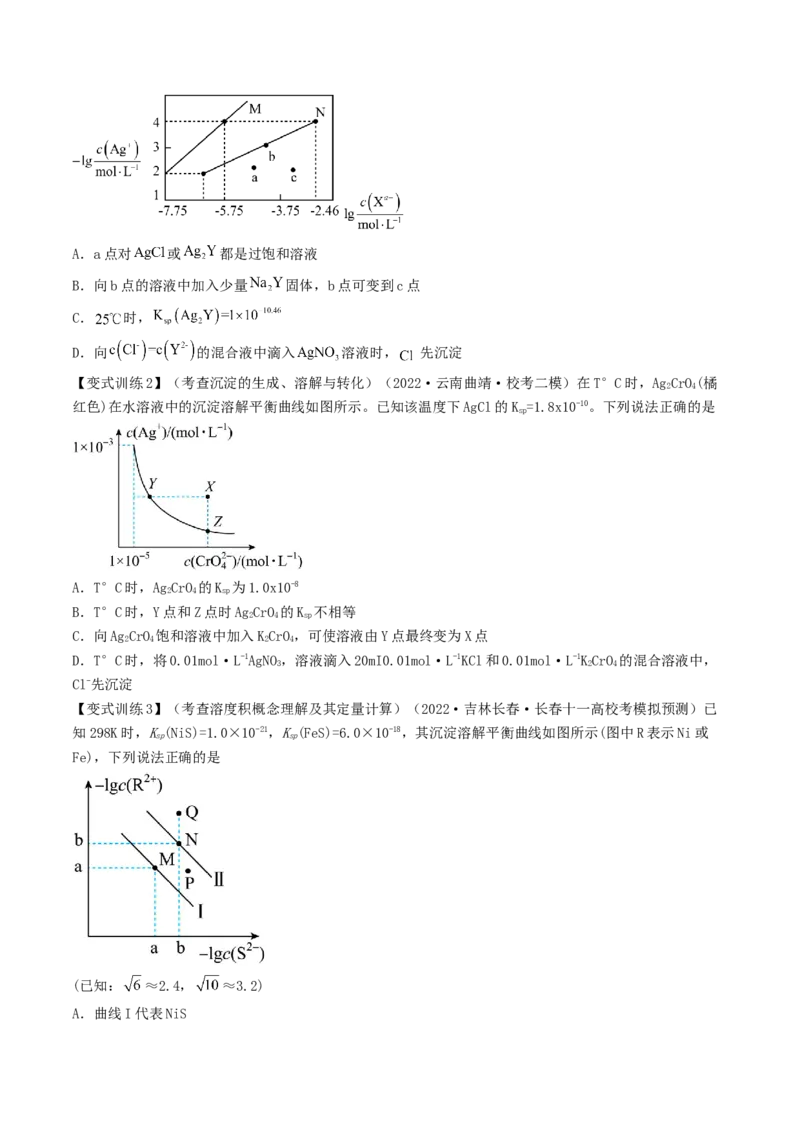
【变式训练1】(考查沉淀溶解平衡及其影响因素)(2022·重庆·统考二模) 时,用 溶液分
别滴定浓度均为 的 溶液,所得的沉淀溶解平衡图象分别是下图中的N和M。下列叙
述不正确的是A.a点对 或 都是过饱和溶液
B.向b点的溶液中加入少量 固体,b点可变到c点
C. 时,
D.向 的混合液中滴入 溶液时, 先沉淀
【变式训练2】(考查沉淀的生成、溶解与转化)(2022·云南曲靖·校考二模)在T°C时,AgCrO(橘
2 4
红色)在水溶液中的沉淀溶解平衡曲线如图所示。已知该温度下AgCl的K =1.8x10-10。下列说法正确的是
sp
A.T°C时,AgCrO 的K 为1.0x10-8
2 4 sp
B.T°C时,Y点和Z点时AgCrO 的K 不相等
2 4 sp
C.向AgCrO 饱和溶液中加入KCrO,可使溶液由Y点最终变为X点
2 4 2 4
D.T°C时,将0.01mol·L-1AgNO,溶液滴入20mI0.01mol·L-1KCl和0.01mol·L-1KCrO 的混合溶液中,
3 2 4
Cl-先沉淀
【变式训练3】(考查溶度积概念理解及其定量计算)(2022·吉林长春·长春十一高校考模拟预测)已
知298K时,K(NiS)=1.0×10-21,K(FeS)=6.0×10-18,其沉淀溶解平衡曲线如图所示(图中R表示Ni或
sp sp
Fe),下列说法正确的是
(已知: ≈2.4, ≈3.2)
A.曲线I代表NiSB.FeS+Ni2+ NiS+Fe2+的平衡常数K=60000
⇌
C.与P点相对应的FeS的分散系是均一稳定的
D.M点对应的溶液中,c(S2-)≈3.2×10-11 mol•L-1