文档内容
高频考点 20 氨气和铵盐
题点(一)氨气和铵盐的性质
1.(2022·江苏卷)氮及其化合物的转化具有重要应用。下列说法不正确的是( )
A.自然固氮、人工固氮都是将 转化为
B.侯氏制碱法以 、 、 、 为原料制备 和
C.工业上通过 催化氧化等反应过程生产
D.多种形态的氮及其化合物间的转化形成了自然界的“氮循环”
1. A A.自然固氮是将N 转化为含氮化合物,不一定是转化为NH,比如大气固氮是将N 会转化为NO,A
2 3 2
错误;B.侯氏制碱法以HO、NH、CO、NaCl为原料制备NaHCO 和NHCl,反应的化学方程式为
2 3 2 3 4
HO+NH+CO+NaCl=NaHCO↓+NHCl,B正确;C.工业上通过NH 催化氧化等反应过程生产HNO,相关的化学
2 3 2 3 4 3 3
反应方程式为4NH+5O 4NO+6HO、2NO+O=2NO、3NO+HO=2HNO+NO、4NO+O+2HO=4HNO,C正确;
3 2 2 2 2 2 2 3 2 2 2 3
D.氮元素在自然界中既有游离态又有化合态,多种形态的氮及其化合物间的转化形成了自然界的“氮循
环”,D正确;故选A。
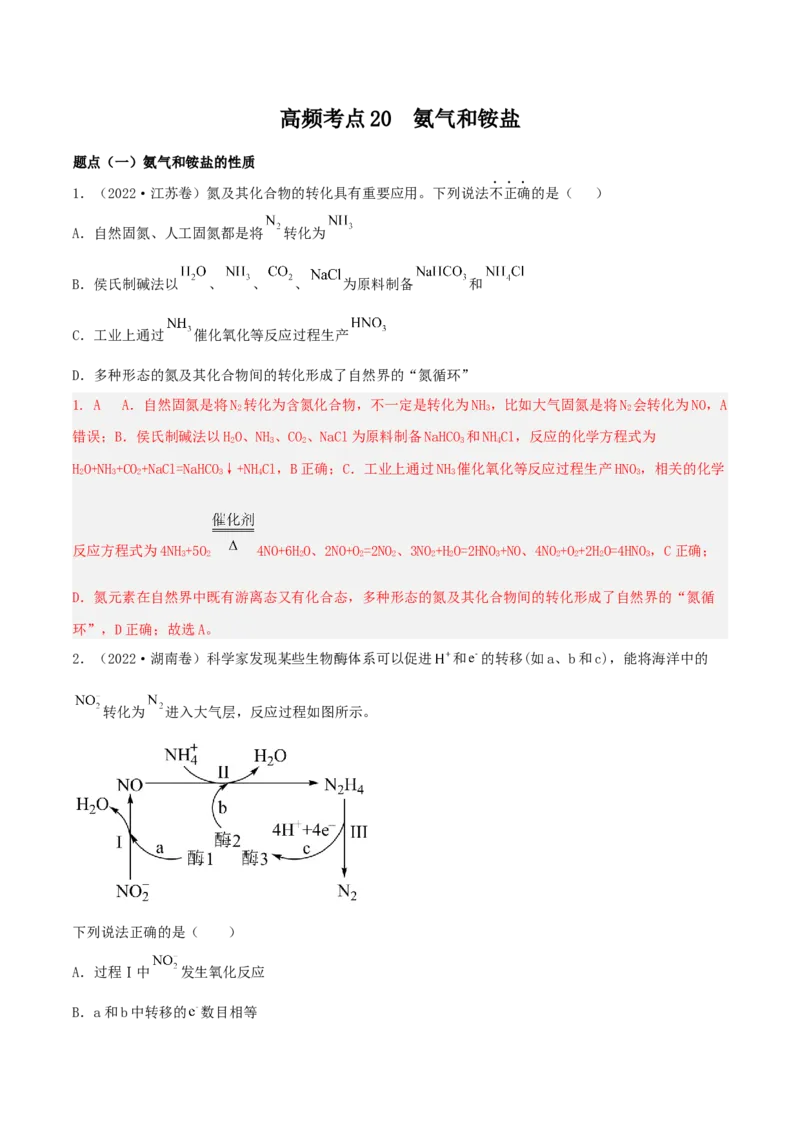
2.(2022·湖南卷)科学家发现某些生物酶体系可以促进 和 的转移(如a、b和c),能将海洋中的
转化为 进入大气层,反应过程如图所示。
下列说法正确的是( )
A.过程Ⅰ中 发生氧化反应
B.a和b中转移的 数目相等C.过程Ⅱ中参与反应的
D.过程Ⅰ→Ⅲ的总反应为
2.D A.由图示可知,过程I中NO 转化为NO,氮元素化合价由+3价降低到+2价,NO 作氧化剂,被还
原,发生还原反应,A错误;B.由图示可知,过程I为NO 在酶1的作用下转化为NO和HO,依据得失电
2
子守恒、电荷守恒和原子守恒可知,反应的离子方程式为:NO +2H++e- NO+HO,生成1molNO,a过程转
2
移1mole-,过程II为NO和NH 在酶2的作用下发生氧化还原反应生成HO和NH,依据得失电子守恒、电
2 2 4
荷守恒和原子守恒可知,反应的离子方程式为:NO+NH +3e-+2H+ HO+NH,消耗1molNO,b过程转移
2 2 4
4mol e-,转移电子数目不相等,B错误;C.由图示可知,过程II发生反应的参与反应的离子方程式为:
NO+NH +3e-+2H+ HO+NH,n(NO):n(NH )=1:1,C错误;D.由图示可知,过程I的离子方程式为NO +2H+
2 2 4
+e- NO+HO,过程II的离子方程式为NO+NH +3e-+2H+ HO+NH,过程III的离子方程式为NH
2 2 2 4 2 4
N↑+4H++4e-,则过程Ⅰ→Ⅲ的总反应为NO + NH = N↑+2HO,D正确;答案选D。
2 2 2
3.(2022·上海黄浦·二模)用下图装置吸收中学常见的某种气体,上层溶液变红。有关该气体的描述
错误的是( )A.具有刺激性气味 B.可用作制冷剂 C.属于碱 D.含有极性键
3.C A.NH 是一种有强烈的刺激性气味的气体,A正确;B.液氨气化过程中吸收热量,可用作制冷剂,
3
B正确;C.氨气是氮的氢化物,溶于水生成碱一水合氨,氨气不属于碱,C错误;D.NH 含有3条N-H键,
3
为极性键,D正确;答案选C。
4.(双选)(2022·广东高三期中)美好生活离不开化学。下列人类活动中,运用了相应的化学原理的
是( )
选项 人类活动 化学原理
A NHCl溶液除铁锈 NH 水解呈酸性
4
B 游轮底部定期更换锌块 利用原电池原理可防止腐蚀
C 铝罐贮运浓硝酸 铝具有良好导热性
D NHHCO 可用作氮肥 NHHCO 受热易分解
4 3 4 3
4.AB A.NHCl溶液由于NH 水解呈酸性NH +HO NH∙HO+H+,H+可以和铁锈反应,故NHCl溶液常用于
4 2 3 2 4
除铁锈,A符合题意;B.在游轮底部连接一块锌块,这样锌、铁和海水中的电解质溶液能够形成原电池,
由于锌比铁活泼,锌作负极,只需定期更换锌块就能达到保护船体的作用,故利用的是原电池原理,B符
合题意;C.铝在常温下被浓硝酸钝化后,在表面形成了一层致密的氧化物保护膜后,阻止金属铝继续与
浓硝酸反应,故常温下用铝罐贮运浓硝酸,与金属铝的导热性无关,C不合题意;D.NHHCO 可用作氮肥是
4 3
由于其中含有N元素,与其受热易分解无关,D不合题意;故答案为:AB。
5.(2022·广东·高三开学考试)下列性质与用途均正确且具有对应关系的是( )
选项 物质性质 物质用途A 氮气有还原性 可用作食品包装袋中的保护气
B 受热易分解 可用作氨肥
C 液氨分解吸热 可用作制冷剂
D 硝酸铵溶于水吸热 可用于制作医用速冷冰袋
A.A B.B C.C D.D
5.D A.氮气用作保护气是因为氮气性质稳定,不易发生化学反应,A不符合题意;B. 用作氮
肥是因为其含有N元素,与其受热易分解没有直接关系,B不符合题意;C.液氨汽化时吸收大量的热,可
用作制冷剂,C不符合题意;D. 溶于水吸热,可以使环境温度降低,用于制作医用速冷冰袋,D符
合题意;故选D。
6.(2022·全国·高三专题练习)氨催化氧化是工业制硝酸的重要反应:4NH(g)+5O(g) 4NO(g)
3 2
+6HO(g) ΔH<0。在T℃时,向1L密闭容器中投入4molNH、5molO,平衡时测得NH 的转化率为60%。在
2 3 2 3
指定条件下,下列选项所示的物质间转化不能实现的是( )
A.NH·HO(aq) NHHSO B.HNO(浓) NO
3 2 4 4 3 2
C.NHCl NH D.NO N
4 3 2
6.A A.一水合氨与SO 反应生成NHHSO 或(NH)SO,A符合题意;B.浓硝酸不稳定,光照条件下分解
2 4 3 4 2 3
生成NO、HO和O,B不符合题意;C.氯化铵不稳定,受热分解生成NH 和HCl,C不符合题意;D.NO与
2 2 2 3
CO在催化剂作用下可发生氧化还原反应生成N 和CO,D不符合题意;故选A。
2 2
7.(2022·北京二中高三阶段练习)某同学进行如下实验:
实验步骤 实验现象
试纸变蓝色(pH≈10),试管中部有
将NHCl固体加入试管中,并将湿润的
4 白色固体附着
Ⅰ pH试纸置于试管口,试管口略向下倾
斜,对试管底部进行加热
收集试管口气体溶于水,将溶液滴在
Ⅱ 试纸颜色无明显变化(pH≈7)
pH试纸上
试纸变红色(pH≈2)
继续加热试管一段时间后,将湿润的
Ⅲ
pH试纸置于试管口
下列说法不正确的是( )A.根据I中试纸颜色变化,说明氨气比氯化氢气体扩散速率快
B.根据Ⅱ颜色无明显变化,说明试管口收集到的气体是等物质的量的氨气和氯化氢
C.Ⅲ中试纸变成红色,不是由于NHCl水解造成的
4
D.根据试管中部有白色固体附着,说明不宜用加热NHC1的方法制备NH
4 3
7.B A.根据I中试纸颜色变化即试纸变蓝色(pH≈10),已知氨气溶于水呈碱性,故能说明氨气比氯化氢
气体扩散速率快,A正确;B.已知NH+HCl=NHCl,而NHCl为强酸弱碱盐,水解呈酸性,故根据Ⅱ颜色无
3 4 4
明显变化,说明试管口收集到的气体中氨气较多,不可能是等物质的量的氨气和氯化氢,B错误;C.继续
加热试管,Ⅲ中试纸变成红色(pH≈2),与NHCl分解产生的HCl有关,而不是由于NHCl水解造成的,C
4 4
正确;D.氯化铵分解后,在试管中部化合生成氯化铵,则不宜用加热NHCl的方法制备NH,D正确;故答
4 3
案为B。
题点(二)与氨气制备相关的实验
8.(2021·全国)实验室制备下列气体的方法可行的是( )
气体 方法
A 氨气 加热氯化铵固体
B 二氧化氮 将铝片加到冷浓硝酸中
C 硫化氢 向硫化钠固体滴加浓硫酸
D 氧气 加热氯酸钾和二氧化锰的混合物
A.A B.B C.C D.D
8.D A.氯化铵不稳定,加热易分解生成氨气和氯化氢,但两者遇冷又会化合生成氯化铵固体,所以不
能用于制备氨气,A不可行;B.将铝片加到冷浓硝酸中会发生钝化现象,不能用于制备二氧化氮,B不可
行;C.硫化氢为还原性气体,浓硫酸具有强氧化性,不能用浓硫酸与硫化钠固体反应制备该硫化氢气体,
因为该气体会与浓硫酸发生氧化还原反应,C不可行;D.实验室加热氯酸钾和二氧化锰的混合物,生成氯
化钾和氧气,二氧化锰作催化剂,可用此方法制备氧气,D可行;故选D。
9.(2021·云南昆明市·高三月考)用图示装置(夹持仪器略)及所给试剂能够制取并收集相应气体的是
()
选项 A B C D
KClO
X中试剂 浓氨水 浓硫酸 稀硝酸
3
Y中试剂 CaO CaF MnO Cu
2 2气体 NH HF O NO
3 2
9.D A.NH 极易溶解于水,不能用排水集气法收集,A错误;B.HF可腐蚀玻璃,不能用玻璃仪器制取,
3
且HF极易溶解于水,不能用排水集气法收集,B错误;C.MnO 催化KClO 热分解制取O,应选用固体加热
2 3 2
制气体的发生装置,C错误;D.稀硝酸与Cu在常温下就能发生反应,产物NO难溶于水,可用排水集气法
收集,D正确;故选:D。
10.(2022·潍坊高三期末)某学习小组设计实验探究NH 与CuO的反应,所选择的装置及操作正确的是
3
( )
A B C D
制备NH 干燥NH 验证NH 能还原CuO 吸收NH 尾气
3 3 3 3
10.C A.加热分解NHCl,会得到氨气与氯化氢,两者迅速结合生成氯化铵,故制备NH 不能用加热分解
4 3
NHCl的方法,A项错误;B.NH 会与CaCl 发生反应,不能用无水CaCl 干燥NH,要用碱石灰干燥NH,B
4 3 2 2 3 3
项错误;C.气体与固体反应,可选择此装置,如果发生反应,则固体由黑色变为红色,C项正确;D.装
置中的NH 能与水直接接触,无法防倒吸,D项错误;答案选C。
3
11.(2022·上海徐汇·三模)水合肼( )可用作还原剂。其制备原理为:
。用下图装置制取水合肼的相关说法正确的是( )
A.装置的连接顺序:f→a→b→d→c→e B.装置M可快速制
C.可用 代替水 D.操作过程中要快速滴加NaClO溶液11.B A.M中制备氨气,氨气通过安全瓶防倒吸,为使氨气充分反应,氨气由长导管通入次氯酸钠溶液
中反应生成水合肼,最后尾气处理,装置的连接顺序为f→a→b→c→d→e,故A错误;B.氧化钙和水反
应生成氢氧化钙,该反应放热,温度升高,氢氧化钙使氨水中氢氧根离子浓度增大,所以装置M可快速制
,故B正确 ;C.水吸收尾气,氨气难溶于四氯化碳,不能用 代替水,故C错误;D.次氯酸钠
具有氧化性,若操作过程中快速滴加NaClO溶液,可能 被NaClO氧化,故D错误;选B。