文档内容
高频考点 25 离子交换膜作用
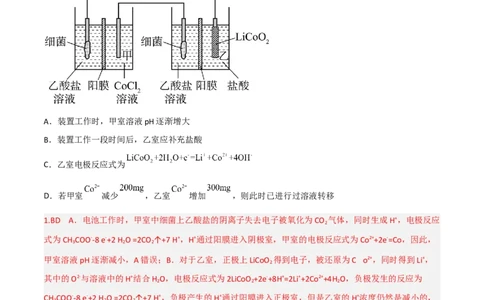
1.(双选)(2022·山东卷)设计如图装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸盐生
成 ,将废旧锂离子电池的正极材料 转化为 ,工作时保持厌氧环境,并定时将乙室溶液
转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法正确的是( )
A.装置工作时,甲室溶液pH逐渐增大
B.装置工作一段时间后,乙室应补充盐酸
C.乙室电极反应式为
D.若甲室 减少 ,乙室 增加 ,则此时已进行过溶液转移
1.BD A.电池工作时,甲室中细菌上乙酸盐的阴离子失去电子被氧化为CO 气体,同时生成H+,电极反应
2
式为CH COO--8 e-+2 H O =2CO ↑+7 H+,H+通过阳膜进入阴极室,甲室的电极反应式为Co2++2e-=Co,因此,
3 2 2
甲室溶液pH逐渐减小,A错误;B.对于乙室,正极上LiCoO 得到电子,被还原为C o2+,同时得到Li+,
2
其中的O2-与溶液中的H+结合H O,电极反应式为2LiCoO +2e-+8H+=2Li++2Co2++4H O,负极发生的反应为
2 2 2
CH COO--8 e-+2 H O =2CO ↑+7 H+,负极产生的H+通过阳膜进入正极室,但是乙室的H+浓度仍然是减小的,
3 2 2
因此电池工作一段时间后应该补充盐酸,B正确;C.电解质溶液为酸性,不可能大量存在OH-,乙室电极
反应式为:LiCoO +e-+4H+=Li++Co2++2H O,C错误;D.若甲室Co2+减少200 mg,则电子转移物质的量为
2 2
n(e-)= ;若乙室Co2+增加300 mg,则转移电子的物质的量为n(e-)=,由于电子转移的物质的量不等,说明此时已进行过溶液转移,即将乙室部分溶液
转移至甲室,D正确;故合理选项是BD。
2.(2021·湖北卷)Na Cr O 的酸性水溶液随着H+浓度的增大会转化为CrO 。电解法制备CrO 的原理如图
2 2 7 3 3
所示。下列说法错误的是( )
A.电解时只允许H+通过离子交换膜
B.生成O 和H 的质量比为8∶1
2 2
C.电解一段时间后阴极区溶液OH-的浓度增大
D.CrO 的生成反应为:Cr O +2H+=2CrO +H O
3 2 3 2
2.A A.由以上分析知,电解时通过离子交换膜的是 ,A项错误;B.根据各电极上转移电子数相同,
由阳极反应和阴极反应,知生成 和 的物质的量之比为1∶2,其质量比为8∶1,B项正确;C.根据阴极
反应知,电解一段时间后阴极区溶液 的浓度增大,C项正确:D.电解过程中阳极区 的浓度增大,
转化为 ,D项正确。故选A。
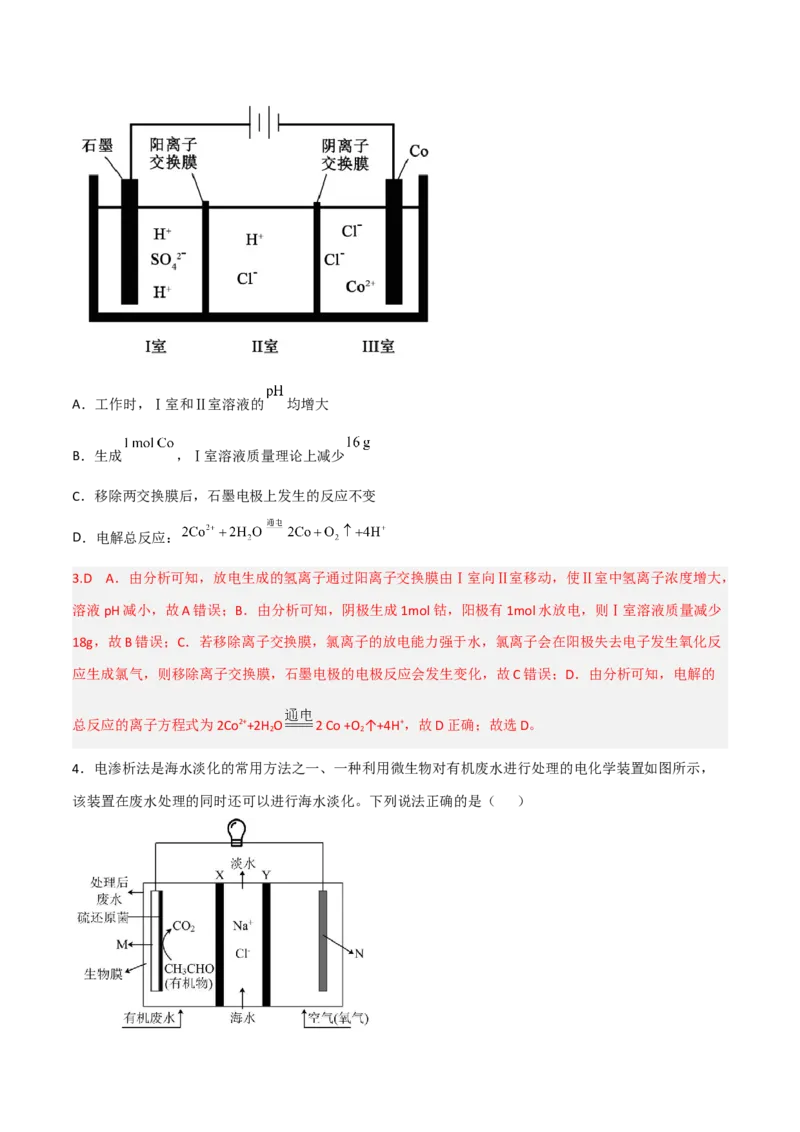
3.(2021·广东卷)钴( )的合金材料广泛应用于航空航天、机械制造等领域。如图为水溶液中电解制备
金属钴的装置示意图。下列说法正确的是( )A.工作时,Ⅰ室和Ⅱ室溶液的 均增大
B.生成 ,Ⅰ室溶液质量理论上减少
C.移除两交换膜后,石墨电极上发生的反应不变
D.电解总反应:
3.D A.由分析可知,放电生成的氢离子通过阳离子交换膜由Ⅰ室向Ⅱ室移动,使Ⅱ室中氢离子浓度增大,
溶液pH减小,故A错误;B.由分析可知,阴极生成1mol钴,阳极有1mol水放电,则Ⅰ室溶液质量减少
18g,故B错误;C.若移除离子交换膜,氯离子的放电能力强于水,氯离子会在阳极失去电子发生氧化反
应生成氯气,则移除离子交换膜,石墨电极的电极反应会发生变化,故C错误;D.由分析可知,电解的
总反应的离子方程式为2Co2++2H O 2 Co +O ↑+4H+,故D正确;故选D。
2 2
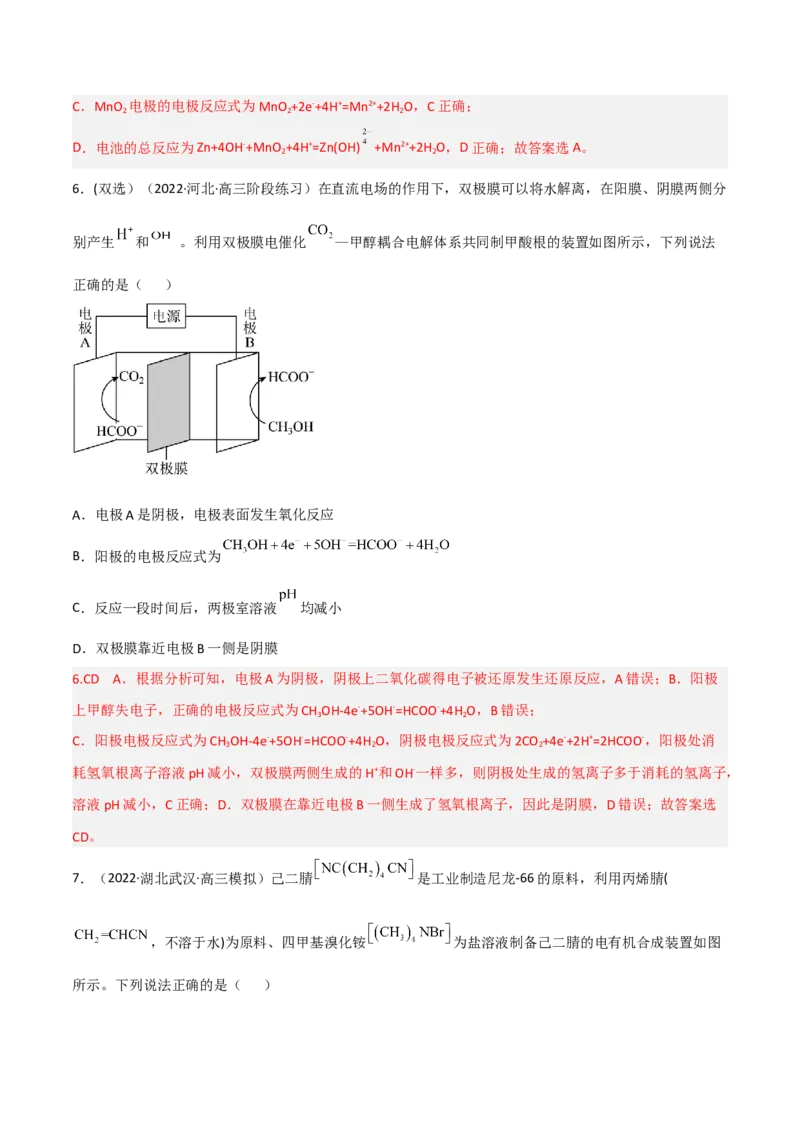
4.电渗析法是海水淡化的常用方法之一、一种利用微生物对有机废水进行处理的电化学装置如图所示,
该装置在废水处理的同时还可以进行海水淡化。下列说法正确的是( )A.该装置工作时,化学能转化为电能,M为正极
B.X为阴离子交换膜,Y为阳离子交换膜
C.M极电极反应式为CH CHO+10OH--10e-=2CO ↑+7H O
3 2 2
D.当有1molNa+通过离子交换膜时,N极消耗的空气体积约为26.7L
4.B A.由图可知,该装置为原电池,是将化学能转化为电能,电极N中氧气发生还原反应,作正极;电
极M甲醛发生氧化反应做负极;故A项错误;B.电极N中氧气发生还原反应,电极反应式为5O +20 e-
2
+10H O =20OH-,生成阴离子,故钠离子向N极移动,Y为阳离子交换膜,电极M甲醛发生氧化反应,电极
2
反应式为CH CHO+3H O-10e-=2CO ↑+10H+,X为阴离子交换膜,故B项正确;C.电极M甲醛发生氧化反应,
3 2 2
电极反应式为2CH CHO+6H O-20e-=4CO ↑+20H+,故C项错误;
3 2 2
D.N电极反应式为5O +20 e-+10H O =20OH-,当有20molNa+通过离子交换膜时,标准状况消耗氧气的体积为5
2 2
;标准状况,当有1molNa+通过离子交换膜时,N极消耗的空气体积约为5 ,
选项无标准状况这一前提,故D项错误。故答案选B。
5.一种水性电解液Zn-MnO 离子选择双隔膜电池如图所示(KOH溶液中,Zn2+以Zn(OH) 存在)。电池放电
2
时,下列叙述错误的是( )
A.Ⅱ区的K+通过隔膜向Ⅲ区迁移
B.Ⅰ区的SO 通过隔膜向Ⅱ区迁移
C. MnO 电极反应:MnO +2e-+4H+=Mn2++2H O
2 2 2
D.电池总反应:Zn+4OH-+MnO +4H+=Zn(OH) +Mn2++2H O
2 2
5.A A.根据分析,Ⅱ区的K+只能向Ⅰ区移动,A错误;B.根据分析,Ⅰ区的SO 向Ⅱ区移动,B正确;C.MnO 电极的电极反应式为MnO +2e-+4H+=Mn2++2H O,C正确;
2 2 2
D.电池的总反应为Zn+4OH-+MnO +4H+=Zn(OH) +Mn2++2H O,D正确;故答案选A。
2 2
6.(双选)(2022·河北·高三阶段练习)在直流电场的作用下,双极膜可以将水解离,在阳膜、阴膜两侧分
别产生 和 。利用双极膜电催化 —甲醇耦合电解体系共同制甲酸根的装置如图所示,下列说法
正确的是( )
A.电极A是阴极,电极表面发生氧化反应
B.阳极的电极反应式为
C.反应一段时间后,两极室溶液 均减小
D.双极膜靠近电极B一侧是阴膜
6.CD A.根据分析可知,电极A为阴极,阴极上二氧化碳得电子被还原发生还原反应,A错误;B.阳极
上甲醇失电子,正确的电极反应式为CH OH-4e-+5OH-=HCOO-+4H O,B错误;
3 2
C.阳极电极反应式为CH OH-4e-+5OH-=HCOO-+4H O,阴极电极反应式为2CO +4e-+2H+=2HCOO-,阳极处消
3 2 2
耗氢氧根离子溶液pH减小,双极膜两侧生成的H+和OH-一样多,则阴极处生成的氢离子多于消耗的氢离子,
溶液pH减小,C正确;D.双极膜在靠近电极B一侧生成了氢氧根离子,因此是阴膜,D错误;故答案选
CD。
7.(2022·湖北武汉·高三模拟)己二腈 是工业制造尼龙-66的原料,利用丙烯腈(
,不溶于水)为原料、四甲基溴化铵 为盐溶液制备己二腈的电有机合成装置如图
所示。下列说法正确的是( )A.交换膜为阴离子交换膜
B.当电路中转移 时,阳极室溶液质量减少8g
C. 在电化学合成中作电解质,并有利于丙烯腈的溶解
D.正极区的电极反应为
7.C A.由分析可知,氢离子由阳极区进入阴极区,故交换膜为阳离子交换膜,A错误;
B.当电路中转移 时,阳极室生成氧气质量为8g,同时有1mol氢离子进入阴极区,故溶液质量减少
9g,B错误;C.丙烯腈为有机物, 在电化学合成中作电解质,并有利于丙烯腈的溶解,C正确;
D.阴极区的电极反应为 ,D错误;故选C。
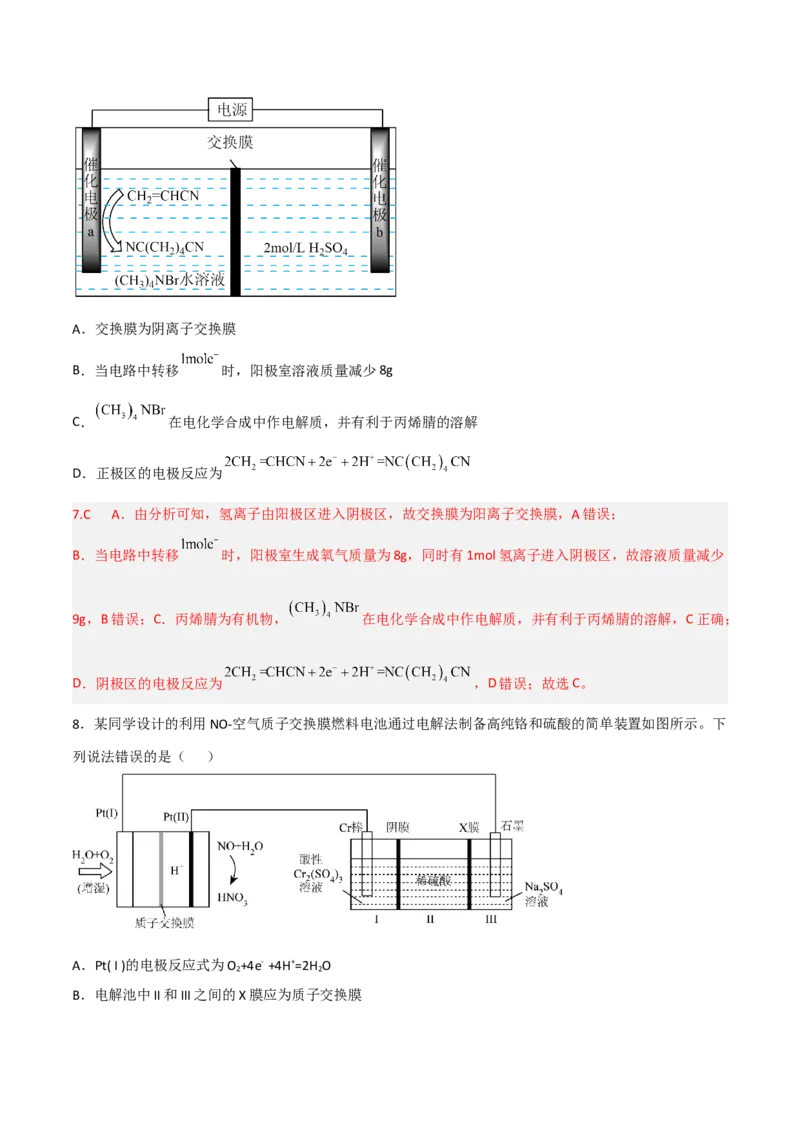
8.某同学设计的利用NO-空气质子交换膜燃料电池通过电解法制备高纯铬和硫酸的简单装置如图所示。下
列说法错误的是( )
A.Pt( I )的电极反应式为O +4e- +4H+=2H O
2 2
B.电解池中II和III之间的X膜应为质子交换膜C.工作时,I池中 通过阴膜向II池中移动
D.若Pt(II )极消耗11.2 L NO,则Cr棒质量增加26 g
8.D A.Pt(I)作正极,O 在此得电子并结合通过质子交换膜迁移来的H+,电极反应方程式为O +4e-
2 2
+4H+=2H O,A选项正确;B.作为阳极的石墨电极处,水中OH-在此失电子被氧化为O ,H+透过质子交换
2 2
膜(X膜)迁移到II区域,获得硫酸,B选项正确;C.工作时,I池中 通过阴膜向II池中移动获得硫酸,C
选项正确;D.未标明气体所处环境的温度与压强,无法计算,D选项错误;答案选D。