文档内容
高频考点 28 化学平衡常数和转化率
1.(2022·潍坊高三模拟)在淀粉KI溶液中存在下列平衡:I (aq)+I-(aq) (aq)。测得不同温度下该反应
2
的平衡常数K如表所示:
t/℃ 5 15 25 35 50
K 1 100 841 689 533 409
下列说法正确的是( )
A.反应I (aq)+I-(aq) I (aq)的ΔH>0
2
B.其他条件不变,升高温度,溶液中c(I )减小
C.该反应的平衡常数表达式为K=
D.25 ℃时,向溶液中加入少量KI固体,平衡常数K小于689
1.B A.温度升高,平衡常数减小,该反应是放热反应,ΔH<0,A错误;B.升高温度,平衡逆向移动,
c( )减小,B正确;C. ,C错误;D.平衡常数仅与温度有关,25 ℃时,向溶液中加入少量KI
固体,平衡正向移动,但平衡常数不变,仍然是689,D错误;故答案选B。
2.(2022·北京·高三期中)利用丙烷(C H )在无氧条件下制备丙烯(C H )的反应方程式为:C H (g)
3 8 3 6 3 8
C H (g)+H (g) H=+124kJ·mol-1。在一体积可变的容器中,不同起始压强下(0.1MPa、0.01MPa)进行上述反应,
3 6 2
达到化学平衡△时,测得丙烷和丙烯的物质的量分数随温度变化如图所示,则下列说法中正确的是()
A.c曲线表示的是0.01MPa压强下丙烯随温度变化的物质的量分数B.A点对应的该反应平衡常数K=1.25MPa(K 为以分压表示的平衡常数)
p p
C.B点丙烷的平衡转化率为33.3%
D.实际生产过程中需通入一定量水蒸气,其目的是稀释原料气,增大丙烯的平衡产率
2.D A.由分析可知,c曲线表示的是0.1MPa压强下丙烯随温度变化的物质的量分数,A错误;B.假设
丙烷初始量为1mol
A点丙烷含量为50%,则 ,x= ,反应后总的物质的量为 ,则A点对应的该反
应平衡常数K= ,B错误;
p
C.假设丙烷初始量为1mol
B点丙烯含量为40%,则 ,x= ,B点丙烷的平衡转化率为 66.7%,C错误;
D.实际生产过程中需通入一定量水蒸气,其目的是稀释原料气,可以促进平衡正向移动,增大丙烯的平
衡产率,D正确;故选D。
3.(2022·浙江·高三开学考试)接触法制硫酸生产中的关键工序是SO 的催化氧化:SO (g)+ O (g)
2 2 2
SO (g),起始的物质的量分数分别为7.5%、10.5%和82%时,在0.5MPa、2.5MPa和5.0MPa压强
3
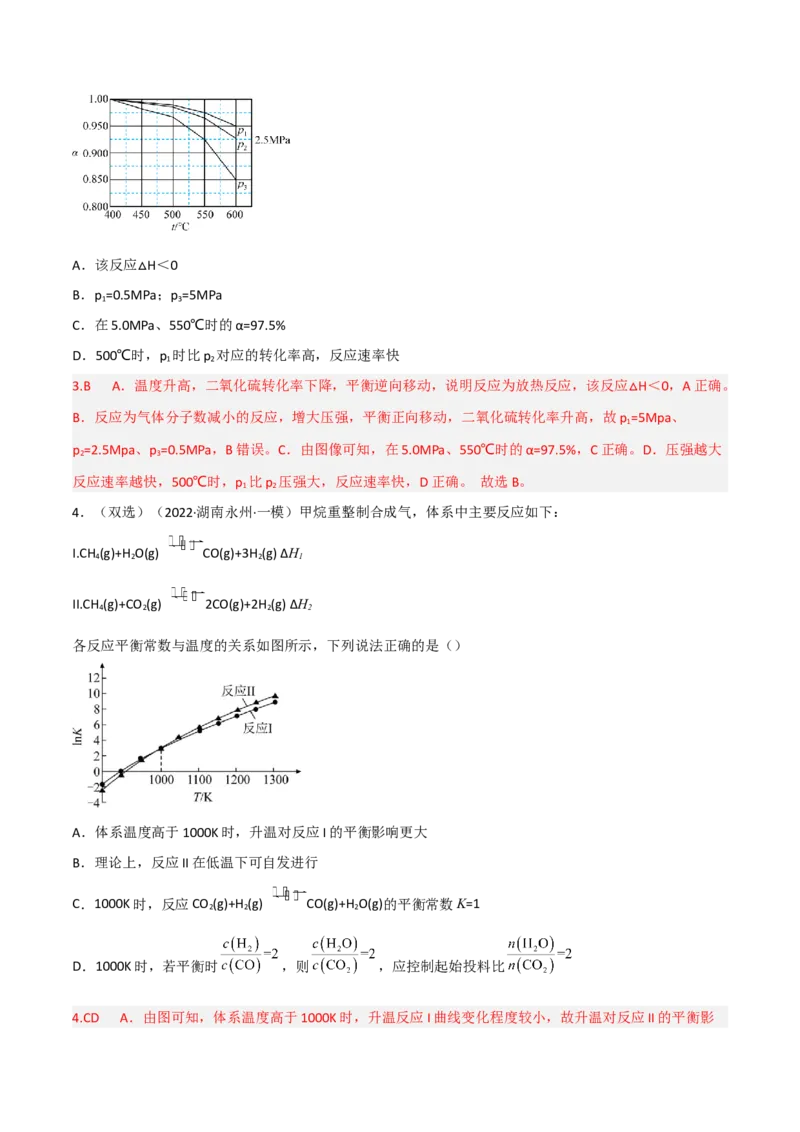
下,SO 平衡转化率α随温度的变化如图所示。下列有关说法不正确的是( )
2A.该反应 H<0
B.p =0.5M△Pa;p =5MPa
1 3
C.在5.0MPa、550℃时的α=97.5%
D.500℃时,p 时比p 对应的转化率高,反应速率快
1 2
3.B A.温度升高,二氧化硫转化率下降,平衡逆向移动,说明反应为放热反应,该反应 H<0,A正确。
B.反应为气体分子数减小的反应,增大压强,平衡正向移动,二氧化硫转化率升高,故p△=5Mpa、
1
p =2.5Mpa、p =0.5MPa,B错误。C.由图像可知,在5.0MPa、550℃时的α=97.5%,C正确。D.压强越大
2 3
反应速率越快,500℃时,p 比p 压强大,反应速率快,D正确。 故选B。
1 2
4.(双选)(2022·湖南永州·一模)甲烷重整制合成气,体系中主要反应如下:
I.CH (g)+H O(g) CO(g)+3H (g) ΔH
4 2 2 1
II.CH (g)+CO (g) 2CO(g)+2H (g) ΔH
4 2 2 2
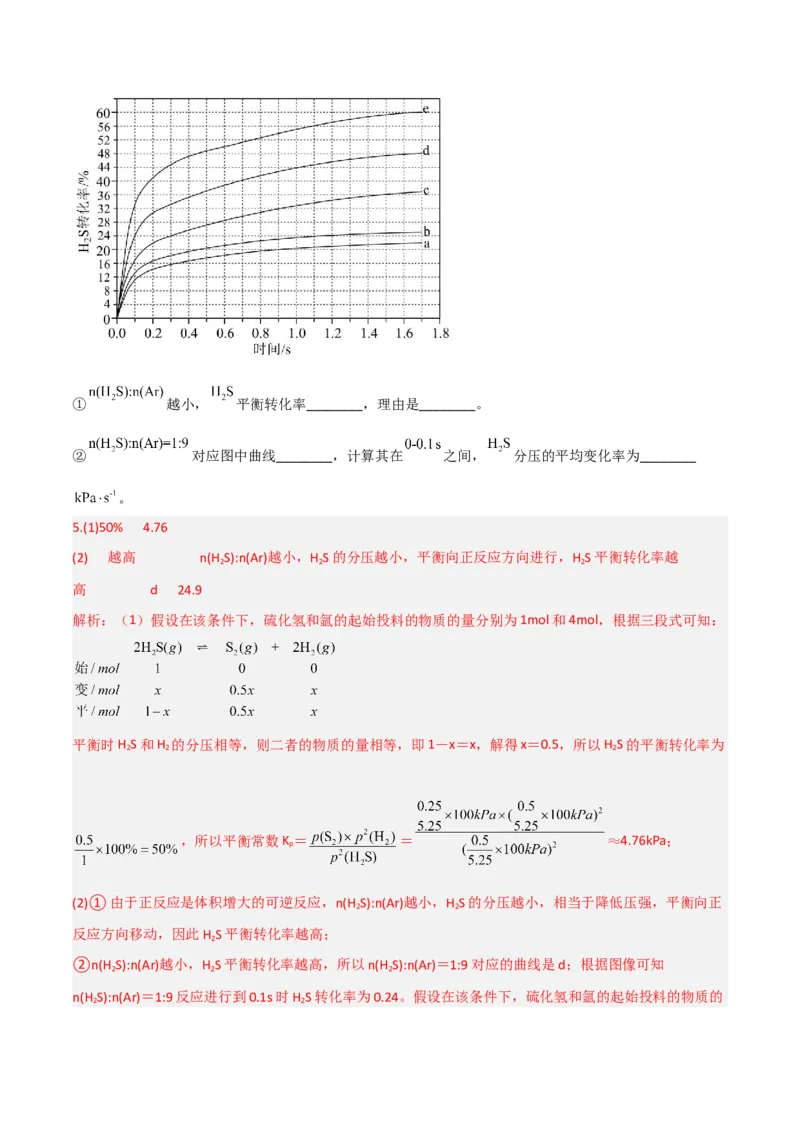
各反应平衡常数与温度的关系如图所示,下列说法正确的是()
A.体系温度高于1000K时,升温对反应I的平衡影响更大
B.理论上,反应II在低温下可自发进行
C.1000K时,反应CO (g)+H (g) CO(g)+H O(g)的平衡常数K=1
2 2 2
D.1000K时,若平衡时 ,则 ,应控制起始投料比
4.CD A.由图可知,体系温度高于1000K时,升温反应I曲线变化程度较小,故升温对反应II的平衡影响更大,A错误; B.反应II为吸热的熵增反应,故根据∆H-T∆S<0反应可自发进行,理论上反应II在高温
下可自发进行,B错误; C.根据盖斯定律可知,反应II-反应I得到反应CO (g)+H (g) CO(g)+H O(g);
2 2 2
1000K时,反应II、反应I的K值相等,则反应CO (g)+H (g) CO(g)+H O(g)的平衡常数K= 1,C正
2 2 2
确;D.据C分析可知,1000K时,反应CO (g)+H (g) CO(g)+H O(g)的平衡常数K= 1,
2 2 2
若平衡时 ,则 ,由于反应在同一容器中进行,且反应中二氧化碳、水的系数相等,则
起始投料比 ,D正确。故选CD。
5.(2022·全国卷节选)油气开采、石油化工、煤化工等行业废气普遍含有的硫化氢,需要回收处理并加
以利用。回答下列问题:已知 热分解反应
(1)在 、 反应条件下,将 的混合气进行 热分解反应。平衡时混合气
中 与 的分压相等, 平衡转化率为________,平衡常数 ________ 。
(2)在 、 反应条件下,对于 分别为 、 、 、 、 的 混合气,
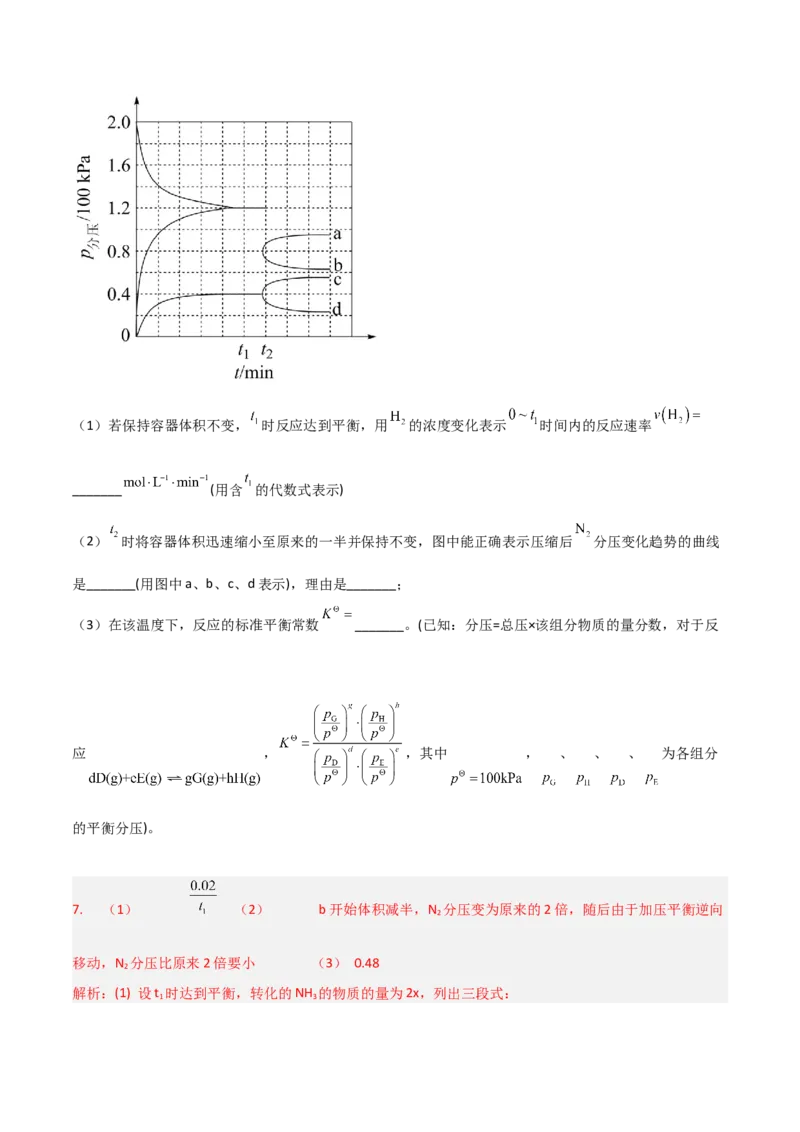
热分解反应过程中 转化率随时间的变化如下图所示。① 越小, 平衡转化率________,理由是________。
② 对应图中曲线________,计算其在 之间, 分压的平均变化率为________
。
5.(1)50% 4.76
(2) 越高 n(H S):n(Ar)越小,H S的分压越小,平衡向正反应方向进行,H S平衡转化率越
2 2 2
高 d 24.9
解析:(1)假设在该条件下,硫化氢和氩的起始投料的物质的量分别为1mol和4mol,根据三段式可知:
平衡时H S和H 的分压相等,则二者的物质的量相等,即1-x=x,解得x=0.5,所以H S的平衡转化率为
2 2 2
,所以平衡常数K= = ≈4.76kPa;
p
(2)①由于正反应是体积增大的可逆反应,n(H S):n(Ar)越小,H S的分压越小,相当于降低压强,平衡向正
2 2
反应方向移动,因此H S平衡转化率越高;
2
②n(H S):n(Ar)越小,H S平衡转化率越高,所以n(H S):n(Ar)=1:9对应的曲线是d;根据图像可知
2 2 2
n(H S):n(Ar)=1:9反应进行到0.1s时H S转化率为0.24。假设在该条件下,硫化氢和氩的起始投料的物质的
2 2量分别为1mol和9mol,则根据三段式可知
此时H S的压强为 ≈7.51kPa,H S的起始压强为10kPa,所以H S分压的平均
2 2 2
变化率为 =24.9kPa·s-1。
6.(2022·河北卷节选)氢能是极具发展潜力的清洁能源,以氢燃料为代表的燃料电池有良好的应用前景。
工业上常用甲烷水蒸气重整制备氢气,体系中发生如下反应。
Ⅰ.
Ⅱ.
(1)下列操作中,能提高 平衡转化率的是_______ (填标号)。
A.增加 用量 B.恒温恒压下通入惰性气体
C.移除 D.加入催化剂
(2)恒温恒压条件下, 和 反应达平衡时, 的转化率为 , 的物质
的量为 ,则反应Ⅰ的平衡常数 _______ (写出含有a、b的计算式;对于反应
, ,x为物质的量分数)。其他条件不变, 起始量
增加到 ,达平衡时, ,平衡体系中 的物质的量分数为_______(结果保留两位有效
数字)。
6.(1) BC (2)解析:(1)A.增加CH (g)用量可以提高H O(g)的转化率,但是CH (g)平衡转化率减小,A不符合题意;
4 2 4
B.恒温恒压下通入惰性气体,相当于减小体系压强,反应混合物中各组分的浓度减小,反应Ⅰ的化学平
衡正向移动,能提高CH (g)平衡转化率,B符合题意;C.移除CO(g),减小了反应混合物中CO(g)的浓度,
4
反应Ⅰ的化学平衡正向移动,能提高CH (g)平衡转化率,C符合题意;D.加入催化剂不能改变平衡状态,
4
故不能提高CH (g)平衡转化率,D不符合题意;
4
综上所述,上述操作中,能提高CH (g)平衡转化率的是BC;
4
(2)恒温恒压条件下,1 mol CH (g)和1 mol H O(g)反应达平衡时,CH (g)的转化率为α,CO (g)的物质的
4 2 4 2
量为b mol,则转化的CH (g)为α mol,剩余的CH (g)为(1-α )mol,根据C元素守恒可知,CO(g)的物质的
4 4
量为(α-b)mol,根据H和O守恒可知,H O(g)的物质的量为(1-α-b )mol,H (g)的物质的量为(3α+b )mol,则反
2 2
应混合物的总物质的量为(2α+2 )mol,平衡混合物中,CH (g)、H O(g)、 CO(g) 、H (g)的物质的量分数分别
4 2 2
为 、 、 、 ,因此,反应I的平衡常数K=
x
;其他条件不变,H O(g)起始量增加到5mol,达平衡时,a
2
=0.90,b =0.65,则平衡时,CH (g)为0.1mol,根据C元素守恒可知,CO(g)的物质的量为0.25mol,,根据
4
H和O守恒可知,H O(g)的物质的量为(5-0.90-0.65 )mol=3.45mol,H (g)的物质的量为(3α+b )mol=3.35mol,
2 2
平衡混合物的总物质的量为(2α+6 )mol=7.8mol,平衡体系中H (g)的物质的量分数为 ;
2
7.(2021·湖南卷节选)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将
通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如
图所示。(1)若保持容器体积不变, 时反应达到平衡,用 的浓度变化表示 时间内的反应速率
_______ (用含 的代数式表示)
(2) 时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后 分压变化趋势的曲线
是_______(用图中a、b、c、d表示),理由是_______;
(3)在该温度下,反应的标准平衡常数 _______。(已知:分压=总压×该组分物质的量分数,对于反
应 , ,其中 , 、 、 、 为各组分
的平衡分压)。
7. (1) (2) b开始体积减半,N 分压变为原来的2倍,随后由于加压平衡逆向
2
移动,N 分压比原来2倍要小 (3) 0.48
2
解析:(1) 设t 时达到平衡,转化的NH 的物质的量为2x,列出三段式:
1 3根据同温同压下,混合气体的物质的量等于体积之比, = ,解得x=0.02mol, (H )=
2
= mol L-1 min-1,故答案为: ;
(2)t 时将容器体积压缩到原来的一半,开始N 分压变为原来的2倍,随后由于加压平衡逆向移动,N
2 2 2
分压比原来2倍要小,故b曲线符合,故答案为:b;开始体积减半,N 分压变为原来的2倍,随后由于加
2
压平衡逆向移动,N 分压比原来2倍要小;
2
(3)由图可知,平衡时,NH 、N 、H 的分压分别为120 kPa、40 kPa、120 kPa,反应的标准平衡常数 =
3 2 2
=0.48,故答案为:0.48;
8.(2022·广东·高三模拟)甲醇是重要的化工原料,在生产生活中应用广泛,碳氧化物与氢气在一定条件
下可合成甲醇。回答下列问题:
Ⅰ.一氧化碳与氢气合成甲醇的反应为CO(g)+2H (g) CH OH(g)。在①、②、③容积不等的恒容密闭容器
2 3
中,均充入0.1molCO和0.2molH ,在催化剂作用下发生上述反应,测得三个容器中平衡混合物中CH OH
2 3
的体积分数随温度的变化如图所示:
(1)该反应的正反应为____反应(填“放热”或“吸热”)。(2)容器的容积①____③(填“>”“<”或“=”)。
(3)P点时,H 的转化率为____;若其他条件不变,将恒容密闭容器改为恒压密闭容器,平衡后H 的转化率
2 2
将____(填“增大”“减小”或“不变”)。
Ⅱ.二氧化碳与氢气合成甲醇的主要反应如下:
反应①:CO (g)+3H (g) CH OH(g)+H O(g) H =-58kJ/mol
2 2 3 2 1
△
反应②:CO (g)+H (g) CO(g)+H O(g) H =+41kJ/mol
2 2 2 2
△
(4)反应时温度控制在230~280℃之间,温度不能过高的原因是___。
(5)一定条件下,向刚性容器中充入物质的量之比为1:3的CO (g)和H (g)发生上述反应。达到平衡时CO 的
2 2 2
转化率为20%,CH OH的选择性为75%[CH OH的选择性= ×100%],则反应②的平衡常数
3 3
K=____。(K 为以分压表示的平衡常数)
p p
8.(1)放热(2)<(3) 75% 增大
(4)温度过高,反应①逆向移动,反应②正向移动,CH OH产率(选择性)低
3
(5)5×10-3
解析:(1)由图示可知,当温度升高,甲醇的的体积分数降低,反应逆向进行,该反应是放热反应。
(2)反应为气体分子数减小的反应,增大压强平衡正向移动,甲醇体积分数增大,①、②、③容积不等但充
入一氧化碳和氢气初始量相同,可看成压强的影响,容积越小、压强越大,甲醇体积分数越高,由图示可
知,相同温度下①中甲醇体积分数高、③中甲醇体积分数低,则容积①<③。
(3)设一氧化碳的转化量为xmol,依据题意列三段式: ,
由图可知,P点甲醇的体积分数为50%,则有 ,解得x=0.075,则氢气的转化率为:
;若其他条件不变,将恒容密闭容器改为恒压密闭容器,此反应是一个气体分子
数减小的反应,要想压强不变,随着反应进行,容器体积减小,相当于加压,平衡正向移动,氢气转化率
增大。(4)反应①为放热反应,温度升高,平衡逆向移动,反应②为吸热反应,温度升高,平衡正向移动,使得甲
醇的产率降低,因此温度不能过高,应控制在230~280℃之间。
(5)设初始二氧化碳和氢气的物质的量分别为amol、3amol,反应①中二氧化碳转化了xmol,而达到平衡时
CO 的转化率为20%,则反应②中二氧化碳转化了(0.2a-x)mol,依据信息列三段式:
2
,
,则甲醇的选择性= =
100%=75%,解得x=0.15a,故平衡时二氧化碳为0.8amol,氢气为2.5amol,甲醇为0.15amol,
一氧化碳为0.05amol,水蒸气为0.2amol,则体系中二氧化碳的分压为: =
,氢气分压为: ,一氧化碳分压为: ,水蒸气分压为: ,所以反应②的平衡常数
K= = =5×10-3。
p
9.(2022·河南·商丘市第一高级中学高三模拟)乙烯年产量的高低是衡量一个国家石油化工发展水平的一
个极为重要的指标,乙烷裂解制乙烯具有极高的经济效益。回答下列问题:
(1)已知:①2C H (g)+7O (g) 4CO (g)+6H O(l) H =-3120kJ·mol-1;
2 6 2 2 2 1
△
②C H (g)+3O (g) 2CO (g)+2H O(l) H =-1411kJ·mol-1;
2 4 2 2 2 2
△③2H (g)+O (g) 2H O(l) H =-566kJ·mol-1 H =-1411kJ·mol-1。
2 2 2 3 2
△ △
乙烷脱氢制备乙烯的热化学方程式为_____;生产中会间断性地向容器中通入适量O ,使其发生反应
2
2C H (g)+O (g) 2C H (g)+2H O(g) H<0,发生此反应的意义是____。
2 6 2 2 4 2
△
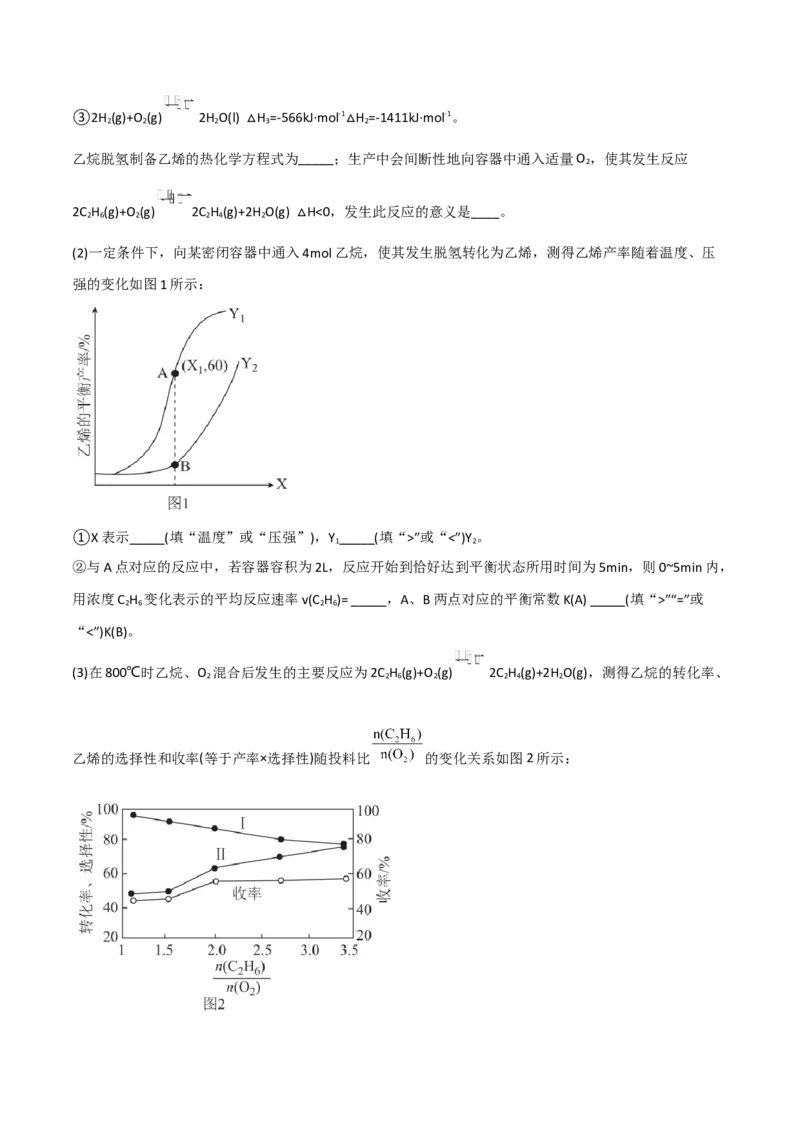
(2)一定条件下,向某密闭容器中通入4mol乙烷,使其发生脱氢转化为乙烯,测得乙烯产率随着温度、压
强的变化如图1所示:
①X表示_____(填“温度”或“压强”),Y _____(填“>”或“<”)Y 。
1 2
②与A点对应的反应中,若容器容积为2L,反应开始到恰好达到平衡状态所用时间为5min,则0~5min内,
用浓度C H 变化表示的平均反应速率v(C H )= _____,A、B两点对应的平衡常数K(A) _____(填“>”“=”或
2 6 2 6
“<”)K(B)。
(3)在800℃时乙烷、O 混合后发生的主要反应为2C H (g)+O (g) 2C H (g)+2H O(g),测得乙烷的转化率、
2 2 6 2 2 4 2
乙烯的选择性和收率(等于产率×选择性)随投料比 的变化关系如图2所示:I、II两条曲线表示乙烷转化率的是_____(填“I”或“II”),当 <2时, 越小,乙烯的选择性
和收率越小的原因是_____。
9.(1) C H (g) C H (g)+H (g) H=+134kJ·mol-1 为乙烷脱氢生成乙烯提供能量
2 6 2 4 2
△
(2) 温度 < 0.24mol·L-1·min-1 =
(3) I 当 <2时,O 过量, 越小,O 过量的越多,乙烷的转化率越大,过量的O 可氧
2 2 2
化乙烯,导致乙烯的选择性和收率越低
解析:(1)①2C H (g)+7O (g) 4CO (g)+6H O(l) H =-3120kJ·mol-1;
2 6 2 2 2 1
△
②C H (g)+3O (g) 2CO (g)+2H O(l) H =-1411kJ·mol-1;
2 4 2 2 2 2
△
③2H (g)+O (g) 2H O(l) H =-566kJ·mol-1
2 2 2 3
△
根据盖斯定律,0.5×①-②-0.5×③可得 ;由于乙烷脱氢
生成乙烯需要吸收热量,而乙烷部分氧化时会放出热量,放出的热量满足乙烷脱氢需要吸收的热量。
(2)①由于乙烷脱氢是吸热反应,其他条件相同时,温度越高乙烯的平衡产率越大,而压强越大,越不
利于平衡正向进行,故X代表温度,Y代表压强。
②乙烯的理论产量是 ,由此知平衡时 , ,
;平衡常数是温度的函数,只和温度有关,A、B两点温度相同,
故平衡常数相等。
(3)原料中 含量越低,乙烷的转化率一定是越低的,故Ⅰ表示乙烷的转化率;高温下,乙烷除脱氢生
成乙烯外,还可以转化为C、CO、 等物质,由化学方程式可知,当 时, 过量,越小, 过量的越多,乙烷的转化率越大, 越小, 过量的越多,乙烷的转化率越大,
过量的 可氧化乙烯,导致乙烯的选择性和收率降低。