文档内容
高频考点 7 离子检验与推断
1.(2022·广东卷)实验室进行粗盐提纯时,需除去 和 ,所用试剂包括 以及(
)
A. B.
C. D.
1. A 除杂过程中不能引入新杂质,同时为保证除杂完全,所加除杂试剂一般过量,然后选择合适的试
剂将所加过量的物质除去。粗盐中主要成分为NaCl。除去Ca2+选用 将其转化为沉淀,为了不引入新杂
质,所加物质的阳离子为Na+,即选用Na CO 除去Ca2+,同理可知,除去Mg2+需选用NaOH,除去 需
2 3
选用BaCl ,因所加除杂试剂均过量,因此向粗盐样品中加入除杂试剂的顺序中,BaCl 先于Na CO 加入,
2 2 2 3
利用Na CO 除去Ca2+和多余的BaCl ,因Na CO 、NaOH均过量,成为新杂质,需要过滤后向滤液中加入
2 3 2 2 3
HCl,至溶液中不再有气泡产生,以此除去Na CO 、NaOH,然后将溶液蒸干得到较为纯净的食盐产品,综
2 3
上所述,答案为A。
2.(2022·全国乙卷)某白色粉末样品,可能含有 、 、 和 。取少量样品进
行如下实验:
①溶于水,得到无色透明溶液
②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出。离心分离
③取②的上层清液,向其中滴加 溶液有沉淀生成。
该样品中确定存在的是( )
A. B.
C. D.
2. A 由题意可知,①取少量样品溶于水得到无色透明溶液,说明固体溶于水且相互之间能共存,②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体放出,说明固体中存在Na S O ,发生反应S O
2 2 3 2
+2H+=S↓+H O+SO ↑,离心分离,③取②的上层清液,向其中滴加BaCl 溶液,有沉淀生成,则沉淀为
2 2 2
BaSO ,说明固体中存在Na SO ,不能确定是否有Na SO 和Na CO ,Na SO 与过量盐酸反应生成二氧化硫,
4 2 4 2 3 2 3 2 3
Na CO 与过量盐酸反应生成二氧化碳,而这些现象可以被Na S O 与过量盐酸反应的现象覆盖掉,综上分析,
2 3 2 2 3
该样品中确定存在的是:Na SO 、Na S O ,答案选A。
2 4 2 2 3
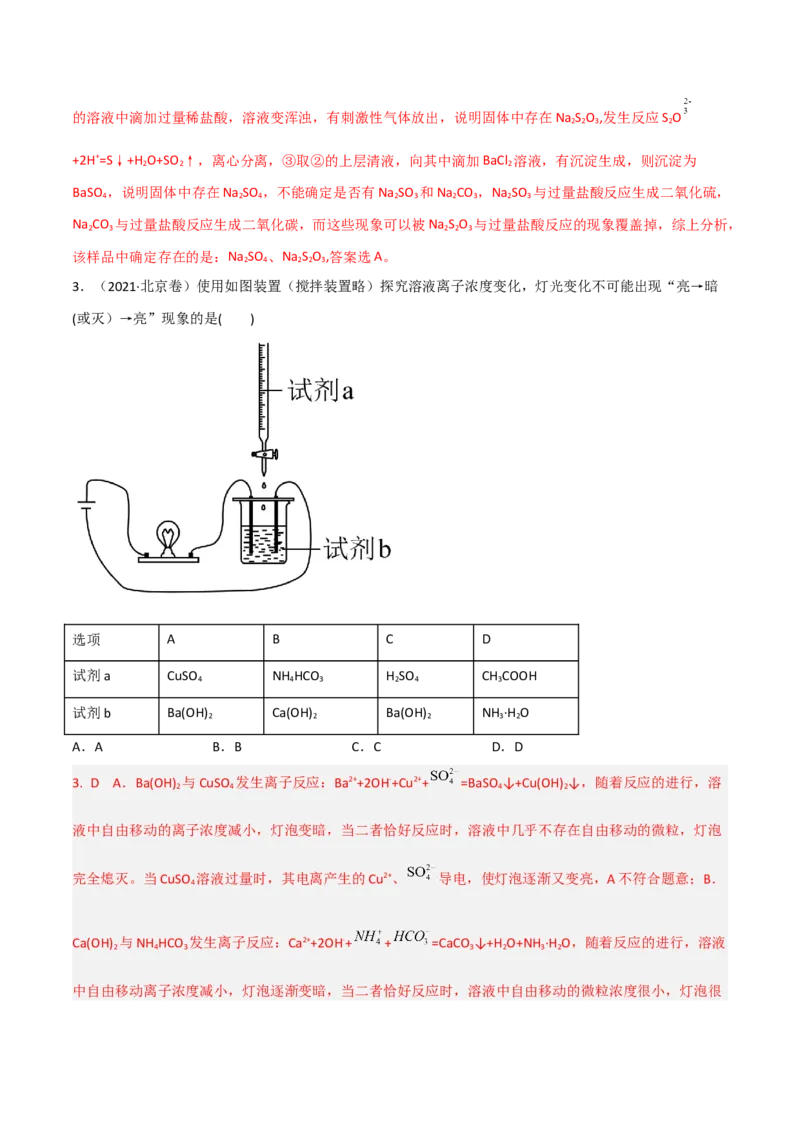
3.(2021·北京卷)使用如图装置(搅拌装置略)探究溶液离子浓度变化,灯光变化不可能出现“亮→暗
(或灭)→亮”现象的是( )
选项 A B C D
试剂a CuSO NH HCO H SO CH COOH
4 4 3 2 4 3
试剂b Ba(OH) Ca(OH) Ba(OH) NH ·H O
2 2 2 3 2
A.A B.B C.C D.D
3. D A.Ba(OH) 与CuSO 发生离子反应:Ba2++2OH-+Cu2++ =BaSO ↓+Cu(OH) ↓,随着反应的进行,溶
2 4 4 2
液中自由移动的离子浓度减小,灯泡变暗,当二者恰好反应时,溶液中几乎不存在自由移动的微粒,灯泡
完全熄灭。当CuSO 溶液过量时,其电离产生的Cu2+、 导电,使灯泡逐渐又变亮,A不符合题意;B.
4
Ca(OH) 与NH HCO 发生离子反应:Ca2++2OH-+ + =CaCO ↓+H O+NH ·H O,随着反应的进行,溶液
2 4 3 3 2 3 2
中自由移动离子浓度减小,灯泡逐渐变暗,当二者恰好反应时,溶液中自由移动的微粒浓度很小,灯泡很暗。当 NH HCO 溶液过量时,其电离产生的 、 导电,使灯泡逐渐又变亮,B不符合题意;C.
4 3
Ba(OH) 与H SO 发生离子反应:Ba2++2OH-+2H++ =BaSO ↓+2H O,随着反应的进行,溶液中自由移动的
2 2 4 4 2
离子浓度减小,灯泡变暗,当二者恰好反应时,溶液中几乎不存在自由移动的微粒,灯泡完全熄灭。当
H SO 溶液过量时,其电离产生的H+、 导电,使灯泡逐渐又变亮,C不符合题意;D.CH COOH与氨水
2 4 3
发生离子反应:CH COOH+NH ·H O=CH COO-+ +H O,反应后自由移动的离子浓度增大,溶液导电能力
3 3 2 3 2
增强,灯泡更明亮,不出现亮—灭(或暗)—亮的变化,D符合题意;故合理选项是D。
4.(2021·海南卷)一次性鉴别等浓度的 、 、 三种溶液,下列方法不可行的是
( )
A.测定 B.焰色试验
C.滴加 溶液 D.滴加饱和 溶液,微热
4.C A. 溶液显中性, 溶液显酸性, 溶液显碱性,故可以用测定pH的方法鉴别,
故A正确;B. 的焰色试验中现象为透过蓝色钴玻璃为紫色, 的焰色试验中无现象,
的焰色试验中现象为黄色,故可以用焰色试验的方法鉴别,故B正确;C. 、 、 中只
有 能与 反应有现象,故 和 不能鉴别,故C错误;D.2 +
CaCl2+2NH +2H O有刺激性气味气体产生, + =CaCO +2NaOH有白色沉淀产生,而 不
3 2 3
反应无现象,故可以鉴别,故D正确;故选C。
5.(2022·西安中学高三期中)向含 的水溶液中,加入足量的 固
体,充分反应后再加入过量的稀盐酸,所得溶液与起始溶液相比,上述离子数目没有变化的有()
A.1种 B.2种 C.3种 D.4种
5. B NaO 能与水反应生成NaOH,则Na+数目增多,Al3+、Fe3+和Fe2+都不能和OH 大量共存,沉淀后的氢
2 2
氧化亚铁被氧化,加入盐酸后Cl 增加,氢氧化铝又溶解,所以上述离子数目没有变化的只有Al3+和SO,B正确。
6.(2022·河南·焦作市第一中学模拟)现有一包粉末样品,可能由 中的
两种或三种组成。现进行如下实验:
ⅰ.取适量固体样品于试管中,加足量蒸馏水充分振荡,溶液变浑浊;
ⅱ.将ⅰ中的混合物过滤、洗涤;
ⅲ.向滤渣中加入足量稀盐酸,滤渣部分溶解并产生刺激性气味的气体。
则该样品中一定存在的物质是()
A. B.
C. D.
6.C 取适量固体样品于试管中,加足量蒸馏水充分振荡,溶液变浑浊,沉淀为钡或铁的沉淀;将ⅰ中的
混合物过滤、洗涤,向滤渣中加入足量稀盐酸,滤渣部分溶解并产生刺激性气味的气体,不溶于酸的沉淀
为硫酸钡沉淀、溶于酸的沉淀为铁的沉淀,说明存在氯化钡、氯化铁;产生刺激性气味的气体可能为生成
一氧化氮气体或二氧化硫气体,由于铁离子会将亚硫酸根离子转化为硫酸根离子生成不溶于酸的硫酸钡沉
淀,且亚硫酸根离子会和盐酸生成二氧化硫气体,故样品还存在亚硫酸钠,不确定硝酸钠是否存在。由分
析可知,选C。
7.(2022·邢台市第二中学高三月考)今有一混合物的水溶液,含有以下离子中的若干种:
,现取两份100 mL的该溶液进行如下实验:
第1份加足量NaOH溶液,加热,收集到标准状况下的气体448 mL;
第2份加足量Ba(OH) 溶液,得沉淀4.30 g,再用足量盐酸洗涤、干燥得沉淀2.33 g。
2
根据上述实验,下列推测正确的是( )
A.Ba2+一定存在 B.100 mL该溶液中含
C.Na+不一定存在 D.Cl-不确定,可向原溶液中加入AgNO 溶液进行检验
3
7. B A.根据上述分析可知溶液中含有0.01 mol ,由于Ba2+与 会反应产生BaSO 沉淀,可知原
4
溶液中一定不存在Ba2+,A错误;B.根据上述计算可知在100 mL的溶液中含有 的物质的量为0.01mol,B正确;C.根据上述分析可知,在100 mL溶液中含有的离子,n( )=0.01 mol,n( )=0.01
mol,n( )=0.02 mol,根据电荷守恒可知该溶液中一定含有阳离子Na+,C错误;D.不能确定Cl-是否
存在,若向原溶液中加入AgNO 溶液,由于溶液中含有 , Ag+与 会产生AgSO 白色沉淀,因此不能
3 2 4
检验Cl-是否存在,D错误;故合理选项是B。
8.(2022· 天津八校期中联考)某试液中只可能含有 K+、N 、Fe2+、Al3+、Cl-、S 、C 、Al 中
H+ O2− O2− O-
4 4 3 2
的若干种离子,离子浓度均为0.1 mol·L-1,某同学进行了如下实验。下列说法正确的是( )
A.原溶液中存在N 、Fe2+、Cl-、S
H+ O2−
4 4
B.滤液X中大量存在的阳离子有N 、Fe3+和Ba2+
H+
4
C.无法确定沉淀C的成分
D.无法确定原试液中是否含有Al3+、Cl-
8.A 加入过量稀硫酸无明显现象,说明无C ;加入过量Ba(NO) 溶液有气体A生成,说明溶液中存在还原
O2− 3 2
3
性离子,即含有Fe2+,因Fe2+能与Al 发生相互促进的水解反应,故溶液中无Al ;因为前面加入了稀硫酸,
O- O-
2 2
故由生成沉淀A(硫酸钡)不能说明溶液中存在S ;向滤液X中加入过量NaOH溶液有气体B生成,说明存在
O2−
4
N ,沉淀B为氢氧化铁;向滤液Y中通入少量CO 得到沉淀C,则沉淀C可以是BaCO 或Al(OH) 或二者的混
H+ 2 3 3
4
合物,又因为试液中各离子的浓度均为0.1 mol·L-1,根据电荷守恒及以上分析可知,原溶液中一定存在S
、Cl-,一定不存在K+、Al3+,故沉淀C为BaCO 。由上述分析知,原溶液中存在N 、Fe2+、S 、Cl-, A
O2− 3 H+ O2−
4 4 4项正确;滤液X中大量存在的阳离子为Fe3+、N 、Ba2+、H+, B项错误;沉淀C为BaCO, C项错误;原溶液中
H+ 3
4
存在Cl-,不存在Al3+, D项错误。
9.(2021·青岛高三期中)某同学在实验室中进行如下实验,以下结论正确的是()
编
Ⅰ Ⅱ Ⅲ
号
实
验
+
现 有白色沉淀生成,溶液为蓝
没有明显变化溶液仍为无色 有无色气体放出
象 色
A.Ⅰ中无明显变化,说明两溶液不反应
B.Ⅱ中的白色沉淀为CuCl
2
C.Ⅲ中同时发生氧化还原反应和离子反应
D.Ⅱ、Ⅲ恰好完全反应后的溶液中阴离子种类不同
9.C A.氢氧化钠溶液与稀硫酸溶液反应生成硫酸钠和水,反应时无明显实验现象,选项A错误;B.氯
化钡溶液与硫酸铜溶液反应生成硫酸钡白色沉淀和氯化铜,白色沉淀为硫酸钡,选项B错误;C.锌粒与
稀盐酸反应生成氯化锌和氢气,该反应既是有化合价变化的氧化还原反应,又是在溶液中进行的离子反应,
选项C正确;D.氯化钡溶液与硫酸铜溶液恰好反应生成硫酸钡白色沉淀和氯化铜,锌粒与稀盐酸恰好反
应生成氯化锌和氢气,溶液中的阴离子都是氯离子,种类相同,选项D错误;答案选C。
10.(2022·湖南雅礼中学高三期中)溶液A中可能含有如下离子中的若干种: 、 、 、
、 、 、 、 。某同学设计并完成了如下的实验:则下列有关说法正确的是( )
A.滤液C中一定存在的阳离子有 、 、
B.溶液A中一定存在 、 、 ,可能存在
C.4.50g沉淀B若改为加入足量的稀硝酸最终同样只得到2.33g沉淀
D.如果气体F能使湿润的红色石蕊试纸变蓝,说明该溶液中一定含有
10.D A.由分析可知,滤液C中一定不存在Mg2+,A错误;B.由分析可知,溶液A中一定存在Na+,B错
误;C.由分析可知,沉淀B为BaSO 和BaSO 的混合物,其中BaSO 遇硝酸可以被氧化为BaSO,故加入足
4 3 3 4
量的稀硝酸最终得到4.66g BaSO 沉淀,C错误;D.只有含有 的溶液加强碱溶液加热才能产生使湿润
4
的红色石蕊试纸变蓝的气体,D正确; 故选D。