文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(辽宁专用)
黄金卷07
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64
第Ⅰ卷
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项符合题目要
求。
1.党的二十大报告指出我国已进入创新型国家行列。下列说法正确的是
A.“华龙一号”核电机组使用的氦气不存在分子
B.“祖冲之二号”中的半导体存储器主要成分为硅
C.“奋斗者号”潜水器含钛合金,其熔点、强度都高于纯钛金属
D.“嫦娥五号”带回的月壤中含有磁铁矿,其主要成分为三氧化二铁
2.化学用语可以表达化学过程,下列化学用语的表达错误的是
A. 分子的VSEPR模型:
B.中子数为10的氧原于:
C.用电子云轮廓图表示 的 键形成的示意图:
D.用电子式表示 的形成:
3.设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.9.2g甲苯分子中含有碳碳双键的数目为0.3N
A
B.5.8g由NO和CO组成的混合气体中,原子总数为0.4N
A
C.标准状况下,22.4LO 与足量金属镁反应,转移的电子数为4N
2 A
D. 的 溶液中 和Na+的数目之和大于0.1N
A
4.下列说法不正确的是
A.不是所有的共价键( 键)都具有方向性
B. 键的键能比 键与 键的键能和大,所以 键不易发生加成反应C.根据电负性及价层电子对互斥理论可知, 分子的极性大于 分子的极性
D.基态Mg原子核外电子占有3个能层、4种能级、6个原子轨道、12种电子运动状态
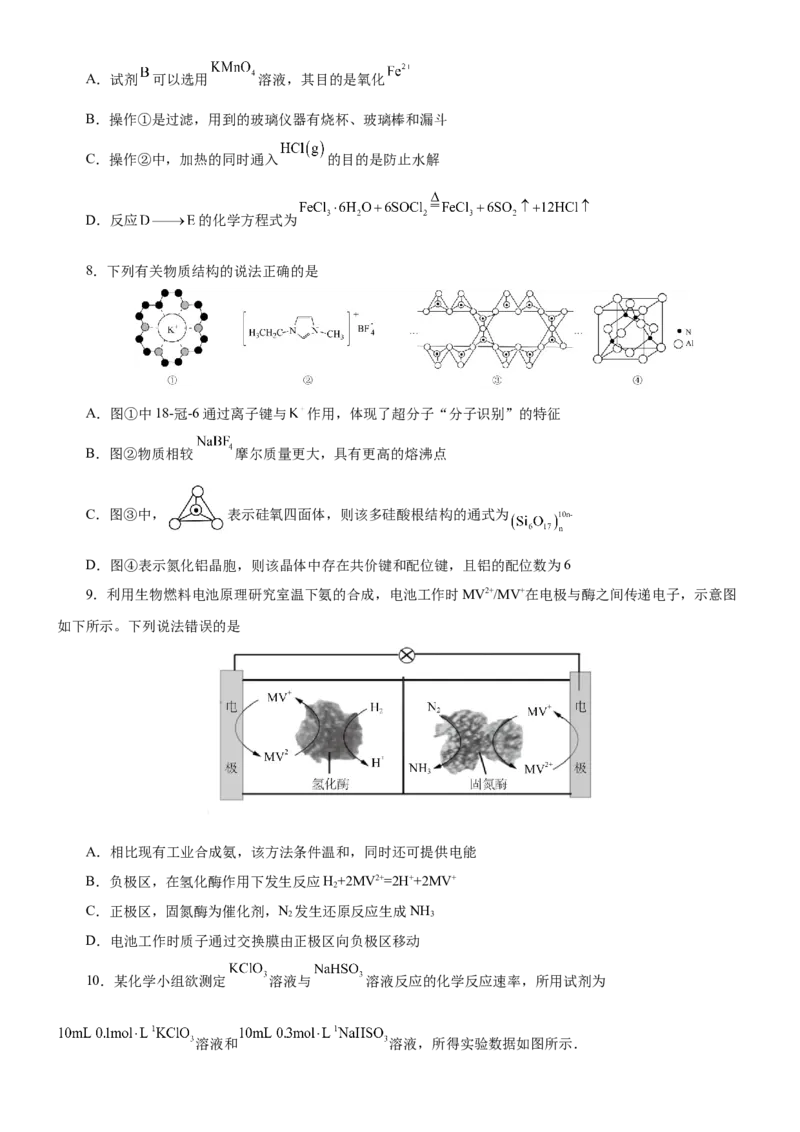
5.有机物M和N是合成药物的中间体,在一定条件下M可以转化为N,其过程如图所示,下列说法错误
的是
A.该反应类型为消去反应 B.可用金属Na鉴别M和N
C.M的分子式为 D.N可使酸性 溶液褪色
6. 是原子序数依次增大的前20号元素, 与 分子均含有14个电子, 元素的
基态原子都只有一个未成对电子且形成的离子具有相同的电子层结构, 的基态原子 轨道上电子数比 轨道
多5,下列说法不正确的是
A. 与 形成的化合物可能含非极性键
B.同周期第一电离能比 小的有5种
C. 原子形成稀有气体电子构型的简单离子的半径:
D. 形成的某种单质含有极性键
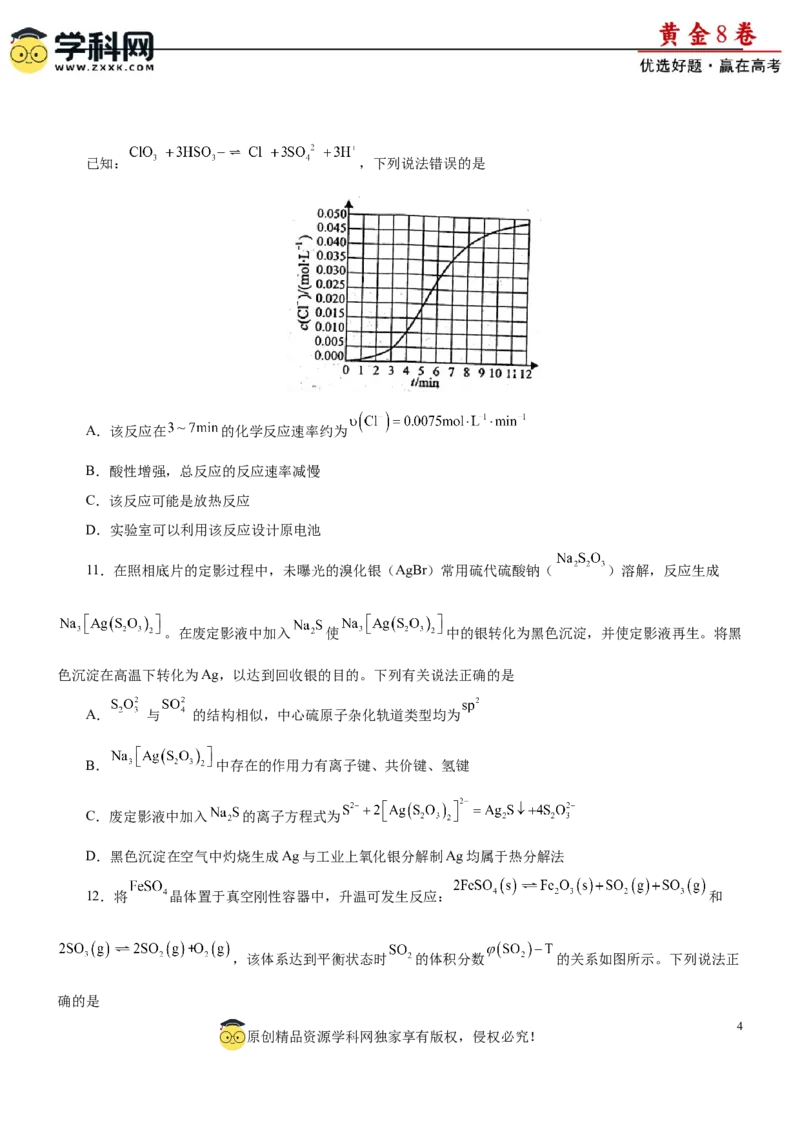
7.无水 常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和 杂
质)为原料制备无水 。
下列说法不正确的是
2
原创精品资源学科网独家享有版权,侵权必究!A.试剂 可以选用 溶液,其目的是氧化
B.操作①是过滤,用到的玻璃仪器有烧杯、玻璃棒和漏斗
C.操作②中,加热的同时通入 的目的是防止水解
D.反应 的化学方程式为
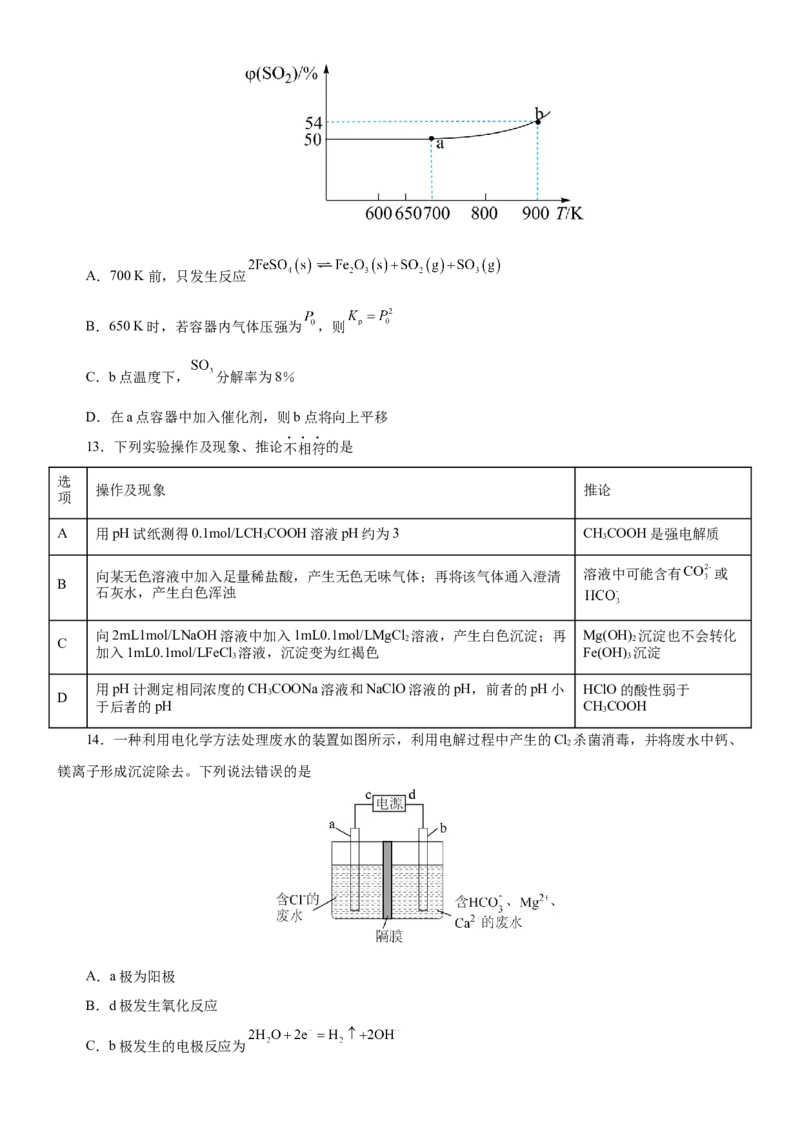
8.下列有关物质结构的说法正确的是
A.图①中18-冠-6通过离子键与 作用,体现了超分子“分子识别”的特征
B.图②物质相较 摩尔质量更大,具有更高的熔沸点
C.图③中, 表示硅氧四面体,则该多硅酸根结构的通式为
D.图④表示氮化铝晶胞,则该晶体中存在共价键和配位键,且铝的配位数为6
9.利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图
如下所示。下列说法错误的是
A.相比现有工业合成氨,该方法条件温和,同时还可提供电能
B.负极区,在氢化酶作用下发生反应H+2MV2+=2H++2MV+
2
C.正极区,固氮酶为催化剂,N 发生还原反应生成NH
2 3
D.电池工作时质子通过交换膜由正极区向负极区移动
10.某化学小组欲测定 溶液与 溶液反应的化学反应速率,所用试剂为
溶液和 溶液,所得实验数据如图所示.已知: ,下列说法错误的是
A.该反应在 的化学反应速率约为
B.酸性增强,总反应的反应速率减慢
C.该反应可能是放热反应
D.实验室可以利用该反应设计原电池
11.在照相底片的定影过程中,未曝光的溴化银(AgBr)常用硫代硫酸钠( )溶解,反应生成
。在废定影液中加入 使 中的银转化为黑色沉淀,并使定影液再生。将黑
色沉淀在高温下转化为Ag,以达到回收银的目的。下列有关说法正确的是
A. 与 的结构相似,中心硫原子杂化轨道类型均为
B. 中存在的作用力有离子键、共价键、氢键
C.废定影液中加入 的离子方程式为
D.黑色沉淀在空气中灼烧生成Ag与工业上氧化银分解制Ag均属于热分解法
12.将 晶体置于真空刚性容器中,升温可发生反应: 和
,该体系达到平衡状态时 的体积分数 的关系如图所示。下列说法正
确的是
4
原创精品资源学科网独家享有版权,侵权必究!A.700 K前,只发生反应
B.650 K时,若容器内气体压强为 ,则
C.b点温度下, 分解率为8%
D.在a点容器中加入催化剂,则b点将向上平移
13.下列实验操作及现象、推论不相符的是
选
操作及现象 推论
项
A 用pH试纸测得0.1mol/LCH COOH溶液pH约为3 CHCOOH是强电解质
3 3
向某无色溶液中加入足量稀盐酸,产生无色无味气体;再将该气体通入澄清 溶液中可能含有 或
B
石灰水,产生白色浑浊
向2mL1mol/LNaOH溶液中加入1mL0.1mol/LMgCl 溶液,产生白色沉淀;再 Mg(OH) 沉淀也不会转化
C 2 2
加入1mL0.1mol/LFeCl 溶液,沉淀变为红褐色 Fe(OH) 沉淀
3 3
用pH计测定相同浓度的CHCOONa溶液和NaClO溶液的pH,前者的pH小 HClO的酸性弱于
D 3
于后者的pH CHCOOH
3
14.一种利用电化学方法处理废水的装置如图所示,利用电解过程中产生的Cl 杀菌消毒,并将废水中钙、
2
镁离子形成沉淀除去。下列说法错误的是
A.a极为阳极
B.d极发生氧化反应
C.b极发生的电极反应为D.每产生0.5molCl ,在阴极室产生1molCaCO 沉淀
2 3
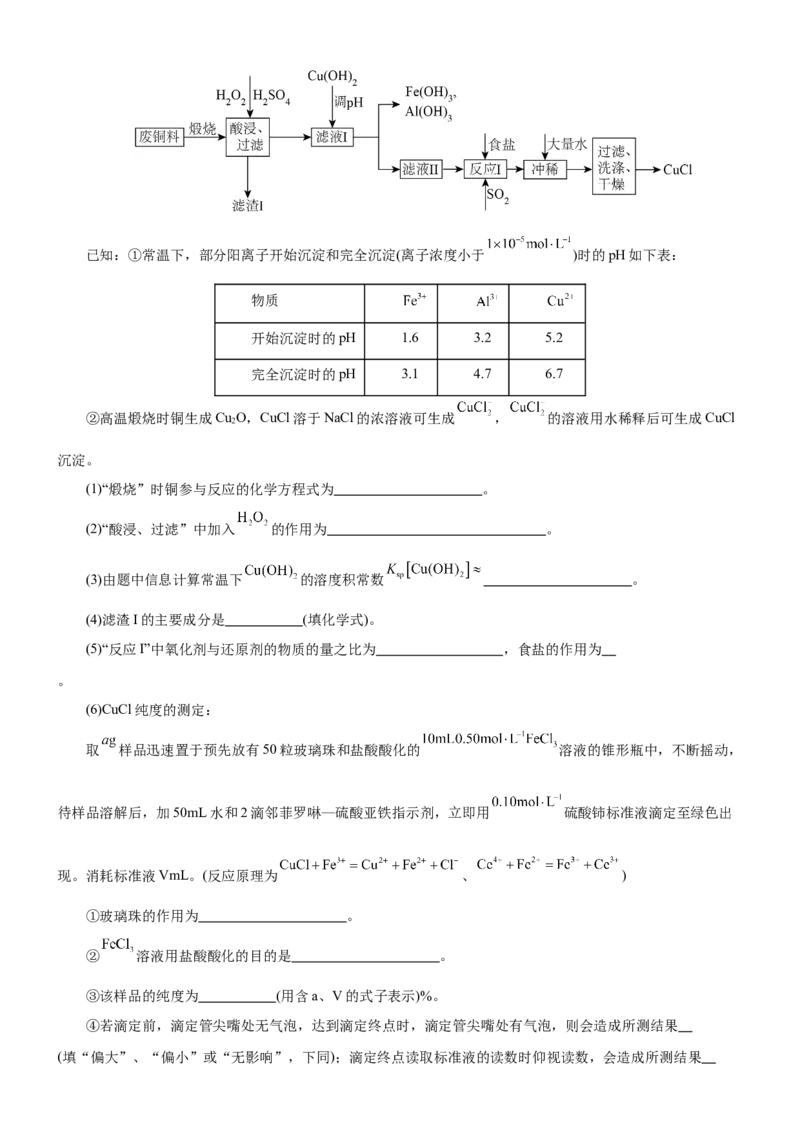
15.常温下,实验室用 的NaOH溶液滴定 的HA溶液。溶液中,含A微粒a、b
的分布系数δ、NaOH溶液的体积V与pH的关系如图所示。已知:HA的分布系数 。下
列叙述错误的是
A.x点对应溶液的pH约为5
B.p点对应的溶液中存在:
C.p→q对应的溶液中,水的电离程度一直增大
D.n点对应的溶液中存在:
第Ⅱ卷
二、非选择题:本题共4小题,共55分。
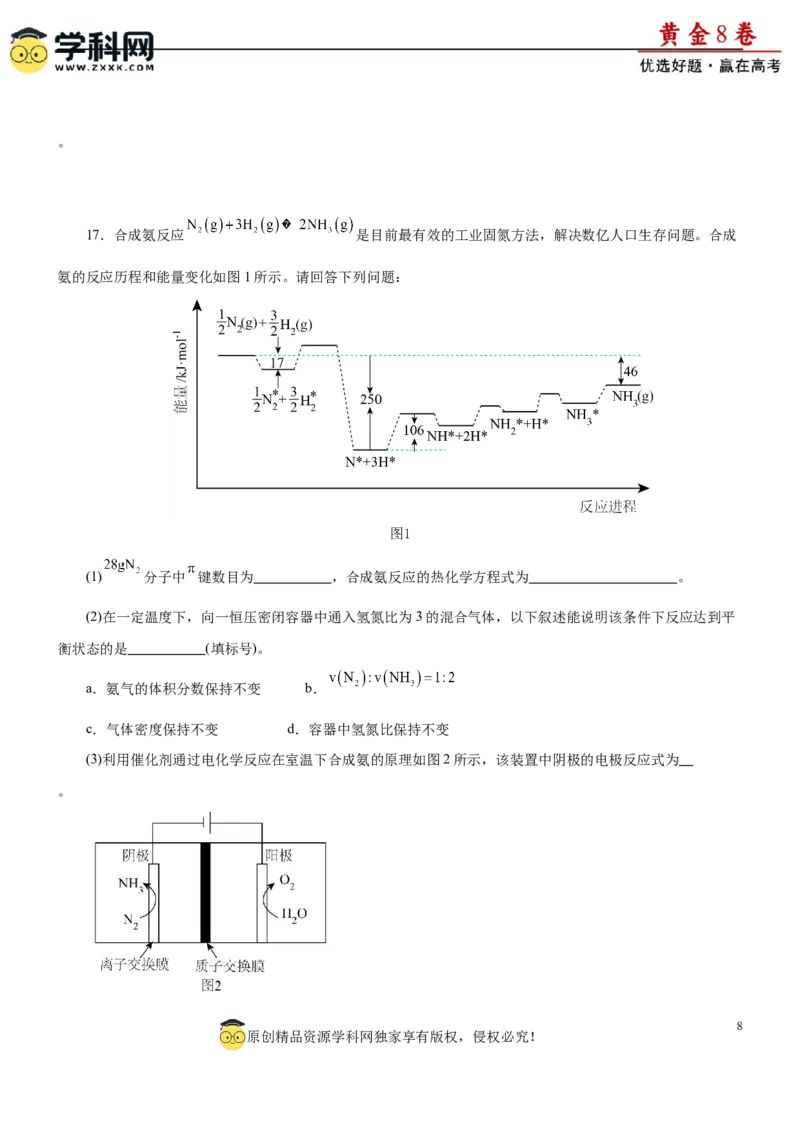
16.CuCl是有机合成的重要催化剂,可用于颜料、防腐等工业、工业上由废铜料(主要成分为金属铜,还
含Fe、Al及其化合物、 杂质)生产CuCl的工艺流程如下:
6
原创精品资源学科网独家享有版权,侵权必究!已知:①常温下,部分阳离子开始沉淀和完全沉淀(离子浓度小于 )时的pH如下表:
物质
开始沉淀时的pH 1.6 3.2 5.2
完全沉淀时的pH 3.1 4.7 6.7
②高温煅烧时铜生成Cu O,CuCl溶于NaCl的浓溶液可生成 , 的溶液用水稀释后可生成CuCl
2
沉淀。
(1)“煅烧”时铜参与反应的化学方程式为 。
(2)“酸浸、过滤”中加入 的作用为 。
(3)由题中信息计算常温下 的溶度积常数 。
(4)滤渣I的主要成分是 (填化学式)。
(5)“反应I”中氧化剂与还原剂的物质的量之比为 ,食盐的作用为
。
(6)CuCl纯度的测定:
取 样品迅速置于预先放有50粒玻璃珠和盐酸酸化的 溶液的锥形瓶中,不断摇动,
待样品溶解后,加50mL水和2滴邻菲罗啉—硫酸亚铁指示剂,立即用 硫酸铈标准液滴定至绿色出
现。消耗标准液VmL。(反应原理为 、 )
①玻璃珠的作用为 。
② 溶液用盐酸酸化的目的是 。
③该样品的纯度为 (用含a、V的式子表示)%。
④若滴定前,滴定管尖嘴处无气泡,达到滴定终点时,滴定管尖嘴处有气泡,则会造成所测结果
(填“偏大”、“偏小”或“无影响”,下同);滴定终点读取标准液的读数时仰视读数,会造成所测结果。
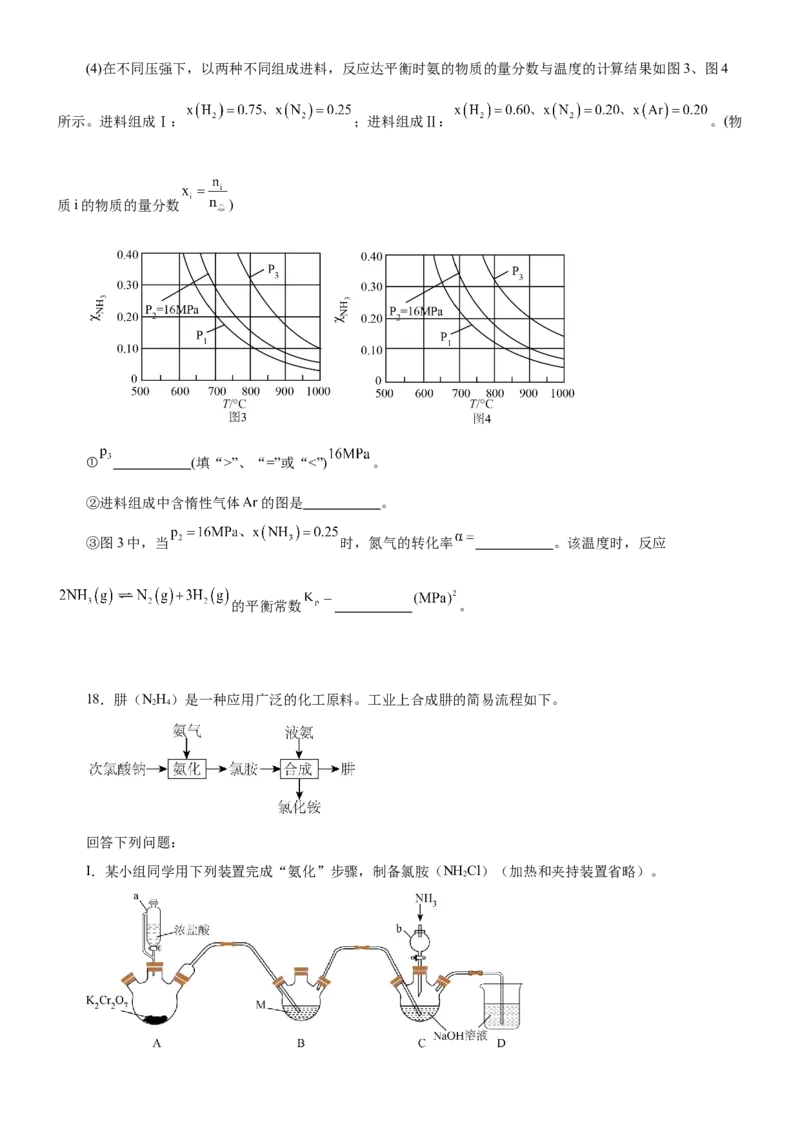
17.合成氨反应 是目前最有效的工业固氮方法,解决数亿人口生存问题。合成
氨的反应历程和能量变化如图1所示。请回答下列问题:
(1) 分子中 键数目为 ,合成氨反应的热化学方程式为 。
(2)在一定温度下,向一恒压密闭容器中通入氢氮比为3的混合气体,以下叙述能说明该条件下反应达到平
衡状态的是 (填标号)。
a.氨气的体积分数保持不变 b.
c.气体密度保持不变 d.容器中氢氮比保持不变
(3)利用催化剂通过电化学反应在室温下合成氨的原理如图2所示,该装置中阴极的电极反应式为
。
8
原创精品资源学科网独家享有版权,侵权必究!(4)在不同压强下,以两种不同组成进料,反应达平衡时氨的物质的量分数与温度的计算结果如图3、图4
所示。进料组成Ⅰ: ;进料组成Ⅱ: 。(物
质i的物质的量分数 )
① (填“>”、“=”或“<”) 。
②进料组成中含惰性气体 的图是 。
③图3中,当 时,氮气的转化率 。该温度时,反应
的平衡常数 。
18.肼(NH)是一种应用广泛的化工原料。工业上合成肼的简易流程如下。
2 4
回答下列问题:
I.某小组同学用下列装置完成“氨化”步骤,制备氯胺(NH Cl)(加热和夹持装置省略)。
2(1)与普通分液漏斗相比,仪器a的优点为 ,该仪器使用前需进行的操作为
。
(2)装置A中发生反应的离子方程式为 ,仪器b的作用除导气外,还有
。
(3)试剂M为 (填名称),若省略装置B,造成的后果是 。
(4)装置C中由次氯酸钠制备氯胺的化学方程式为 。
Ⅱ.测定最终所得肼的纯度。
称取0.40g产品配成250mL待测溶液,取25.00mL待测溶液加入20.00mL0.1000mol·L-1碘标准溶液,再加
入适量NaHCO 溶液调节pH,待NH 完全转化为N 后,加盐酸调节溶液的pH并加入少量淀粉溶液,立即用
3 2 4 2
0.02000mol·L-1NaSO 溶液滴定至终点。进行三次平行实验,测得平均消耗NaSO 溶液的体积为20.00mL(已
2 2 3 2 2 3
知: , )。
(5)滴定时盛放NaSO 溶液的是 (填“酸式滴定管”或“碱式滴定管”)。
2 2 3
(6)若滴定管用蒸馏水洗涤后,未润洗直接盛放NaSO 溶液,最终测得肼的纯度会 (填“偏
2 2 3
高”“偏低”或“无影响”)。
(7)肼的纯度为 。
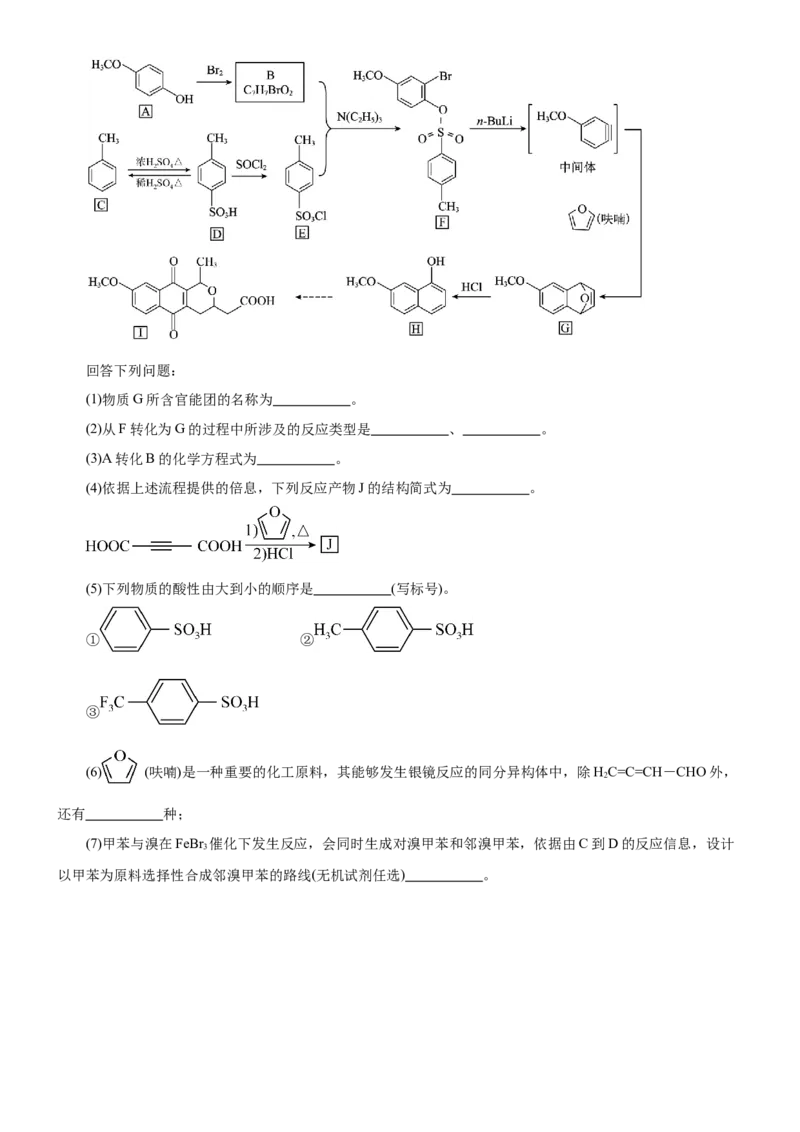
19.含有吡喃柒醌骨架的化合物常只有抗菌、抗病逛等生物活性,一-种合成该类化合物的路线如下(部分
反应条件已简化):
10
原创精品资源学科网独家享有版权,侵权必究!回答下列问题:
(1)物质G所含官能团的名称为 。
(2)从F转化为G的过程中所涉及的反应类型是 、 。
(3)A转化B的化学方程式为 。
(4)依据上述流程提供的倍息,下列反应产物J的结构简式为 。
(5)下列物质的酸性由大到小的顺序是 (写标号)。
① ②
③
(6) (呋喃)是一种重要的化工原料,其能够发生银镜反应的同分异构体中,除HC=C=CH-CHO外,
2
还有 种;
(7)甲苯与溴在FeBr 催化下发生反应,会同时生成对溴甲苯和邻溴甲苯,依据由C到D的反应信息,设计
3
以甲苯为原料选择性合成邻溴甲苯的路线(无机试剂任选) 。