文档内容
原子结构与元素周期表(3)
重难点 题型 分值
1. 了解碱金属、卤素在周期表中的位置。
重点 2. 了解碱金属、卤素原子结构特点,了解原子结构
填 空 和
与元素性质的关系。 6-8分
选择
了解碱金属、卤素性质的相似性与递变性,并能初
难点
步运用原子结构理论解释。
核心知识点一:
一、碱金属元素
1. 碱金属元素的原子结构
元素 元素 核电 原子结构 最外层 电子 原子
名称 符号 荷数 示意图 电子数 层数 半径/nm
碱金属 锂 Li 3 1 2 0.152
第1页钠 Na 11 1 3 0.186
钾 K 19 1 4 0.227
元素
铷 Rb 37 1 5 0.248
铯 Cs 55 1 6 0.265
结论:碱金属元素原子结构的共同点是 最外层电子数均为 1 ,不同点是电子层数和原子
半径不同,其变化规律是随着核电荷数的增加,电子层数逐渐增多,原子半径逐渐增大
2. 碱金属单质的物理性质
元素 Li、Na、K、Rb、Cs(原子序数增大)
除铯外,其余都呈银白色,它们都比较软,有延展性,密度较
相同点
小,熔点较低,导电、导热性强
递变 密度 逐渐增大(钾反常)
规律 熔、沸点 逐渐降低
①铯略带金属光泽;②锂的密度比煤油的小;③钠的密度比钾
个性特点
大
3. 碱金属单质的化学性质
(1)碱金属与氧气的反应
①实验现象:都能在空气中燃烧,钠产生黄色火焰(透过蓝色钴玻璃观察),钾产生
紫色火焰,钾燃烧更剧烈。
②反应方程式:2Na+O NaO、K+O KO 。
2 2 2 2 2
(2)碱金属与水的反应
碱金属单质 钠 钾
实验操作
第2页相同点:金属浮在水面上;熔成闪亮的小球;小球四处游动;发出嘶
实验现象 嘶的响声;反应后的溶液呈红色,
不同点:钾与水的反应有轻微爆炸声并着火燃烧
实验原理 2Na+2HO=== 2NaOH + H ↑ 2K+2HO=== 2KOH + H ↑
2 2 2 2
与水反应剧烈程度:K>Na;
实验结论
金属的活泼性:K>Na
4. 碱金属元素的原子结构与性质的关系
(1)相似性(R表示碱金属元素)
原子都容易失去最外层的一个电子,化学性质活泼,它们的单质都具有较强的还原性,
它们都能与氧气等非金属单质及水反应。碱金属与水反应的通式为2R+2HO===2ROH+
2
H↑。
2
(2)递变性
随着原子序数的递增,原子半径逐渐增大,原子核对最外层电子的引力逐渐减小,碱
金属元素的原子失电子能力逐渐增强,金属性逐渐增强。
①
②与O 的反应越来越剧烈,产物更加复杂,如Li与O 反应只能生成LiO,Na与O
2 2 2 2
反应还可以生成 NaO,而K与O 反应能够生成KO 等。
2 2 2 2
③与HO的反应越来越剧烈,如K与HO反应可能会发生轻微爆炸,Rb与Cs遇水发
2 2
生剧烈爆炸。
④最高价氧化物对应水化物的碱性逐渐增强,CsOH的碱性最强。
核心知识点二
一、卤族元素
1. 卤族元素的原子结构
①随着原子序数的递增,卤族元素原子核外电子层数依次增多,原子半径逐渐增大。
原子最外层电子数相同,都为7,都易得到1个电子,单质具有较强的氧化性
2. 卤素单质的物理性质
F Cl Br I
2 2 2 2
颜色、 淡黄绿色 黄绿色 深红棕色 紫黑色
状态 气体 气体 液体 固体
密度 逐渐增大
熔、沸点 逐渐升高
第3页卤素的原子结构特点
①卤族元素位于周期表第 Ⅶ A 族;
相同点
②最外层上都有7 个电子。
递变性 从F→I核电荷数依次增大,电子层数依次增多,原子半径依次增大
3. 卤素单质的化学性质
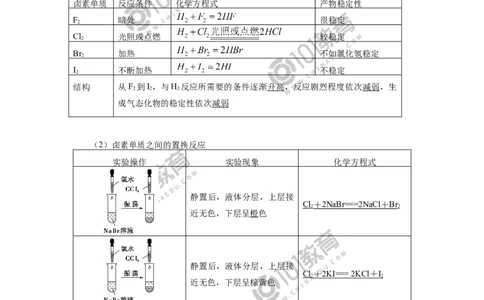
(1)卤素单质与氢气的反应
卤素单质 反应条件 化学方程式 产物稳定性
F 暗处 很稳定
2
Cl 光照或点燃 较稳定
2
Br 加热 不如氯化氢稳定
2
I 不断加热 不稳定
2
结构 从F 到I ,与H 反应所需要的条件逐渐升高,反应剧烈程度依次减弱,生
2 2 2
成气态化物的稳定性依次减弱
(2)卤素单质之间的置换反应
实验操作 实验现象 化学方程式
静置后,液体分层,上层接
Cl + 2NaB r == =2NaC l + B r
2 2
近无色,下层呈橙色
静置后,液体分层,上层接
Cl + 2K I == = 2KC l + I
2 2
近无色,下层呈棕黄色
静置后,液体分层,上层接
Br + 2K I == = 2KB r + I
2 2
近无色,下层呈棕黄色
结论 Cl→I 氧化性逐渐减弱,相应卤素离子还原性逐渐增强
2 2
微点拨:因为F 能与HO发生反应(2F +2HO===4HF+O ),所以F 不能从其他卤
2 2 2 2 2 2
第4页化物的盐溶液中置换出卤素单质。
4. 卤素的原子结构与化学性质的关系
(1)相似性(X表示卤素元素)
卤素原子都容易得到一个电子使其最外层达到8个电子的稳定结构,它们的单质都是
活泼的非金属单质,都具有较强的氧化性。
(1)与H 反应:X+H========2HX。
2 2 2
(2)与活泼金属(如Na)反应:2Na+X=====2NaX。
2
(3)与HO反应
2
①X+HO===HX+HXO(X=Cl、Br、I);
2 2
②2F+2HO===4HF+O。
2 2 2
(4)与NaOH溶液反应
X+2NaOH===NaX+NaXO+HO(X=Cl、Br、I)。
2 2
(2)递变性(X表示卤素元素)
随着原子序数的递增,原子半径逐渐增大,原子核对最外层电子的引力逐渐减小,卤
素原子得电子的能力逐渐减弱,非金属性逐渐减弱。
①
与H 反应越来越难,对应氢化物的稳定性逐渐减弱,还原性逐渐增强,即:稳定性:
2
HF>HCl>HBr>HI;还原性:HF<HCl<HBr<HI。
②卤素单质与变价金属(如Fe)反应时,F 、Cl 、Br 生成高价卤化物(如FeX ),
2 2 2 3
而I 只能生成低价卤化物(如FeI)。
2 2
③氢化物都易溶于水,其水溶液酸性依次增强,氢化物中 HCl、HBr、HI的熔、沸点
依次升高,HF的熔、沸点最高。
④最高价氧化物的水化物的酸性逐渐减弱,即酸性:HClO >HBrO >HIO ,HClO 是
4 4 4 4
已知含氧酸中酸性最强的酸。
核心知识点一:
下列关于碱金属按Li、Na、K、Rb、Cs的顺序叙述中不正确的是( )
A. 碱金属原子最外层都只有一个电子,在化学反应中容易失电子表现出强还原性
B. 单质的熔点和沸点依次递减
C. 单质都能与水反应生成碱,都能在空气中燃烧生成过氧化物
D. 原子半径逐渐增大,单质与水反应的剧烈程度逐渐增强
第5页【答案】C
【解析】金属锂在空气中燃烧只生成氧化物。
【考点】碱金属的性质
下列叙述不正确的是( )
A. 锂与水反应不如钠与水反应剧烈
B. 还原性:K>Na>Li,故K可以从NaCl溶液中置换出金属钠
C. 熔、沸点:Li>Na>K
D. 碱性:LiOH<NaOH<KOH
【答案】B
【解析】A中锂的活泼性比钠弱,与水反应不如钠剧烈;B中还原性,K>Na>Li,但
K不能置换出NaCl溶液中的Na,而是先与HO反应;C中碱金属元素从Li到Cs,熔、沸
2
点逐渐降低,即Li>Na>K>Rb>Cs;D中从Li到Cs,碱金属元素的金属性逐渐增强,
对应最高价氧化物的水化物的碱性依次增强,即碱性:LiOH<NaOH<KOH<RbOH<
CsOH。
【考点】碱金属的性质
核心知识点二:
下列说法正确的是( )
A. F、Cl、Br原子的最外层电子数都是7,次外层电子数都是8
B. 从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属性递增规律
C. 酸性:HFO >HClO>HBrO >HIO
4 4 4 4
D. 砹是原子序数最大的卤族元素,根据卤素性质的相似性,砹微溶于水,易溶于CCl
4
【答案】D
【解析】F的次外层电子数为2,Br的次外层电子数为18,A项错误;元素的非金属
性强弱可以根据其最高价氧化物对应水化物的酸性强弱比较,不能根据氢化物的酸性强弱
比较,B项错误;F无正化合价,不能形成HFO ,C项错误;由碘微溶于水、易溶于四氯
4
化碳可推知,砹微溶于水,易溶于CCl ,D项正确。
4
【考点】卤素的化学性质
第6页关于卤素(用X表示)的下列叙述正确的是( )
A. 卤素单质与水反应均可用X+HO===HXO+HX表示
2 2
B. HX热稳定性随核电荷数增加而增强
C. 卤素单质的颜色从F→I 随相对分子质量增大而逐渐加深
2 2
D. X-的还原性依次为F-<Cl-<Br-<I-,因此相对分子质量小的卤素单质可将相对
分子质量大的卤素从其盐溶液中置换出来
【答案】C
【解析】2F +2HO===O +4HF,A错;HX热稳定性随核电荷数增加而减弱,B错;
2 2 2
F 优先与水反应,故不能用F 从其他盐溶液中置换出来卤素单质,D错。
2 2
【考点】卤素的化学性质
(答题时间:25分钟)
选择题:本题包括12小题,每小题4分,共48分。
1. 我国西部地区蕴藏着丰富的锂资源,开发锂的用途是一个重要的科学课题。关于锂的
叙述不正确的是( )
A. 锂是较轻的金属
B. LiOH的碱性比NaOH弱
C. 锂的金属性比钠强
D. 锂在空气中燃烧生成LiO
2
2. 按氟、氯、溴、碘顺序,下列说法不正确的是( )
A. 它们的单质的熔、沸点逐渐升高
B. 原子半径逐渐增大,单质氧化性逐渐增强
C. 单质的颜色逐渐加深
D. 它们气态氢化物的稳定性逐渐减弱
3. 下列有关碱金属元素的叙述正确的是( )
A. 碱金属单质均为银白色,密度均小于水
B. 碱金属单质从Li到Cs,熔点依次升高
C. 氢氧化铯碱性强于氢氧化钠
D. 碱金属元素形成的阳离子,从Li+到Cs+氧化性依次增强
4. 向含有NaBr和KI的混合溶液中通入过量Cl ,充分反应后将溶液蒸干并灼烧所得物
2
质,最后剩余的固体是( )
A. NaCl和KI B. NaCl、KCl、I
2
第7页C. KCl和NaBr D. KCl和NaCl
5. (1)卤素氢化物中最不稳定的是________(写化学式)。
(2)下列两个族的元素,单质熔、沸点随原子序数递增而升高的是________(填序
号)。
A. 碱金属 B. 卤素
(3)下列反应中,更剧烈的是________(填序号)。
A. 钠与水反应 B. 钾与水反应
(4)取下列溶液分装两试管,再分别依次加入少量氯水和少量四氯化碳,用力振荡、
静置后,四氯化碳层显紫红色的是________(填序号)。
A. 溴化钠溶液 B. 碘化钾溶液
第8页1. 答案:C
解析:锂比钠的活泼性弱,在空气中燃烧只生成LiO,LiOH的碱性比NaOH弱,锂
2
的金属性比钠弱,C项错误。
2. 答案:B
解析:氟、氯、溴、碘的单质的熔、沸点逐渐升高,A正确;氟、氯、溴、碘同为第
ⅦA族元素,同主族从上到下,原子半径逐渐增大,非金属性逐渐减弱,因此单质氧化性
逐渐减弱,B错误;氟、氯、溴、碘的单质的颜色逐渐加深,C正确;非金属性F>Cl>Br
>I,非金属性越强,氢化物越稳定,则它们气态氢化物的稳定性逐渐减弱,D正确。
3. 答案:C
解析:碱金属单质中除了Rb、Cs,其他的密度均小于水,Cs略带金属光泽,其他的
都是银白色的,A错误;碱金属单质从Li到Cs,熔点依次降低,还原性依次增强,形成的
阳离子的氧化性依次降低,对应的氢氧化物碱性依次增强,C正确,B、D错误。
4. 答案:D
解析:过量的Cl 将I-、Br-从溶液中完全置换出来,在蒸干、灼烧过程中溴挥发、碘
2
升华,所得固体为NaCl和KCl。此题也可利用Cl、Br 、I 活泼性强弱用排除法选出D项。
2 2 2
5. 答案:(1)HI (2)B (3)B (4)B
解析:卤素中碘元素的非金属性最弱,氢化物最不稳定的是 HI;碱金属元素单质熔、
沸点随原子序数递增而降低,卤素单质熔、沸点随原子序数递增而升高;钾比钠活泼,与
水反应更剧烈;氯水与NaBr、KI溶液分别生成Br 、I ,而二者的四氯化碳溶液分别为橙
2 2
色、紫红色。
第9页