文档内容
浅析化学三大守恒规律同步练习
(答题时间:40分钟)
一、选择题
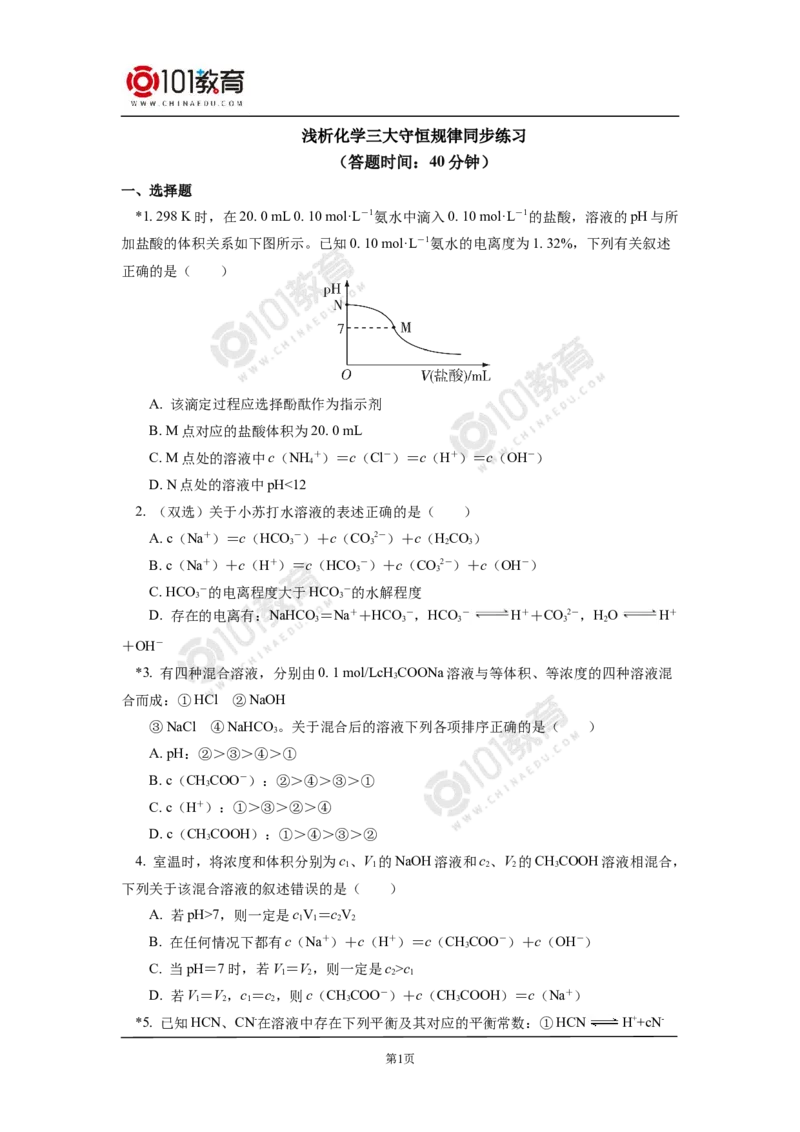
*1. 298 K时,在20. 0 mL 0. 10 mol·L-1氨水中滴入0. 10 mol·L-1的盐酸,溶液的pH与所
加盐酸的体积关系如下图所示。已知0. 10 mol·L-1氨水的电离度为1. 32%,下列有关叙述
正确的是( )
A. 该滴定过程应选择酚酞作为指示剂
B. M点对应的盐酸体积为20. 0 mL
C. M点处的溶液中c(NH +)=c(Cl-)=c(H+)=c(OH-)
4
D. N点处的溶液中pH<12
2. (双选)关于小苏打水溶液的表述正确的是( )
A. c(Na+)=c(HCO -)+c(CO2-)+c(HCO)
3 3 2 3
B. c(Na+)+c(H+)=c(HCO -)+c(CO2-)+c(OH-)
3 3
C. HCO -的电离程度大于HCO -的水解程度
3 3
D. 存在的电离有:NaHCO =Na++HCO -,HCO - H++CO2-,HO H+
3 3 3 3 2
+OH-
*3. 有四种混合溶液,分别由0. 1 mol/LcHCOONa溶液与等体积、等浓度的四种溶液混
3
合而成:①HCl ②NaOH
③NaCl ④NaHCO 。关于混合后的溶液下列各项排序正确的是( )
3
A. pH:②>③>④>①
B. c(CHCOO-):②>④>③>①
3
C. c(H+):①>③>②>④
D. c(CHCOOH):①>④>③>②
3
4. 室温时,将浓度和体积分别为c、V 的NaOH溶液和c、V 的CHCOOH溶液相混合,
1 1 2 2 3
下列关于该混合溶液的叙述错误的是( )
A. 若pH>7,则一定是cV=cV
1 1 2 2
B. 在任何情况下都有c(Na+)+c(H+)=c(CHCOO-)+c(OH-)
3
C. 当pH=7时,若V=V,则一定是c>c
1 2 2 1
D. 若V=V,c=c,则c(CHCOO-)+c(CHCOOH)=c(Na+)
1 2 1 2 3 3
*5. 已知HCN、CN-在溶液中存在下列平衡及其对应的平衡常数:①HCN H++cN-
第1页H >0,K ②CN-+H O HCN+OH- H >0,K,常温下(K= 6. 2×10-10),将
1 1 2 2 2 1
等体积、等物质的量浓度的HCN和NaCN溶液混合,下列叙述正确的是( )
△ △
A. 混合溶液的pH<7
B. 对混合溶液进行微热,K 增大、K 减小
1 2
C. K≈ 1. 6×10-5
2
D. c(Na+)=c(HCN)+c(CN—)
二、非选择题
6. 现有室温下浓度均为1×10-3 mol·L-1的几种溶液:①盐酸、②硫酸、③醋酸、④氯化
铵、⑤氨水、⑥NaOH溶液。回答下列问题:
(1)上述6种溶液中,水电离出的c(H+)最大的是________(填序号,下同),最
小的是________。
(2)将③、⑥混合后,若溶液呈中性,则消耗两溶液的体积为③________⑥(填“>”、
“<”或“=”),溶液中的离子浓度由大到小的顺序为______________________。
(3)将等体积的①、⑤混合,则溶液的pH________7(填“>”、“<”或“=”),用
离子方程式说明其原因:_________________________________________。
(4)向相同体积的①、②、③溶液中分别加入相同且足量的锌粒,反应的初始速率由
快到慢的顺序为________________,最终产生H 总量的关系为________。
2
(5)向相同体积的①、③溶液中分别加入相同浓度、相同体积的CHCOONa溶液,
3
充分混合后,混合液的pH大小关系为① ________③(填“>”、“<”或“=”,下同)。
(6)若将等体积的⑤、⑥溶液加热至相同温度后,溶液的pH大小关系为
⑤________⑥。
第2页浅析化学三大守恒规律同步练习参考答案
1. 【答案】D
【解析】将盐酸滴加到氨水中,滴定至终点时,由于生成强酸弱碱盐使溶液显酸性,
所以应选择甲基橙作指示剂,A错误;M点对应的pH=7,溶液为中性。当加入盐酸为20.
0 mL时,氨水与盐酸正好反应生成氯化铵,氯化铵是强酸弱碱盐,在水溶液中NH +发生
4
水解导致溶液呈酸性,B错误;根据电荷守恒,有:c(NH +)+c(H+)=c(Cl-)+c
4
(OH-),因298K时,溶液pH=7,c(H+)=c(OH-)=1×10-7mol·L-1,因此c(NH
4
+)=c(Cl-),但是c(NH +)=c(Cl-)>c(H+)=c(OH-),C错误;N点是滴定
4
的起点,因氨水是弱碱,0. 10 mol·L-1氨水的电离度为1. 32%,因此在0. 10mol·L-1氨水中,
c(OH-)=0. 10 mol·L-1×1. 32%=1. 32×10-3 mol·L-1,根据水的离子积常数,溶液中的c
(H+)=1×10-14/1. 32×10-3 =7. 6×10-12mol·L-1,pH<12,D正确。
2. 【答案】AD
【解析】由物料守恒可知A项正确;由电荷守恒可知c(Na+)+c(H+)=c(HCO
3
-)+2c(CO2-)+c(OH-),B项错误;由于小苏打水显碱性,所以HCO -的水解程度
3 3
大于它的电离程度,C项错误;由电解质存在电离平衡可知D项正确。
3. 【答案】B
【解析】等浓度的①②③④溶液的碱性:NaOH>NaHCO >NaCl>HCl,所以它们与
3
CHCOONa混合时溶液的碱性:②>④>③>①,即c(H+):①>③>④>②,pH:②
3
>④>③>①,A、C错误;HCl促进CHCOONa的水解,NaOH、NaHCO 抑制
3 3
CHCOONa的水解,且NaOH的抑制程度大于NaHCO 的抑制程度,NaCl对CHCOONa
3 3 3
的水解无影响,所以c(CHCOO-):②>④>③>①,c(CHCOOH):①>③>④>
3 3
②,B正确,D错误。
4. 【答案】A
【解析】当NaOH和CHCOOH按照等物质的量反应时,形成的是强碱弱酸盐,显碱
3
性,pH>7,而NaOH过量时,其pH也大于7,故A选项错误;根据电荷守恒关系式可知
c(Na+)+c(H+)=c(CHCOO-)+c(OH-),故B选项正确;当pH=7时,
3
CHCOOH的物质的量需大于NaOH的物质的量,若V=V,一定是c>c,C选项正确;
3 1 2 2 1
若V=V,c=c,则NaOH和CHCOOH恰好中和,依据物料守恒,知D选项正确。
1 2 1 2 3
5. 【答案】C
【解析】A. 由于不能确定HCN的电离程度与CN—的水解程度的相对大小,因此不能
确定溶液的酸碱性,则混合溶液的pH不一定小于7,A错误;
B. 水解和电离都是吸热的,所以对混合溶液进行微热,K、K 均增大,B错误;
1 2
第3页c(HCN)⋅c(OH−) c(HCN)⋅c(OH−)⋅c(H+) K 10−14
W
C. K= = = = ≈1.
2 c(CN−) c(CN−)⋅c(H+) K 6.2×10−10
1
6×10-5,C正确;
D. 根据物料守恒可知2c(Na+)=c(HCN)+c(CN-),D错误,答案选C。
6. 【答案】(1)④ ②
(2)> c(Na+)=c(CHCOO-)>c(H+)=c(OH-)
3
+
(3)< NH +HONH ·H O+H+
4 2 3 2
(4)②>①>③ ②>①=③
(5)< (6)<
【解析】(1)酸和碱会抑制水的电离,c(H+)或c(OH-)越大,水的电离程度越
小。能水解的盐可促进水的电离,故④中水的电离程度最大,②中水的电离程度最小。
(2)若③和⑥等体积反应,则恰好生成CHCOONa,水解呈碱性,现反应后呈中性,
3
则醋酸过量。由于溶液中c(H+)=c(OH-),根据电荷守恒得c(Na+)=c(CHCOO
3
-),由此可得溶液中离子浓度的大小关系。
+
(3)等体积的①、⑤混合,恰好完全反应生成NH Cl,NH 水解呈酸性。
4 4
(4)由于起始时c(H+)>c(H+)1>c(H+),c(H+)越大,反应速率越快。由
2 3
于酸提供的H+总量n(H+)>n(H+)=n(H+),由此可知产生H 的总量关系为②>①
2 1 3 2
=③。
(5)由于在盐酸中加入CHCOONa溶液会先反应生成醋酸,因此溶液pH上升较慢,
3
故混合液的pH:①<③。
(6)虽然加热能促使氨水的电离,但仍不可能完全电离,而且由于温度升高,NH 会
3
挥发,因此溶液的pH:⑤<⑥。
第4页突破溶液中粒子浓度的大小比较同步练习
(答题时间:40分钟)
一、选择题
1. HA为酸性略强于醋酸的一元弱酸。在0. 1 mol·L-1 NaA溶液中,离子浓度关系正确的
是( )
A. c(Na+)>c(A-)>c(H+)>c(OH-)
B. c(Na+)>c(OH-)>c(A-)>c(H+)
C. c(Na+)+c(OH-)=c(A-)+c(H+)
D. c(Na+)+c(H+)=c(A-)+c(OH-)
*2. t ℃时,某浓度氯化铵溶液的pH=4,下列说法中一定正确的是( )
A. 由水电离出的氢离子浓度为10-10 mol·L-1
B. 溶液中c(H+)·c(OH-)=1×10-14
+
C. 溶液中c(Cl-)>c(NH )>c(H+)>c(OH-)
4
+
D. 溶液中c(NH ·H O)+c(NH )=c(Cl-)+c(OH-)
3 2 4
3. 一定温度下,下列溶液的离子浓度关系式正确的是( )
A. pH=5的HS溶液中,c(H+)=c(HS-)=1×10-5 mol·L-1
2
B. pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C. pH=2的HC O 溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)
2 2 4
−
=c(OH-)+c(HC O )
2 4
D. pH相同的①CHCOONa ②NaHCO ③NaClO三种溶液的c(Na+):①>②>③
3 3
4. 室温下,下列溶液中粒子浓度关系正确的是( )
A. Na S溶液:c(Na+)>c(HS-)>c(OH-)>c(HS)
2 2
−
B. Na C O 溶液:c(OH-)=c(H+)+c(HC O )+2c(HC O)
2 2 4 2 4 2 2 4
2−
C. Na CO 溶液:c(Na+)+c(H+)=2c(CO )+c(OH-)
2 3 3
D. cH COONa和CaCl 混合溶液:c(Na+)+c(Ca2+)=c(CHCOO-)+c
3 2 3
(CHCOOH)+2c(Cl-)
3
*5. 已知0. 1molL-1的二元酸HA溶液的pH=4. 0则下列说法中正确的是
2
A. 在NaA、NaHA两溶液中,离子种类不相同
2
B. 在溶质物质的量相等的NaA、NaHA两溶液中有:2c(Na+)=3c(A2-)+3c
2
(HA-)+3c(HA)
C. 在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+c(A2-)
D. 在NaA溶液中一定有:c(Na+)>c(A2-)>c(H+)>c(OH-)
2
6. 常温下,有体积相同的四种溶液:①pH=2的CHCOOH溶液;②pH=2的硫酸;
3
第5页③pH=12的氨水;④pH=12的NaOH溶液。下列说法正确的是
2−
A. ①和②混合后c(H+)=c(CHCOO-)+c(OH-)+2c(SO )
3 4
B. ①和④溶液中:c(Na+)=c(CHCOO-)+c(CHCOOH)=0. 01mol·L−1
3 3
2− +
C. ②和③混合溶液中:c(SO )>c(NH )>c(OH-)>c(H+)
4 4
D. 四种溶液各稀释100倍,溶液pH:④>③>①>②
*7. 25℃时,向20. 00mL的NaOH溶液中逐滴加入某浓度的CHCOOH溶液。滴定过程
3
中,溶液的pH与滴入CHCOOH溶液的体积关系如图所示,点②时NaOH溶液恰好被中和。
3
则下列说法中,正确的是
A. CHCOOH溶液的pH=1
3
B. 图中点①到点③所示溶液中,水的电离程度增大
C. 点④所示溶液中存在:c(CHCOOH)+2c(H+)=c(CHCOO-)+2c(OH-)
3 3
D. 滴定过程中会存在:c(CHCOO-)>c(Na+)=c(OH-)>c(H+)
3
二、非选择题
8. (1)0. 020 mol·L-1的HCN(aq)与0. 020 mol·L-1 NaCN(aq)等体积混合,已知该
混合溶液中c(Na+)>c(CN-),用“>”“<”“=”符号填空。
①溶液中c(OH-)________c(H+)。
②溶液中c(HCN)________c(CN-)。
+
(2)已知某溶液中存在OH-、H+、NH 、Cl-四种离子,某同学推测其离子浓度大
4
小顺序有如下四种关系:
+
A. c(Cl-)>c(NH )>c(H+)>c(OH-)
4
+
B. c(Cl-)>c(NH )>c(OH-)>c(H+)
4
+
C. c(NH )>c(Cl-)>c(OH-)>c(H+)
4
+
D. c(Cl-)>c(H+)>c(NH )>c(OH-)
4
填写下列空白:
①若溶液中只溶解了一种溶质,则该溶质是________,上述四种离子浓度的大小顺序
为________(填序号)。
②若上述关系中C是正确的,则溶液中的溶质为__________________;
第6页若上述关系中D是正确的,则溶液中的溶质为____________________。
③若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c
(HCl)________c(NH ·H O)(填“大于”“小于”或“等于”,下同),混合前酸中c
3 2
(H+)和碱中c(OH-)的关系为c(H+)________c(OH-)。
第7页突破溶液中粒子浓度的大小比较同步练习参考答案
1.【答案】D
【解析】HA为一元弱酸,则NaA为强碱弱酸盐,溶液由于A-的水解显碱性,离子浓
度大小为c(Na+)>c(A-)>c(OH-)>c(H+),A项错误,B项错误;根据溶液中电
荷守恒,则c(Na+)+c(H+)=c(A-)+c(OH-),C项错误,D项正确。
2.【答案】C
+
【解析】NH 水解促进了HO的电离,溶液中的c(H+)即为HO电离的
4 2 2
+
c(H+),A错;在25 ℃时,水的离子积为1×10-14,B错;NH 水解生成H+,故c
4
+ +
(Cl-)>c(NH )>c(H+)>c(OH-),C正确;由物料守恒可知c(Cl-)=c(NH
4 4
)+c(NH ·H O),D错误。
3 2
3.【答案】D
【解析】A. pH=5的HS溶液中H+的浓度为1×10-5 mol·L-1,但是HS-的浓度会小
2
于H+的浓度,H+来自于HS的第一步电离、HS-的电离和水的电离,故H+的浓度大于
2
HS-的浓度,错误。B. 弱碱不完全电离,弱碱稀释10倍时,pH减小不到一个单位,a碳酸的
酸性>次氯酸的酸性,根据越弱越水解的原则,pH相同的三种钠盐,浓度的大小关系为醋
酸钠>碳酸氢钠>次氯酸钠,则钠离子的浓度为①>②>③,故D正确。
4.【答案】B
【解析】A. Na S溶液中微粒关系为:c(Na+)>c(S2-)>c(OH-)>
2
c(HS-)>c(HS),A错误。
2
2− −
B. Na C O 溶液中,由电荷守恒得:c(Na+)+c(H+)=2c(C O )+c(HC O
2 2 4 2 4 2 4
)+c(OH-)①
2− −
由物料守恒得:c(Na+)=2c(C O )+2c(HC O )+2c(HC O)②
2 4 2 4 2 2 4
−
由①-②得:c(OH-)=c(H+)+c(HC O )+2c(HC O),B正确。
2 4 2 2 4
2− −
C. Na CO 溶液中,由电荷守恒得:c(Na+)+c(H+)=2c(CO )+c(HCO )
2 3 3 3
+c(OH-),C错误。
D. cH COONa和CaCl 混合溶液中存在:c(Na+)=c(CHCOO-)+c
3 2 3
(CHCOOH)①2c(Ca2+)=c(Cl-)②
3
①+②得:c(Na+)+2c(Ca2+)=c(CHCOO-)+c(CHCOOH)+c(Cl-),D
3 3
错误。
5.【答案】B
【解析】A、在NaA、NaHA两溶液中,A2-离子水解,HA-存在电离和水解,所以离
2
第8页子种类相同,A错误;
B. 根据物料守恒中,在NaA中存在c(Na+)=2c(A2-)+2c(HA-)+2c(HA),
2
在NaHA中存在c(Na+)=c(A2-)+c(HA-)+c(HA),两种物质的物质的量浓度相等,
所以得2c(Na+)=3c(A2-)+3c(HA-)+3c(HA),B正确;
C. 根据电荷守恒得c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-),C错误;
D. 在NaA溶液中,A2-离子分步水解,溶液呈碱性;一定有:c(Na+)>c(OH-)
2
>c(A2-)>c(H+),D错误;
选B。
6.【答案】A
【解析】A. pH=2的CHCOOH溶液和pH=2的硫酸溶液中c(H+)均为10-2mol/L,醋
3
酸的浓度大于10-2mol/L,根据反应量的关系,混合后得到的是硫酸和醋酸的混合物,根据
2−
电荷守恒:c(H+)=c(CHCOO-)+c(OH-)+2c(SO ),故A正确;
3 4
B. ①和④溶液发生反应得到的是醋酸钠溶液,醋酸的浓度大于氢氧化钠,得到的是醋
酸和醋酸钠的混合物,所以c(Na+)≠c(CHCOO-)+c(CHCOOH),故B错误;
3 3
C. 体积相同的pH=2的硫酸和pH=12的氨水混合后,氨水过量,得到的是氨水和硫酸
+ 2−
铵得混合物,c(NH )>c(SO )>c(OH-)>c(H+),故C错误;
4 4
D. ①pH=2的CHCOOH溶液,加水稀释促进弱电解质的电离,溶液的pH变化小于2
3
个单位,pH<4②pH=2的硫酸,稀释100倍,pH=4,③pH=12的氨水加水稀释促进弱电解
质的电离,溶液的pH变化小于2个单位,pH>10,④pH=12的NaOH溶液,稀释100倍,
pH=10,所以溶液pH大小顺序:③>④>②>①,故D错误。
7.【答案】C
【解析】A. 根据图象可知,没有加入CHCOOH溶液时,NaOH溶液的pH=13,说明
3
c(NaOH)=0.1mol/L,②点时NaOH溶液恰好被中和消耗醋酸溶液20mL,则醋酸的浓度
为0.1mol/L,由于CHCOOH为弱酸,0.1mol/L的CHCOOH溶液的pH>1,故A错误;
3 3
B. 图中点①到点③所示溶液中随滴入醋酸反应,水的电离被抑制程度减小,恰好反应
时水的电离程度最大,之后继续滴加醋酸,对水电离起到抑制作用,所以图中点①到点③
所示溶液中,水的电离程度先增大后减小,故B错误;
C. 点④所示溶液是等浓度的醋酸和醋酸钠溶液,根据物料守恒可知:c(CHCOOH)
3
+c(CHCOO-)=2c(Na+),溶液中存在电荷守恒:c(Na+)+c(H+)=c(CHCOO-)+c
3 3
(OH-),二者结合可得:c(CHCOOH)+2c(H+)=c(CHCOO-)+2c(OH-),故C正
3 3
确;
D. 溶液中满足电荷守恒,而c(CHCOO-)>c(Na+)=c(OH-)>c(H+)违反了电荷
3
守恒,不可能存在该浓度关系,故D错误;
答案:C。
第9页8.【答案】(1)①> ②>
(2)①NH Cl A
4
②NH Cl和NH ·H O NH Cl和HCl
4 3 2 4
③小于 大于
【解析】(1)c(Na+)>c(CN-),说明NaCN的水解程度比HCN的电离程度大,c
(OH-)>c(H+),c(HCN)>c(CN-)。
+
(2)①若溶液中只有一种溶质,该溶质为NH Cl,因NH 水解溶液呈酸性,离子浓
4 4
+
度的大小关系为c(Cl-)>c(NH )>c(H+)>c(OH-)。
4
+
②因为c(OH-)>c(H+)、c(NH )>c(Cl-),所以溶液中除含有NH Cl外,还
4 4
+
必须含有NH ·H O。若c(Cl-)>c(H+)>c(NH )>c(OH-),则说明溶液中含有
3 2 4
NH Cl和HCl。
4
③NH Cl水解溶液呈酸性,若等体积稀盐酸与氨水混合后呈中性,说明氨水过量,故
4
c(HCl)