文档内容
溶液的酸碱性和pH同步练习
(答题时间:40分钟)
一、选择题
1. 25 ℃时,向V mL pH=a的盐酸中,滴加pH=b的NaOH溶液10V mL时,溶液中的
Cl-和Na+的物质的量相等,则a+b的值是( )
A. 13 B. 14
C. 15 D. 不能确定
2. 313 K 时,水的 K =3.0×10-14,则在 313 K 时,c(H+)=10-7 mol·L-1的溶液
W
( )
A. 呈酸性 B. 呈中性
C. 呈碱性 D. 无法判断
3. 用pH试纸测定溶液的pH,正确操作是( )
A. 将一小块试纸放在表面皿上,用玻璃棒蘸取少量待测液点在试纸上,再与标准比色
卡对照
B. 将一小块试纸用蒸馏水润湿后放在表面皿上,用玻璃棒蘸取少量待测液点在试纸上,
再与标准比色卡对照
C. 将一小块试纸在待测液中蘸一下,取出后放在表面皿上,与标准比色卡对照
D. 将一小块试纸先用蒸馏水润湿后,再在待测液中蘸一下,取出后与标准比色卡对照
*4. 常温下,下列各组离子在指定溶液中能大量共存的是( )
A. pH=1的溶液中:Fe2+、NO、SO、Na+
B. 由水电离的c(H+)=1×10-14mol·L-1的溶液中:Ca2+、K+、Cl-、HCO
C. c(H+)/c(OH-)=1012的溶液中:NH、Al3+、NO、Cl-
D. c(Fe3+)=0.1 mol·L-1的溶液中:K+、ClO-、SO、SCN-
*5. 已知温度T时水的离子积常数为K ,该温度下,将浓度为a mol·L-1的一元酸HA与
w
b mol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
A. a=b
B. 混合溶液的pH=7
C. 混合溶液中,c(H+)= mol·L-1
D. 混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
6. 下列叙述正确的是( )
A. 95 ℃纯水的pH<7,说明加热可导致水呈酸性
B. pH=3的醋酸溶液,稀释至10倍后pH=4
C. 0.2 mol·L-1的盐酸,与等体积水混合后pH=1
D. pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7
第1页二、填空题
7. 某温度下,纯水中 c(H+)=2×10-7 mol·L-1,则此溶液中c(OH-)为________
mol·L-1,该温度时的 K =________。如温度不变,滴入稀盐酸使 c(H+)=5.0×10-6
W
mol·L-1,则c(OH-)为________ mol·L-1。
8. 常温下,求算下列溶液中水电离出的c(H+)和c(OH-)。
(1)pH=2的HSO 溶液中,c(H+)=________,c(OH-)=________。
2 4
(2)pH=10的NaOH溶液中,c(H+)=________,c(OH-)=________。
*9. 有一学生在实验室测某溶液的pH,实验时,他先用蒸馏水润湿pH试纸,然后用洁
净干燥的玻璃棒蘸取试样进行检测。
(1)该学生的操作________(填“正确”或“错误”),其理由是__________
_______________________________________________________________;
(2)该操作是否一定有误差?______________________________________
______________________________________________________________;
(3)若用此方法分别测定c(OH-)相等的氢氧化钠溶液和氨水的pH,误差较大的
是________________,原因是_______________________________________
______________________________________________________________;
(4)只从下列试剂中选择实验所需的试剂,你能否区分 0.1 mol·L-1硫酸溶液和0.01
mol·L-1硫酸溶液?
________________(填“能”或“否”),简述操作过程:_______________
_______________________________________________________________。
试剂:a.紫色石蕊试液 b. 酚酞试液 c. 甲基橙溶液 d. 蒸馏水 e. 氯化钡溶液 f.
pH试纸
第2页溶液的酸碱性和pH同步练习参考答案
1. 【答案】A
【解析】由HCl+NaOH===NaCl+HO知,当Cl-和Na+的物质的量相等时,HCl和
2
NaOH完全反应,即盐酸中的 n(H+)等于NaOH中的n(OH-),则10-a·V=10-14+
b·10V,则a+b=13。
2. 【答案】C
【解析】根据溶液中c(H+)与c(OH-)的相对大小判断。由K =c(H+)·c(OH
W
-)可得:c(OH-)= mol·L-1=3.0×10-7 mol·L-1,c(H+)10 mL
C. ab
6. 25 ℃时,将某强酸和某强碱溶液按1∶10的体积比混合后,溶液恰好呈中性,则混合
第5页前此强酸和强碱的pH和为( )
A. 12 B. 13
C. 14 D. 15
*7. 常温下,若1体积硫酸与2体积pH=11的氢氧化钠溶液混合后的溶液的pH=3(混
合后体积变化不计),则二者物质的量浓度之比应为( )
A. 5∶1 B. 5∶2
C. 1∶5 D. 2∶5
二、填空题
*8. 室温下,有一pH为12的NaOH溶液100 mL,如果将其pH降为11,则:
(1)若用蒸馏水应加入________mL;
(2)若用pH=10的NaOH溶液,应加入______mL;
(3)若用pH=2的盐酸,应加入________mL;
(4)若用0.01 mol·L-1硫酸,应加入________mL。
第6页溶液的pH的计算同步练习参考答案
1. 【答案】B
【解析】硫酸是强电解质,完全电离,醋酸是弱电解质,加水稀释,醋酸继续电离出
H+,分别加水稀释100倍后,硫酸溶液的pH为5,醋酸溶液的pH小于5,所以硫酸溶液
的pH变化比醋酸溶液大,故A错误;pH均为3的醋酸和硫酸,溶液中c(H+)=1×10-3
mol·L-1,溶液中c(OH-)= mol·L-1=1×10-11 mol·L-1,溶液中c (H+)=c
水
(OH-),故两种溶液中,c (H+)=1×10-11 mol·L-1,故B正确;硫酸为强酸,pH=3
水
的硫酸与pH=11的氢氧化钠溶液等体积混合恰好中和,而醋酸为弱酸,若 pH=3的醋酸
与pH=11的氢氧化钠溶液等体积混合,醋酸过量,故C错误;硫酸是强电解质,完全电
离,醋酸是弱电解质,溶液中主要以醋酸分子形式存在,与足量的 Zn反应,醋酸提供的H
+大于硫酸,Zn与醋酸反应产生氢气的物质的量较大,故D错误。
2. 【答案】B
【解析】pH=11的烧碱溶液稀释1 000倍后,pH=8;pH=11的氨水稀释1 000倍后,
由于稀释促进电离,pH>8;pH=4的醋酸和pH=10的烧碱溶液等体积混合后,醋酸过量,
溶液呈酸性,pH<7;pH=5的盐酸稀释1 000倍后,pH接近7但小于7;所以B的pH最
大。
3. 【答案】C
【解析】相同体积、相同pH的一元强酸和一元中强酸中,H+浓度相等,所以刚开始
与锌反应的速率是相同的,随着反应的进行,中强酸继续电离,故反应速率较强酸快,排
除B、D;又因中强酸的物质的量浓度大于强酸,所以与足量的锌反应生成氢气的量较多,
排除A项。
4. 【答案】C
【解析】设原溶液的浓度为c,两者反应后碱过量,应先求c(OH-),c(OH-)=
=0.01 mol·L-1,解得c=0.05 mol·L-1。
5. 【答案】D
【解析】因为醋酸是弱酸,盐酸是强酸,在稀释相同体积后,醋酸的 pH变化相对盐
酸小,则当稀释后两者的pH仍相等,故a>b。
6. 【答案】B
【解析】强酸和强碱溶液按1∶10的体积比混合恰好呈中性,则说明酸溶液中的氢离
子浓度等于碱溶液中的氢氧根离子的浓度的10倍,故pH和为13,选B。
7. 【答案】B
第7页【解析】HSO +2NaOH===Na SO +2HO,设硫酸的物质的量浓度为c mol·L-1,体
2 4 2 4 2
积为V L,氢氧化钠溶液浓度为10-3 mol·L-1,体积为2V L,混合后pH=3,即c(H+)
= mol·L-1=10-3 mol·L-1,解得c= ×10-3,则二者物质的量浓度之比
应为5∶2,B项正确。
8. 【答案】(1)900 (2)1 000 (3)81.8 (4)42.86
【解析】(1)由c(OH-) =10-3 mol·L-1= ,得V(HO)
稀释 2
=0.9 L=900 mL。
(2)设加入pH=10的NaOH溶液的体积为x,c(OH-)=10-3 mol·L-1
=
得x=1 L=1 000 mL。
(3)设加入pH=2的盐酸的体积为y,
c(OH-)=10-3 mol·L-1
=
得y=0.081 8 L=81.8 mL。
(4)设加入硫酸的体积为z
c(OH-)=10-3 mol·L-1
=
得z=0.042 86 L=42.86 mL。
第8页酸碱中和滴定同步练习
(答题时间:40分钟)
一、选择题
1. 用NaOH溶液滴定盐酸时,由于滴定速率太快,当混合溶液变红时不知 NaOH是否过
量,判断它是否过量的方法是( )
A. 加入5 mL盐酸再进行滴定
B. 返滴一滴待测盐酸
C. 重新进行滴定
D. 以上方法均不适用
2. 下列是一段关于中和滴定的实验叙述:
(1)取一锥形瓶,用待测NaOH溶液润洗两次;
(2)在锥形瓶中放入25 mL待测NaOH溶液;
(3)加入几滴石蕊试剂作指示剂;
(4)取一支酸式滴定管,洗涤干净;
(5)直接往酸式滴定管中注入标准酸溶液,进行滴定;
(6)左手旋转滴定管的玻璃活塞,右手不停摇动锥形瓶;
(7)两眼注视着滴定管内盐酸溶液液面下降,直至滴定终点。
其中错误的是( )
A. (4)(6)(7) B. (1)(5)(6)(7)
C. (3)(5)(7) D. (1)(3)(5)(7)
3. 在25 ℃时,用0.125 mol·L-1的标准盐酸溶液滴定25.00 mL未知浓度的NaOH溶液所
得滴定曲线如图所示,图中K点代表的pH为( )
A. 13 B. 12
C. 10 D. 11
*4. 使用酸碱中和滴定的方法,用0.01 mol·L-1盐酸滴定锥形瓶中未知浓度的NaOH溶液,
下列操作会使测定结果偏高的是( )
①用量筒量取浓盐酸配制0.01 mol·L-1稀盐酸时,量筒用蒸馏水洗净后未经干燥直接
量取浓盐酸 ②配制稀盐酸定容时,俯视容量瓶刻度线 ③滴定结束时,读数后发现滴定
管下端尖嘴处悬挂有一滴液滴 ④滴定过程中用少量蒸馏水将锥形瓶内壁附着的盐酸冲下
A. ①③ B. ②④
C. ②③④ D. ①②③④
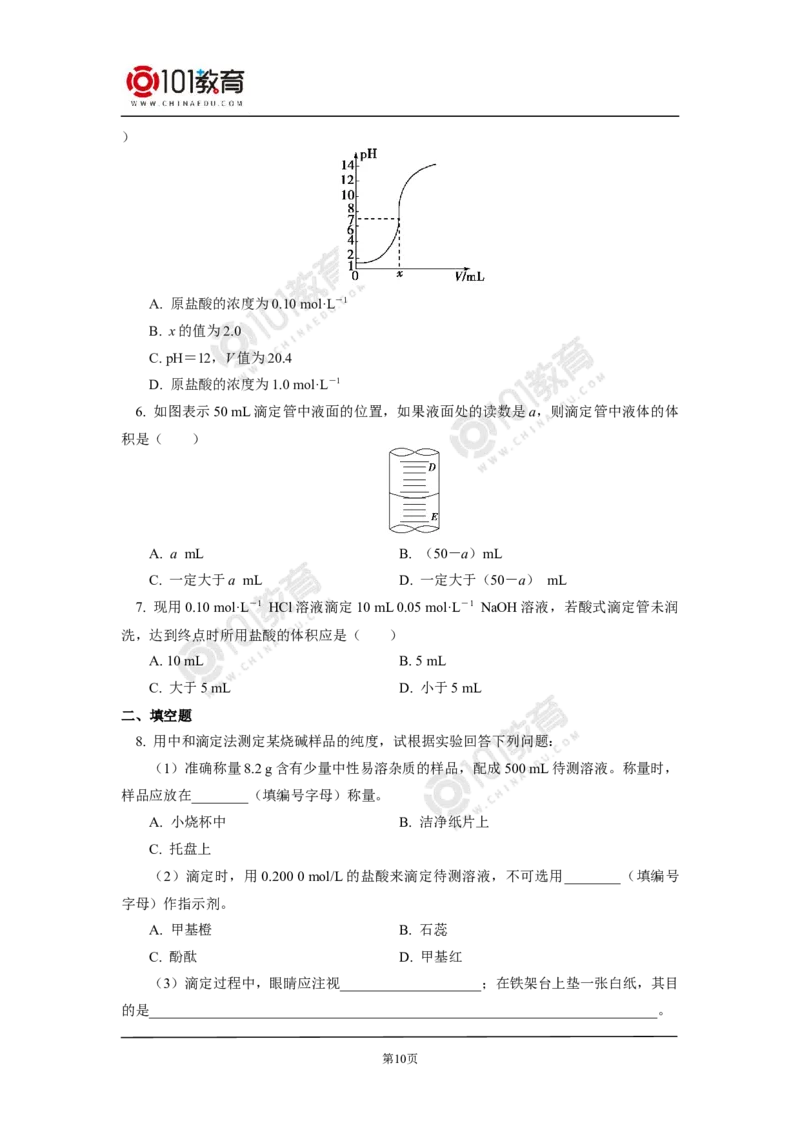
*5. 如图是常温下向20.0 mL的盐酸中,逐滴加入0.10 mol·L-1 NaOH溶液时,溶液的
pH随NaOH溶液的体积V(mL)变化的曲线,根据图像所得的下列结论中正确的是 (
第9页)
A. 原盐酸的浓度为0.10 mol·L-1
B. x的值为2.0
C. pH=12,V值为20.4
D. 原盐酸的浓度为1.0 mol·L-1
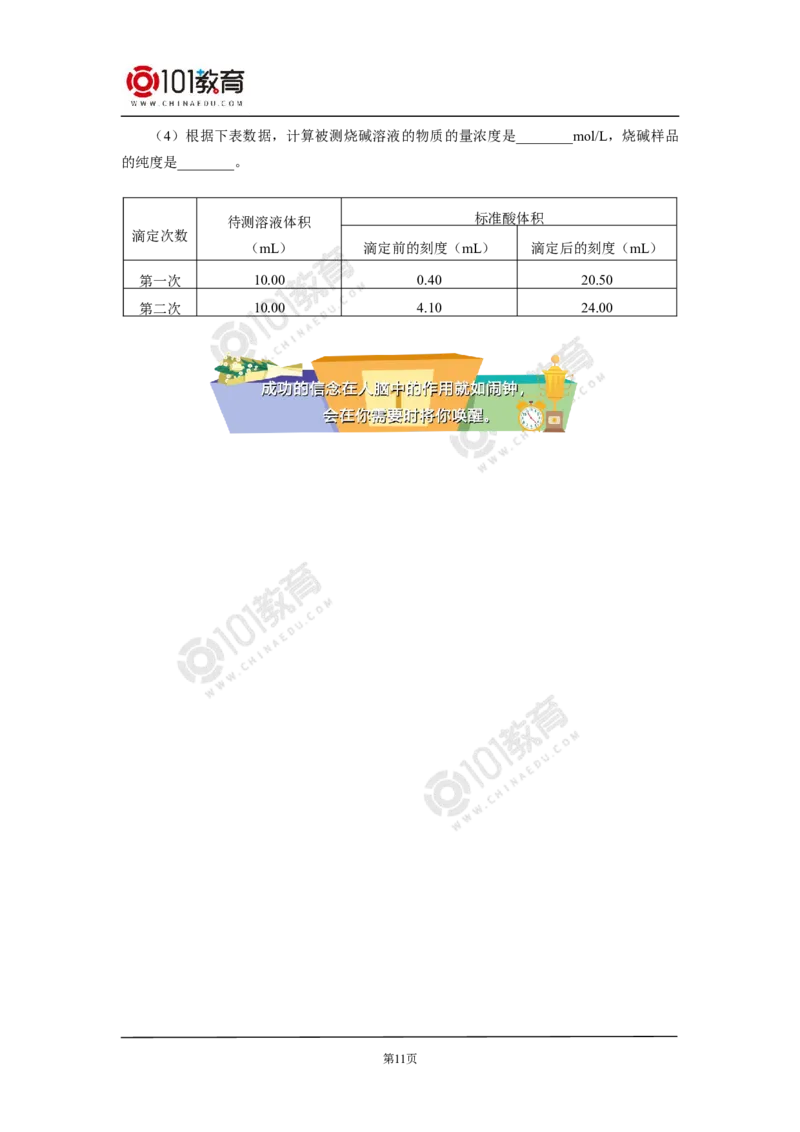
6. 如图表示50 mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体
积是( )
A. a mL B. (50-a)mL
C. 一定大于a mL D. 一定大于(50-a) mL
7. 现用0.10 mol·L-1 HCl溶液滴定10 mL 0.05 mol·L-1 NaOH溶液,若酸式滴定管未润
洗,达到终点时所用盐酸的体积应是( )
A. 10 mL B. 5 mL
C. 大于5 mL D. 小于5 mL
二、填空题
8. 用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:
(1)准确称量8.2 g含有少量中性易溶杂质的样品,配成500 mL待测溶液。称量时,
样品应放在________(填编号字母)称量。
A. 小烧杯中 B. 洁净纸片上
C. 托盘上
(2)滴定时,用0.200 0 mol/L的盐酸来滴定待测溶液,不可选用________(填编号
字母)作指示剂。
A. 甲基橙 B. 石蕊
C. 酚酞 D. 甲基红
(3)滴定过程中,眼睛应注视____________________;在铁架台上垫一张白纸,其目
的是________________________________________________________________________。
第10页(4)根据下表数据,计算被测烧碱溶液的物质的量浓度是________mol/L,烧碱样品
的纯度是________。
待测溶液体积 标准酸体积
滴定次数
(mL) 滴定前的刻度(mL) 滴定后的刻度(mL)
第一次 10.00 0.40 20.50
第二次 10.00 4.10 24.00
第11页酸碱中和滴定同步练习参考答案
1. 【答案】B
【解析】若NaOH过量,则返滴一滴待测盐酸,若红色消失,说明NaOH未过量,若
红色不消失,则说明NaOH过量。
2. 【答案】D
【解析】操作(1)的锥形瓶只能用水洗;操作(3)中不能用石蕊作为中和滴定的指
示剂,因为它的显色效果不明显;操作(5)中滴定管必须用标准液润洗后才能注入标准液;
操作(7)中两眼应主要注视锥形瓶中溶液颜色的变化。
3. 【答案】A
【解析】由图示可知,在V(HCl)=20.00 mL时,pH=7,HCl与NaOH恰好完全反
应 , 由 c ( HCl ) ·V ( HCl ) = c ( NaOH ) ·V ( NaOH ) , 知 c ( NaOH ) =
=0.1 mol·L-1,c(OH-)=0.1 mol·L-1,c(H
+)=10-13 mol·L-1,pH=13。
4. 【答案】A
【解析】①未干燥,相当于稀释盐酸,滴定时将消耗盐酸偏多,使结果偏高,③滴定
管下端尖嘴处悬挂有一滴盐酸,相当于消耗盐酸偏多,使结果偏高。
5. 【答案】A
【解析】当V(NaOH)=0 mL时,盐酸溶液的pH=1,因此c(HCl)=0.10 mol·L-
1;当反应后溶液pH=7时,HCl与NaOH恰好完全反应,因此n(HCl)=n(NaOH),
故 V ( NaOH ) = 20.0 mL ; 当 反 应 后 溶 液 pH = 12 时 ,
=1×10-2 mol·L-1,解得 V(NaOH)=
24.4 mL。
6. 【答案】D
【解析】滴定管的零刻度在上面,50 mL的刻度在下面,但刻度线以下仍有一部分容
积,因此液体体积一定是大于(50-a) mL。
7. 【答案】C
【解析】用0.10 mol·L-1 HCl溶液滴定10 mL 0.05 mol·L-1 NaOH溶液正好需5 mL
HCl溶液。现盐酸被稀释,其浓度小于0.10 mol·L-1,故中和NaOH所需体积大于5 mL。
8. 【答案】(1)A (2)B
(3)锥形瓶内溶液颜色的变化 便于观察锥形瓶内液体颜色的变化,减小滴定误差
(4)0.400 0 97.56%
第12页【解析】(1)称量氢氧化钠等易潮解、腐蚀性强的试剂时,样品应放在小烧杯中;
(2)酸碱中和滴定时,一般应选甲基橙、酚酞、甲基红等颜色变化较明显的指示剂,石蕊
在酸或碱溶液中颜色变化不明显,易造成误差;(4)由表中数据知,滴定时所用盐酸的体
积为20.00 mL,根据c(NaOH)= ,求得c(NaOH)=0.400 0 mol/L。
第13页