文档内容
第一章 物质及其变化
第一节 物质的分类及转化
第二课时 分散系及其分类
【学习目标】1.通过阅读教材、讨论交流,熟知溶液、浊液、胶体三种分散系的本质区别,了解胶体
的性质及其应用,会鉴别胶体和溶液,培养“宏观辨识与微观探析”的化学素养。
2.通过动手实验、现象观察、原理分析,掌握Fe(OH) 胶体的制备方法,理解胶体的丁达尔效应及其
3
应用,初步了解实验研究的方法和步骤,培养“科学态度与科学探究”的化学素养。
【学习重点】分散系的分类及本质区别、氢氧化铁胶体的制备和性质。。
【学习难点】理解胶体的性质及应用。
【课前预习】
旧知回顾:1.现有下列物质:① HO ② 空气 ③ Mg ④CaO ⑤H SO ⑥Ca(OH)
2 2 4 2
⑦CuSO ·5H O ⑧碘酒 ⑨C HOH和⑩NaHCO 。其中属于混合物的是________(填序号,下同);属
4 2 2 5 3
于酸的是______;属于盐的是________;属于氧化物的是________;
2.溶液是一种或几种物质________到另一种物质里,形成的________________________。具有均
匀、透明、___________的特征。其中 分散于其中的物质叫做_______,被分散的物质叫做______。如食
盐水等。
新知预习: 1.分散系是_____________________________________________所得到的体系。分散系间
的本质区别是___________________________不同。从物质分类的角度看,CuSO 溶液、泥水、振荡后的植
4
物油与水的混合物分别属于____________________________________________。
2.胶体是分散质粒子的直径为 _______________ _ 的分散系。当光束通过Fe(OH) 胶体时,可以看
3
到一条光亮的“通路”,叫做 _______________ _ ,可被用来 __________________ _ 胶体和溶液。
【课中探究】
情景导入:同学们,在阳光灿烂的清晨,在茂密的树林里,我们会看到阳光透过树林,形成一道道光亮
的光柱,非常的美丽!。这些自然现象是怎样产生的?这一节课我们就探讨这方面的有关知识。(见PPT
图片)
一、分散系及其分类
活动一、认识分散系及分类
任务一、阅读教材P8第一自然段,回答分散系的定义是什么?并举例说明生活中有哪些常见的分散
系?任务二、讨论交流:结合物质的分类方法,思考如何对分散系进行交叉分类和树状分类?举例说明。
【对应训练】1.根据气象台报道,近年来每到春季,沿海一些城市经常出现大雾天气,致使高速公路
关闭,航班停飞。雾属于下列分散系中的( )
A.溶液 B.悬浊液
C.乳浊液 D.胶体
2.我国在国际上首次实现从一氧化碳到蛋白质的合成。已经形成万吨级的工业生产能力,获得首个饲
料和饲料添加剂新产品证书。蛋白质是高分子有机化合物,其分子直径在2nm-20nm。下列分散质粒子直
径在1nm-100nm之间的是( )
A.稀硫酸 B.硫酸铜溶液
C.有色玻璃 D.酒精溶液
活动二、探究分散系的本质及性质
任务一、阅读教材P8第二自然段,比较溶液、浊液和胶体三种分散系性质,完成下表内容,由此说
明三种分散系的本质区别是什么?
分散系 溶液 胶体 浊液
外观
分散质微粒组成
微粒直径
三种分散系的本质区别:
任务二、阅读教材P8第三自然段,思考胶体的定义、本质特征及分类,并举例说明。
任务三、问题探究:Fe(OH) 胶体的胶粒数与Fe(OH) 分子数相等吗?
3 3
【对应训练】1.在物质分类中,前者包括后者的是( )A.氧化物、化合物 B.溶液、胶体
C.分散系、溶液 D.酸性氧化物、化合物
2.FeCl 溶液、Fe(OH) 胶体、Fe(OH) 浊液是三种重要的分散系,下列叙述中错误的是( )
3 3 3
A.Fe(OH) 胶体区别于其他分散系的本质特征是分散质粒子的直径在10-9~10-7 m
3
B.分别用一束光透过三种分散系,只有Fe(OH) 胶体具有丁达尔效应
3
C.三种分散系的颜色都相同,且均能与盐酸反应,具有吸附性
D.三种分散系均属于混合物
二、胶体的制备及性质
活动一、胶体的制备
任务一、制备Fe(OH) 胶体:结合教材P9页【实验1-1】完成实验,填写下表内容。
3
步骤 实验内容 现象 原理及装置
步骤1 取100mL小烧杯,加入
40ml的蒸馏水加热至沸腾。
步骤2 向沸水中滴加5-6滴饱
和FeCl 溶液
3
步骤3 继续煮沸至液体呈红褐
色,停止加热。
任务二:结合上述实验讨论交流Fe(OH) 胶体的制备要注意哪些问题?
3
【对应训练】1.下列关于氢氧化铁胶体制备的说法正确的是( )
A.将氯化铁稀溶液慢慢滴入沸腾的自来水中,继续加热煮沸
B.将氯化铁饱和溶液慢慢滴入沸腾的蒸馏水中,并用玻璃棒搅拌
C.将氢氧化钠溶液慢慢滴入饱和的氯化铁溶液中
D.在沸腾的蒸馏水中慢慢滴入氯化铁饱和溶液,继续煮沸至溶液呈红褐色
2.用下列方法制备胶体:①0.5 mol/L的BaCl 溶液和等体积2 mol/L的硫酸混合振荡;②把1 mol/L
2
饱和的FeCl 溶液逐滴加入20 mL沸水中,边加边振荡;③1 mol/L NaOH溶液滴到1 mol/L FeCl 溶液中,
3 3可行的是( )
A.①② B.①③
C.② D.①②③
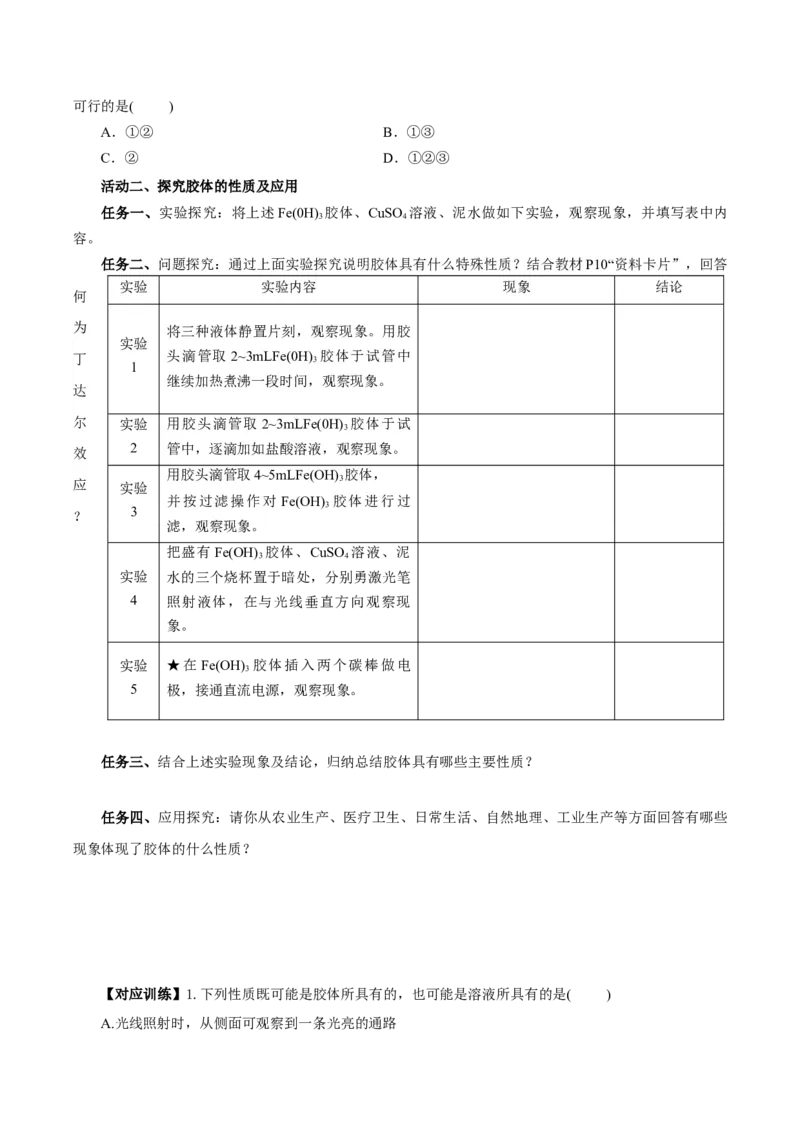
活动二、探究胶体的性质及应用
任务一、实验探究:将上述Fe(0H) 胶体、CuSO 溶液、泥水做如下实验,观察现象,并填写表中内
3 4
容。
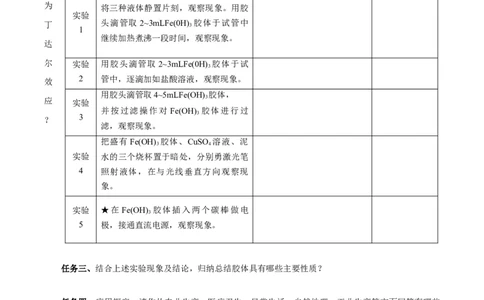
任务二、问题探究:通过上面实验探究说明胶体具有什么特殊性质?结合教材P10“资料卡片”,回答
实验 实验内容 现象 结论
何
为 将三种液体静置片刻,观察现象。用胶
实验
丁 头滴管取 2⁓3mLFe(0H) 3 胶体于试管中
1
继续加热煮沸一段时间,观察现象。
达
尔 实验 用胶头滴管取 2⁓3mLFe(0H) 胶体于试
3
2 管中,逐滴加如盐酸溶液,观察现象。
效
用胶头滴管取4⁓5mLFe(OH) 胶体,
应 实验 3
并按过滤操作对 Fe(OH) 胶体进行过
3
? 3
滤,观察现象。
把盛有Fe(OH) 胶体、CuSO 溶液、泥
3 4
实验 水的三个烧杯置于暗处,分别勇激光笔
4 照射液体,在与光线垂直方向观察现
象。
实验 ★在 Fe(OH) 胶体插入两个碳棒做电
3
5 极,接通直流电源,观察现象。
任务三、结合上述实验现象及结论,归纳总结胶体具有哪些主要性质?
任务四、应用探究:请你从农业生产、医疗卫生、日常生活、自然地理、工业生产等方面回答有哪些
现象体现了胶体的什么性质?
【对应训练】1.下列性质既可能是胶体所具有的,也可能是溶液所具有的是( )
A.光线照射时,从侧面可观察到一条光亮的通路B.加入少量稀硫酸立即产生沉淀
C.分散质粒子直径小于1 nm
D.装入半透膜袋中并将其浸入盛水的烧杯中一段时间,袋内外均含分散质粒子
2.下列现象与胶体知识无关的是 ( )
A.夏日的傍晚常常看到万丈霞光穿云而过美不胜收
B.过滤除去氯化钠溶液中的泥沙
C.食品加工厂利用豆浆中加入盐卤做豆腐
D.化工厂利用静电除尘技术去除废气中的固体悬浮物
【课后巩固】1.(易)教材作业:P12习题3、4
2.(易)在物质分类中,前者包括后者的是
A.溶液、浊液 B.胶体、分散系
C.化合物、氧化物 D.纯净物、电解质溶液
3.(易)下列关于分散系的叙述正确的是( )
A.分散系的分类:
B.可利用过滤的方法分离胶体和溶液
C.溶液是混合物,胶体是纯净物
D.溶液是电中性的,胶体是带电的
4.(中)用饱和的氯化铁溶液制取氢氧化铁胶体,正确的操作是 ( )
A.将饱和氯化铁溶液滴入蒸馏水中即可
B.将饱和氯化铁溶液滴入热水中,生成棕黄色液体即可
C.将饱和氯化铁溶液滴入沸水中,并继续煮沸至生成红褐色液体即可
D.将饱和氯化铁溶液滴入沸水中,并继续煮沸至生成红褐色沉淀即可
5.(中)下列说法正确的是( )
①胶体产生丁达尔效应是由胶粒直径大小决定的
②胶体与溶液的分离可用渗析的方法
③胶体都是均匀、透明的液体
④江河入海口处形成沙洲与胶体的性质有关
⑤胶体不稳定,静置后容易产生沉淀
⑥水泥厂和冶金厂常用高压直流电除去大量烟尘,减少对空气的污染
A.①②③④ B.①②④⑥
C.①③④⑥ D.②③④⑥
6.(难)下列说法中正确的是( )A.不能发生丁达尔效应的分散系有氯化钠溶液、水等
B.用饱和的FeCl 溶液制得的Fe(OH) 胶体中,胶粒数与Fe3+数目相等
3 3
C.在Fe(OH) 胶体中滴入少量稀硫酸将有沉淀产生
3
D.淀粉胶体中含有少量的NaCl,可用适量AgNO 溶液除去
3
7.(难)下列说法正确的是( )
A.硫酸、纯碱、碳酸氢钠和生石灰分别属于酸、碱、盐和氧化物
B.用丁达尔效应区别FeCl 溶液和Fe(OH) 胶体
3 3
C.生石灰与水混合的过程只发生物理变化
D.HO、HCOOH、Cu(NH )SO 均含有氧元素,都是氧化物
2 3 4 4
8.(中)(1)有甲、乙、丙、丁四种分散系,它们分别为 Fe(OH) 胶体、硅酸胶体、As S 胶体、
3 2 3
NaOH溶液。现将有关实验现象记录如下:
①电泳:甲液体的阳极周围颜色变浅,阴极周围颜色变深。
②将一束光通过乙液体,无丁达尔效应。
③将乙液体加入到丙液体中,先出现聚沉,后变澄清。
则甲为________,乙为________,丙为________,丁为________。
(2)取少量Fe O 粉末(红棕色)加入适量盐酸,所发生反应的化学方程式为____________________,
2 3
反应后得到的FeCl 溶液呈棕黄色。用此溶液进行以下实验:
3
①取少量溶液置于试管中,滴入 NaOH溶液,可观察到有红褐色沉淀生成,反应的化学方程式为
______________,此反应属于________反应。
②在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴FeCl 溶液,继续煮沸至溶液呈
3
________色,停止加热,制得的分散系为________。