文档内容
第三章 烃的衍生物
第二节 醇、酚
第二课时 酚
【学习目标】
1.通过分析酚类的结构,认识和理解酚类的结构共性和酚的定义。
2.通过分析苯酚的结构,预测苯酚的性质,并通通过实验和素材证实,再归纳总结酚类的化学性质及反应
规律。
3.通过素材,结合苯酚的性质,认识酚类对生产产生活的用途和危害。
【学习重点】苯酚的弱酸性和取代反应
【学习难点】苯酚中基团相互影响的体现
【课前预习】
1.酚的概念、组成和结构
(1)概念
酚是羟基与苯环直接相连而形成的化合物。最简单的酚为苯酚( )。
(2)组成与结构(以苯酚为例)
分子
结构简式 结构特点
式
CH 或
6 6 羟基与苯环直接相连
O CHOH
6 5
2.苯酚的物理性质
3.苯酚的化学性质
(1)羟基中氢原子的反应
①弱酸性
电离方程式为 ,俗称 ,但酸性很弱,不能使紫色石蕊试液变红。
②与活泼金属反应
与Na反应的化学方程式为________________________________。③与碱反应
苯酚的浑浊液 溶液又变浑浊。
该过程中发生反应的化学方程式分别为________________________________________________;
_________________________________________________。
④毒性
苯酚有毒,对皮肤有强烈的腐蚀作用,不慎沾在皮肤上应立即用乙醇清洗。
(2)苯环上氢原子的取代反应
苯酚与浓溴水反应的化学方程式为_____________________________________________。
此反应常用于苯酚的定性检验和定量测定。
(3)显色反应
苯酚与FeCl 溶液作用显 ,利用这一反应可以检验苯酚的存在。
3
4.苯酚的用途
(1)苯酚是一种重要的化工原料,广泛用于制造酚醛树脂、染料、医药、农药等。
(2)苯酚的稀溶液可以直接杀菌消毒,如日常药皂中常加入少量的苯酚。
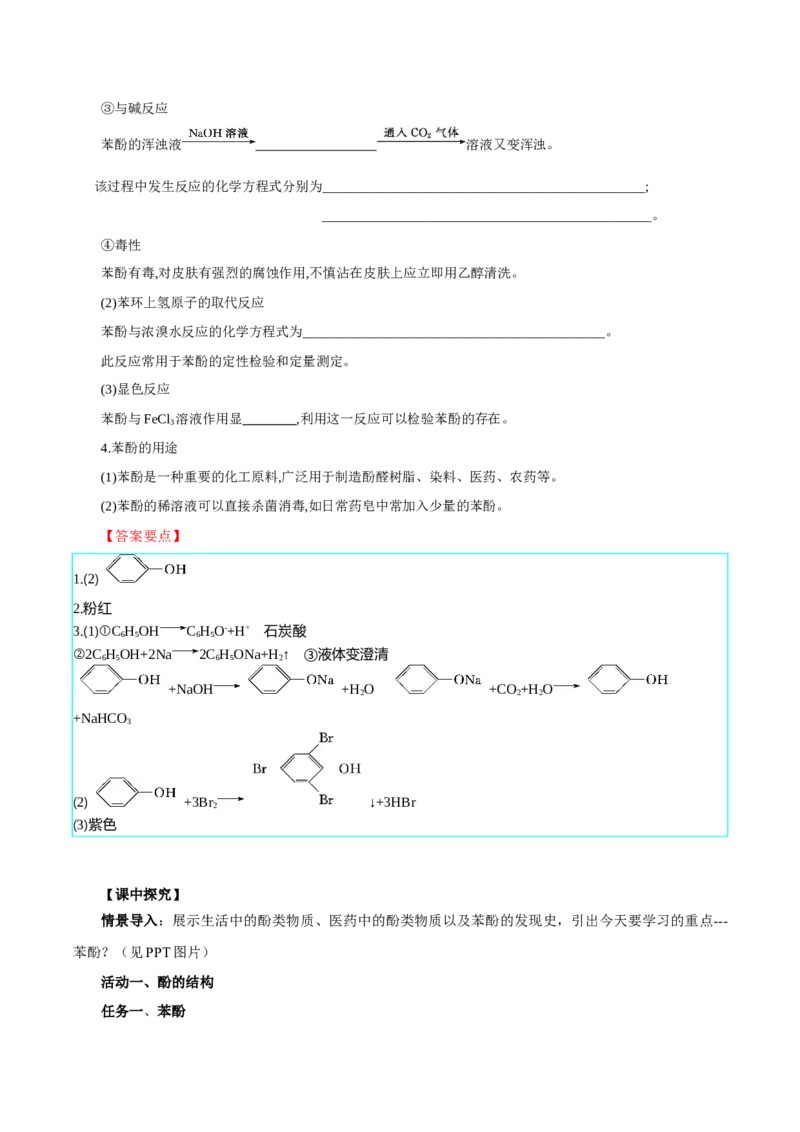
【答案要点】
1.(2)
2.粉红
3.(1)①C HOH C HO-+H+ 石炭酸
6 5 6 5
②2C HOH+2Na 2C HONa+H ↑ ③液体变澄清
6 5 6 5 2
+NaOH +H O +CO +H O
2 2 2
+NaHCO
3
(2) +3Br ↓+3HBr
2
(3)紫色
【课中探究】
情景导入:展示生活中的酚类物质、医药中的酚类物质以及苯酚的发现史,引出今天要学习的重点---
苯酚?(见PPT图片)
活动一、酚的结构
任务一、苯酚【学生活动1】阅读教材P ,总结酚的基本概念
63
【总结】 1.定义:羟基与苯环直接相连的化合物称为酚。
2.官能团:羟基(-OH )
3.代表物
【学生活动2】请写出苯酚的分子式、结构简式
【总结】 1.C HO
6 6
2.结构简式
【学生活动3】苯酚所有原子一定共平面吗?
【总结】不一定,最少有12个原子共面,最多有13个原子共面。
【典型例题】
例1:下列有机物与苯酚互为同系物的是( )。
A. B.
C. D.
【答案要点】C
解析 苯酚和苯甲醇虽然在组成上相差一个CH 原子团,但结构并不相似,苯酚的官能团—OH直接连在
2
苯环上,而苯甲醇的官能团—OH连在烷基上。B、C、D三项的—OH都直接连在苯环上,都属于酚类,但B、
D不与苯酚相差若干CH 原子团,所以都不符合题意。
2
活动二、酚的性质
任务一、酚的物理性质
【学生活动1】阅读教材P ,总结酚的物理性质:
63
【总结】
1.颜色:无色晶体,空气中被氧化成粉红色。
2.气味:有特殊气味3.状态:晶体
4.溶解性:室温可溶于水(S=9.2g),65℃以上与水互溶;易溶于乙醇等有机溶剂。
5.熔点:43℃
6.毒性:有毒
【学生活动2】思考与讨论下列两个问题:
1.苯酚有毒,如不慎沾到皮肤上,该如何处理?
2.如何洗去试管壁粘有的苯酚有毒?
【总结】
1.苯酚有毒,对皮肤有腐蚀性,使用时一定要小心。如不慎沾到皮肤上,应立即用乙醇冲洗,再
用大量水冲洗。
2.用热水或者酒精洗涤
任务二、苯酚的化学性质
【学生活动1】观看苯酚久置之后,颜色的变化?初此之外,苯酚还可以发生什么氧化反应?
【总结】氧化反应:
1.在空气中被O 氧化呈粉红色
2
2.可以燃烧
3.使酸性KMnO 溶液褪色
4
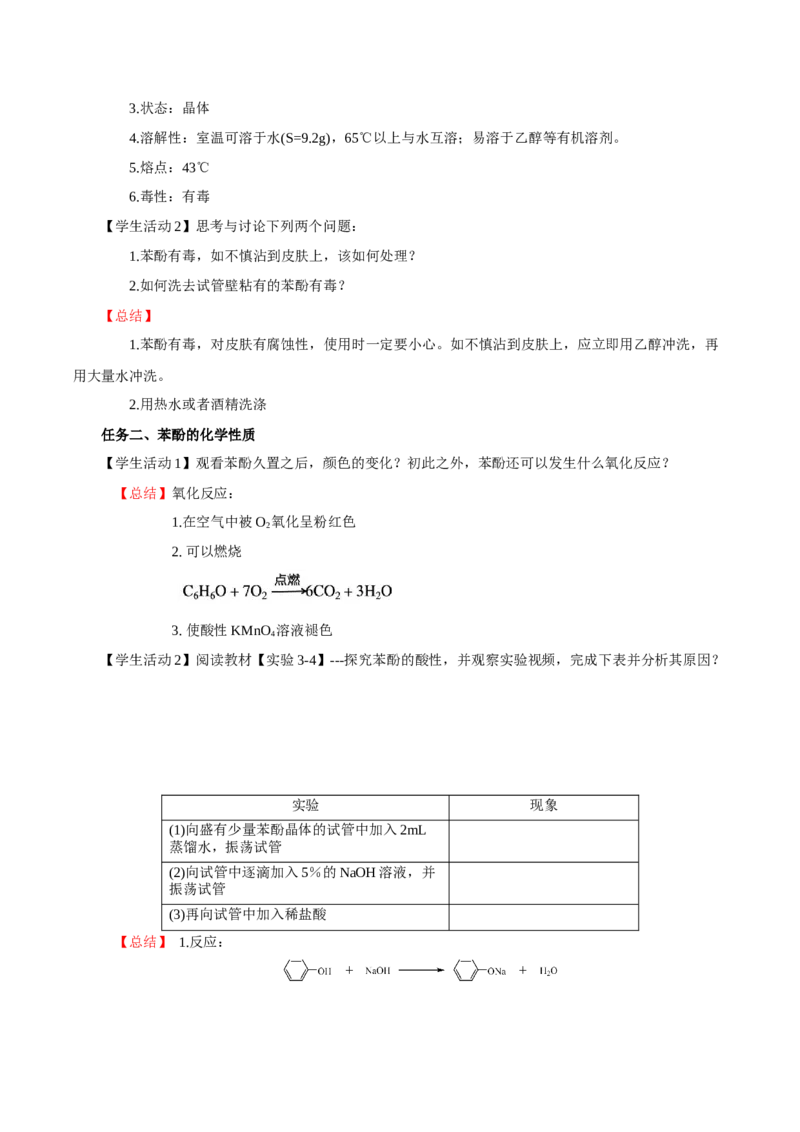
【学生活动2】阅读教材【实验3-4】---探究苯酚的酸性,并观察实验视频,完成下表并分析其原因?
实验 现象
(1)向盛有少量苯酚晶体的试管中加入2mL
蒸馏水,振荡试管
(2)向试管中逐滴加入5%的NaOH溶液,并
振荡试管
(3)再向试管中加入稀盐酸
【总结】 1.反应:2.酸性强弱对比:盐酸大于苯酚
3.原因:苯环对羟基的性质产生影响,使氢原子更加活泼。
【学生活动3】如何设计实验验证苯酚的酸性弱碳酸?
【总结】 1.实验装置:
2.原因:
3.酸性强弱对比:碳酸大于苯酚
【学生活动4】向NaCO 溶液中滴入2滴酚酞溶液,再将此溶液加入苯酚浊液中,充分振荡后可观
2 3
察到浊液变澄清,溶液红色褪去,且无气泡生成,解释原因:
【总结】
1.原因:
2.酸性强弱对比:苯酚强于碳酸氢根
【学生活动5】上述反应所涉及的酸的酸性强弱?
【总结】
苯酚溶液,又称为石炭酸,虽然显酸性,但酸性极弱,不能使酸碱指示剂变色。
【学生活动6】阅读教材P 【3-5】探究苯酚与浓溴水的取代反应?
65
【总结】苯酚能与饱和溴水(浓溴水)反应,生成难溶于水的2,4,6-三溴苯酚:
羟基对苯环的性质产生影响,使得羟基邻、对位的氢原子较易被取代注意:(1)苯酚与溴反应灵敏,可用于苯酚的定性检验和定量测定。
(2)实验中苯酚不能过量,否则产生的三溴苯酚易溶于苯酚而观察不到白色沉淀。
【学生活动7】思考与交流:如何分离苯和苯酚的混合溶液?
【总结】
【学生活动8】思考与交流:如何分离乙醇和苯酚的混合溶液?
【总结】
【学生活动9】阅读教材P 的【思考与讨论】并回答问题:
65
【总结】
1.由于苯环对羟基影响,O―H极性变强,氢原子易电离而使苯酚表现弱酸性。
2.
【学生活动10】阅读教材P 【3-6】探究苯酚与FeCl 溶液的显色反应?
66 3
【总结】1.苯酚遇FeCl 溶液显紫色,酚类物质一般都可以与FeCl 溶液作用显色,可用于检验其存
3 3
在。
2.用途:检验苯酚(酚类)或Fe3+ 的存在
任务三、酚的用途与危害
【学生活动1】阅读教材P ,总结苯酚的用途与危害:
66
【总结】
1.用途---一种重要的化工原料,用于生产酚醛树脂、染料、医药、农药等。
2.危害---含酚类物质的废水对生物具有毒害作用,会对水体造成严重污染;化工厂和炼焦厂的废水中常含有酚类物质,在排放前必须经过处理。
【典型例题】
例3.有机物分子中的原子(团)之间会相互影响,导致相同的原子(团)表现不同的性质。下列各项事实
不能说明上述观点的是( )。
A.甲苯能使酸性高锰酸钾溶液褪色,而甲基环己烷不能使酸性高锰酸钾溶液褪色
B.乙烯能与溴水发生加成反应,而乙烷不能与溴水发生加成反应
C.苯酚可以与NaOH溶液反应,而乙醇不能与NaOH溶液反应
D.苯酚与溴水可直接反应,而苯与液溴反应则需要FeBr3作催化剂.
【答案要点】B
解析 甲苯中苯环对—CH 的影响,使 —CH 可被KMnO (H+)溶液氧化为—COOH,从而使酸性
3 3 4
KMnO 溶液褪色;苯酚中羟基对苯环产生影响,使苯酚分子中羟基邻、对位氢原子更活泼,更易被取代;乙烯能
4
与溴水发生加成反应,是因为含碳碳双键;苯环对羟基产生影响,使羟基中氢原子更易电离,表现出弱酸性。
A、C、D三项符合题意,B项不符合题意。
例4.A、B的结构简式如下:
(1)A分子中含有的官能团的名称是________;B分子中含有的官能团的名称是_________。
(2)A能否与氢氧化钠溶液反应?_______(填“能”或“不能”,下同);B能否与氢氧化钠溶液反应?
_______。
(3)A在浓硫酸作用下加热可得到B,其反应类型是____________。
(4)A、B各1 mol分别加入足量溴水,完全反应后消耗单质溴的物质的量分别是_______mol,_______mol。
【答案要点】
(1)醇羟基、碳碳双键 酚羟基
(2)不能 能
(3)消去反应
(4)1 2
解析 (1)A中的官能团是醇羟基、碳碳双键,B中的官能团是酚羟基。(2)A属于醇类不能与氢氧化钠溶液反
应,B属于酚类能与氢氧化钠溶液反应。(3)由A到B属于消去反应。(4)A中含有1 mol碳碳双键,消耗1 mol
单质溴,B中只有与羟基相连的碳原子的邻位碳原子上的H原子与单质溴发生取代反应,消耗2 mol单质溴。