文档内容
3.3.2盐类水解的应用(分层作业)
1.采取下列措施后,溶液颜色变深的是
A.加热0.10mol/L明矾溶液(滴有酚酞试液)
B.加热0.10mol/L NaCO 溶液(滴有酚酞试液)
2 3
C.0.10mol/L氨水(滴有酚酞试液)中加入少量NH Cl固体
4
D.0.10mol/L小苏打溶液(滴有酚酞试液)中加入少量NaCl固体
2.为了配制NH 的浓度与Cl-的浓度比为1:1的溶液,可在NH Cl溶液中加入
4
①适量NH NO ;②适量NaCl;③适量氨水;④适量HCl
4 3
A.①② B.②③ C.①③ D.②④
3.中华优秀传统文化涉及了很多化学知识,下列有关说法错误的是
A.《本草纲目拾遗》中对强水的记载:“性最猛烈,能蚀五金。”强水涉及到强电解质
B.《本草纲目》中“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”,利用的是盐类的水解
C.刘长卿诗云“水声冰下咽,砂路雪中平”,固态冰转化为液态水为熵增的过程
D.《本草图经》记载“盖此矾色绿,味酸,烧之则赤”,因绿矾能电离出H+,所以“味酸”
4.下列事实与盐类水解原理无关的是
A.明矾用于净水 B.实验中常将FeCl 晶体溶于较浓盐酸中配制FeCl 溶液
3 3
C.用小苏打中和过多的胃酸 D.用氯化铵和氯化锌溶液除铁锈
5.下列离子方程式不正确的是
A.明矾用于净水:Al3++3H O Al(OH) (胶体)+3H+
2 3
B.泡沫灭火器灭火:Al3++3HCO Al(OH) ↓+3CO ↑
3 2
C.用纯碱清洗油污:CO +H O HCO +OH-
2
D.HS-的水解反应:HS-+H O S2-+H O+
2 3
6.将下列溶液加热蒸干灼烧后,可以得到该固体物质的是
A.NaSO B.Al (SO ) C.NaHCO D.CuCl
2 3 2 4 3 3 2
7.下列物质的应用正确并与盐类水解有关的是
A.加热蒸干Al (SO ) 溶液得到Al(OH) 固体
2 4 3 3B.实验室配制FeSO 溶液时,要在溶液中加入少许铁粉
4
C.金属焊接时,用NH Cl和ZnCl 溶液作除锈剂
4 2
D.铵肥和草木灰可以混合使用,以增强肥效
8.25℃时部分弱酸的电离平衡常数如下表:
弱酸 HCOOH HClO
电离平衡常
数
(1)室温下① ,② ③ ,溶液的pH由大到小的关系为
。
(2)草木灰的主要成分是 ,使用时不能与铵态氮肥混合使用,原因是 。
(3)下列离子方程式书写正确的是 。(填字母)。
a.2ClO+H O+CO=2HClO+CO2-
2 2 3
b.2HCOOH+CO2- =2HCOO-+H O+CO↑
3 2 2
c.H SO +2HCOO-=2HCOOH+SO2-
2 3 3
d.Cl+H O+2CO2- =2HCO- +Cl-+ClO-
2 2 3 3
(4)泡沫灭火器的主要成分是硫酸铝溶液和碳酸氢钠溶液,这两种溶液混合后,反应的离子方程式为
。
(5)某二元酸(化学式用HB表示)在水中的电离方程式是HB=H++HB-,HB-⇌H++B2-。已知0.1mol·L-1
2 2
NaHB溶液pH=2,则0.1mol·L-1 HB溶液中氢离子的物质的量浓度可能 (填“>”“<”或“=”)
2
,理由是 。0.1mol·L-1 NaHB溶液中各种离子浓度由大到小的顺序是 。
9.物质的量的浓度相等的以下溶液①(NH )SO 溶液、②NH Fe(SO ) 溶液、③(NH )CO 溶液、
4 2 4 4 4 2 4 2 3
④NH Cl,其中c(NH+ )的浓度由大到小的顺序为
4 4
A.①③②④ B.①③④② C.③①②④ D.③①④②
10.下列叙述错误的是
A.NaCO 稀溶液加水稀释,溶液的碱性减弱
2 3
B.稀溶液中,盐的浓度越小,水解程度越大,其溶液酸性(或碱性)也越强C.在滴有酚酞的NaCO 溶液中慢慢滴入BaCl 溶液,溶液的红色逐渐褪去
2 3 2
D.pH相等的①NaHCO ②NaCO ③NaOH溶液的物质的量浓度大小:①>②>③
3 2 3
11.相同温度、相同物质的量浓度的五种溶液:① ,② ,③NaCl,④NaOH,
⑤NH Cl;按pH由大到小排列正确的是
4
A.①>④>③>⑤>② B.④>①>②>③>⑤
C.④>③>①>⑤>② D.④>①>③>⑤>②
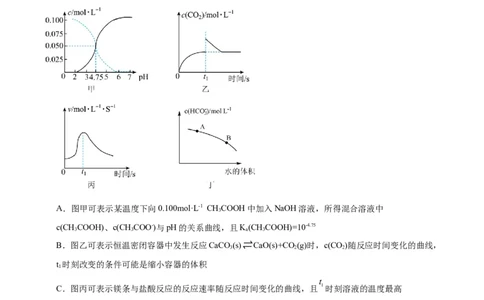
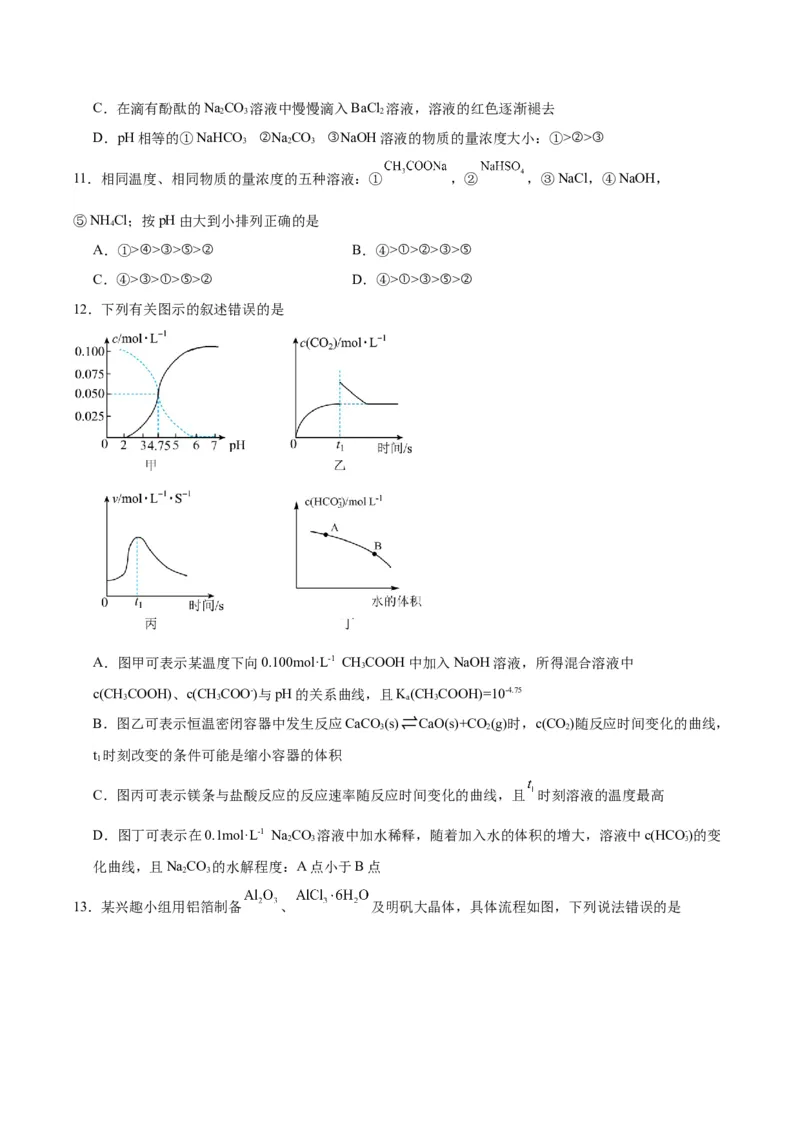
12.下列有关图示的叙述错误的是
A.图甲可表示某温度下向0.100mol·L-1 CHCOOH中加入NaOH溶液,所得混合溶液中
3
c(CHCOOH)、c(CHCOO-)与pH的关系曲线,且K(CHCOOH)=10-4.75
3 3 a 3
B.图乙可表示恒温密闭容器中发生反应CaCO (s)⇌CaO(s)+CO (g)时,c(CO)随反应时间变化的曲线,
3 2 2
t 时刻改变的条件可能是缩小容器的体积
1
C.图丙可表示镁条与盐酸反应的反应速率随反应时间变化的曲线,且 时刻溶液的温度最高
D.图丁可表示在0.1mol·L-1 NaCO 溶液中加水稀释,随着加入水的体积的增大,溶液中c(HCO- )的变
2 3 3
化曲线,且NaCO 的水解程度:A点小于B点
2 3
13.某兴趣小组用铝箔制备 、 及明矾大晶体,具体流程如图,下列说法错误的是A.步骤Ⅲ,为了得到纯Al O,需灼烧至恒重
2 3
B.步骤Ⅴ中抽滤所需仪器:布氏漏斗、吸滤瓶、抽气泵等
C.通入HCl的作用是抑制AlCl 水解和增大溶液中 的浓度,有利于AlCl 6HO结晶
3 3· 2
D.步骤Ⅳ的操作是:配制高于室温10~20℃的明矾饱和溶液,选规则明矾小晶体并悬挂在溶液中央,
快速冷却至室温,得到明矾大晶体
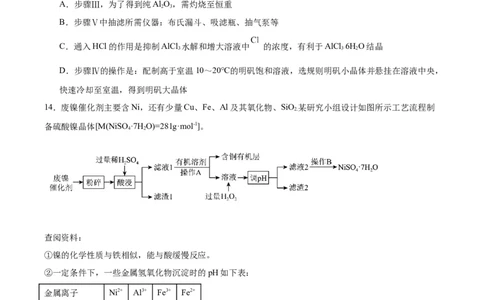
14.废镍催化剂主要含Ni,还有少量Cu、Fe、Al及其氧化物、SiO 某研究小组设计如图所示工艺流程制
2.
备硫酸镍晶体[M(NiSO ·7H O)=281g·mol-1]。
4 2
查阅资料:
①镍的化学性质与铁相似,能与酸缓慢反应。
②一定条件下,一些金属氢氧化物沉淀时的pH如下表:
金属离子 Ni2+ Al3+ Fe3+ Fe2+
开始沉淀的pH 7.2 4.0 2.2 7.5
沉淀完全的pH 9.0 5.6 3.2 9.0
(1)“滤渣2”的成分是 (用化学式表示)。溶液中加入HO 的目的是 (用离子方程式表
2 2
示)。
(2)“调pH”可选用的物质 (填序号)。
A.NaCO B.NiCO C.HSO D.NiSO
2 3 3 2 4 4“调pH”的范围为 。
(3)下列有关说法不正确的是___________。
A.酸浸步骤可用水浴加热,以加速反应
B.操作A中的有机溶剂可选用乙醇
C.调pH后过滤,需用玻璃棒对漏斗中的混合物充分搅拌
D.操作B中包含“结晶、过滤、洗涤、煅烧”等操作
(4)测定产品的纯度。
操作步骤 涉及反应
①准确称取制备的硫酸镍样品5.620g,加入含0.0200molEDTA的二钠盐溶液(用
HY2-表示),充分反应后定容成100mL。
2
②取25.00mL上述溶液于锥形瓶中,加二甲酚橙作指示剂,用
标准液滴定到终点,平行实验三次,平均消耗20.00mLZn2+标准液。
计算产品的纯度为 。
15. 、CuCl是重要的化工原料,常用来作为有机合成的催化剂。实验室常用如下装置来制备 。
已知:CuCl 易潮解;CuCl不溶于乙醇和稀盐酸;KCr O 在酸性条件下被还原成Cr3+。
2 2 2 7
Ⅰ.CuCl 的制备
2
(1)实验开始时需要先打开A装置中分液漏斗活塞滴加浓盐酸,一段时间后再点燃D处酒精灯,目的是
。
(2)装置A中发生反应的化学方程式是 ;该反应氧化剂与还原剂的物质的量之比为 。
(3)B装置所盛试剂为 ;E装置的作用是 。
Ⅱ.CuCl的制备
将上述实验制得的粉末加水溶解,滴加少量稀盐酸,向溶液中通入适量的 气体,加热即可得到白色沉
淀,将过滤后的白色沉淀用乙醇洗涤2~3次后,干燥即可得到CuCl晶体。
(4)加少量盐酸的作用是 。(5)用CuCl 和SO ,制备CuCl的离子方程式为 。
2 2