文档内容
3.4.1沉淀溶解平衡(分层作业)
1.对饱和AgCl溶液(有AgCl固体存在)进行下列操作后,c(Ag+)保持不变的是
A.加少量水稀释 B.加热
C.加入少量浓盐酸 D.加入少量固体AgNO
3
2.已知:向难溶电解质饱和溶液中加入与该电解质没有相同离子的强电解质时,使难溶物溶解度增大的
效应称为盐效应。常温下,在含大量BaSO 固体的浊液中加入0.01mol下列物质(忽略体积变化),溶液中
4
c(Ba2+)由大到小的排序正确的是
①BaSO ②Na SO ③KNO
4 2 4 3
A.②①③ B.③②① C.③①② D.①③②
3.变化观念和平衡思想是化学核心素养之一,以下对电离平衡、水解平衡、溶解平衡符号表征的表示不
正确的是
A.碳酸钙的电离方程式:CaCO =Ca2++CO2-
3 3
B.碳酸钙的溶解平衡:CaCO (s)⇌Ca2+(aq)+CO2- (aq)
3 3
C.碳酸氢钠溶液电离平衡:HCO- +H O⇌CO2- +H O+
3 2 3 3
D.NH Cl溶于DO中水解平衡:NH+ +D O⇌NH ·D O+H+
4 2 4 2 3 2
4.三明市围绕萤石(CaF )资源打造全产业链,把氟化工作为未来重要的支柱产业培育。下列叙述错误的是
2
A.萤石悬浊液中含有氟离子
B.氯化氢的水溶液中存在电离平衡
C.锂电池中的六氟磷酸锂是非电解质
D.氟利昂不易燃、易液化,可做制冷剂
5.在某温度下,向含有AgCl固体的AgCl饱和溶液中加入少量稀盐酸,下列说法不正确的是
A.AgCl的溶解度不变 B.AgCl的K 不变
sp
C.溶液中银离子的浓度减小 D.溶液中氯离子的浓度增大
6.在平衡体系Ca(OH) (s) Ca2+(aq)+2OH-(aq) △H<0中,能使c(Ca2+)减小,而使c(OH-)增大的是
2
A.加入少量CuCl 固体 B.加入少量NaCl固体
2
C.加入少量KCO 固体 D.升高体系温度
2 3
7.按要求填空
(1)KAl(SO )·1HO可做净水剂,其原理是(用离子方程式表示) 。
4 2 2 2
(2)将体积相等的NaOH稀溶液和CHCOOH稀溶液充分混合后,若溶液中c(Na+)=c(CHCOO-),则混合前
3 3c(NaOH) (填“ ”“ ”或“ ”)c(CHCOOH)。
3
(3)将AgCl分别放入①5mL HO、②10mL 0.2mol/L MgCl 溶液、③20mL 0.5mol/L AgNO 溶液、④40mL
2 2 3
0.1mol/L HCl溶液中溶解至饱和,各溶液中Ag+的浓度由大到小的顺序是 (用序号填空)。
(4)常温下a mol/L CH COOH稀溶液和b mol/L KOH稀溶液等体积混合,若溶液呈中性则CHCOOH的电离
3 3
平衡常数K = 。
a
(5)室温下,1mol/L相同体积的下列四种溶液①BaCl 、②FeCl 、③HF、④NaCO 所含阳离子数由少到多
2 3 2 3
的顺序是(用序号填空) 。
(6)标准状况下,将2.24L CO 通入100mL浓度为1.5mol/L的NaOH溶液中,用溶液中微粒的浓度符号完成
2
下列等式:2c(Na+)= 。
8.下列有关电解质溶液的说法正确的是
c(N H+ )
4
A.向盐酸中加入氨水至中性,溶液中 >1
c(Cl−
)
c(CH COO− )
3
B.将CHCOONa溶液从20℃升温至30℃,溶液中 增大
3 c(CH COOH)·c(OH− )
3
C.常温下,pH为3的醋酸溶液中加入醋酸钠固体,溶液pH增大
D.0.1molAgCl和0.1molAgI混合后加入1L水中,所得溶液中c(Cl-)=c(I-)
9.水溶液中的离子反应与平衡在生活中应用广泛。下列说法不正确的是
A.已知人体体液中存在如下平衡:CO+H O⇌HCO⇌H++HCO ,当静脉滴注大量生理盐水时,平
2 2 2 3
衡向右移动,体液的pH增大
B.牙齿表面覆盖的牙釉质存在如下平衡:Ca (PO )OH(s)⇌5Ca2+(ag)+3PO (aq)+OH-(aq),牙齿上残余
5 4 3
的糖会发酵产生H+,加快牙釉质的酸蚀
C.用100mL0.01mol/L硫酸洗涤BaSO 沉淀,与用等体积的蒸馏水洗涤相比,BaSO 损失更多
4 4
D.人们洗发时所用的洗发液的pH约为7.5,洗净后再使用具有保护头发、调节pH功能的护发素
10.如图所示,有T、T 两种温度下两条BaSO 在水中的沉淀溶解平衡曲线,在T 温度下,下列说法不正
1 2 4 1
确的是A.加入NaSO 可使溶液由a点变到b点
2 4
B.在T 曲线上方区域(不含曲线)任意一点时,均有BaSO 沉淀生成
1 4
C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b)
D.升温可使溶液由b点变为d点
11.下列说法中正确的是
c(H+
)
A.向水中加入少量亚硫酸氢钠固体, 减小
c(OH−
)
B.常温下,将相同体积、pH均为9的烧碱溶液和氨水加水稀释,若两溶液的pH仍相等,则烧碱溶液
中加的水少
C.常温下,NH HSO 溶液中滴加NaOH溶液至溶液pH=7,则c(Na+)=2c(SO )
4 4
D.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1mol/L盐酸、③0.1mol/L氯化
镁溶液、④0.1mol/L硝酸银溶液中,则Ag+浓度:①>④=②>③
12.下列图示与对应的叙述相符的是
A.图甲表示0.1molMgCl •6H O在空气中充分加热时固体质量随时间的变化
2 2
B.图乙表示常温下,稀释等体积、等pH的HA、HB两种弱酸的稀溶液时溶液pH随加水量的变化,
则:K(HA)<K(HB)
a a
C.图丙表示0.1mol•L-1NaOH溶液滴定20.00mL0.10mol•L-1醋酸溶液得到的滴定曲线
D.图丁表示一定温度下,溴化银在水中的沉淀溶解平衡曲线,则加入AgNO 固体,a点向b点迁移
3
13.钴配合物[Co(NH )]Cl 溶于热水,在冷水中微溶,可通过如下反应制备:
3 6 3具体步骤如下:2CoCl +2NHCl+10NH +H O 2[Co(NH )]Cl +2H O。
2 4 3 2 2 3 6 3 2
Ⅰ.称取2.0glNH Cl,用5mL水溶解。
4
Ⅱ.分批加入3.0gCoCl •6H O后,将溶液温度降至10℃以下,加入1g活性炭、7mL浓氨水,搅拌下逐滴加
2 2
入10mL6%的双氧水。
Ⅲ.加热至55~60℃反应20min。冷却,过滤。
Ⅳ.将滤得的固体转入含有少量盐酸的25mL沸水中,趁热过滤。
Ⅴ.滤液转入烧杯,加入4mL浓盐酸,冷却结晶、过滤、干燥,得到橙黄色晶体。
回答下列问题:
(1)[Co(NH )]Cl 中Co元素的化合价为 ,双氧水的作用是 。
3 6 3
(2)加快NH Cl溶解的操作有 (任写一条)。
4
(3)步骤Ⅱ中,将温度降至10℃以下以避免 、 ;可选用 来降低溶液温度。
(4)过滤所需的玻璃仪器有: 。
(5)步骤Ⅳ中,趁热过滤,除掉的不溶物主要为 。
(6)步骤Ⅴ中加入浓盐酸的目的是 。
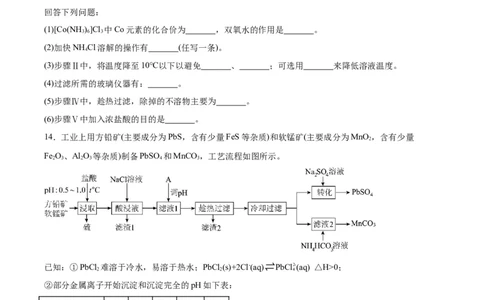
14.工业上用方铅矿(主要成分为PbS,含有少量FeS等杂质)和软锰矿(主要成分为MnO ,含有少量
2
Fe O、Al O 等杂质)制备PbSO 和MnCO ,工艺流程如图所示。
2 3 2 3 4 3
已知:①PbCl 难溶于冷水,易溶于热水;PbCl (s)+2Cl-(aq)⇌PbCl2- (aq) △H>0;
2 2 4
②部分金属离子开始沉淀和沉淀完全的pH如下表:
金属离子 Fe2+ Fe3+ Al3+ Mn2+ Pb2+
开始沉淀的pH 7.0 1.7 3.7 7.6 7.0
沉淀完全的pH 9.6 3.2 4.7 9.8 9.0
③ 时,HCOK =4.2×10-7,K =5.6×10-11;K (MnCO )=2.2×10-11。
2 3 a1 a2 sp 3
回答下列问题:
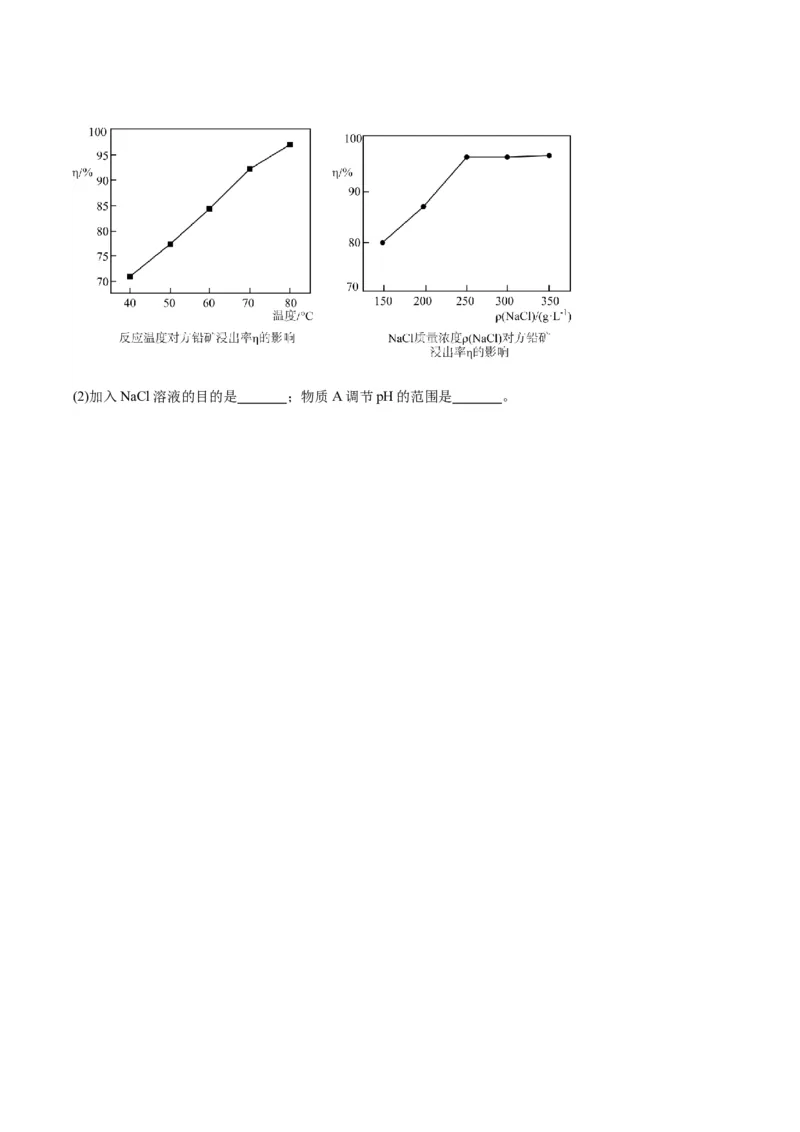
(1)为提高方铅矿的浸出率,结合下图信息,选择“浸取”的合适条件 。“浸取”过程中发生的主
要反应的化学方程式为 ,“酸浸液”中含有的金属阳离子有Pb2+、 。(2)加入NaCl溶液的目的是 ;物质A调节pH的范围是 。