文档内容
2020—2021 学年人教版(2019)选择性必修三章节自我
强化训练 1.2.2 确定实验式—元素分析
1.有机物的天然提取和人工合成往往得到的是混合物,假设给你一种这样的有机混合物让你研
究,一般要采取的几个步骤是( )
A.确定化学式→确定实验式→确定结构式→分离、提纯
B.分离、提纯→确定化学式→确定实验式→确定结构式
C.分离、提纯→确定结构式→确定实验式→确定化学式
D.分离、提纯→确定实验式→确定分子式→确定结构式
2.将2.4g某有机物M置于密闭容器中燃烧,定性实验表明产物是 、 和水蒸气。将燃烧
产物依次通过浓硫酸、碱石灰和灼热的氧化铜(试剂均足量,且充分反应),测得浓硫酸增重1.44g,
碱石灰增重1.76g,氧化铜减轻0.64g。下列说法中不正确的是( )
A.M的实验式为
B.若要得到M的分子式,还需要测得M的相对分子质量或物质的量
C.若M的相对分子质量为60,则M一定为乙酸
D.通过红外光谱仪可分析M中的官能团
3.25℃和101kPa时,乙烷、乙炔和丙烯组成的混合烃32mL与过量氧气混合并完全燃烧,除去水
蒸气,恢复到原来的温度和压强,气体的总体积缩小了72mL,原混合烃中乙炔的体积分数为( )
A.12.5% B.25% C.50% D.75%
4.A是一种含碳、氢、氧三种元素的有机化合物。已知:A中碳的质量分数为44.1%,氢的质量分
数为8.82%,那么A的实验式是( )
A.C H O B.C H O C.C H O D.C H O
5 12 4 5 12 3 4 10 4 5 10 4
5.现有乙酸和两种链状单烯烃的混合物,若其中氧的质量分数为a,则碳的质量分数是( )
A.
B.C.
D.
6.某种有机物完全燃烧后,生成44g CO 、18g H O,下列说法正确的( )
2 2
A.有机物一定是烯烃或环烷烃
B.有机物分子中C、H、O原子个数比为1:2:3
C.有机物分子中碳氢原子个数比为1:2
D.可以确定有机物中有O,但不知原子个数
7.1mol某烃完全燃烧可得到2mol CO ;在一定条件下,1mol该烃能与2mol H 发生加成反应,
2 2
这种烃是( )
A.CH B.C H C.C H D.C H
4 2 4 2 2 3 4
8.某气态烃的组成中碳元素的质量分数为81.8%,其密度是相同条件下氢气密度的22倍,则该
烃的分子式为( )
A.C H B.C H C.C H D.C H
2 6 3 6 3 8 4 8
9.下列化学用语表达正确的是( )
A.—氯乙烷的结构式:
B.丁烷的结构简式:
C.四氯化碳的电子式:
D.苯的分子式:
10.氯仿(CHCl )可用做麻醉剂,但常因保存不慎,而被空气氧化,生成有剧毒的光气(COCl ),发
3 2
生反应的化学方程式为2CHCl +O →2HCl+2COCl ,为防止发生事故,在使用氯仿前要检验其是否
3 2 2
变质,应选用的试剂是( )
A.氢氧化钠溶液
B.硝酸银溶液
C.溴水
D.淀粉碘化钾试剂11.在乙醛和乙酸乙酯组成的混合物中,已知氢元素占总质量的 ,则氧元素占总质量的( )
A.
B.
C.
D.
12.有机物键线式结构的特点是以线示键,每个折点和线端点处表示有一个碳原子,并以氢补
足四价,C、H不表示出来。降冰片烷立体结构如图所示:
(1)写出其分子式 。
(2)当降冰片烷发生一氯取代时,能生成 种沸点不同的产物。
(3)根据降冰片烷的键线式结构,请你判断:降冰片烷属于 。
a.环烷烃 b.饱和烃 c.不饱和烃 d.芳香烃
(4)降冰片烷具有的性质是 。
a.能溶于水 b.能燃烧 c.能使酸性高锰酸钾溶液褪色
d.能发生加成反应 e. 能发生取代反应 f. 常温常压下为气体
13.已知某有机物A:
①由C、H、O三种元素组成,经燃烧分析实验测定其碳的质量分数是64.86%,氢的质量分数
是13.51%
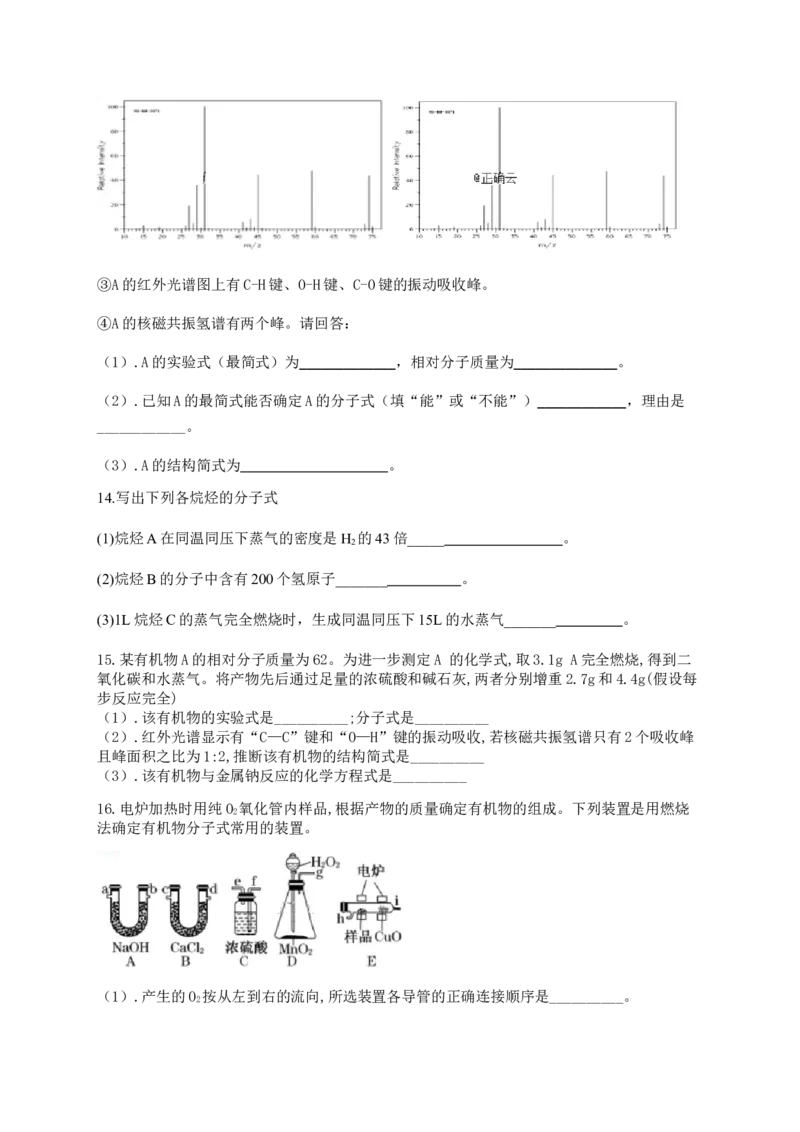
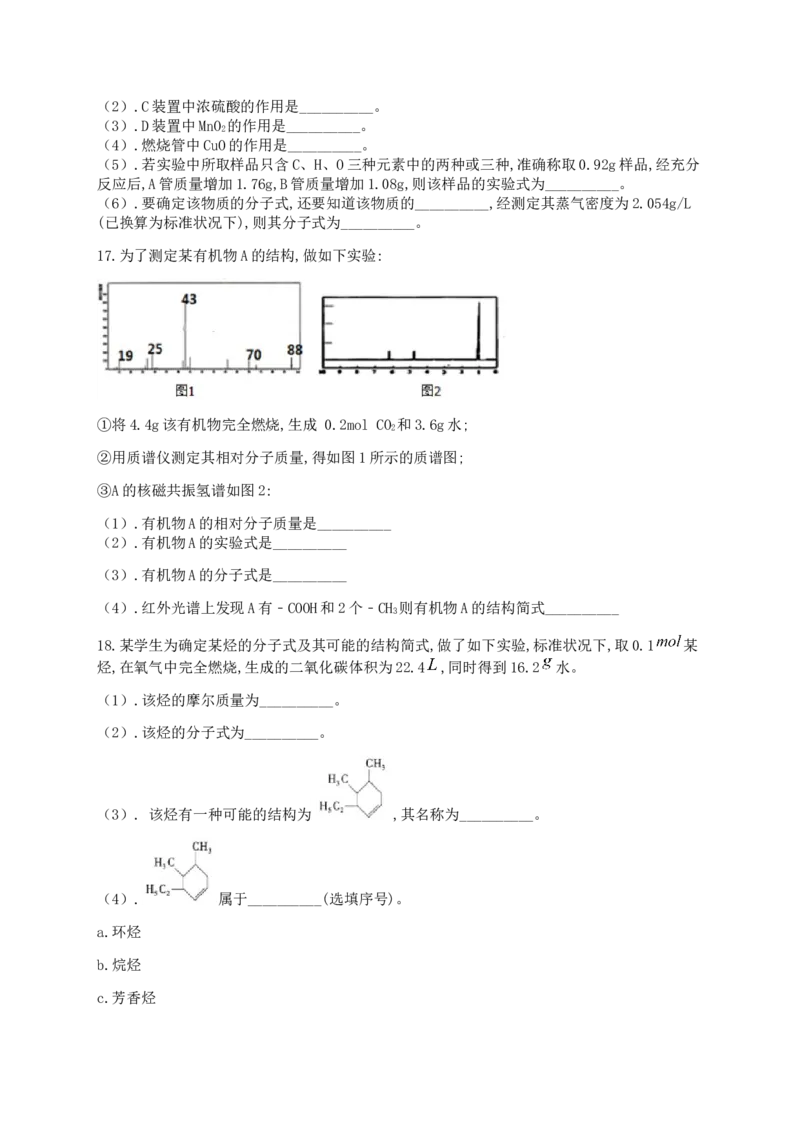
②下图是该有机物的质谱图,③A的红外光谱图上有C-H键、O-H键、C-O键的振动吸收峰。
④A的核磁共振氢谱有两个峰。请回答:
(1).A的实验式(最简式)为 _ ___________ _,相对分子质量为 _ ____________ _。
(2).已知A的最简式能否确定A的分子式(填“能”或“不能”) _ __________ _,理由是
____________。
(3).A的结构简式为 _ __________________ _。
14.写出下列各烷烃的分子式
(1)烷烃A在同温同压下蒸气的密度是H 的43倍_____ 。
2
(2)烷烃B的分子中含有200个氢原子_______ 。
(3)1L烷烃C的蒸气完全燃烧时,生成同温同压下15L的水蒸气_______ 。
15.某有机物A的相对分子质量为62。为进一步测定A 的化学式,取3.1g A完全燃烧,得到二
氧化碳和水蒸气。将产物先后通过足量的浓硫酸和碱石灰,两者分别增重2.7g和4.4g(假设每
步反应完全)
(1).该有机物的实验式是__________;分子式是__________
(2).红外光谱显示有“C—C”键和“O—H”键的振动吸收,若核磁共振氢谱只有2个吸收峰
且峰面积之比为1:2,推断该有机物的结构简式是__________
(3).该有机物与金属钠反应的化学方程式是__________
16.电炉加热时用纯O 氧化管内样品,根据产物的质量确定有机物的组成。下列装置是用燃烧
2
法确定有机物分子式常用的装置。
(1).产生的O 按从左到右的流向,所选装置各导管的正确连接顺序是__________。
2(2).C装置中浓硫酸的作用是__________。
(3).D装置中MnO 的作用是__________。
2
(4).燃烧管中CuO的作用是__________。
(5).若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取0.92g样品,经充分
反应后,A管质量增加1.76g,B管质量增加1.08g,则该样品的实验式为__________。
(6).要确定该物质的分子式,还要知道该物质的__________,经测定其蒸气密度为2.054g/L
(已换算为标准状况下),则其分子式为__________。
17.为了测定某有机物A的结构,做如下实验:
①将4.4g该有机物完全燃烧,生成 0.2mol CO 和3.6g水;
2
②用质谱仪测定其相对分子质量,得如图1所示的质谱图;
③A的核磁共振氢谱如图2:
(1).有机物A的相对分子质量是__________
(2).有机物A的实验式是__________
(3).有机物A的分子式是__________
(4).红外光谱上发现A有﹣COOH和2个﹣CH 则有机物A的结构简式__________
3
18.某学生为确定某烃的分子式及其可能的结构简式,做了如下实验,标准状况下,取0.1 某
烃,在氧气中完全燃烧,生成的二氧化碳体积为22.4 ,同时得到16.2 水。
(1).该烃的摩尔质量为__________。
(2).该烃的分子式为__________。
(3). 该烃有一种可能的结构为 ,其名称为__________。
(4). 属于__________(选填序号)。
a.环烃
b.烷烃
c.芳香烃d.不饱和烃
19.为测定某有机化合物A的结构,进行如下实验:
(一).分子式的确定
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4g H O和8.8g CO ,消耗氧气
2 2
6.72L(标准状况下),则该物质的实验式是__________
(2)用质谱仪测定该有机化合物的相对分子质量,得到如图①所示质谱图,则其相对分子质量为
__________,该物质的分子式是__________。
(3)根据价键理论,预测A的可能结构并写出结构简式:__________
(二).结构式的确定
核磁共振氢谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可
以确定分子中氢原子的种类和数目。例如:甲基氯甲基醚(Cl-CH -O-CH )有两种氢原子如图②。
2 3
经测定,有机物A的核磁共振氢谱示意图如图③,则A的结构简式为__________。
20.为了测定某有机物A的结构,做如下实验:
①将2.3g该有机物完全燃烧,生成0.1molCO 和2.7g水。
2
②用质谱仪测定其相对分子质量,得到如图一示的质谱图。
③用核磁共振仪处理该化合物,得到如图二所示图谱,图中三个峰的面积之比是1:2:3。
④用红外光谱仪处理该化合物,得到如图三所示图谱。试回答下列问题:
(1)有机物A的相对分子质量是____________。
(2)有机物A的实验式是_____________。
(3)能否根据A的实验式确定A的分子式?__________(填“能”或“不能”)。若能,则
A的分子式是___________(若不能,则此空不填)。
(4)写出有机物A的结构简式:__________________。参考答案
1.答案:D
解析:
2.答案:C
解析:浓硫酸增重1.44g,说明燃烧产物水的物质的量为 =0.08mol;碱石灰增重1.76g,说
明燃烧产物CO 的物质的量为 =0.04mol;氧化铜减轻0.64g,说明燃烧产物CO的物质的
2
量为 =0.04mol;则此有机物中含有碳原子0.08mol,氢原子0.16mol,氧原子的物质的量为
=0.08mol;A.有机物M中C:H:O=0.08mol:0.16mol:0.08mol=1:2:1,
则 M的实验式为CH O,故A正确;B.有M的最简式,若要得到M的分子式,则还需要测得M的
2
相对分子质量或物质的量,故B正确;C.若M的相对分子质量为60,则M的分子式为C H O ,但不
2 4 2
一定为乙酸,还可能是甲酸甲酯或2-羟基乙醛,故C错误;D.利用红外光谱仪可分析有机物中的官
能团,故D正确;答案为C。
3.答案:B
解析: ; ; .设混
合烃中 为a mL, 为b mL, 为c mL,则有a+b+c=32①;2.5(a+c)+1.5b=72②,解方程
组①②可得b=8,故原混合烃中乙炔的体积分数为 。
4.答案:A
解析:由于A中碳的质量分数为44.1%,氢的质量分数为8.82%,故A中氧的质量分数为1-
44.1%-8.82%=47.08%。由此可算出 ,故该有机
物的实验式为 ,A正确。
5.答案:C
解析:乙酸的化学式为C H O ,链状单烯烃的通式为C H ,则混合物中C、H原子数目之比
2 4 2 n 2n
为1︰2,C、H元素质量之比为12︰2=6︰1,混合物中一共有三种元素,氧的质量分数为a,则碳、氢元素的质量分数之和为1-a,所以化合物中碳元素质量分数为(1-a)×6/7= ,
C正确。
6.答案:C
解析:因为氧气也提供氧元素,所以不能判断有机物中是否含氧,可排除ABD
7.答案:C
解析:
8.答案:C
解析:该气态烃的相对分子质量:M =22×2=44,则该气态烃中含碳原子: =3,含氢原
r
子: =8,该烃的分子式:C H
3 8
本题求分子式的方法很多,也可以直接利用“商余法”求分子式: =3……2即:C H ,或根据
3 8
碳和氢的质量分数,先求出实验式:C H ,利用有机物的组成关系(C H 已达饱和)推理实验式即分
3 8 3 8
子式。
9.答案:B
解析:一氯乙烷的结构式为 ,四氯化碳的电子式为: ,苯的分子式为
,所以A、C、D项均不正确。
10.答案:B
解析:A.加入NaOH溶液,没有明显的现象,不能用来检验,故A错误;
B.氯仿被氧化时生成HCl,加入硝酸酸化的硝酸银溶液生成AgCl白色沉淀,可检验,故B正确;
C.反应中各物质与溴水不反应,加入溴水没有明显现象,所以不能用水检验,故C错误;
D.淀粉碘化钾试剂与氯化氢不发生反应,无法检验氯仿是否变质,故D错误;
故选B。
11.答案:A解析:乙醛( )、乙酸乙酯( ),两者实验式相同,都为 , ,
故应为A。
考点:考查有机物混合的有关计算
点评:该题是中等难度的试题,试题基础性强,侧重能力的培养,有利于培养学生的创新思维能力。
该题的关键是根据有机物的化学式得出混合物的最简式,然后直接列式计算即可。
12.答案:(1)C H ;炔;CH≡CCH CH CH CH CH
7 12 2 2 2 2 3
(2)3
(3)ab
(4)be
解析: (1)由结构简式可知分子式为为C7H12,故答案为:C7H12;
(2)由结构对称性可知,含3种位置的H,则一氯取代时,能生成3种沸点不同的产物,故答案
为:3;
(3)A、降冰片烷只存在碳碳单键且成环,故为环烷烃,故A正确;
B. 由于结构中无不饱和键,故为饱和烃,故B正确;
C. 由于结构中无不饱和键,故不属于不饱和烃,故C错误;
D. 此物质中不含苯环,故不是芳香烃,故D错误。
故选ab.
13.答案:(1). C H O;74
4 10
(2).能, 因为A的最简式为C H O,氢原子已经达到饱和。所以A的最简式就是A的分子式
4 10
(3).
解析:
14.答案:(1)C H
6 14
(2)C H
99 200
(3)C H
14 30
解析:
15.答案:(1).CH O, C H O
3 2 6 2
(2).CH OHCH OH
2 2
(3).CH OHCH OH+2Na→CH ONaCH ONa+H
2 2 2 2 2
解析:16.答案:(1).g→f→e→h→i→c(或d)→d(或c)→a(或b)→b(或a)
(2).吸收H O,得到干燥O
2 2
(3).催化剂,加快O 的生成
2
(4).使有机物充分氧化生成CO 和H O
2 2
(5).C H O
2 6
(6).相对分子质量 C H O
2 6
解析:
17.答案:(1).88;(2).C H O
2 4
(3).C H O
4 8 2
.(CH ) CHCOOH
(4) 3 2
解析:
18.答案:(1).138g/mol ; (2).C H
10 18
(3).4,5-二甲基-3-乙基-1-环己烯; (4).a、d
解析:0.1 某烃完全燃烧可生成 ,
,根据元素守恒可知:每个该烃分子中应含10个碳原子,18个
氢原子。故其分子式为 ,摩尔质量为138 。
19.答案:(一).(1)C H O
2 6
(2)46 C H O
2 6
(3)CH CH OH或CH OCH
3 2 3 3
(二).CH CH OH
3 2
解析:(一).(1)由题意可知
,根据氧原子
守恒可知有机物中含有n(O)=0.3mol+0.2mol×2-0.3mol×2=0.1mol,则有机物中
N(C):N(H):N(O)=0.2mol:0.6mol:0.1mol=2:6:1,实验式为C H O
2 6
(2)该物质中各元素的原子个数比为N(C):N(H):N(O)=2:6:1,则最简式为C H O,根据质谱图中最
2 6
大质荷比为46可得该有机物的相对分子质量为46,则有机物的分子式为C H O。
2 6
(3)有机物的分子式为C H O,分子中可能存在C-C、C-H、C-O、O-H等化学键,可能的结构简式
2 6
为CH CH OH或CH OCH 。
3 2 3 3
(二).有机物A分子中有三种不同化学环境的氢原子,应为乙醇,即结构简式为CH CH OH,二甲
3 2
醚分子中只有一种不同化学环境的氢原子。
20.答案:(1)46
(2)C H O
2 6
(3)能;C H O
2 6(4)CH CH OH
3 2
解析: