文档内容
第2课时 离子晶体 过渡晶体与混合型晶体
发 展 目 标 体 系 构 建
1.借助离子晶体模型认识离子晶体的结构和性质。
2.能利用离子键的有关理论解释离子晶体的物理性质。
3.知道介于典型晶体之间的过渡晶体及混合型晶体是普遍存
在的。
一、离子晶体
1.结构特点
(1)构成粒子:阳离子和阴离子。
(2)作用力:离子键。
(3)配位数:一个离子周围最邻近的异电性离子的数目。
微点拨:大量离子晶体的阴离子或阳离子不是单原子离子,有的还存在电中性分子。离子晶体
中不仅有离子键还存在共价键、氢键等。
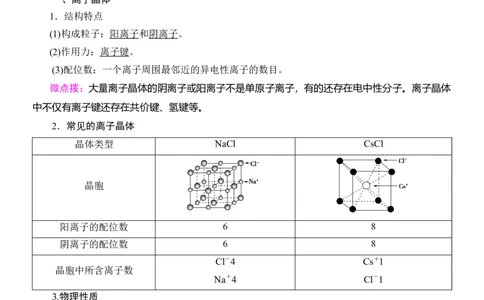
2.常见的离子晶体
晶体类型 NaCl CsCl
晶胞
阳离子的配位数 6 8
阴离子的配位数 6 8
Cl-4 Cs+1
晶胞中所含离子数
Na+4 Cl-1
3.物理性质
(1)硬度较大,难于压缩。
(2)熔点和沸点较高。
(3)固体不导电,但在熔融状态或水溶液时能导电。
离子晶体是否全由金属元素与非金属元素组成?
[提示] 不一定,如NH Cl固体是离子晶体但它不含金属元素。
4
二、过渡晶体与混合型晶体
1.过渡晶体
(1)四类典型的晶体是指分子晶体、共价晶体、金属晶体和离子晶体。(2)过渡晶体:介于典型晶体之间的晶体。
①几种氧化物的化学键中离子键成分的百分数
氧化物 Na O MgO Al O SiO
2 2 3 2
离子键的百分
62 50 41 33
数/%
从上表可知,表中4种氧化物晶体中的化学键既不是纯粹的离子键,也不是纯粹的共价键,这
些晶体既不是纯粹的离子晶体也不是纯粹的共价晶体,只是离子晶体与共价晶体之间的过渡晶体。
②偏向离子晶体的过渡晶体在许多性质上与纯粹的离子晶体接近,因而通常当作离子晶体来处
理,如Na O 等。同样,偏向共价晶体的过渡晶体则当作共价晶体来处理,如Al O 、SiO 等。
2 2 3 2
微点拨:四类典型晶体都有过渡晶体存在。
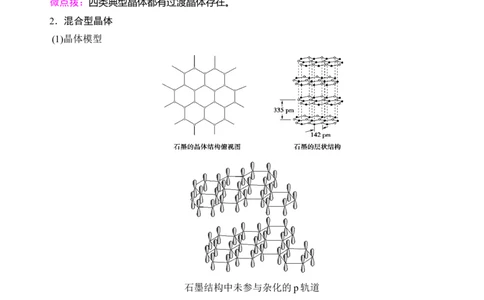
2.混合型晶体
(1)晶体模型
石墨结构中未参与杂化的p轨道
(2)结构特点——层状结构
①同层内碳原子采取sp2杂化,以共价键(σ键)结合,形成平面六元并环结构。
②层与层之间靠范德华力维系。
③石墨的二维结构内,每个碳原子的配位数为 3,有一个未参与杂化的2p电子,它的原子轨道
垂直于碳原子平面。
(3)晶体类型:石墨晶体中,既有共价键,又有金属键和范德华力,属于混合晶体。
(4)性质:熔点很高、质软、易导电等。
微点拨:石墨为什么具有良好的导电性?
提示:由于碳原子的p轨道相互平行且相互重叠,p轨道中的电子可在整个碳原子平面中运动,所以石墨具有导电性。
1.判断正误(对的在括号内打“√”,错的在括号内打“×”。)
(1)金属晶体和离子晶体的导电实质是一样的 (×)
(2)固态不导电、水溶液能导电,这一性质能说明某晶体一定是离子晶体
(×)
(3) Al O 含有金属元素,属于离子晶体 (×)
2 3
(4)石墨为混合晶体,因层间存在分子间作用力,故熔点低于金刚石。
(×)
2.离子晶体一般不具有的特征是( )
A.熔点较高,硬度较大
B.易溶于水而难溶于有机溶剂
C.固体时不能导电
D.离子间距离较大,其密度较大
D [离子晶体的结构决定着离子晶体具有一系列特性,这些特性包括A、B、C项所述。]
3.下列7种物质:①白磷(P );②水晶;③氯化铵;④氢氧化钙;⑤氟化钠;⑥过氧化钠;⑦
4
石墨。固态下都为晶体,回答下列问题(填写序号):
(1)不含金属离子的离子晶体是________,只含离子键的离子晶体是________,既有离子键又
有非极性键的离子晶体是________,既有离子键又有极性键的离子晶体是________。
(2)既含范德华力,又有非极性键的晶体是________,熔化时既要克服范德华力,又要破坏化
学键的是________,熔化时只破坏共价键的是________。
[答案] (1)③ ⑤ ⑥ ③④ (2)①⑦ ⑦ ②
离子晶体的结构与性质
离子化合物在我们周围比比皆是。常温下,许多离子化合物都是以晶体形态存在的。
(1)含金属阳离子的晶体一定是离子晶体吗?有阳离子的晶体中一定存在阴离子吗?
提示:不一定。也可能是金属晶体;晶体中含有阳离子,不一定存在阴离子,如金属晶体由阳
离子和自由电子构成。
(2)离子晶体中一定含有金属元素吗?由金属元素和非金属元素组成的晶体一定是离子晶体吗?
提示:不一定。离子晶体中不一定含金属元素,如 NH Cl、NH NO 等铵盐。由金属元素和非
4 4 3
金属元素组成的晶体不一定是离子晶体,如AlCl 是分子晶体。
3
(3)离子晶体的熔点一定低于共价晶体吗?提示:不一定。离子晶体的熔点不一定低于共价晶体,如 MgO是离子晶体,SiO 是共价晶体,
2
MgO的熔点高于SiO 的熔点。
2
(4)离子晶体中除含有离子键外,是否含有共价键?
提示:离子晶体中除含有离子键外,还有可能含有共价键、配位键。如 Na O 、NaOH、
2 2
Ba(OH) 、Na SO 中均含离子键和共价键,NH Cl中含有离子键、共价键、配位健。
2 2 4 4
1.离子晶体的性质
性质 原因
离子晶体中有较强的离子键,熔化或汽化时需消耗较多的能量。所以离子晶体
熔、沸点 有较高的熔点、沸点和难挥发性。通常情况下,同种类型的离子晶体,离子半
径越小,离子键越强,熔、沸点越高
硬而脆。离子晶体表现出较高的硬度。当晶体受到冲击力作用时,部分离子键
硬度
发生断裂,导致晶体破碎
不导电,但熔融或溶于水后能导电。离子晶体中,离子键较强,阴、阳离子不
能自由移动,即晶体中无自由移动的离子,因此离子晶体不导电。当升高温度
时,阴、阳离子获得足够的能量克服了离子间的相互作用力,成为自由移动的
导电性
离子,在外加电场的作用下,离子定向移动而导电。离子晶体溶于水时,阴、
阳离子受到水分子的作用成了自由移动的离子(或水合离子),在外加电场的作用
下,阴、阳离子定向移动而导电
大多数离子晶体易溶于极性溶剂(如水)中,难溶于非极性溶剂(如汽油、苯、
CCl )中。当把离子晶体放入水中时,水分子对离子晶体中的离子产生吸引,使
4
溶解性
离子晶体中的离子克服离子间的相互作用力而离开晶体,变成在水中自由移动
的离子
离子晶体中阴、阳离子交替出现,层与层之间如果滑动,同性离子相邻而使斥
延展性
力增大导致不稳定,所以离子晶体无延展性
2.离子晶体的判断
判断一种物质是不是离子晶体,我们可以根据物质的分类、组成和性质等方面进行判断。
(1)利用物质的分类
金属离子和酸根离子、OH-形成的大多数盐、强碱,活泼金属的氧化物和过氧化物(如Na O和
2
Na O ),活泼金属的氢化物(如NaH),活泼金属的硫化物等都是离子晶体。
2 2
(2)利用元素的性质和种类
如成键元素的电负性差值大于1.7的物质,金属元素(特别是活泼的金属元素,ⅠA、ⅡA族元
素)与非金属元素(特别是活泼的非金属元素,ⅥA、ⅦA族元素)组成的化合物。
(3)利用物质的性质
离子晶体一般具有较高的熔、沸点,难挥发,硬而脆;固体不导电,但熔融或溶于水时能导电,大多数离子晶体易溶于极性溶剂而难溶于非极性溶剂。
1.下列性质适合于离子晶体的是( )
①熔点1 070 ℃,易溶于水,水溶液能导电
②熔点10.31 ℃,液态不导电,水溶液能导电
③能溶于CS ,熔点112.8 ℃,沸点444.6 ℃
2
④熔点97.81 ℃,质软,导电,密度0.97 g/cm3
⑤熔点-218 ℃,难溶于水
⑥熔点3 900 ℃,硬度很大,不导电
⑦难溶于水,固体时导电,升温时导电能力减弱
⑧难溶于水,熔点高,固体不导电,熔化时导电
A.①⑧ B.②③⑥
C.①④⑦ D.②⑤
A [离子晶体液态时能导电,难溶于非极性溶剂,熔点较高、质硬而脆,固体不导电,故
②③④⑤⑦均不符合离子晶体的特点;⑥中熔点达3 900 ℃,硬度很大,应是共价晶体。故只有
①⑧符合题意。]
2.氧化钙在2 973 K时熔化,而氯化钠在1 074 K时熔化,二者的离子间距离和晶体结构都类
似,有关它们熔点差别较大的原因叙述不正确的是( )
A.氧化钙晶体中阴、阳离子所带的电荷数多
B.氧化钙中氧离子与钙离子之间的作用力更强
C.氧化钙晶体的结构类型与氯化钠晶体的结构类型不同
D.在氧化钙与氯化钠的离子间距离类似的情况下,熔点主要由阴、阳离子所带电荷数的多少
决定
C [氧化钙和氯化钠的离子间距离和晶体结构都类似,故熔点主要由阴、阳离子所带电荷数的
多少决定。]
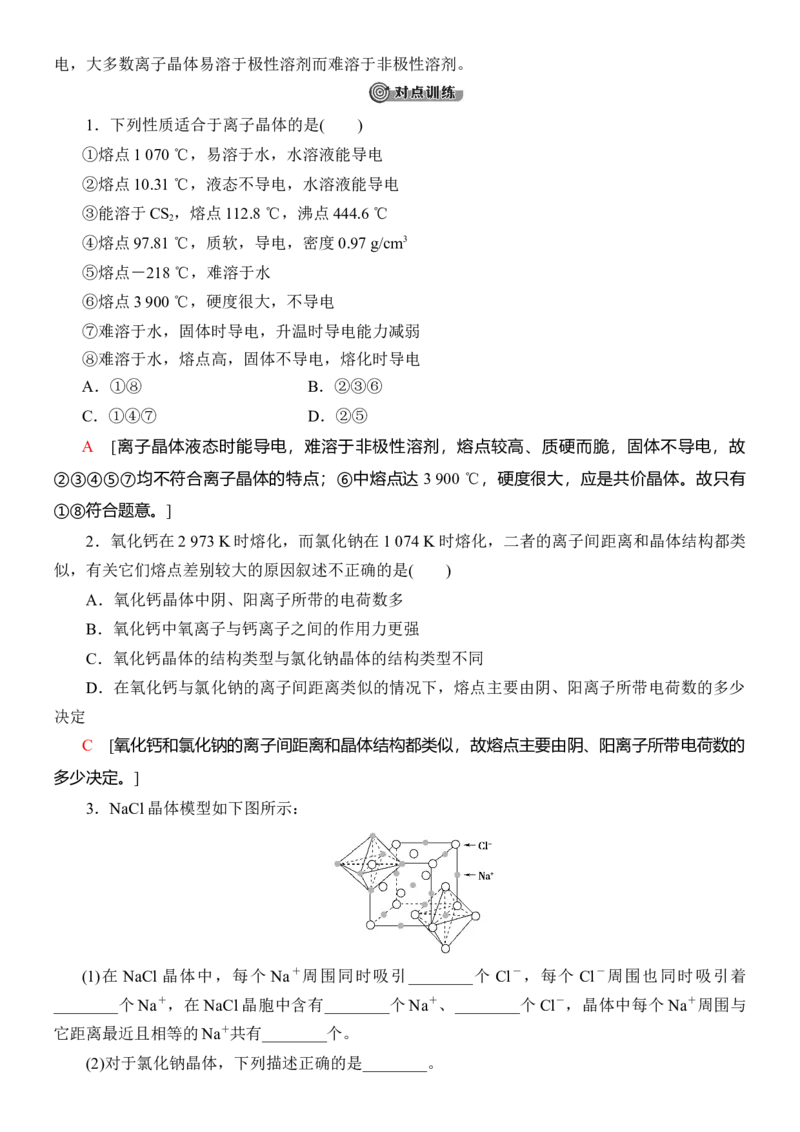
3.NaCl晶体模型如下图所示:
(1)在 NaCl 晶体中,每个 Na+周围同时吸引________个 Cl-,每个 Cl-周围也同时吸引着
________个Na+,在NaCl晶胞中含有________个Na+、________个Cl-,晶体中每个Na+周围与
它距离最近且相等的Na+共有________个。
(2)对于氯化钠晶体,下列描述正确的是________。A.相邻的正、负离子核间距等于正、负离子半径之和
B.与氯化铯晶体结构相同
C.每个Na+与6个Cl-作为近邻
[解析] (1)在氯化钠晶体中,一个Na+位于晶胞的中心,12个Na+分别位于晶胞的12条棱上,
则属于该晶胞的Na+相当于3个,因此一个晶胞中共含有 4个Na+,8个Cl-分别位于晶胞的8个
顶点上,则属于该晶胞的Cl-相当于1个,6个Cl-分别位于晶胞的6个面心上,则属于该晶胞的
Cl-相当于3个,所以一个晶胞中共含有4个Cl-。可见NaCl晶体中Na+、Cl-的个数比为1∶1。
图中位于晶胞中心的Na+实际上共有3个平面通过它,通过中心Na+的每个平面都有4个Na+
位于平面的四角,这4个Na+与中心Na+距离最近且距离相等。所以在 NaCl晶体中,每个Na+周
围与它距离最近且距离相等的 Na+共有12个,按相似的方法可推出每个 Cl-周围与它最近且距离
相等的Cl-也共有12个。
(2)氯化铯晶体结构呈体心立方堆积,B错误,氯化钠晶体中以Na+为中心向三维方向伸展,有
6个Cl-近邻,C正确,相邻的正、负离子核间距不等于正、负离子半径之和,A错误。
[答案] (1)6 6 4 4 12 (2)C
判断物质结构图是否表示晶胞的方法
整块晶体是由完全相同的晶胞“无隙并置”地堆积而成的。“完全相同”包括“化学上等同”
——晶胞里原子的数目和种类完全等同;还包括“几何上等同”——晶胞的形状、取向、大小等
同,而且原子的排列完全等同。“无隙并置”即一个晶胞与它的相邻晶胞完全共顶角、共面、共
棱。晶胞的这种本质属性可归纳为晶胞具有平移性。因此可根据结构图在晶体中是否具有平移性
来判断是否表示晶胞。
1.自然界中的CaF 又称萤石,是一种难溶于水的固体,属于典型的离子晶体。下列一定能说
2
明CaF 是离子晶体的实验是( )
2
A.CaF 难溶于水,其水溶液的导电性极弱
2
B.CaF 的熔、沸点较高,硬度较大
2
C.CaF 固体不导电,但在熔融状态下可以导电
2
D.CaF 在有机溶剂(如苯)中的溶解度极小
2
C [离子晶体中含有离子键,离子键在熔融状态下被破坏,电离出自由移动的阴、阳离子,所
以离子晶体在熔融状态下能够导电,这是判断某晶体是否为离子晶体的依据。]
2.(双选)泽维尔研究发现,当用激光脉冲照射 NaI,使Na+和I-两核间距为1.0~1.5 nm时,
呈离子键;当两核靠近约距0.28 nm时,呈共价键。根据泽维尔的研究成果能得出的结论是( )A.NaI晶体是过渡晶体
B.离子晶体可能含有共价键
C.NaI晶体中既有离子键,又有共价键
D.共价键和离子键没有明显的界线
AD [化学键既不是纯粹的离子键也不是纯粹的共价键,共价键和离子键没有明显的界线。]
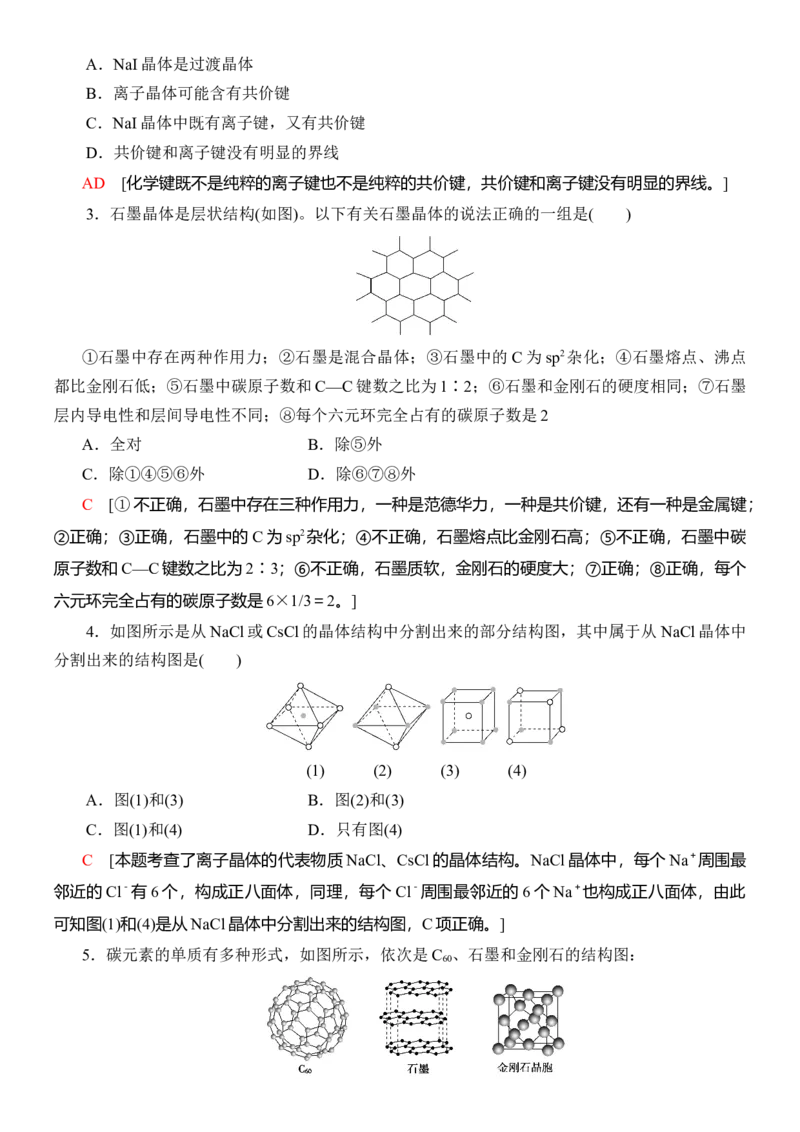
3.石墨晶体是层状结构(如图)。以下有关石墨晶体的说法正确的一组是( )
①石墨中存在两种作用力;②石墨是混合晶体;③石墨中的C为sp2杂化;④石墨熔点、沸点
都比金刚石低;⑤石墨中碳原子数和C—C键数之比为1∶2;⑥石墨和金刚石的硬度相同;⑦石墨
层内导电性和层间导电性不同;⑧每个六元环完全占有的碳原子数是2
A.全对 B.除⑤外
C.除①④⑤⑥外 D.除⑥⑦⑧外
C [①不正确,石墨中存在三种作用力,一种是范德华力,一种是共价键,还有一种是金属键;
②正确;③正确,石墨中的C为sp2杂化;④不正确,石墨熔点比金刚石高;⑤不正确,石墨中碳
原子数和C—C键数之比为2∶3;⑥不正确,石墨质软,金刚石的硬度大;⑦正确;⑧正确,每个
六元环完全占有的碳原子数是6×1/3=2。]
4.如图所示是从NaCl或CsCl的晶体结构中分割出来的部分结构图,其中属于从NaCl晶体中
分割出来的结构图是( )
(1) (2) (3) (4)
A.图(1)和(3) B.图(2)和(3)
C.图(1)和(4) D.只有图(4)
C [本题考查了离子晶体的代表物质NaCl、CsCl的晶体结构。NaCl晶体中,每个Na+周围最
邻近的Cl-有6个,构成正八面体,同理,每个 Cl-周围最邻近的6个Na+也构成正八面体,由此
可知图(1)和(4)是从NaCl晶体中分割出来的结构图,C项正确。]
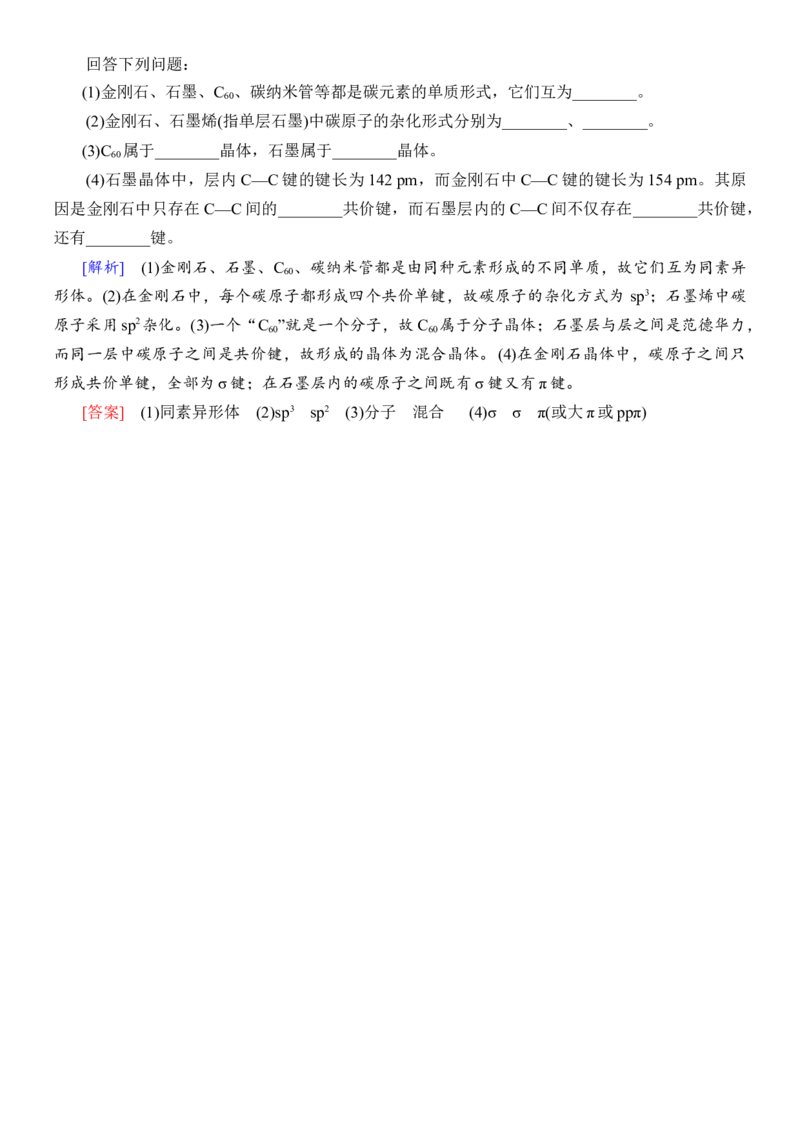
5.碳元素的单质有多种形式,如图所示,依次是C 、石墨和金刚石的结构图:
60回答下列问题:
(1)金刚石、石墨、C 、碳纳米管等都是碳元素的单质形式,它们互为________。
60
(2)金刚石、石墨烯(指单层石墨)中碳原子的杂化形式分别为________、________。
(3)C 属于________晶体,石墨属于________晶体。
60
(4)石墨晶体中,层内 C—C键的键长为142 pm,而金刚石中C—C键的键长为154 pm。其原
因是金刚石中只存在C—C间的________共价键,而石墨层内的 C—C间不仅存在________共价键,
还有________键。
[解析] (1)金刚石、石墨、C 、碳纳米管都是由同种元素形成的不同单质,故它们互为同素异
60
形体。(2)在金刚石中,每个碳原子都形成四个共价单键,故碳原子的杂化方式为 sp3;石墨烯中碳
原子采用sp2杂化。(3)一个“C ”就是一个分子,故C 属于分子晶体;石墨层与层之间是范德华力,
60 60
而同一层中碳原子之间是共价键,故形成的晶体为混合晶体。(4)在金刚石晶体中,碳原子之间只
形成共价单键,全部为σ键;在石墨层内的碳原子之间既有σ键又有π键。
[答案] (1)同素异形体 (2)sp3 sp2 (3)分子 混合 (4)σ σ π(或大π或ppπ)