文档内容
九年级化学下册期末质量检测题
可能用到的相对原子质量:Al:27 O:16 Ca:40 C:12 Mg:24 Fe:56 Zn:65
Na:23 H:1 Cl:35.5
一.选择题(每题有一个正确答案,每题2分,共46分)
1.下列物质的分类正确的是( )
A.活泼金属:镁、铝、铜 B.碳单质:金刚石、石墨、碳—60
C.氧化物:水、氧化铁、熟石灰 D.混合物:空气、石油、甲烷
2.下列说法错误的是( )
A.铁粉可以除去氯化亚铁溶液中的氯化铜
B.保持干燥、外加保护层可以铁制品生锈
C.配制一定浓度的氯化钠溶液所需要的都是玻璃仪器
D.我国研制出吸附能力超强的“碳海绵”(见右上图),它很轻、可用于吸附油污
3.在托盘天平的两盘上各放一只质量相同的烧杯,在两只烧杯里分别加入等质量、等溶质质
量分数的稀硫酸,将天平调节至平衡。然后向左盘的烧杯中加入8.4g铁,反应物之间恰好完
全反应。欲使天平恢复平衡,则可向右盘的烧杯中加入 ( )
A.8.4g 铝 B.8.4g氧化钙 C.8.4g 铜 D.8.4g碳酸镁
4.现有甲、乙、丙三种金属,如果把甲和乙分别放入稀硫酸中,甲溶解并产生气体,乙不反应;
如果把乙和丙分别放入硝酸银溶液中,过一会在乙表面有银析出,丙没有变化.根据以上实
验事实,判断甲、乙、丙三种金属的活动性强弱顺序是( )
A.甲>乙>丙 B.甲>丙>乙 C.乙>甲>丙 D.乙>丙>甲
5.某金属加工厂生产过程中的废液含有少量的硝酸银和硝酸铜,为回收利用资源和防止污染,
该厂向废液中加入一定量的铁粉,反应停止后过滤,向滤液中加入少量的稀盐酸,无沉淀产
生,则下列有关说法中正确的是 ( )
A.滤出的固体中一定含有银,可能含有铜
B.滤出的固体中一定含有银和铜,一定不含有铁
C.滤液中一定含有硝酸铁,一定没有硝酸银
D.滤液中一定含有有硝酸亚铁,可能含有硝酸银和硝酸铜
6.下列离子能在pH=11的溶液中大量共存的是( )
A.K+、NO -、Na+、OH- B. CO2-、K+、Cl-、Ca2+
3 3
C. H+、Ba2+、Cl-、SO 2- D.K+、OH-、SO 2-、Cu2+
4 4
7.一定质量的锌、铁分别和等量的盐酸反应,产生氢气 质
量与时间的关系如右图所示,下列说法不正确的是 (
)
A.t 时,产生氢气的质量锌比铁大
1
B.t 时,产生氢气的速率锌比铁大
1C.t 时,参加反应锌的质量与铁相同
2
D.t 时,锌、铁消耗的盐酸质量相同
2
8.右下表是同学们做溶液形成的实验记录。以下说法不正确的是( )
A.衣服上不慎沾上碘酒,可用汽油擦洗
B.同一物质在不同溶剂中的溶解性不同
C.水、汽油、酒精都可以作溶剂
D.溶液都是均一、稳定、无色的混合物
9. 下列关于溶液的说法,正确的是 (
)
A. 溶液都是无色透明的 B. 面粉与水混合可形成溶液
C. 饱和溶液不能再溶解任何物质 D. 硝酸铵溶解在水中,溶液温度会降低
10.关于溶液和乳化的下列说法这种错误的是( )
A. 溶液中可以含有多种溶质 B. 溶液是均一、稳定的混合物
C. 用汽油洗去衣服上的油污是乳化现象 D. 溶液不一定是无色的
11.20℃时,氯化钠的溶解度为36g。对这句话理解错误的是 ( )
A.20℃时,100g水中最多能溶解氯化钠36g
B.20℃时,100g氯化钠饱和溶液中含氯化钠36g
C.20℃时,氯化钠饱和溶液中水与氯化钠的质量比为100:36
D.20℃时,将36g氯化钠溶解于100g水中,所得溶液为该温度下氯化钠的饱和溶液
12.a、b、c 三种物质的溶解度曲线如下图所示。取等质量 ℃的 a、b、c 三种物质的饱和溶液,
分别蒸发等量水后恢复至 ℃。下列说法不正确的是 (
)
A.原饱和溶液中,溶质的质量分数 a>b=c
B.恢复至 t℃℃时,析出溶质的质量 a>b=c
2
C.恢复至t℃时,三种溶液一定都是饱和溶液
2
D.若继续降温至 t℃,三种溶液一定都是饱和溶液
1
13.下列实验方法错误的是( )
A.用稀硝酸除去NaCl中混有的NaCO B.用带火星的木条区别空气和O
2 3 2
C.用水区分NHNO 和固体NaOH 两种固体 D.用湿润的石蕊试纸区别CO和CO
4 3 2
14.人体中一些液体pH的如下:唾液(6.6﹣7.1)、胃液(0.9﹣1.5)、血浆(7.35﹣7.45)、尿
液(4.7﹣8.4).其中酸性最强的是( )
A 唾液 B.胃液 C.血浆 D.尿液
15.生活处处有化学,下列做法正确的是( )
A.碘是人体需要的微量元素,需大量补充 B.霉变大米、花生等含有黄曲霉素,蒸煮后食
用 C.腌制的泡菜虽然含亚硝酸盐,但多吃无妨 D.有的指甲油中国含少量的甲醛,青
少年尽量少用16.盐酸先生闯迷宫(见右图),请你帮他选择行进路
线(不发生化学反应)。( )
17.下列化肥属于磷肥的是( )
A.NH NO B.Ca(H PO ) C.CO(NH ) D.K CO
4 3 2 4 2 2 2 2 3
18.下列各组离子能在指定溶液中大量共存的一组是( )
A.在稀盐酸中:Ba2+、CO2-、Zn2+ B.在氢氧化钠溶液中:H+、Mg2+、Cl-
3
C.在氯化钠溶液中:K+、Ca2+、NO - D.在硫酸铵溶液中:Na+、Cu2+、OH-
3
19.下列除去杂质的方法中正确的是( )
选项 物质 杂质 除杂质的方法
A CaCl 溶液 稀盐酸 过量碳酸钙、过滤
2
B KOH溶液 KCl 适量稀盐酸
C NaCl溶液 NaCO 适量硝酸钙溶液、过滤
2 3
D O CO 通过灼热的氧化铜
2
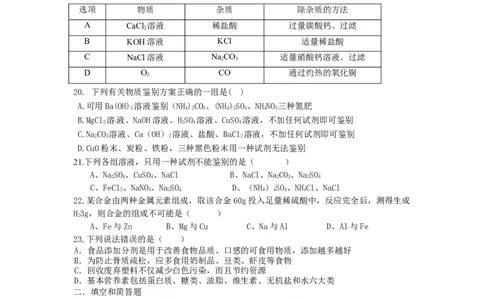
20. 下列有关物质鉴别方案正确的一组是( )
A.可用Ba(OH) 溶液鉴别(NH)CO、(NH)SO、NHNO 三种氮肥
2 4 2 3 4 2 4 4 3
B.MgCl 溶液、NaOH溶液、HSO 溶液、CuSO 溶液,不加任何试剂即可鉴别
2 2 4 4
C.NaCO 溶液、Ca(OH) 溶液、盐酸、BaCl 溶液,不加任何试剂即可鉴别
2 3 2 2
D.CuO粉末、炭粉、铁粉,三种黑色粉末用一种试剂无法鉴别
21.下列各组溶液,只用一种试剂不能鉴别的是( )
A、NaSO、CuSO、NaCl B、NaCl、NaCO、NaSO
2 4 4 2 3 2 4
C、FeCl、NaNO、NaSO D、(NH)SO、NHCl、NaCl
2 3 2 4 4 4 4 4
22.某合金由两种金属元素组成,取该合金60g投入足量稀硫酸中,反应完全后,测得生成
H3g,则合金的组成不可能是( )
2
A、Fe与Zn B、Mg与Cu C、Na与Al D、Al与Fe
23.下列说法错误的是( )
A.食品添加分剂是用于改善食物品质、口感的可食用物质,添加越多越好
B.为防止骨质疏松,应多食用奶制品、豆类、虾皮等食物
C.回收废弃塑料不仅减少白色污染,而且节约资源
D.基本营养素包括蛋白质、糖类、油脂、维生素、无机盐和水六大类
二.填空和简答题
24.(10分)A,B,C,D,E五种物质之间的转化关系如图所示,其中A,B,C三种物质中都含有同
一种元素,A是非金属单质,A的原子核外有6个电子,B,C是氧化物,D是目前世界年产量最
高的金属,E为磁铁矿的主要成分,试回答:
(1)写出下列物质的名称:B: E:
(2)写出下列反应的化学方程式:B→C ,其基本反应类型为
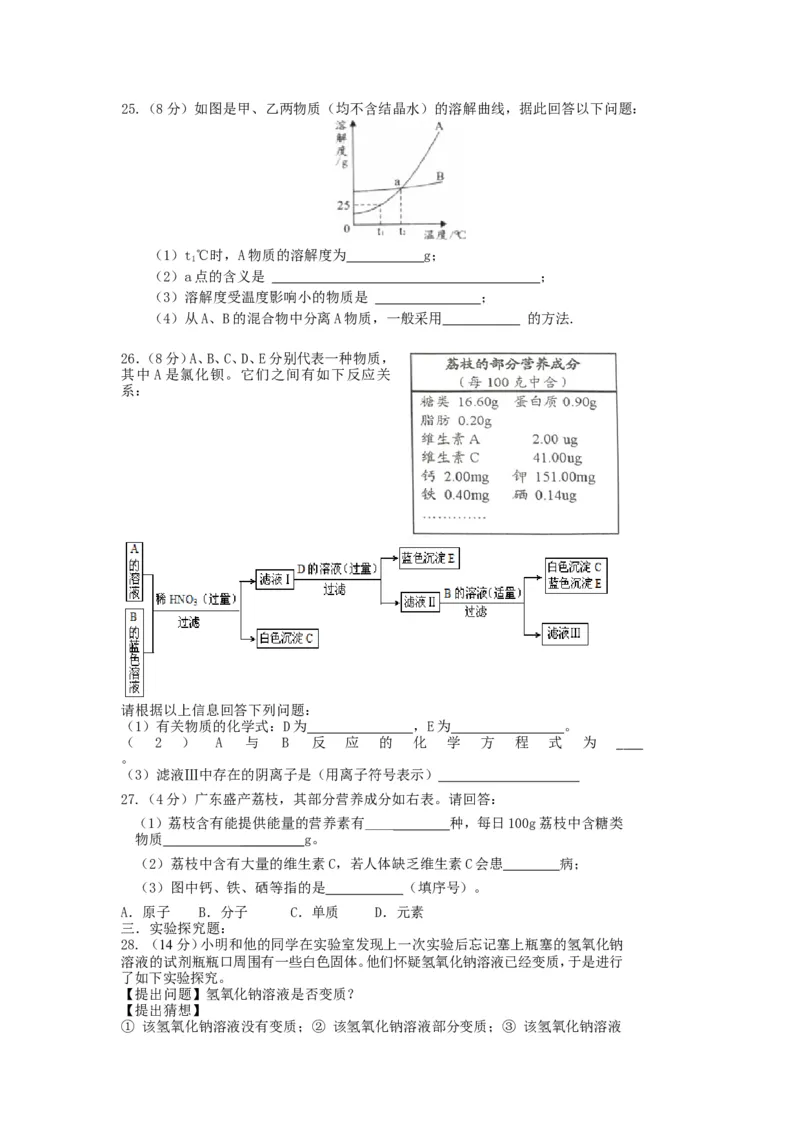
,C+E→B+D .25.(8分)如图是甲、乙两物质(均不含结晶水)的溶解曲线,据此回答以下问题:
(1)t℃时,A物质的溶解度为 g;
1
(2)a点的含义是 ;
(3)溶解度受温度影响小的物质是 ;
(4)从A、B的混合物中分离A物质,一般采用 的方法.
26.(8分)A、B、C、D、E分别代表一种物质,
其中A是氯化钡。它们之间有如下反应关
系:
请根据以上信息回答下列问题:
(1)有关物质的化学式:D为 ,E为 。
( 2 ) A 与 B 反 应 的 化 学 方 程 式 为
。
(3)滤液Ⅲ中存在的阴离子是(用离子符号表示)
27.(4分)广东盛产荔枝,其部分营养成分如右表。请回答:
(1)荔枝含有能提供能量的营养素有____ 种,每日100g荔枝中含糖类
物质 ________ _g。
(2)荔枝中含有大量的维生素C,若人体缺乏维生素C会患 病;
(3)图中钙、铁、硒等指的是 (填序号)。
A.原子 B.分子 C.单质 D.元素
三.实验探究题:
28. (14分)小明和他的同学在实验室发现上一次实验后忘记塞上瓶塞的氢氧化钠
溶液的试剂瓶瓶口周围有一些白色固体。他们怀疑氢氧化钠溶液已经变质,于是进行
了如下实验探究。
【提出问题】氢氧化钠溶液是否变质?
【提出猜想】
① 该氢氧化钠溶液没有变质;② 该氢氧化钠溶液部分变质;③ 该氢氧化钠溶液全部变质。
【实验验证】
操作 现象 结论 化学方程式
取少量溶液于试管中, 无色酚酞变
(1)
滴加无色酚酞溶液 红
(2) 取少量溶液于试管中,
有气泡产生
滴加稀盐酸
【讨论】小明同学认为,根据上述实验(1)(2)可推断,猜想②正确。而小张则认为猜
想③也可能正确,理由是
。
于是小王又设计了如下补充实验:
(1)取原溶液少量于试管中,逐滴加入BaCl 溶液至 。静置,分层。
2
(2)取上层清液,向其中加入CuSO 溶液,若有蓝色沉淀产生,则说明氢氧化钠溶液
4
部分变质,化学方程式: 。反之则说
明氢氧化钠溶液已经全部变质。
【反思】该氢氧化钠溶液变质的原因可能是(用化学方程式表示 ):
四.计算题(10分)
29.工业上侯氏制碱法得到的纯碱产品中常含有少量的氯化钠杂质,化验员要对每
批次的纯碱产品进行检验.在实验室中取27g纯碱样品,平均分成五份依次加入到
盛有100g稀盐酸的锥形瓶中(锥形瓶的质量为60g),每次充分反应
后都进行称量,得到的实验数据如下表:
学科王学科王
第一次 第二次 第三次 第四次 第五次
加入纯碱样品的质量/g 5.4 5.4 5.4 5.4 5.4
电子天平的示数/g 163.2 166.4 169.6 175 180.4
(1)第一次加入纯碱样品充分反应后,生成二氧化碳的质量是 g.
(2)计算纯碱样品中碳酸钠的质量分数是多少?(计算结果精确到0.1%)
(3)计算所用稀盐酸的质量分数是多少?九年级化学下册期末质量检测题答案
一.选择题:
1 2 3 4 5 6 7 8 9 1 1 1 1 1 1 1 1 1 1 2 2 2 2
0 1 2 3 4 5 6 7 8 9 0 1 2 3
B C A A A A C D D C B D A B D B B C A B B A A
24.(1)B 二氧化碳 E 四氧化三铁 (2)C+O2=高温=2CO 化合反应 Fe3O4+4CO=高温
=3Fe+4CO2
25.(1)25(2)在t℃时,A、B两物质的溶解度相同(3)B(4)冷却热饱和溶液
2
26.(1)Ba(OH) Cu(OH) (2)BaCl + CuSO ==BaSO ↓+ CuCl (3)NO-、Cl-
2 2 2 4 4 2 3
27.(1)3 16.60 (2) 坏血 (3)D
28. 【实验验证】 (1)溶 液 显 碱 性
(2)溶液中存在碳酸根离子(或碳酸钠) NaCO+2HCl=2NaCl+HO+CO↑
2 3 2 2
【讨 论 】 碳酸钠溶液也能使酚酞溶液变红(其他说法合理也给分)不再产生沉淀 CuSO+2NaOH=NaSO+Cu(OH)↓
4 2 4 2
【反 思 】 2NaOH+CO=NaCO+HO
2 2 3 2
29. 解:(1)根据质量守恒定律,第一次加入纯碱样品充分反应后,生成二氧化碳的质量
=100g+60g+5.4g﹣163.2g=2.2g
故答案为:2.2;
(2)第三次加入纯碱样品充分反应后与100g盐酸恰好完全反应,共生成二氧化碳的质
量=5.4g×3+100g+60g﹣169.6g=6.6g
设前三次样品中含有碳酸钠的质量为x,所用稀盐酸中溶质的质量为y.
NaCO+2HCl═2NaCl+HO+CO↑
2 3 2 2
106 73 44
x y 6.6g
x=15.9g
y=10.95g
纯碱样品中碳酸钠的质量分数= ×100%=98.1%
答:纯碱样品中碳酸钠的质量分数是98.1%.
(3)所用稀盐酸的质量分数= ×100%=10.95%
答:所用稀盐酸的质量分数是10.95%.