文档内容
专题七 热点题型
专题提升演练
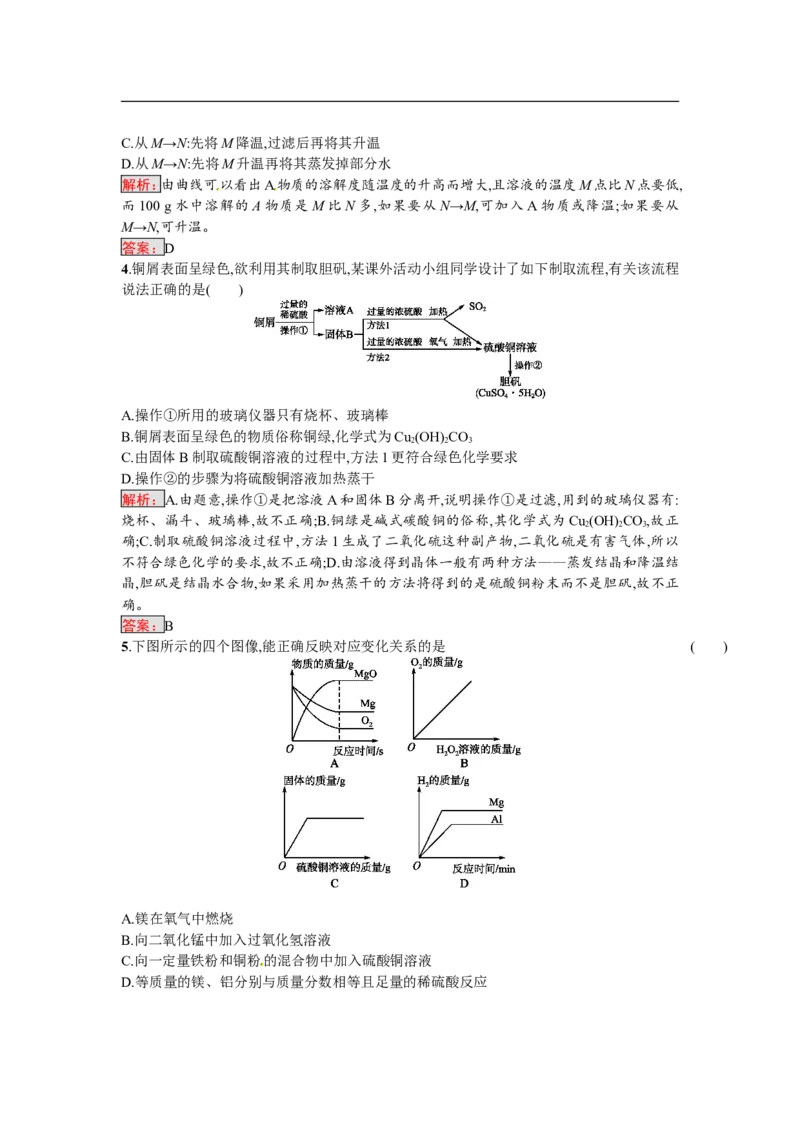
1.全球海水、陆地水储量比如图所示,下列说法错误的是 ( )
A.淡水资源是取之不尽,用之不竭的
B.地球上大部分是含盐量很高的海水
C.为减少水体污染,要合理使用农药、化肥
D.为节约用水,农业、园林浇灌可以改大水漫灌为喷灌、滴灌
解析:地球上的总水量很大,但淡水很少、分布不均,故A错误。
答案:A
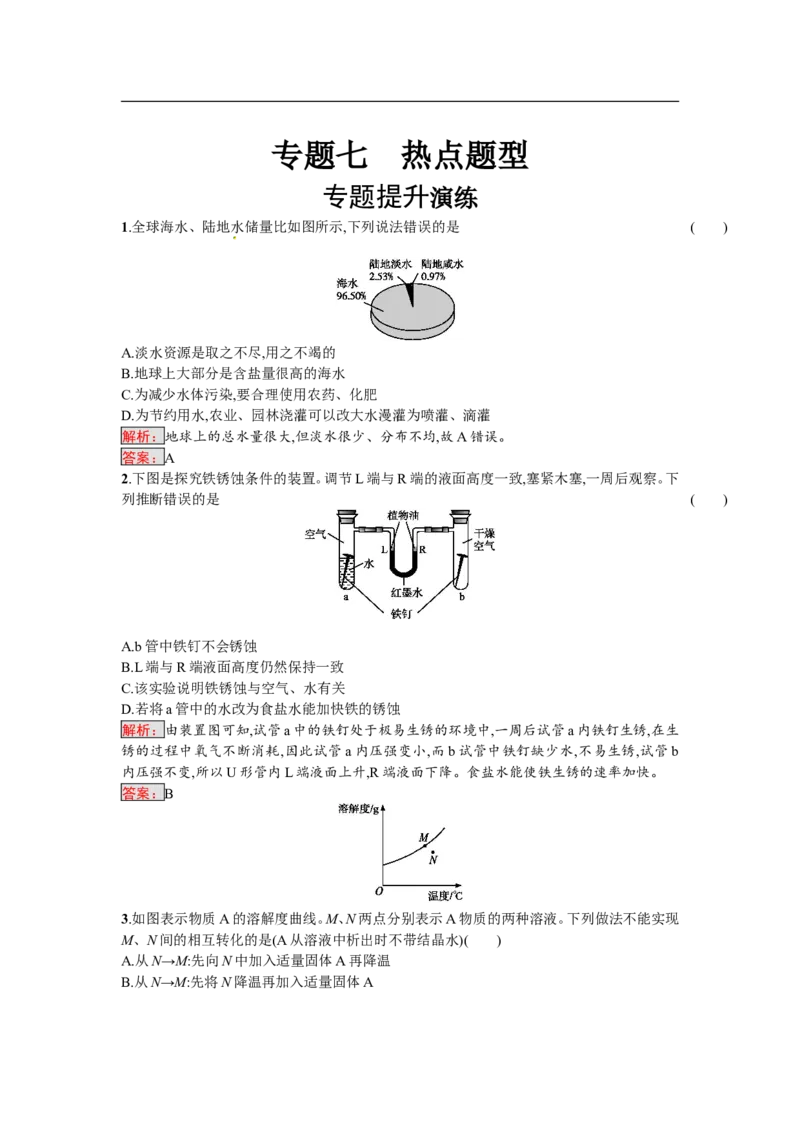
2.下图是探究铁锈蚀条件的装置。调节L端与R端的液面高度一致,塞紧木塞,一周后观察。下
列推断错误的是 ( )
A.b管中铁钉不会锈蚀
B.L端与R端液面高度仍然保持一致
C.该实验说明铁锈蚀与空气、水有关
D.若将a管中的水改为食盐水能加快铁的锈蚀
解析:由装置图可知,试管a中的铁钉处于极易生锈的环境中,一周后试管a内铁钉生锈,在生
锈的过程中氧气不断消耗,因此试管a内压强变小,而b试管中铁钉缺少水,不易生锈,试管b
内压强不变,所以U形管内L端液面上升,R端液面下降。食盐水能使铁生锈的速率加快。
答案:B
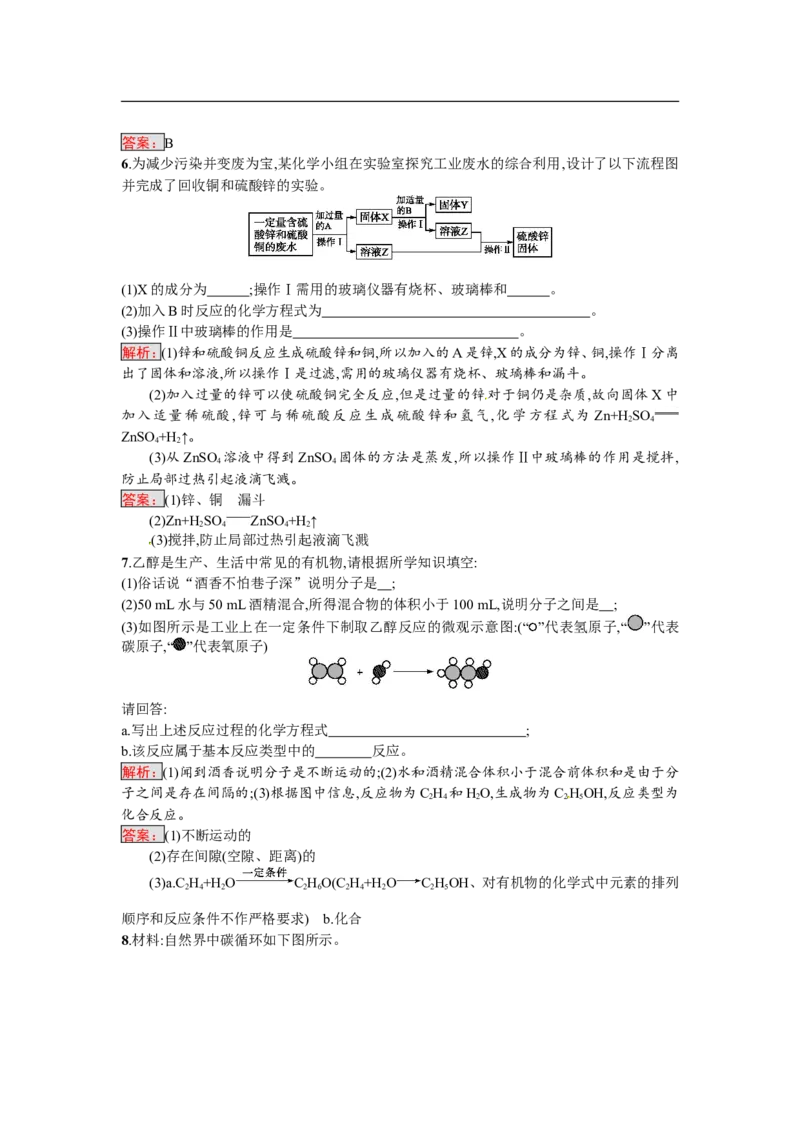
3.如图表示物质A的溶解度曲线。M、N两点分别表示A物质的两种溶液。下列做法不能实现
M、N间的相互转化的是(A从溶液中析出时不带结晶水)( )
A.从N→M:先向N中加入适量固体A再降温
B.从N→M:先将N降温再加入适量固体AC.从M→N:先将M降温,过滤后再将其升温
[来源:Zxxk.Com]
D.从M→N:先将M升温再将其蒸发掉部分水
解析:由曲线可以看出A物质的溶解度随温度的升高而增大,且溶液的温度M点比N点要低,
而100 g水中溶解的A物质是M比N多,如果要从N→M,可加入A物质或降温;如果要从
M→N,可升温。
答案:D
4.铜屑表面呈绿色,欲利用其制取胆矾,某课外活动小组同学设计了如下制取流程,有关该流程
说法正确的是( )
A.操作①所用的玻璃仪器只有烧杯、玻璃棒
B.铜屑表面呈绿色的物质俗称铜绿,化学式为Cu (OH) CO
2 2 3
C.由固体B制取硫酸铜溶液的过程中,方法1更符合绿色化学要求
D.操作②的步骤为将硫酸铜溶液加热蒸干
解析:A.由题意,操作①是把溶液A和固体B分离开,说明操作①是过滤,用到的玻璃仪器有:
烧杯、漏斗、玻璃棒,故不正确;B.铜绿是碱式碳酸铜的俗称,其化学式为Cu (OH) CO,故正
2 2 3
确;C.制取硫酸铜溶液过程中,方法1生成了二氧化硫这种副产物,二氧化硫是有害气体,所以
不符合绿色化学的要求,故不正确;D.由溶液得到晶体一般有两种方法——蒸发结晶和降温结
晶,胆矾是结晶水合物,如果采用加热蒸干的方法将得到的是硫酸铜粉末而不是胆矾,故不正
确。
答案:B
5.下图所示的四个图像,能正确反映对应变化关系的是 ( )
A.镁在氧气中燃烧
B.向二氧化锰中加入过氧化氢溶液
C.向一定量铁粉和铜粉的混合物中加入硫酸铜溶液
D.等质量的镁、铝分别与质量分数相等且足量的稀硫酸反应答案:B
6.为减少污染并变废为宝,某化学小组在实验室探究工业废水的综合利用,设计了以下流程图
并完成了回收铜和硫酸锌的实验。
(1)X的成分为 ;操作Ⅰ需用的玻璃仪器有烧杯、玻璃棒和 。
(2)加入B时反应的化学方程式为 。
(3)操作Ⅱ中玻璃棒的作用是 。
解析:(1)锌和硫酸铜反应生成硫酸锌和铜,所以加入的A是锌,X的成分为锌、铜,操作Ⅰ分离
出了固体和溶液,所以操作Ⅰ是过滤,需用的玻璃仪器有烧杯、玻璃棒和漏斗。
(2)加入过量的锌可以使硫酸铜完全反应,但是过量的锌对于铜仍是杂质,故向固体X中
加入适量稀硫酸,锌可与稀硫酸反应生成硫酸锌和氢气,化学方程式为 Zn+H SO
2 4
ZnSO+H ↑。
4 2
(3)从ZnSO 溶液中得到ZnSO 固体的方法是蒸发,所以操作Ⅱ中玻璃棒的作用是搅拌,
4 4
防止局部过热引起液滴飞溅。
答案:(1)锌、铜 漏斗
(2)Zn+H SO ZnSO+H ↑
2 4 4 2
(3)搅拌,防止局部过热引起液滴飞溅
7.乙醇是生产、生活中常见的有机物,请根据所学知识填空:
(1)俗话说“酒香不怕巷子深”说明分子是 ;
(2)50 mL水与50 mL酒精混合,所得混合物的体积小于100 mL,说明分子之间是 ;
(3)如图所示是工业上在一定条件下制取乙醇反应的微观示意图:(“ ”代表氢原子,“ ”代表
碳原子,“ ”代表氧原子)
请回答:
a.写出上述反应过程的化学方程式 ;
b.该反应属于基本反应类型中的 反应。
解析:(1)闻到酒香说明分子是不断运动的;(2)水和酒精混合体积小于混合前体积和是由于分
子之间是存在间隔的;(3)根据图中信息,反应物为C H 和HO,生成物为C HOH,反应类型为
2 4 2 2 5
化合反应。
答案:(1)不断运动的
(2)存在间隙(空隙、距离)的
(3)a.C H+H O C HO(C H+H O C HOH、对有机物的化学式中元素的排列
2 4 2 2 6 2 4 2 2 5
顺序和反应条件不作严格要求) b.化合
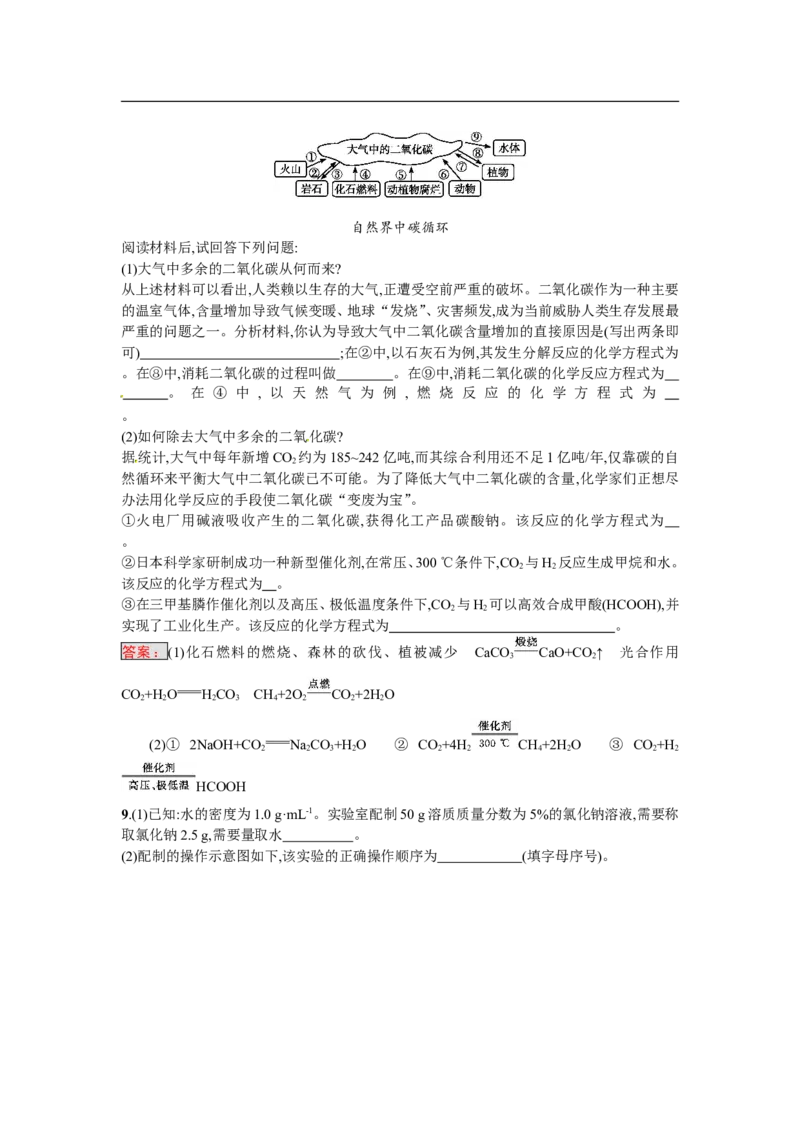
8.材料:自然界中碳循环如下图所示。自然界中碳循环
阅读材料后,试回答下列问题:
(1)大气中多余的二氧化碳从何而来?
从上述材料可以看出,人类赖以生存的大气,正遭受空前严重的破坏。二氧化碳作为一种主要
的温室气体,含量增加导致气候变暖、地球“发烧”、灾害频发,成为当前威胁人类生存发展最
严重的问题之一。分析材料,你认为导致大气中二氧化碳含量增加的直接原因是(写出两条即
可) ;在②中,以石灰石为例,其发生分解反应的化学方程式为
。在⑧中,消耗二氧化碳的过程叫做 。在⑨中,消耗二氧化碳的化学反应方程式为
。 在 ④ 中 , 以 天 然 气 为 例 , 燃 烧 反 应 的 化 学 方 程 式 为
。
(2)如何除去大气中多余的二氧化碳?
据统计,大气中每年新增CO 约为185~242亿吨,而其综合利用还不足1亿吨/年,仅靠碳的自
2
然循环来平衡大气中二氧化碳已不可能。为了降低大气中二氧化碳的含量,化学家们正想尽
办法用化学反应的手段使二氧化碳“变废为宝”。
①火电厂用碱液吸收产生的二氧化碳,获得化工产品碳酸钠。该反应的化学方程式为
。
②日本科学家研制成功一种新型催化剂,在常压、300 ℃条件下,CO 与H 反应生成甲烷和水。
2 2
该反应的化学方程式为 。
③在三甲基膦作催化剂以及高压、极低温度条件下,CO 与H 可以高效合成甲酸(HCOOH),并
2 2
实现了工业化生产。该反应的化学方程式为 。
答案:(1)化石燃料的燃烧、森林的砍伐、植被减少 CaCO CaO+CO ↑ 光合作用
3 2
CO+H O HCO CH+2O CO+2H O
2 2 2 3 4 2 2 2
(2)① 2NaOH+CO NaCO+H O ② CO+4H CH+2H O ③ CO+H
2 2 3 2 2 2 4 2 2 2
HCOOH
9.(1)已知:水的密度为1.0 g·mL-1。实验室配制50 g溶质质量分数为5%的氯化钠溶液,需要称
取氯化钠2.5 g,需要量取水 。
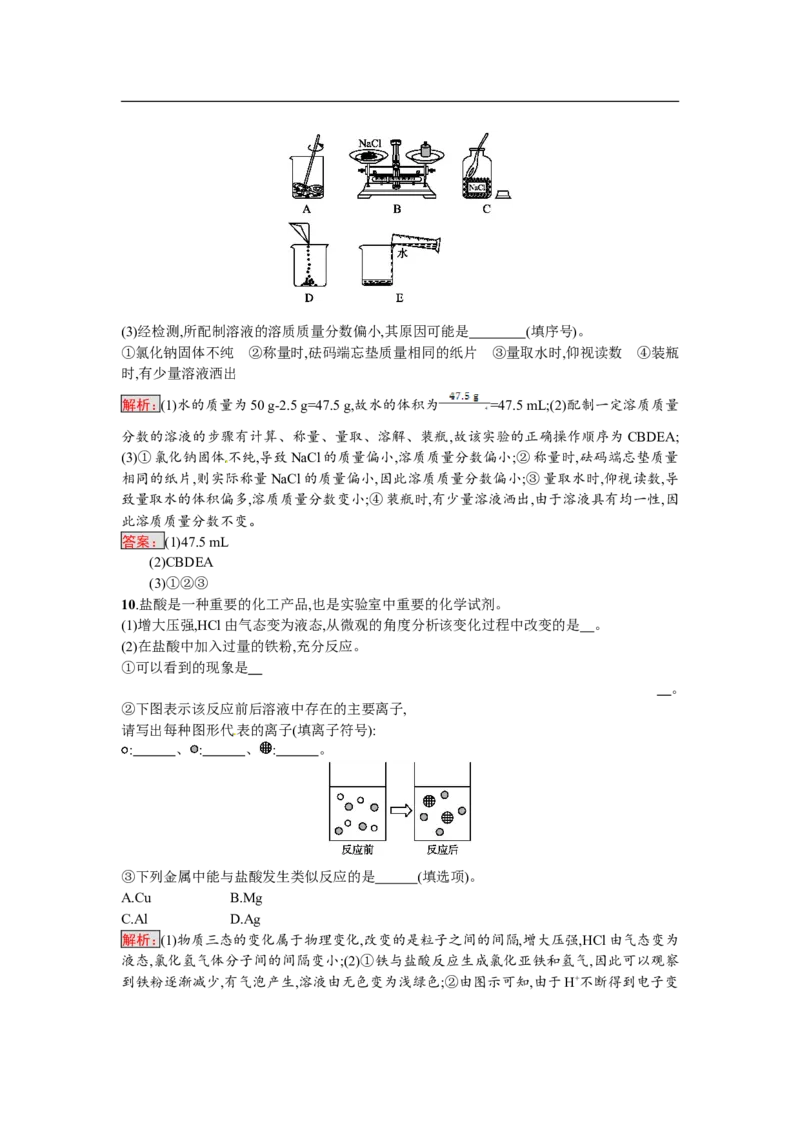
(2)配制的操作示意图如下,该实验的正确操作顺序为 (填字母序号)。(3)经检测,所配制溶液的溶质质量分数偏小,其原因可能是 (填序号)。
①氯化钠固体不纯 ②称量时,砝码端忘垫质量相同的纸片 ③量取水时,仰视读数 ④装瓶
时,有少量溶液洒出
解析:(1)水的质量为50 g-2.5 g=47.5 g,故水的体积为 =47.5 mL;(2)配制一定溶质质量
分数的溶液的步骤有计算、称量、量取、溶解、装瓶,故该实验的正确操作顺序为CBDEA;
(3)①氯化钠固体不纯,导致NaCl的质量偏小,溶质质量分数偏小;②称量时,砝码端忘垫质量
相同的纸片,则实际称量NaCl的质量偏小,因此溶质质量分数偏小;③量取水时,仰视读数,导
致量取水的体积偏多,溶质质量分数变小;④装瓶时,有少量溶液洒出,由于溶液具有均一性,因
此溶质质量分数不变。
答案:(1)47.5 mL
(2)CBDEA
(3)①②③
10.盐酸是一种重要的化工产品,也是实验室中重要的化学试剂。
[来源:学科网ZXXK]
(1)增大压强,HCl由气态变为液态,从微观的角度分析该变化过程中改变的是 。
(2)在盐酸中加入过量的铁粉,充分反应。
①可以看到的现象是
。
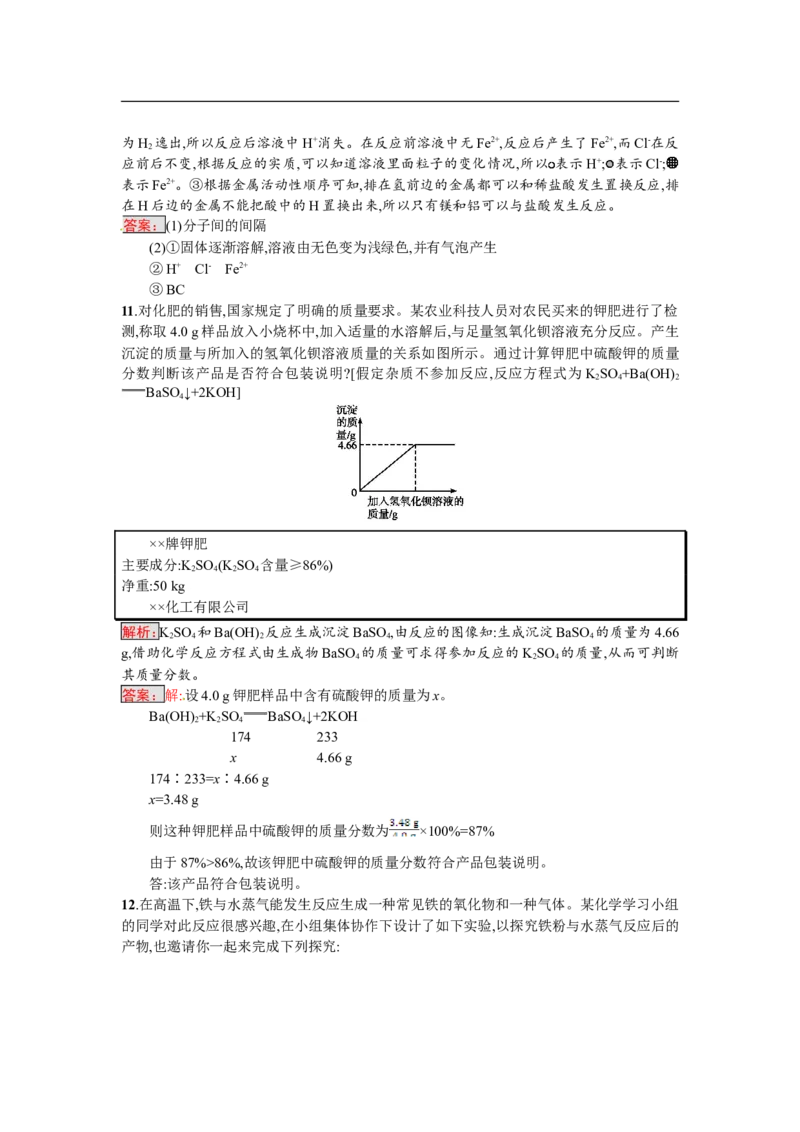
②下图表示该反应前后溶液中存在的主要离子,
请写出每种图形代表的离子(填离子符号):
: 、 : 、 : 。
③下列金属中能与盐酸发生类似反应的是 (填选项)。
A.Cu B.Mg
C.Al D.Ag
解析:(1)物质三态的变化属于物理变化,改变的是粒子之间的间隔,增大压强,HCl由气态变为
液态,氯化氢气体分子间的间隔变小;(2)①铁与盐酸反应生成氯化亚铁和氢气,因此可以观察
到铁粉逐渐减少,有气泡产生,溶液由无色变为浅绿色;②由图示可知,由于H+不断得到电子变为H 逸出,所以反应后溶液中H+消失。在反应前溶液中无Fe2+,反应后产生了Fe2+,而Cl-在反
2
应前后不变,根据反应的实质,可以知道溶液里面粒子的变化情况,所以 表示H+; 表示Cl-;
表示Fe2+。③根据金属活动性顺序可知,排在氢前边的金属都可以和稀盐酸发生置换反应,排
在H后边的金属不能把酸中的H置换出来,所以只有镁和铝可以与盐酸发生反应。
答案:(1)分子间的间隔
(2)①固体逐渐溶解,溶液由无色变为浅绿色,并有气泡产生
②H+ Cl- Fe2+
③BC
11.对化肥的销售,国家规定了明确的质量要求。某农业科技人员对农民买来的钾肥进行了检
测,称取4.0 g样品放入小烧杯中,加入适量的水溶解后,与足量氢氧化钡溶液充分反应。产生
沉淀的质量与所加入的氢氧化钡溶液质量的关系如图所示。通过计算钾肥中硫酸钾的质量
分数判断该产品是否符合包装说明?[假定杂质不参加反应,反应方程式为KSO +Ba(OH)
2 4 2
BaSO↓+2KOH]
4
××牌钾肥
主要成分:K SO (K SO 含量≥86%)
2 4 2 4
净重:50 kg
[来源:Z+xx+k.Com]
××化工有限公司
解析:KSO 和Ba(OH) 反应生成沉淀BaSO,由反应的图像知:生成沉淀BaSO 的质量为4.66
2 4 2 4 4
g,借助化学反应方程式由生成物BaSO 的质量可求得参加反应的KSO 的质量,从而可判断
4 2 4
其质量分数。
答案:解:设4.0 g钾肥样品中含有硫酸钾的质量为x。
Ba(OH) +K SO BaSO↓+2KOH
2 2 4 4 [来源:Z_xx_k.Com]
174 233
x 4.66 g
174∶233=x∶4.66 g
x=3.48 g
则这种钾肥样品中硫酸钾的质量分数为 ×100%=87%
由于87%>86%,故该钾肥中硫酸钾的质量分数符合产品包装说明。
答:该产品符合包装说明。
12.在高温下,铁与水蒸气能发生反应生成一种常见铁的氧化物和一种气体。某化学学习小组
的同学对此反应很感兴趣,在小组集体协作下设计了如下实验,以探究铁粉与水蒸气反应后的
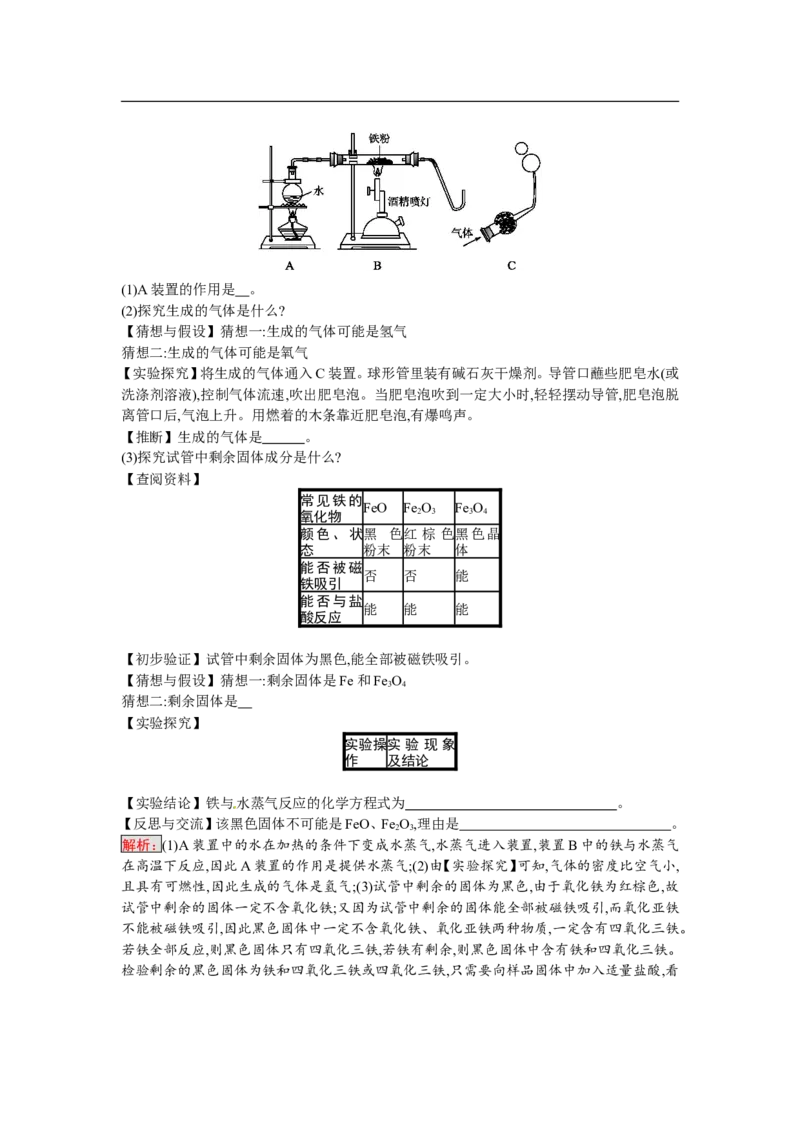
产物,也邀请你一起来完成下列探究:(1)A装置的作用是 。
(2)探究生成的气体是什么?
【猜想与假设】猜想一:生成的气体可能是氢气
猜想二:生成的气体可能是氧气
【实验探究】将生成的气体通入C装置。球形管里装有碱石灰干燥剂。导管口蘸些肥皂水(或
洗涤剂溶液),控制气体流速,吹出肥皂泡。当肥皂泡吹到一定大小时,轻轻摆动导管,肥皂泡脱
离管口后,气泡上升。用燃着的木条靠近肥皂泡,有爆鸣声。
【推断】生成的气体是 。
(3)探究试管中剩余固体成分是什么?
【查阅资料】
常见铁的
FeO Fe O Fe O
氧化物 2 3 3 4
颜色、状黑 色红 棕 色黑色晶
态 粉末 粉末 体
能否被磁
否 否 能
铁吸引
能否与盐
能 能 能
酸反应
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引。
【猜想与假设】猜想一:剩余固体是Fe和Fe O
3 4
猜想二:剩余固体是
【实验探究】
实验操实 验 现 象
作 及结论
【实验结论】铁与水蒸气反应的化学方程式为 。
【反思与交流】该黑色固体不可能是FeO、Fe O,理由是 。
2 3
解析:(1)A装置中的水在加热的条件下变成水蒸气,水蒸气进入装置,装置B中的铁与水蒸气
在高温下反应,因此A装置的作用是提供水蒸气;(2)由【实验探究】可知,气体的密度比空气小,
且具有可燃性,因此生成的气体是氢气;(3)试管中剩余的固体为黑色,由于氧化铁为红棕色,故
试管中剩余的固体一定不含氧化铁;又因为试管中剩余的固体能全部被磁铁吸引,而氧化亚铁
不能被磁铁吸引,因此黑色固体中一定不含氧化铁、氧化亚铁两种物质,一定含有四氧化三铁。
若铁全部反应,则黑色固体只有四氧化三铁,若铁有剩余,则黑色固体中含有铁和四氧化三铁。
检验剩余的黑色固体为铁和四氧化三铁或四氧化三铁,只需要向样品固体中加入适量盐酸,看是否有气泡产生进行判断即可得出结论。由上述推断可知,在高温下,铁与水蒸气反应生成氢
气和四氧化三铁。
答案:(1)提供水蒸气
(2)H
2
(3)Fe O
3 4
实验操作 实验现象及结论
取少量黑色固体于试管中,加 若固体全部溶解,没有气泡冒出,剩余固体是Fe O 。若固
3 4
入足量的稀盐酸(合理答案即 体全部溶解,有气泡冒出,剩余固体是Fe和Fe O(合理答
3 4
可) 案即可)
[来源:Zxxk.Com]
3Fe+4H O(g) Fe O+4H
2 3 4 2
Fe O 是红棕色粉末,FeO不能被磁铁吸引(合理答案即可)
2 3