文档内容
2018 年中考化学一轮复习·《溶质质量分数》真题练习
一、选择题
1.(2017山东省聊城市)下列关于溶液说法正确的是( D )
A.将氯化钠和植物油放入水中,充分搅拌后都能形成溶液
B.把20%的蔗糖溶液均分成两份,每份溶液的溶质质量分数为10%
C.向20℃时的蔗糖饱和溶液中加入食盐,食盐不再溶解
D.配制50g16%的氯化钠溶液一般经过计算、称量(或量取)、溶解、装瓶存放
等步骤
2.(2017河池)一杯70℃的硝酸钾饱和溶液,冷却后有晶体析出(晶体不含结晶
水),若不考虑溶剂的蒸发,则剩余溶液与原溶液相比( A )
A.溶质的质量分数减小 B.溶质质量不变
C.溶液质量不变 D.由饱和溶液变为不饱和溶液
3.(2017辽阳)实验室配制50g溶质质量分数为6%的氯化钠溶液,下列做法正确
的是( B )
A.用托盘天平称取5g氯化钠
B.用50ml量筒量取所需水的体积
C.溶解氯化钠时,使用的玻璃仪器有量筒、玻璃棒
D.将配制好的溶液装入广口瓶中,塞好瓶塞并贴上标签
4.(2017荆州)实验室配制100g 10%的NaCl溶液,不需要用到的仪器是( A)
A.酒精灯 B.托盘天平 C.胶头滴管 D.烧杯
5.(2017日照)在实验室中,配制质量分数为10%的NaOH溶液,用于制作“叶
脉书签”,下列说法正确的是( B )
A.将NaOH固体直接放在托盘上称量
B.NaOH有强烈的腐蚀性,实验时最好戴防护眼镜
C.溶解时玻璃棒的作用是搅拌,增大NaOH的溶解度
D.若在量取水时俯视凹液面的最低处,则配制溶液的质量分数小于10%
6.(2017辽宁省沈阳市) 按下列方法配制的溶液,其溶质质量分数为5%的是(
A )
A.称取5.0g氯化钾,溶解在95mL水中,充分搅拌
1B.称取5.0g生石灰,放入95mL水中,充分搅拌
C. 量取5.OmL浓盐酸,倒入95mL水中,充分搅拌
D.称取5.0g二氧化锰,放入95mL水中,充分搅拌
7.(2017年湖南省株州市)除质量分数以外,人们有时也用体积分数来表示溶液
的浓度。例如,52%的饮用白酒就是100体积的饮用白酒中含有52体积的乙醇。
下列溶液的浓度属于用体积分数来表示的是( D )
A. 0.9%的生理盐水 B.5%的葡萄水注射液
C.10%的氢氧化钠溶液 D.75%的医用酒精
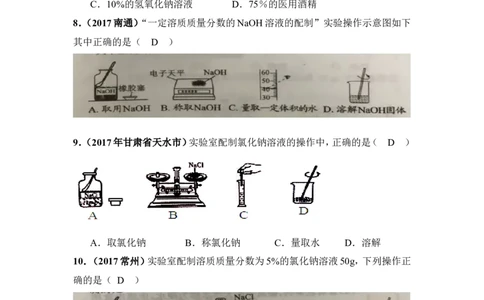
8.(2017南通)“一定溶质质量分数的NaOH溶液的配制”实验操作示意图如下
其中正确的是( D )
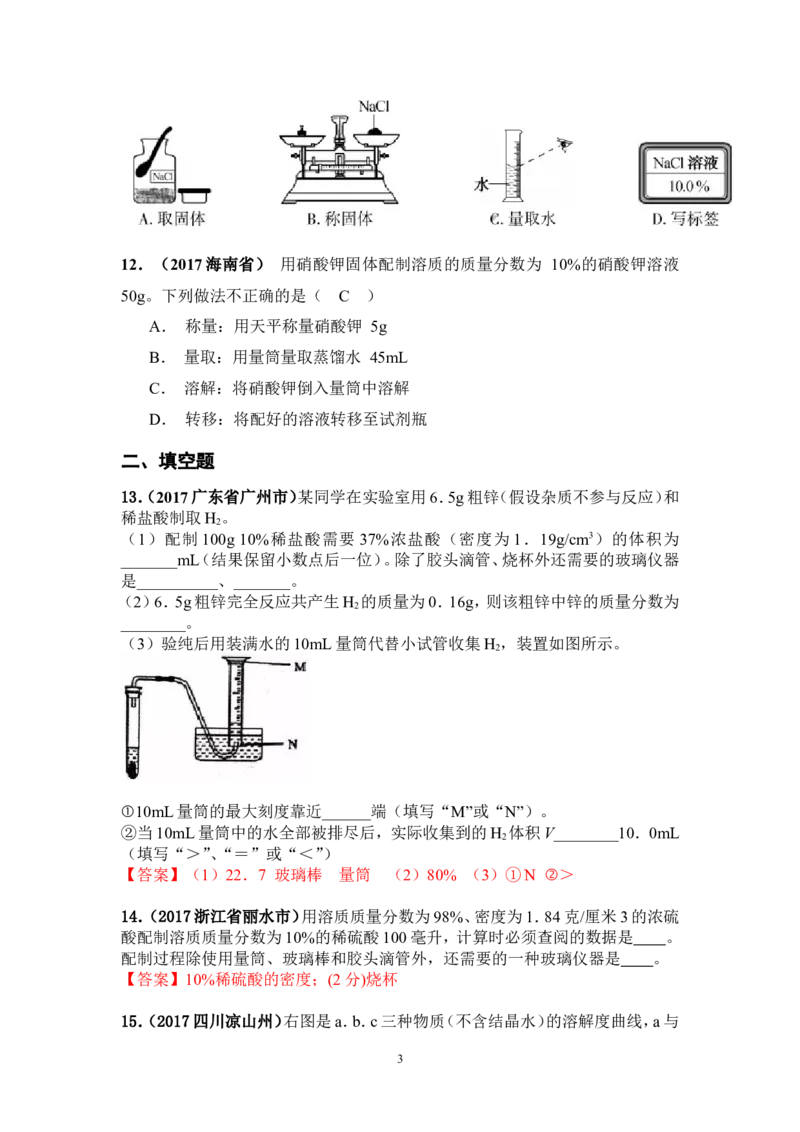
9.(2017年甘肃省天水市)实验室配制氯化钠溶液的操作中,正确的是( D )
A.取氯化钠 B.称氯化钠 C.量取水 D.溶解
10.(2017常州)实验室配制溶质质量分数为5%的氯化钠溶液50g,下列操作正
确的是( D )
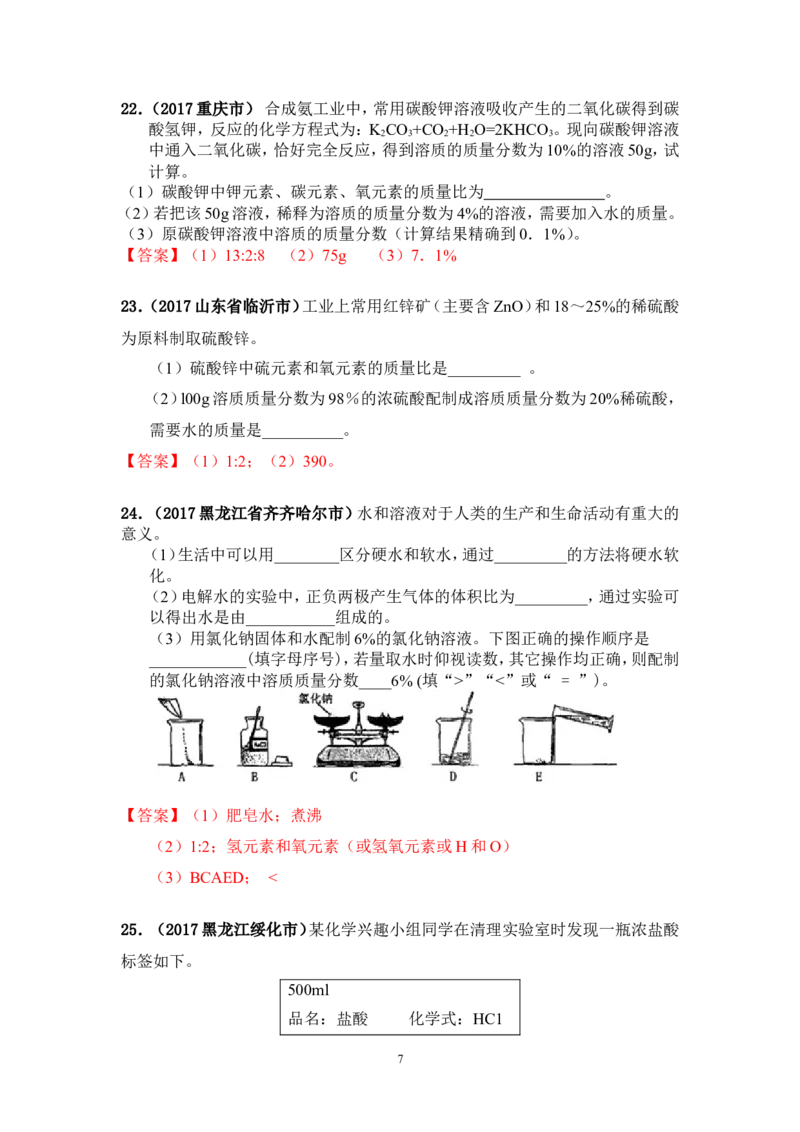
11.(2017福建省) 欲配制10.0%的氯化钠溶液50g,部分操作如下图所示正确
的是( D )
212.(2017海南省) 用硝酸钾固体配制溶质的质量分数为 10%的硝酸钾溶液
50g。下列做法不正确的是( C )
A. 称量:用天平称量硝酸钾 5g
B. 量取:用量筒量取蒸馏水 45mL
C. 溶解:将硝酸钾倒入量筒中溶解
D. 转移:将配好的溶液转移至试剂瓶
二、填空题
13.(2017广东省广州市)某同学在实验室用6.5g粗锌(假设杂质不参与反应)和
稀盐酸制取H 。
2
(1)配制 100g 10%稀盐酸需要 37%浓盐酸(密度为 1.19g/cm3)的体积为
_______mL(结果保留小数点后一位)。除了胶头滴管、烧杯外还需要的玻璃仪器
是__________、_______。
(2)6.5g粗锌完全反应共产生H 的质量为0.16g,则该粗锌中锌的质量分数为
2
________。
(3)验纯后用装满水的10mL量筒代替小试管收集H ,装置如图所示。
2
①10mL量筒的最大刻度靠近______端(填写“M”或“N”)。
②当10mL量筒中的水全部被排尽后,实际收集到的H 体积V________10.0mL
2
(填写“>”、“=”或“<”)
【答案】(1)22.7 玻璃棒 量筒 (2)80% (3)①N ②>
14.(2017浙江省丽水市)用溶质质量分数为98%、密度为1.84克/厘米3的浓硫
酸配制溶质质量分数为10%的稀硫酸100毫升,计算时必须查阅的数据是 。
配制过程除使用量筒、玻璃棒和胶头滴管外,还需要的一种玻璃仪器是 。
【答案】10%稀硫酸的密度;(2分)烧杯
15.(2017四川凉山州)右图是a.b.c三种物质(不含结晶水)的溶解度曲线,a与
3c的溶解度曲线交于p点,请据图回答:
(1)p点的含义是 ;
(2)将t1℃ 时a.b.c三种物质的饱和溶液温度升高到t2℃时,
三种溶液的溶质质量分数大小关系是 (填选项符号)
A. c=a>b B. a=b>c C. a>b>c D. b>a>c
【答案】 (1) t1℃ ,a c两种物质的溶解度相等。 (2)D
16.(2017浙江省台州市)硫酸铵【化学式为(NH )SO 】是一种能促进植物茎、叶
4 2 4
生长的氮肥。
(1)硫酸铵中氮元素的化合价为_______。
(2)施肥浓度过高,会造成烧苗现象。小柯通过实验发现,质量分数为2%的硫酸
铵溶液不会导致植物烧苗。他用50克30%的硫酸铵溶液配制2%的硫酸铵溶液,
需要加水_______毫升
【答案】(1)—3(2)700
17.(2017广东省 ) “题17图”是实验室配制一定溶质质量分数的NaCl溶液的
流程图。
请回答
(1) 应称量 gNaCl,需加水 mL。
(2)若称量NaCl固体时指针向右偏转 ,则应 直到
天平平衡。
(3)取上述溶液10g加水稀释到 g,可得到5%的NaCl溶液。
【答案】(1)7.5 42.5 (2)往左盘中继续添加氯化钠固体 (3)30
418.(2017浙江省嘉兴市)实验室有一瓶由氯化钾和硝酸钾组成的化肥,但标注的
质量分数己模糊不清,小明想通过实验重新标注,以下是他进行的实验步骤:
①取10克样品于烧杯中,加入蒸馏水充分溶解,配制成60克溶液;
②在配制的溶液中,加入一定量的硝酸银溶液,恰好完全反应;
⑧将上述混合液过滤,沉淀经洗涤、干燥后,称得质量为14.35克。
请根据上述实验回答:(相关反应的化学方程式为:
KCl+AgNO =AgCl↓+KNO )
3 3
(1)在过滤操作中使用的玻璃仪器有:烧杯、______和玻璃棒。
(2)样品中氯化钾的质量分数为多少?(要求列式计算)
(3)完全反应后,混合液中的硝酸钾质量是多少克?
(4)为了回收硝酸钾,小明对滤液进行蒸发、结晶、称量,发现所得的晶体质量
小于计算得出的理论值。造成这种结果的原因可能是 ______。 (选填编号)
A.晶体没有干燥 B.蒸发时液体飞溅 C.硝酸钾残留在玻璃棒上
【答案】(1)漏斗;(2)74.5%;(3)12.65g;(4)BC。
19.(2017长春市)配制50g质量分数6%的氯化钠溶液,结合实验回答下列问题。
(1)用托盘天平称量 g氯化钠固体;
(2)溶解时需要用到的仪器是 和玻璃棒;
(3)下列操作中,会引起溶质的质量分数偏差的是 。
A.称量读数时天平指针偏左 B.量取水时仰视读数 C.装瓶时洒出少量溶液
【答案】(1)3;(1分)(2)烧杯;(1分)(3)AB。(1分)
20.(2017·雅安)化学与我们的生活息息相关.
(1)包饺子的食材有面粉、韭菜、瘦肉、植物油、食盐等.其中富含糖类的是
不属于有机物的是 .
(2)老年人缺 会发生骨质疏松,容易骨折.
(3)塑料盆、铁锅,陶瓷茶杯等是生活常见用品,其中属于有机合成材料的是
.
(4)活性炭能除去家庭装修中产生的有害气体,这是利用了活性炭的 性.
(5)加了洗涤剂的水能除去衣服上的油污,是利用了洗涤剂的 作用.
(6)下列关于水的说法错误的是
A.煮沸可以将硬水转化为软水
5B.工业废气直接排放会造成水污染
C.寻找合适的催化剂,利用光照使水分解是理想的制氢方法
D.大量使用农药、化肥能提高农作物产量,不会造成水污染
(7)过氧化钙( CaO ) 能用于鱼类运输时的制氧剂,与水反应生成碱和一种气体
2
写出反应的化学方程式 .
(8)某注射用药液的配制方法如下:
①把 1.0g 药品溶于水配制成 4.0mL 溶液 a;
②取 0.1mL 溶液 a,加水稀释至 1.0mL,得溶液 b;
③取 0.1mL 溶液 b,加水稀释至 1.0mL,得溶液 c;
④取 0.4mL 溶液 c,加水稀释至 1.0mL,得溶液 d.
由于在整个配制过程中药液很稀,其密度都可近似看做1g/cm3,1g 该药品可配制
溶液d 的体积是 mL.
【答案】(1)面粉;食盐;(2)钙/Ca;(3)塑料盆;(4)吸附;(5)乳化;(6)D;(7)
2CaO +2H O=2Ca(OH) +O ↑;(8)1000.
2 2 2 2
21.(2017锦州)下列是配制一定溶质质量分数的氯化钠溶液的实验图示。请回答
下列问题:
A.称量 B.量取 C.倾倒
D.溶解
(1)在量取水的操作中,当水面接近所需刻度时,应使用___________添加水。
(2)指出图A中的错误操作___________。
(3)将图A中错误操作改正后,用托盘天平称量所需的氯化钠时,发现托盘天平
的指针偏向左盘, 接下来的操作应是___________。
(4)在其他操作无错误的前提下,量取所需要的水时,按图 B进行操作,一定能
导致所配制溶液的溶质质量分数___________(填“偏大”、“不变”或“偏
小”)。
答案:(1)胶头滴管 (2)砝码和物品位置颠倒(3)减少药品 (4)偏小
622.(2017重庆市) 合成氨工业中,常用碳酸钾溶液吸收产生的二氧化碳得到碳
酸氢钾,反应的化学方程式为:K CO +CO +H O=2KHCO 。现向碳酸钾溶液
2 3 2 2 3
中通入二氧化碳,恰好完全反应,得到溶质的质量分数为10%的溶液50g,试
计算。
(1)碳酸钾中钾元素、碳元素、氧元素的质量比为 。
(2)若把该50g溶液,稀释为溶质的质量分数为4%的溶液,需要加入水的质量。
(3)原碳酸钾溶液中溶质的质量分数(计算结果精确到0.1%)。
【答案】(1)13:2:8 (2)75g (3)7.1%
23.(2017山东省临沂市)工业上常用红锌矿(主要含ZnO)和18~25%的稀硫酸
为原料制取硫酸锌。
(1)硫酸锌中硫元素和氧元素的质量比是_________ 。
(2)l00g溶质质量分数为98%的浓硫酸配制成溶质质量分数为20%稀硫酸,
需要水的质量是__________。
【答案】(1)1:2;(2)390。
24.(2017黑龙江省齐齐哈尔市)水和溶液对于人类的生产和生命活动有重大的
意义。
(1)生活中可以用________区分硬水和软水,通过_________的方法将硬水软
化。
(2)电解水的实验中,正负两极产生气体的体积比为_________,通过实验可
以得出水是由___________组成的。
(3)用氯化钠固体和水配制6%的氯化钠溶液。下图正确的操作顺序是
____________(填字母序号),若量取水时仰视读数,其它操作均正确,则配制
的氯化钠溶液中溶质质量分数____6% (填“>”“<”或“ = ”)。
【答案】(1)肥皂水;煮沸
(2)1:2;氢元素和氧元素(或氢氧元素或H和O)
(3)BCAED; <
25. (2017黑龙江绥化市)某化学兴趣小组同学在清理实验室时发现一瓶浓盐酸
标签如下。
500ml
品名:盐酸 化学式:HC1
7相对分子质量:36.5 密度:1.
19g/ml
溶质质量分数:38%
根据标签计算。
(1) HCl中氢元素和氧元素的质量比为 (结果用最简整数比表示)。
(2)这瓶盐酸溶液的质量为 g。
(3)现要配制3800g溶质质量分数为10%的稀盐酸,需要溶质质量分数为38%
的浓盐酸的质量为 g,需要这种浓盐酸 瓶。
【答案】(1)2:71;(2)595;(3)1000;2。
三、计算题
26.(2017四川省德阳市)某校化学课外活动小组的同学在实验室的一次探究活
动中,他们将50g氢氧化钠溶液与50g硫酸铜溶液混合恰好完全反应,得到9.8g
沉淀。请你计算氢氧化钠溶液中溶质的质量分数。
【解】设反应的氢氧化钠质量为xg,
则CuSO +2NaOH═Cu(OH) ↓+Na SO
4 2 2 4
80 98
x 9.8g
解得x=8g,
氢氧化钠溶液中溶质的质量分数为
答:氢氧化钠溶液中溶质的质量分数为16%。
27.(2017青海省西宁市) 某兴趣小组用73g溶质质量分数为20%的盐酸与足量
锌粒反应,可制得氢气的质量是多少?
【解】设可制的氢气质量为x。
Zn + 2HCl=ZnCl +H ↑
2 2
73 2
73g*20% x
73/73g×0.2=2/x
x=0.4g
答:可制得氢气质量为0.4g.
8