文档内容
第6讲 溶液的浓度
1.认识溶质质量分数的含义,能配制一定溶质的质量分数的溶液。
考试说明 2.能进行溶质质量分数的简单计算。
3.完成基础的学生实验:一定溶质质量分数的氯化钠溶液的配制。
考点1 溶质的质量分数
1.溶质质量分数的概念:______与______之比。
2.溶质质量分数=______/______×100%。
3.饱和溶液中溶质的质量分数=[溶解度/(100g+溶解度)×100%]。
考点2 有关溶液的计算
1.溶液稀释的计算
(1)稀释前溶液的质量×稀释前溶液的溶质质量分数=稀释后溶液的质量×稀释后溶液的溶质质量分数;
(2)溶液稀释前后,______质量不变。
2.其他计算
(1)溶液的质量=溶质的质量+溶剂的质量=溶质的质量÷溶质的质量分数;
(2)溶质的质量=溶液的质量×溶质的质量分数;
(3)溶剂的质量=溶液的质量-溶质的质量。
命题点1 溶质的质量分数
(2014·黔东南)下列有关溶液的说法中正确的是( )
A.常温下将100 mL饱和Ca(OH) 溶液加热到50 ℃,会使溶液由饱和溶液变为不饱和溶液
2
B.从浓度为25%的HSO 溶液中取出10 mL,则取出的10 mLHSO 溶液浓度仍为25%
2 4 2 4
C.20 ℃时,50克水中溶解了18克NaCl,则20 ℃时NaCl的溶解度为36克
D.将95克KCl溶液蒸干得到5克固体,则原溶液中KCl的浓度为5%
思路点拨:Ca(OH) 溶解度随温度升高而减小,将常温下饱和Ca(OH) 溶液升温会析出Ca(OH) ,溶液变为50 ℃
2 2 2
时的饱和溶液。溶液具有均一性,从原溶液中取出的部分溶液浓度不变。20 ℃时,50克水中溶解了18克NaCl,但不
知溶液是否饱和,无法确定20 ℃时的溶解度。将95克KCl溶液蒸干得到5克固体,则原溶液中KCl的浓度为(5 g/95
g)×100%>5%。
1.(2013·遵义)物质M在不同温度下的溶解度数据如下表所示,以下说法正确的是( )
温度/℃ 0 20 40 60 80
溶解度/g 12.6 15.3 20.0 25.0 38.2
A.0 ℃时,15.9 gM溶于150 g水中形成饱和溶液
B.20 ℃时,M形成饱和溶液的溶质质量分数是15.3%
C.若要配制200.0 g 20.0%的M的饱和溶液,对应温度必须是60 ℃
D.80 ℃时,M的饱和溶液138.2 g降温至40 ℃,析出晶体的质量大于20.0 g
命题点2 有关溶液与化学方程式的综合计算
(2014·黔西南)将氯化钠和碳酸钠的混合物33.8 g放入125 g稀盐酸中,恰好完全反应,得氯化钠溶液
150 g。计算:
(1)反应后生成CO 的质量是________g。
2
(2)反应后所得溶液中溶质质量分数为多少?(要求有计算过程)
思路点拨:根据质量守恒定律计算生成二氧化碳的质量。由二氧化碳的质量根据化学方程式计算参加反应的碳
酸钠的质量和生成氯化钠的质量,进而可确定原混合物中氯化钠的质量,所得溶液中氯化钠的质量,计算所得溶液氯
化钠的质量分数。2.(2015·遵义)为测定某稀硫酸的溶质质量分数,在10 g稀硫酸中滴入过量的氯化钡溶液,得到沉淀2.33 g,求该
稀硫酸的溶质质量分数。
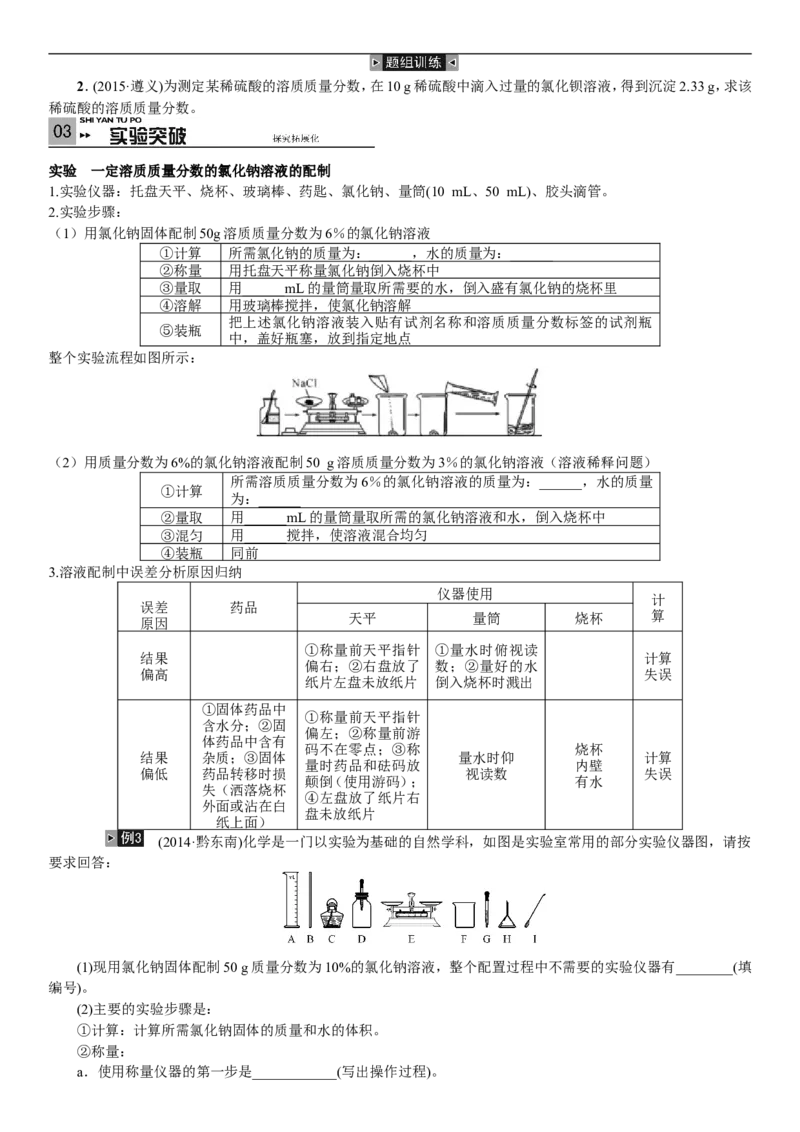
实验 一定溶质质量分数的氯化钠溶液的配制
1.实验仪器:托盘天平、烧杯、玻璃棒、药匙、氯化钠、量筒(10 mL、50 mL)、胶头滴管。
2.实验步骤:
(1)用氯化钠固体配制50g溶质质量分数为6%的氯化钠溶液
①计算 所需氯化钠的质量为:______,水的质量为:______
②称量 用托盘天平称量氯化钠倒入烧杯中
③量取 用______mL的量筒量取所需要的水,倒入盛有氯化钠的烧杯里
④溶解 用玻璃棒搅拌,使氯化钠溶解
把上述氯化钠溶液装入贴有试剂名称和溶质质量分数标签的试剂瓶
⑤装瓶
中,盖好瓶塞,放到指定地点
整个实验流程如图所示:
(2)用质量分数为6%的氯化钠溶液配制50 g溶质质量分数为3%的氯化钠溶液(溶液稀释问题)
所需溶质质量分数为6%的氯化钠溶液的质量为:______,水的质量
①计算
为:______
②量取 用______mL的量筒量取所需的氯化钠溶液和水,倒入烧杯中
③混匀 用______搅拌,使溶液混合均匀
④装瓶 同前
3.溶液配制中误差分析原因归纳
仪器使用
计
误差 药品
天平 量筒 烧杯 算
原因
①称量前天平指针 ①量水时俯视读
结果 计算
偏右;②右盘放了 数;②量好的水
偏高 失误
纸片左盘未放纸片 倒入烧杯时溅出
①固体药品中
①称量前天平指针
含水分;②固
偏左;②称量前游
体药品中含有
码不在零点;③称 烧杯
结果 杂质;③固体 量水时仰 计算
量时药品和砝码放 内壁
偏低 药品转移时损 视读数 失误
颠倒(使用游码); 有水
失(洒落烧杯
④左盘放了纸片右
外面或沾在白
盘未放纸片
纸上面)
(2014·黔东南)化学是一门以实验为基础的自然学科,如图是实验室常用的部分实验仪器图,请按
要求回答:
(1)现用氯化钠固体配制50 g质量分数为10%的氯化钠溶液,整个配置过程中不需要的实验仪器有________(填
编号)。
(2)主要的实验步骤是:
①计算:计算所需氯化钠固体的质量和水的体积。
②称量:
a.使用称量仪器的第一步是____________(写出操作过程)。b.称取________g氯化钠固体,量取所需水的体积时应选用________mL(填“10”“50”或“100”)的计量仪器。
③溶解:将称好的氯化钠固体倒入容器中,然后加水使其溶解,并不断搅拌。
④装瓶:将配制好的溶液装入上述仪器________(填仪器名称)中并贴上标签。
⑤误差分析:在量取水的体积时俯视读数,则导致溶液溶质质量分数________(填“偏大”“偏小”或“不变”)。
思路点拨:配制溶液不需要酒精灯和漏斗,配制好的溶液可装入D滴瓶中。配制50 g质量分数为10%的氯化钠
溶液需称量氯化钠50 g×10%=5 g,用50 mL量筒量取45 mL水。若量水时俯视读数会使水的量偏少,导致溶液溶质
质量分数偏大。
在判断溶液配制过程中的误差分析时,要从溶质质量分数的定义入手,即在实验操作中溶质质量和溶剂水的质
量是否改变决定着溶质质量分数的变化,但也不能忽略溶液均一性的应用。
(3)如果配制10%的氯化钠溶液的溶质质量分数偏小,其原因是________。
A.称取的氯化钠固体质量偏大
B.转移称量好的氯化钠固体时,有少量洒落在桌面上
C.量取水的体积偏小
D.转移配制好的溶液时,有少量液体溅出
E.称量时只在左盘上放了纸
(4)在给出的仪器中,B的作用是____________________________________。
一、选择题
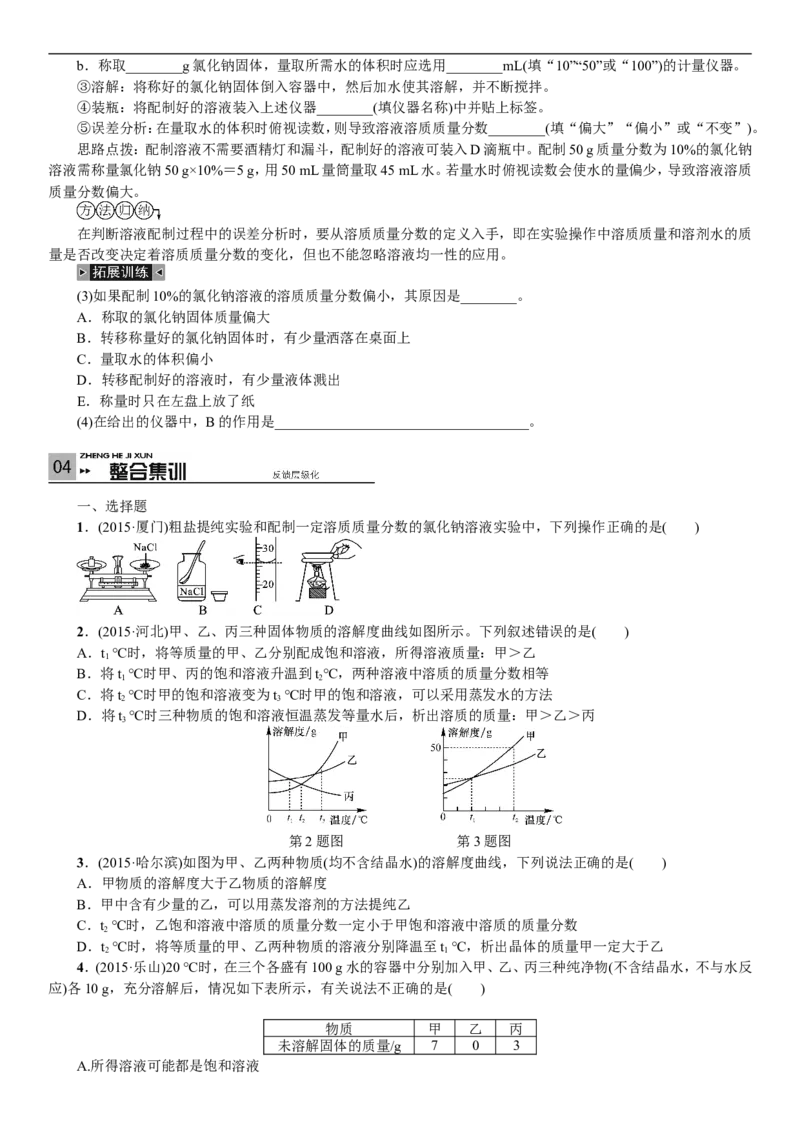
1.(2015·厦门)粗盐提纯实验和配制一定溶质质量分数的氯化钠溶液实验中,下列操作正确的是( )
2.(2015·河北)甲、乙、丙三种固体物质的溶解度曲线如图所示。下列叙述错误的是( )
A.t ℃时,将等质量的甲、乙分别配成饱和溶液,所得溶液质量:甲>乙
1
B.将t ℃时甲、丙的饱和溶液升温到t℃,两种溶液中溶质的质量分数相等
1 2
C.将t ℃时甲的饱和溶液变为t ℃时甲的饱和溶液,可以采用蒸发水的方法
2 3
D.将t ℃时三种物质的饱和溶液恒温蒸发等量水后,析出溶质的质量:甲>乙>丙
3
第2题图 第3题图
3.(2015·哈尔滨)如图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
A.甲物质的溶解度大于乙物质的溶解度
B.甲中含有少量的乙,可以用蒸发溶剂的方法提纯乙
C.t ℃时,乙饱和溶液中溶质的质量分数一定小于甲饱和溶液中溶质的质量分数
2
D.t ℃时,将等质量的甲、乙两种物质的溶液分别降温至t ℃,析出晶体的质量甲一定大于乙
2 1
4.(2015·乐山)20 ℃时,在三个各盛有100 g水的容器中分别加入甲、乙、丙三种纯净物(不含结晶水,不与水反
应)各10 g,充分溶解后,情况如下表所示,有关说法不正确的是( )
物质 甲 乙 丙
未溶解固体的质量/g 7 0 3
A.所得溶液可能都是饱和溶液B.三溶液中溶质的质量分数乙>丙>甲
C.升高温度,三溶液中溶质的质量分数一定会改变
D.20 ℃时,甲的溶解度最小
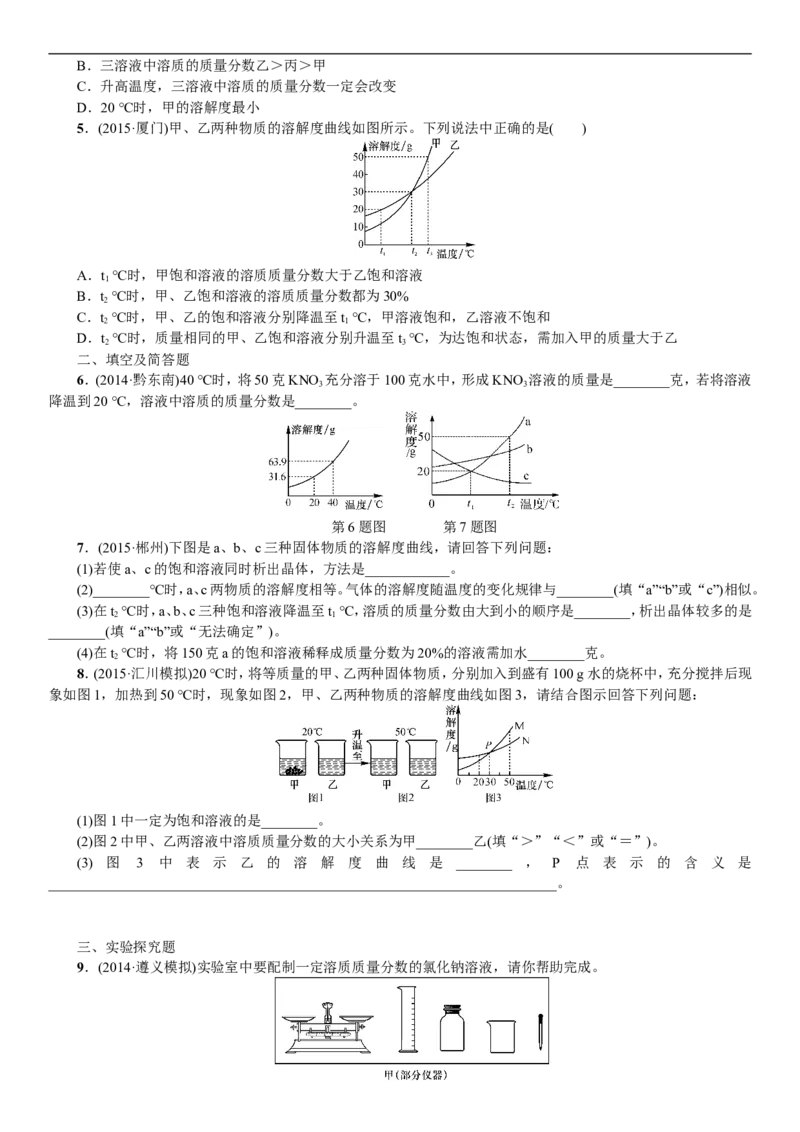
5.(2015·厦门)甲、乙两种物质的溶解度曲线如图所示。下列说法中正确的是( )
A.t ℃时,甲饱和溶液的溶质质量分数大于乙饱和溶液
1
B.t ℃时,甲、乙饱和溶液的溶质质量分数都为30%
2
C.t ℃时,甲、乙的饱和溶液分别降温至t ℃,甲溶液饱和,乙溶液不饱和
2 1
D.t ℃时,质量相同的甲、乙饱和溶液分别升温至t ℃,为达饱和状态,需加入甲的质量大于乙
2 3
二、填空及简答题
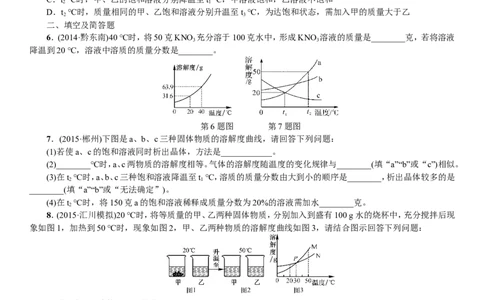
6.(2014·黔东南)40 ℃时,将50克KNO 充分溶于100克水中,形成KNO 溶液的质量是________克,若将溶液
3 3
降温到20 ℃,溶液中溶质的质量分数是________。
第6题图 第7题图
7.(2015·郴州)下图是a、b、c三种固体物质的溶解度曲线,请回答下列问题:
(1)若使a、c的饱和溶液同时析出晶体,方法是____________。
(2)________℃时,a、c两物质的溶解度相等。气体的溶解度随温度的变化规律与________(填“a”“b”或“c”)相似。
(3)在t ℃时,a、b、c三种饱和溶液降温至t ℃,溶质的质量分数由大到小的顺序是________,析出晶体较多的是
2 1
________(填“a”“b”或“无法确定”)。
(4)在t ℃时,将150克a的饱和溶液稀释成质量分数为20%的溶液需加水________克。
2
8.(2015·汇川模拟)20 ℃时,将等质量的甲、乙两种固体物质,分别加入到盛有100 g水的烧杯中,充分搅拌后现
象如图1,加热到50 ℃时,现象如图2,甲、乙两种物质的溶解度曲线如图3,请结合图示回答下列问题:
(1)图1中一定为饱和溶液的是________。
(2)图2中甲、乙两溶液中溶质质量分数的大小关系为甲________乙(填“>”“<”或“=”)。
(3) 图 3 中 表 示 乙 的 溶 解 度 曲 线 是 ________ , P 点 表 示 的 含 义 是
________________________________________________________________________。
三、实验探究题
9.(2014·遵义模拟)实验室中要配制一定溶质质量分数的氯化钠溶液,请你帮助完成。(1)甲图中缺少一种必须用到的玻璃仪器是________(填写名称)。
(2)配制溶液的步骤是:①计算;②称量;③溶解;④装瓶贴标签。
(3)准确称量18 g氯化钠,量取蒸馏水的体积如乙图所示,氯化钠完全溶解后所配制的溶液中溶质的质量分数是
________(水的密度为1 g/cm3)。
(4)丙图中试剂瓶上的标签应该填写____________________________(请具体写明)。
四、计算题
10.(2015·安顺)一定质量的氯化钡溶液和10 g溶质质量分数为9.8%的稀硫酸恰好完全反应后,过滤得到28.47 g
滤液。请计算:
(1)生成硫酸钡沉淀的质量;
(2)氯化钡溶液的溶质质量分数。参考答案
考点解读
考点1 溶质质量 溶液质量 2.溶质质量 溶液质量
考点2 溶质
各个击破
例1 B
例2 (1)8.8 (2)设原混合物中碳酸钠的质量为x,反应生成氯化钠的质量为y。
NaCO+2HCl===2NaCl+HO+CO↑
2 3 2 2
106 117 44
x y 8.8 g
= x=21.2 g
= y=23.4 g
原混合物中氯化钠的质量为
33.8 g-21.2 g=12.6 g
反应后所得溶液中氯化钠的质量分数为
×100%=24%
答:略。
题组训练 1.C 2.设硫酸溶液中HSO 的质量为x。
2 4
HSO +BaCl ===BaSO ↓+2HCl
2 4 2 4
98 233
x 2.33 g
= x=0.98 g
稀硫酸的溶质质量分数为×100%=9.8%
答:稀硫酸的溶质质量分数为9.8%。
实验突破
实验 2.(1)50 g×6%=3 g 50 g-3 g=47 g 50 (2)50 g×3%÷6%=25 g 50 g-25 g =25 g 50 玻璃棒
例4 (1)CH (2)调节天平平衡 5 50 滴瓶 偏大
拓展训练 (3)BE (4)加快氯化钠固体的溶解速率
整合集训
1.C 2.B 3.C 4.C 5.D 6.150 24% 7.(1)蒸发水(溶剂) (2)t c (3)b>a>c 无法确定 (4)100 8.(1)甲
1
(2)= (3)N 30 ℃时,甲、乙两种固体物质的溶解度相等 9.(1)玻璃棒 (3)18% (4)溶液名称与溶质的质量分数
10.解:参加反应的硫酸的质量是10 g×9.8%=0.98 g。
设生成BaSO 的质量是x,参加反应的BaCl 的质量是y。
4 2
BaCl +HSO ===BaSO ↓+2HCl
2 2 4 4
208 98 233
y 0.98 g x
= x=2.33 g
= y=2.08 g
氯化钡(BaCl )溶液的溶质质量分数为:
2
×100%=10%
答:(1)生成BaSO 的质量是2.33 g;(2)氯化钡溶液的溶质质量分数为10%。
4