文档内容
第5讲 溶液
1.认识溶解现象,知道溶液是由溶质和溶剂组成的。
2.知道水是最重要的溶剂,酒精、汽油等也是常见的溶剂。
3.了解饱和溶液和溶解度的含义,了解溶解性表和溶解度曲线的应用。
考试说明
4.能举例说明结晶现象。
5.能说出一些常见的乳化现象。
6.了解溶液在生活、生产中的重要意义。
考点1 溶液的形成
1.溶液的概念:一种或几种物质分散到另一种物质里形成均一的、稳定的______叫做溶液;特征:______、______。
【温馨提示】(1)溶液不一定都是无色的,如CuSO 溶液为蓝色,FeCl 溶液为黄色,FeSO 溶液为浅绿色;(2)一种溶剂
4 3 4
里可以溶解多种溶质;(3)能与水反应的物质放入水中,生成物为该溶液的溶质。
2.溶液的组成:溶液是由______和______组成的,溶液质量=______的质量+______的质量。溶液的质量=溶液的体积×
溶液的密度。
3.溶液中溶质、溶剂的判断:
(1)根据名称判断,溶液的名称一般为______的名称后加溶液,即______在前,______在后。
(2)若是固体或气体与液体相互溶解为溶液,一般习惯将______看作为溶质,______看作为溶剂。
(3)若是由两种液体组成的溶液,一般习惯上把______的看作为溶剂,______的看作为溶质。
(4)其他溶质溶于水形成溶液时,无论水量的多少,______都是溶剂。
考点2 乳浊液与乳化
相溶的物质可以形成,而不相溶的可以形成______浊液(包括悬浊液和乳浊液),乳化并不是溶解,只是使植物油分散
成____________存在水中而不聚集,生活中常用的乳化剂:肥皂、洗洁精等。
考点3 溶解时的吸热或放热
类型 吸热或放热现象 举例
放热 有些物质溶解时,会出现放热现象 NaOH、浓HSO
2 4
吸热 有些物质溶解时,会出现吸热现象 NH NO
4 3
不放热也不吸热 物质溶解时,整个过程溶液温度几乎不变 NaCl
考点4 饱和溶液与不饱和溶液
饱和溶液 不饱和溶液
在一定下,一定量的溶剂里继续溶解某 在一定下,一定量的溶剂里继续溶解某种溶
概念
种溶质的溶液叫做这种溶质的饱和溶液 质的溶液叫做这种溶质的不饱和溶液
区分
加入少量相应的溶质,若溶解,则原溶液是饱和溶液;若溶解,则原溶液是不饱和溶液
方法
相互 (________)(________)(改变温度)
不饱和溶液 饱和溶液
转化
(________)(改变温度)
【温馨提示】浓、稀溶液与饱和溶液、不饱和溶液的关系:①对于含不同溶质的溶液,浓溶液不一定是饱和溶液,稀溶液
也不一定是不饱和溶液,反之亦然;②但对于同种溶质来说,在一定温度下,其饱和溶液一定比其不饱和溶液要浓。
考点5 溶解度与溶解度曲线
1.固体溶解度:在____________,某固态物质在______溶剂里达到______所溶解的质量。
2.影响固体物质溶解度大小的因素有:(1)内因:____________的性质;(2)外因:____________。增大气体溶解度的方
法有______、______。
3.溶解度曲线:物质的溶解度随温度变化的曲线叫做溶解度曲线,运用它可以查出某物质在一定温度时的溶解度。
4.结晶方法:
(1)对溶解度受温度变化影响小的固态物质,一般用______的方法得到晶体,如______。
(2)对溶解度受温度变化影响大的固态物质,一般用______的方法得到晶体,如______。
命题点1 溶液与乳浊液
(2014·遵义模拟)下列说法中,错误的是( )A.洗涤剂可乳化餐具上的油污
B.汽油可溶解衣服上的油渍
C.氢氧化钠溶液可直接用作厨房清洁剂
D.长期用硬水洗涤的衣物会变硬
思路点拨:洗涤剂中有乳化剂,具有乳化功能,能使植物油分散成无数细小的液滴,这些细小的液滴能随着水流
走;油渍可溶解在汽油中形成溶液;氢氧化钠具有强烈的腐蚀性,不能直接用作厨房清洁剂;硬水中含有较多可溶性
钙、镁化合物,遇肥皂水会产生浮渣,长期用硬水洗涤的衣物会变硬。
乳化作用是将大颗粒的油珠变为小颗粒的液滴,与溶解有本质上的区别;溶解则是溶质以分子或离子的形式均
匀分散到溶剂中。
1.(2015·宁夏)洗涤与生活密切相关。下列洗涤方法中利用了乳化原理的是( )
A.用盐酸清洗水垢
B.用洗洁精清洗餐具
C.用汽油洗涤油污
D.用酒精洗去试管中的碘
2.(2015·眉山)关于溶液的说法正确的是( )
A.溶液都是无色透明的
B.水可以溶解任何物质
C.均一、稳定的液体都是溶液
D.饱和溶液不一定是浓溶液
命题点2 溶解时的吸热或放热
(2014·六盘水)下列固体溶于适量水后,液体温度明显升高的是( )
①氢氧化钠 ②氯化钠 ③硝酸铵 ④生石灰
A.②③ B.①②③④
C.①④ D.①③④
思路点拨:氢氧化钠溶于水放热,氯化钠溶于水溶液没有明显温度变化,硝酸铵溶于水吸热,氧化钙与水反应放
热。
3.(2015·济宁)物质在水中溶解是复杂的物理和化学变化过程,往往伴随着热量变化,因此,不同物质溶于水所得
溶液的温度有所不同。下列物质溶于水,溶液温度明显降低的是( )
A.NH NO 固体 B.NaOH固体
4 3
C.NaCl固体 D.浓HSO
2 4
4.(2015·益阳)如图所示,广口瓶中盛有少量饱和澄清石灰水,小试管和U形管中均有适量水,现向小试管中注
入适量浓硫酸。
请回答:
(1)可观察到饱和澄清石灰水________;
(2)U形管中a、b液面变化情况是________(填序号)。
A.a液面上升,b液面下降
B.a液面下降,b液面上升
命题点3 饱和溶液和不饱和溶液
(2013·毕节)硝酸钾在不同温度时的溶解度为:温度/℃ 0 20 40
溶解度/g 13.3 31.6 63.9
在20 ℃时将31.6 g硝酸钾放入100 g水中充分搅拌,此时溶液为________(填“饱和”或“不饱和”)溶液;如
将该溶液降温到0 ℃,应看到的现象是________;再将该溶液升温到40 ℃,溶液应是________(填“饱和”或“不饱
和”)溶液。
思路点拨:20 ℃时硝酸钾的溶解度为31.6 g,在20 ℃时将31.6 g硝酸钾放入100 g水中正好饱和;硝酸钾的溶解
度随温度的升高而增大,将20 ℃硝酸钾的饱和溶液降温到0 ℃会析出晶体;再升高温度到40 ℃,此时硝酸钾的溶解
度是63.9 g,溶液将变为不饱和溶液。
判断某溶液是否饱和,主要看在一定温度下,还能不能继续溶解溶质,如不能再继续溶解,那么这种溶液就是饱
和溶液。
5.(2015·六盘水盘县模拟)在一定温度下,将某物质的饱和溶液加水稀释成不饱和溶液,保持不变的是( )
A.溶剂的质量 B.溶质的质量
C.溶液的质量 D.溶质的质量分数
命题点4 溶解度与溶解度曲线
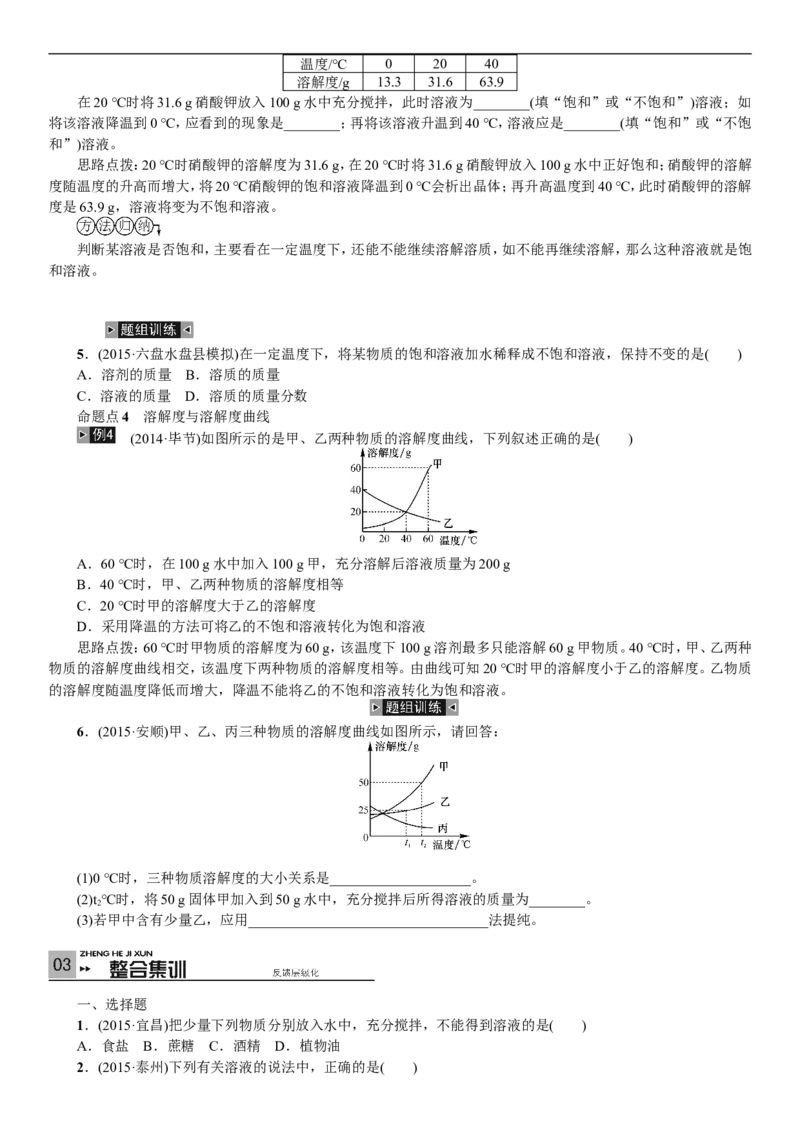
(2014·毕节)如图所示的是甲、乙两种物质的溶解度曲线,下列叙述正确的是( )
A.60 ℃时,在100 g水中加入100 g甲,充分溶解后溶液质量为200 g
B.40 ℃时,甲、乙两种物质的溶解度相等
C.20 ℃时甲的溶解度大于乙的溶解度
D.采用降温的方法可将乙的不饱和溶液转化为饱和溶液
思路点拨:60 ℃时甲物质的溶解度为60 g,该温度下100 g溶剂最多只能溶解60 g甲物质。40 ℃时,甲、乙两种
物质的溶解度曲线相交,该温度下两种物质的溶解度相等。由曲线可知20 ℃时甲的溶解度小于乙的溶解度。乙物质
的溶解度随温度降低而增大,降温不能将乙的不饱和溶液转化为饱和溶液。
6.(2015·安顺)甲、乙、丙三种物质的溶解度曲线如图所示,请回答:
(1)0 ℃时,三种物质溶解度的大小关系是____________________。
(2)t ℃时,将50 g固体甲加入到50 g水中,充分搅拌后所得溶液的质量为________。
2
(3)若甲中含有少量乙,应用__________________________________法提纯。
一、选择题
1.(2015·宜昌)把少量下列物质分别放入水中,充分搅拌,不能得到溶液的是( )
A.食盐 B.蔗糖 C.酒精 D.植物油
2.(2015·泰州)下列有关溶液的说法中,正确的是( )A.溶液都是无色、透明的
B.均一、稳定的液体都是溶液
C.硝酸铵溶于水使溶液的温度降低
D.溶质都以分子形式溶解在溶剂里
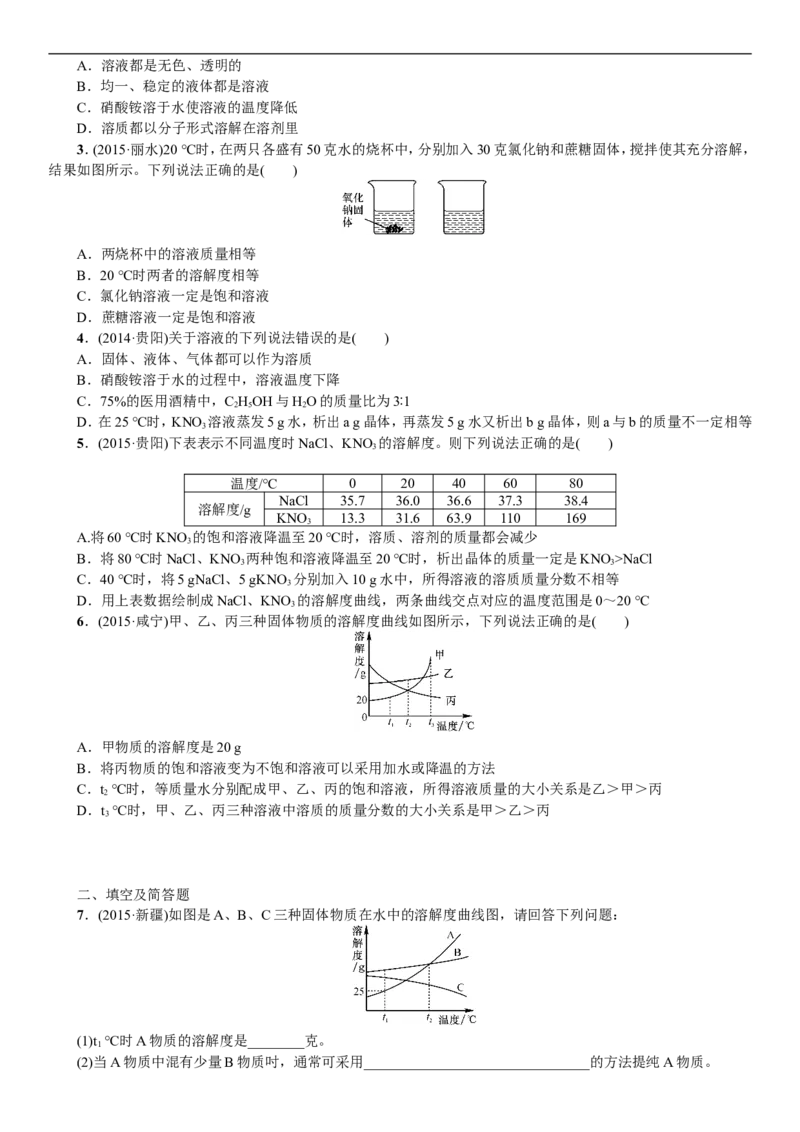
3.(2015·丽水)20 ℃时,在两只各盛有50克水的烧杯中,分别加入30克氯化钠和蔗糖固体,搅拌使其充分溶解,
结果如图所示。下列说法正确的是( )
A.两烧杯中的溶液质量相等
B.20 ℃时两者的溶解度相等
C.氯化钠溶液一定是饱和溶液
D.蔗糖溶液一定是饱和溶液
4.(2014·贵阳)关于溶液的下列说法错误的是( )
A.固体、液体、气体都可以作为溶质
B.硝酸铵溶于水的过程中,溶液温度下降
C.75%的医用酒精中,C HOH与HO的质量比为3∶1
2 5 2
D.在25 ℃时,KNO 溶液蒸发5 g水,析出a g晶体,再蒸发5 g水又析出b g晶体,则a与b的质量不一定相等
3
5.(2015·贵阳)下表表示不同温度时NaCl、KNO 的溶解度。则下列说法正确的是( )
3
温度/℃ 0 20 40 60 80
NaCl 35.7 36.0 36.6 37.3 38.4
溶解度/g
KNO 13.3 31.6 63.9 110 169
3
A.将60 ℃时KNO 的饱和溶液降温至20 ℃时,溶质、溶剂的质量都会减少
3
B.将80 ℃时NaCl、KNO 两种饱和溶液降温至20 ℃时,析出晶体的质量一定是KNO>NaCl
3 3
C.40 ℃时,将5 gNaCl、5 gKNO 分别加入10 g水中,所得溶液的溶质质量分数不相等
3
D.用上表数据绘制成NaCl、KNO 的溶解度曲线,两条曲线交点对应的温度范围是0~20 ℃
3
6.(2015·咸宁)甲、乙、丙三种固体物质的溶解度曲线如图所示,下列说法正确的是( )
A.甲物质的溶解度是20 g
B.将丙物质的饱和溶液变为不饱和溶液可以采用加水或降温的方法
C.t ℃时,等质量水分别配成甲、乙、丙的饱和溶液,所得溶液质量的大小关系是乙>甲>丙
2
D.t ℃时,甲、乙、丙三种溶液中溶质的质量分数的大小关系是甲>乙>丙
3
二、填空及简答题
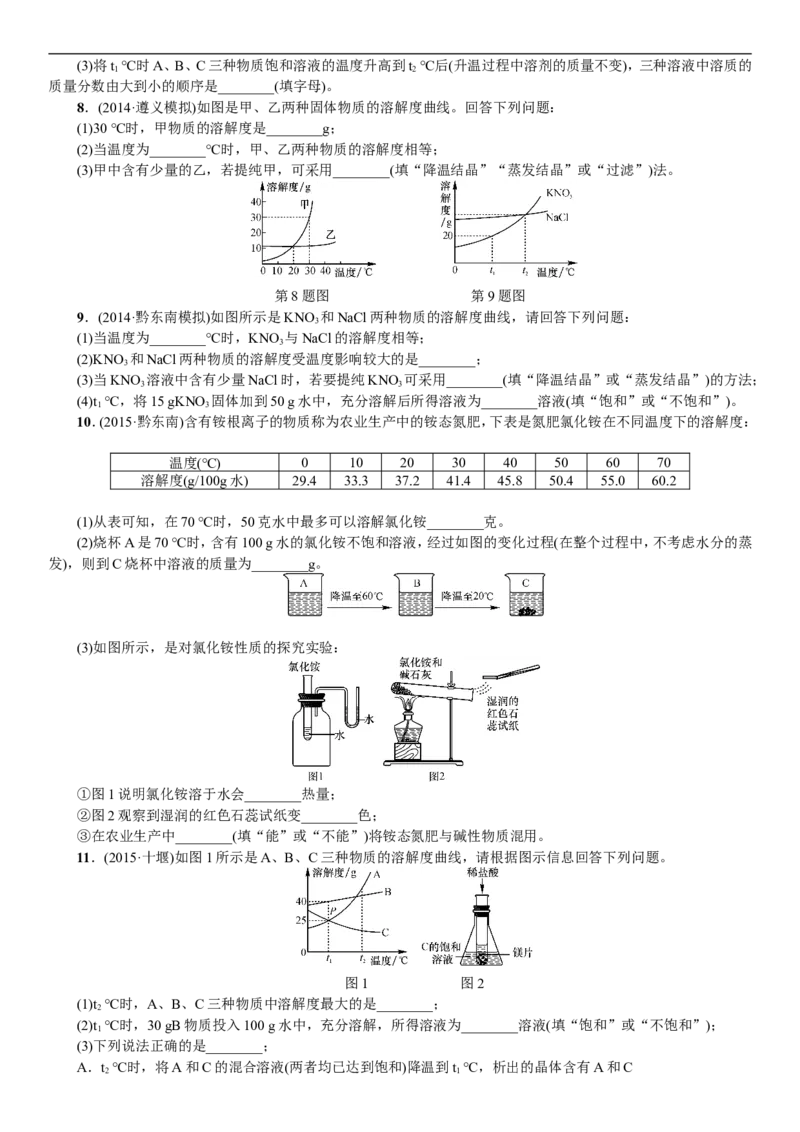
7.(2015·新疆)如图是A、B、C三种固体物质在水中的溶解度曲线图,请回答下列问题:
(1)t ℃时A物质的溶解度是________克。
1
(2)当A物质中混有少量B物质吋,通常可采用________________________________的方法提纯A物质。(3)将t ℃时A、B、C三种物质饱和溶液的温度升高到t ℃后(升温过程中溶剂的质量不变),三种溶液中溶质的
1 2
质量分数由大到小的顺序是________(填字母)。
8.(2014·遵义模拟)如图是甲、乙两种固体物质的溶解度曲线。回答下列问题:
(1)30 ℃时,甲物质的溶解度是________g;
(2)当温度为________℃时,甲、乙两种物质的溶解度相等;
(3)甲中含有少量的乙,若提纯甲,可采用________(填“降温结晶”“蒸发结晶”或“过滤”)法。
第8题图 第9题图
9.(2014·黔东南模拟)如图所示是KNO 和NaCl两种物质的溶解度曲线,请回答下列问题:
3
(1)当温度为________℃时,KNO 与NaCl的溶解度相等;
3
(2)KNO 和NaCl两种物质的溶解度受温度影响较大的是________;
3
(3)当KNO 溶液中含有少量NaCl时,若要提纯KNO 可采用________(填“降温结晶”或“蒸发结晶”)的方法;
3 3
(4)t ℃,将15 gKNO 固体加到50 g水中,充分溶解后所得溶液为________溶液(填“饱和”或“不饱和”)。
1 3
10.(2015·黔东南)含有铵根离子的物质称为农业生产中的铵态氮肥,下表是氮肥氯化铵在不同温度下的溶解度:
温度(℃) 0 10 20 30 40 50 60 70
溶解度(g/100g水) 29.4 33.3 37.2 41.4 45.8 50.4 55.0 60.2
(1)从表可知,在70 ℃时,50克水中最多可以溶解氯化铵________克。
(2)烧杯A是70 ℃时,含有100 g水的氯化铵不饱和溶液,经过如图的变化过程(在整个过程中,不考虑水分的蒸
发),则到C烧杯中溶液的质量为________g。
(3)如图所示,是对氯化铵性质的探究实验:
①图1说明氯化铵溶于水会________热量;
②图2观察到湿润的红色石蕊试纸变________色;
③在农业生产中________(填“能”或“不能”)将铵态氮肥与碱性物质混用。
11.(2015·十堰)如图1所示是A、B、C三种物质的溶解度曲线,请根据图示信息回答下列问题。
图1 图2
(1)t ℃时,A、B、C三种物质中溶解度最大的是________;
2
(2)t ℃时,30 gB物质投入100 g水中,充分溶解,所得溶液为________溶液(填“饱和”或“不饱和”);
1
(3)下列说法正确的是________;
A.t ℃时,将A和C的混合溶液(两者均已达到饱和)降温到t ℃,析出的晶体含有A和C
2 1B.t ℃时,将A、B、C三种物质的饱和溶液降温到t ℃,所得溶液中溶质质量分数的大小关系为B>A>C
2 1
C.从混有少量B的A物质中提纯较纯净的A,可通过冷却它们的热饱和溶液实现
D.t ℃时,欲用A的饱和溶液配制10%的A溶液,只需要量筒、烧杯、胶头滴管三种玻璃仪器
1
(4)如图2所示,向放有镁片的试管中,滴加稀盐酸后,锥形瓶中 C 的饱和溶液变混浊,请解释其原因
_________________________________________________________________________。参考答案
考点解读
考点1 1.混合物 均一性 稳定性 2.溶质 溶剂 溶质 溶剂 3.(1)溶质 溶质 溶剂 (2)固体或气体
液体 (3)量多 量少 (4)水
考点2 溶液 无数细小的液滴
考点4 温度 不能 温度 还能 不能 继续 增加溶质 蒸发溶剂 增加溶剂
考点5 1.一定温度下 100 g 饱和状态 2.溶质、溶剂 温度 增加压强 降低温度 4.(1)蒸发溶剂 NaCl
(2)降温结晶 KNO
3
各个击破
例1 C 例2 C 例3 饱和 析出晶体 不饱和 例4 B
题组训练 1.B 2.D 3.A 4.(1)变浑浊 (2)B 5.B 6.(1)丙>乙>甲(或甲<乙<丙) (2)75 g (3)降温结晶或冷
却热饱和溶液
整合集训
1.D 2.C 3.C 4.C 5.C 6.B 7.(1)25 (2)冷却热饱和溶液或降温结晶 (3)B>C>A 8.(1)30 (2)20 (3)降
温结晶 9.(1)t (2)KNO (3)降温结晶 (4)饱和 10.(1)30.1 (2)137.2 (3)①吸收 ②蓝 ③不能 11.(1)A (2)
2 3
不饱和 (3)B (4)镁与稀盐酸反应放出热量,使得溶液温度升高,物质C的溶解度减小而析出