文档内容
题型复习(五) 化学计算
一、题型简介
中考化学计算题命题与社会、生活和时事紧密相连,题型多样化,具有时代性、社会性、探究性,命题思路多是将
相关的化学知识与几种简单计算相融合,试题的情景多与生产生活、社会热点、科学前沿、时事热点相结合,题干仍
将以文字信息、商标或标签、表格、图像信息等形式呈现,从解决具体、实际的问题出发,考查同学们综合运用化学知
识解决问题的能力。
二、方法指导
初中化学课程标准要求必须掌握三种简单计算:有关化学式的计算,有关化学方程式的计算,有关溶质质量分数
的计算。除此之外,综合计算在中考中的地位也越来越重要,因此了解近几年来中考化学计算题的命题特点和考查方
式,找出自己在化学计算方面失分的原因并找到应对的对策,掌握中考化学计算题的题型和解法是突破中考化学计
算的关键。
题型之一 根据化学式的计算
解此类题的关键就是紧抓化学式,不论化学式熟悉与否,只要熟知化学式的意义,掌握化学式的相关计算,利用
所学知识,不难解决这类问题。化学式的计算主要有两类:
(1)是根据化学式计算物质中各元素的质量比或质量分数,公式如下:①相对分子质量=(原子的相对原子质量×
原子个数)之和;
②各元素的质量比=(原子的相对原子质量×原子个数)之比;
③元素的质量分数=×100%。
(2)是根据元素的质量推算物质的化学式或其他元素的质量:用所给元素的质量除以该元素的原子的相对原子质
量,可得该元素在化学式中的原子个数。若给出的是几种元素的质量比,可用质量比除以相应元素的相对原子质量,
计算出几种元素原子的个数比,选取符合题意的一组,写出化学式。也可以根据一种元素的质量计算其他元素的质量。
糖类在提供人类的营养和丰富人们的物质生活中有着重要的作用,从古到今在食品加工业中占有重要
地位,我们的祖先品尝到香甜的麦芽糖也很早,已知麦芽糖的化学式为C H O ,请回答下列问题:
12 22 11
(1)该物质由________种元素组成。
(2)1个麦芽糖分子中含有________个原子,该物质的相对分子质量为________。
(3)该物质中氢气元素与氧元素的质量比是________。
思路点拨:(1)由麦芽糖的化学式可知该物质由碳、氢、氧三种元素组成。(2)1个分子中原子个数即为化学式中原
子的代数和,相对分子质量为构成分子的各原子的相对原子质量之和。(3)质量比为各原子的相对原子质量乘个数之
比。
1.某硫的化合物中硫与氧的质量比为2∶3,则该化合物中硫的化合价可能是( )
A.-2 B.+2 C.+4 D.+6
2.N(NO) 是一种新型火箭燃料,下列关于N(NO) 的说法正确的是( )
2 3 2 3
①相对分子质量为152 ②氮元素的质量分数为32% ③氮元素和氧元素的质量比为4∶6 ④一个N(NO) 分
2 3
子中含有10个原子
A.①④ B.②③
C.①③ D.②④
3.苏州的“碧螺春”享誉全国。“碧螺春”茶叶中的单宁酸具有抑制血压上升、清热解毒、抗癌等功效,其化学
式为C H O 。下列说法错误的是( )
76 52 46
A.单宁酸由碳、氢、氧三种元素组成
B.一个单宁酸分子由76个碳原子、52个氢原子和46个氧原子构成
C.单宁酸中碳、氧元素的质量比为57∶23
D.单宁酸中氢元素的质量分数最小
4.2015年4月28日召开的国务院常务会议确定,加快清洁油品生产供应,力争提前完成成品油质量升级任务,
清洁汽油添加剂异辛烷(C H ),能改善油品质量,促进汽油燃烧,大幅减少车辆污染物排放,有效保护大气环境。请回
8 18
答:
(1)异辛烷中碳氢元素的原子个数比为________;(2)异辛烷的相对分子质量为________。
5.过氧乙酸与过氧化氢化学性质有相似之处。为了预防禽流感的发生,养殖人员常用15%的过氧乙酸溶液对鸡、
鸭舍进行消毒。过氧乙酸的化学式为CHCOOOH。完成下到空白:
3
(1)过氧乙酸由________种元素组成。
(2)过氧乙酸中碳元素和氢元素的质量比为________。
6.目前,市场上畅销以木糖醇为原料的“口香糖”,对修复蛀牙有所帮助。木糖醇是由三种元素组成的有机物,
其中,氢元素质量分数约为7.89%,氧元素质量分数约为52.6%,且每个分子中含有5个氧原子。请回答:
(1)该有机物还含有的一种元素是________;
(2)木糖醇的化学式量(或相对分子质量)为________;
(3)一个木糖醇分子中氢原子的个数为________。
7.物质A是由地壳中含量最多的元素和含量最多的金属元素组成,与稀盐酸反应得到物质B的水溶液,请根据
题意写出相应物质的化学式并计算其相对分子质量:
A物质的化学式________、相对分子质量________;
B物质的化学式________、相对分子质量________。
8.丙酸钠是一种常用的食品添加剂,其化学式为C HONa。已知该化合物中碳元素与氧元素的质量比为9∶8,请
3 5 x
计算:
(1)丙酸钠由________种元素组成;
(2)x=________;
(3)该物质的相对分子质量是________。
9.人体缺乏维生素C(简写“Vc”)就会患坏血病,哥伦布探险时的许多船员就因此而死亡。如图所示为某种“维
生素C”说明书的一部分。请你回答:
(1)“Vc”中含有________种元素。
(2)若正常成人每天对“Vc”的最低需要量为60 mg。
①当“Vc”完全来自图中的“维生素C”时,每天至少服用________次;
②当“Vc”完全来自某种新鲜蔬菜(每 1 000 g 这种蔬菜含“Vc”120 mg)时,每天至少应食用这种蔬菜
________g。
(3)取2片“维生素C”溶于水,滴入紫色石蕊试液变红色,说明“Vc”的溶液显________性。
10.(2015·毕节)莽草酸(C H O)是制取抗“H1N1流感”药物“达菲”的原料。试求:
7 10 5
(1)每个莽草酸分子所含原子数;
(2)莽草酸中各元素的质量比。
11.钠摄入过量或钾摄入不足都是导致高血压的风险因素。日常生活中选择食用低钠盐能实现减钠补钾。如图为
某品牌低钠盐的标签,请你根据标签回答以下问题:(1)氯化钾的相对分子质量为________。
(2)人体每天摄入钠元素的质量不宜超过2.3 g。如果人体所需的钠元素全部来自该品牌食盐,那么一个人每天摄
入该品牌低钠盐的质量不宜超过多少克?(结果保留一位小数)
题型之二 有关化学方程式的计算
要深刻理解化学方程式的含义,理解反应物和生成物在微观上和质量上的关系,要求明确计算步骤。规范书写格
式,正确解出结果;某些含有杂质的反应物或生成物的相关计算,要尤其注意数据的分析和转化。在计算时,首先应
将含杂质物质的质量转化为纯净物质的质量,然后代入化学方程式中进行相关计算。所有的化学反应方程式都符合
质量守恒定律,所以质量守恒定律是化学反应方程式计算的基础。正确理解化学方程式中“量”的含义是进行计算
的核心,首先在化学方程式中任意两种物质的质量比不变,其次,实际质量比与相对质量比相等。
根据化学方程式计算的几种类型:
(1)基本计算,互求反应物和生成物的质量(或体积、利用密度公式将体积和质量进行换算)。这类题目给出的反应
物是纯净物,涉及的反应也只有一个。做题时写出反应方程式,找出已知物和未知物的质量关系列比例式,求出未知
数。
(2)含杂质物质的计算,注意混合物的质量换算成纯净物的质量才能代入到化学式的下面。给出的反应物是混合
物,涉及的反应有一个或多个。解这类题时首先要写出与题目相关的反应方程式,然后找出已知量和未知量,列比例
式进行计算。
将100 g氯化钾样品(含有碳酸钾杂质)加入到50 g盐酸中,样品完全反应,产生的气体全部逸出,得到
145.6 g溶液。请计算:
(1)产生气体的质量为________g;
(2)样品中氯化钾的质量分数(精确至0.1%)。
思路点拨:本题是一个典型的用差量法求解的计算题,即用反应前的总质量减去反应后剩余的质量,求出反应产
生的气体或沉淀的质量,带入方程式求解。
1.2.3 g钠、2.4 g镁、2.7 g铝分别与足量的盐酸反应,按钠、镁、铝的顺序得到氢气的质量比为( )
A.1∶2∶3 B.1∶1∶1
C.2∶3∶1 D.3∶2∶12.下列说法正确的是( )
A.等质量的CO和CO 中氧元素的质量比为1∶2
2
B.等质量的Al和Mg分别与足量稀硫酸充分反应,生成H 的质量相等
2
C.等质量的NaHCO 和MgCO 分别与足量稀盐酸充分反应,生成CO 的质量相等
3 3 2
D.等质量的质量分数均为4%的氢氧化钠溶液与稀盐酸充分反应,所得溶液显中性
3.有X、Y两种元素,使12克X 与XY 反应生成24克C,反应的化学方程式为X+XY ===3C。则X、Y两元素
2 3 2 3
的原子量之比为( )
A.1∶1 B.1∶2 C.3∶1 D.3∶4
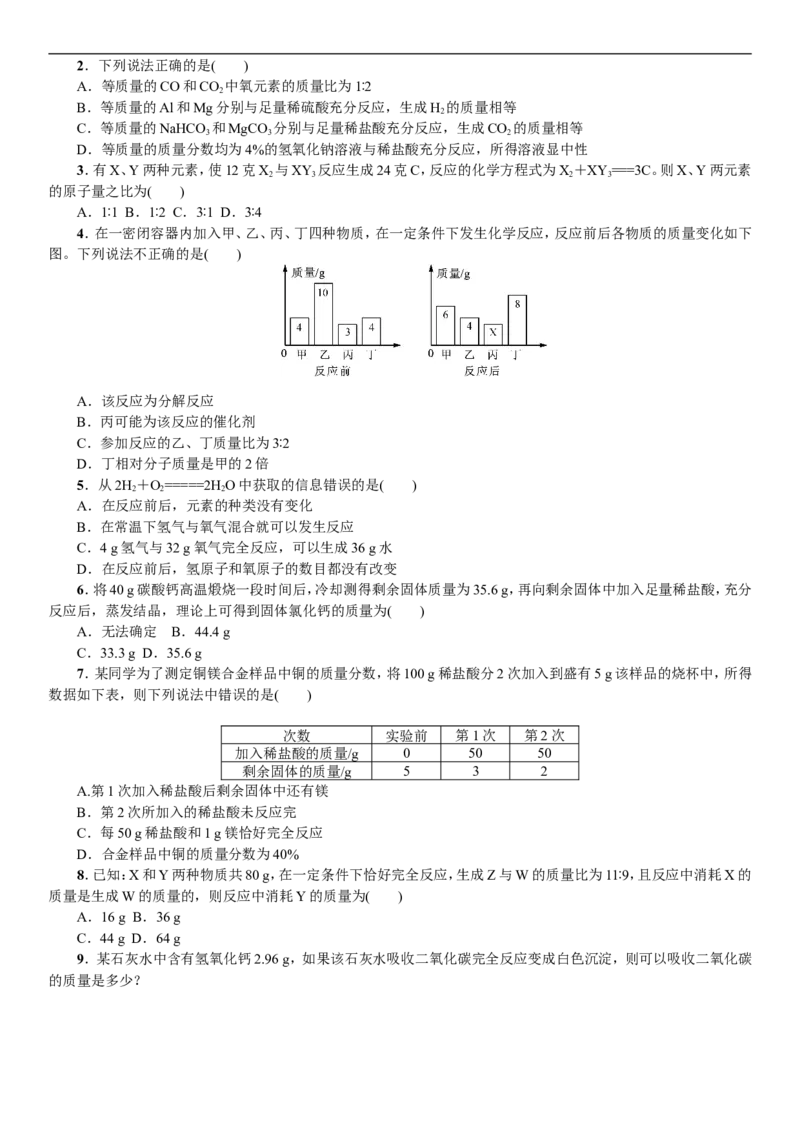
4.在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如下
图。下列说法不正确的是( )
A.该反应为分解反应
B.丙可能为该反应的催化剂
C.参加反应的乙、丁质量比为3∶2
D.丁相对分子质量是甲的2倍
5.从2H+O=====2HO中获取的信息错误的是( )
2 2 2
A.在反应前后,元素的种类没有变化
B.在常温下氢气与氧气混合就可以发生反应
C.4 g氢气与32 g氧气完全反应,可以生成36 g水
D.在反应前后,氢原子和氧原子的数目都没有改变
6.将40 g碳酸钙高温煅烧一段时间后,冷却测得剩余固体质量为35.6 g,再向剩余固体中加入足量稀盐酸,充分
反应后,蒸发结晶,理论上可得到固体氯化钙的质量为( )
A.无法确定 B.44.4 g
C.33.3 g D.35.6 g
7.某同学为了测定铜镁合金样品中铜的质量分数,将100 g稀盐酸分2次加入到盛有5 g该样品的烧杯中,所得
数据如下表,则下列说法中错误的是( )
次数 实验前 第1次 第2次
加入稀盐酸的质量/g 0 50 50
剩余固体的质量/g 5 3 2
A.第1次加入稀盐酸后剩余固体中还有镁
B.第2次所加入的稀盐酸未反应完
C.每50 g稀盐酸和1 g镁恰好完全反应
D.合金样品中铜的质量分数为40%
8.已知:X和Y两种物质共80 g,在一定条件下恰好完全反应,生成Z与W的质量比为11∶9,且反应中消耗X的
质量是生成W的质量的,则反应中消耗Y的质量为( )
A.16 g B.36 g
C.44 g D.64 g
9.某石灰水中含有氢氧化钙2.96 g,如果该石灰水吸收二氧化碳完全反应变成白色沉淀,则可以吸收二氧化碳
的质量是多少?10.小明喜欢养金鱼,他上网查阅资料得知:鱼缸中每升水的溶氧量低于0.003 g时,鱼就会死亡。过氧化钙
(CaO)是一种化学增氧剂,其反应原理是2CaO+2HO===2Ca(OH) +O↑。请回答:
2 2 2 2 2
(1)氧气在水中的溶解度随温度的升高而________。
(2)小明将2.88 g过氧化钙放入盛有200 L水的鱼缸中,请你通过计算分析,当氧气完全释放后,鱼缸中水的溶氧
量是否符合最低要求?(假设产生的氧气完全溶于水,其他因素忽略不计)
11.某品牌洁厕灵的成分是硫酸与盐酸的混合溶液。某课外活动小组想测定20 g该品牌洁厕灵溶液中HSO 和
2 4
HCl的质量。取20 g该品牌的洁厕灵溶液于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,反应过程中烧
杯中产生沉淀质量和烧杯中溶液pH变化的部分数据如下所示:
滴加氢氧化钡溶液的质量/g 5 10 25
烧杯中产生沉淀的质量/g 1.165 2.33 4.66
已知BaCl 溶液的pH=7,Ba的相对原子质量为137。求:20 g该品牌洁厕灵溶液中HSO 的质量和HCl的质量。
2 2 4
题型之三 有关化学方程式与溶液的综合计算
近几年的中考化学计算题多与溶液结合,且出题形式多样,表格数据、图像、标签等形式反映数量关系的题目较
多,这就要求能树立全面联系的观点,并能从文字、表格和图像中提取解决问题的信息。
出题常见的类型有与含杂质的物质参加反应相结合的溶质质量分数的计算。注意杂质溶解与不溶解,能否计入
溶质和溶液的总质量。与函数图像、图文、数据表相结合的计算。
解题时,要善于将综合题分解成几个单一的计算,理清思路,寻找突破口,拟定解题步骤。
某化学兴趣小组对某铜锌合金样品进行探究实验。称取样品10.0克,再用100.0克稀硫酸溶液逐滴滴入,
实验情况如图所示。求:(1)铜锌合金中,Zn的质量分数是________。
(2)所用稀硫酸溶液中溶质的质量分数是多少?
思路点拨:本题考点是化学反应方程式的计算和有关溶质质量分数的简单计算,由于铜为氢以后的金属,不能和
酸发生置换反应,因此合金中只有锌参加反应。根据题意,锌与稀硫酸反应生成硫酸锌和氢气;由反应的实验情况图,
完全反应后剩余固体的质量为3.5 g,即铜锌合金样品中含铜的质量为3.5 g;则锌的质量为10 g-3.5 g=6.5 g;将锌
的质量代入方程式,计算出参加反应硫酸的质量,进而可计算出所用稀硫酸溶液中溶质的质量分数。
1.一块表面氧化的铝片质量为15.6克,将其放入烧杯中,加入213克稀硫酸,恰好完全反应,反应后,称量得烧
杯中溶液质量为228克。
[提示:Al O+3HSO ===Al(SO )+3HO;2Al+3HSO ===Al(SO )+3H↑]求:
2 3 2 4 2 4 3 2 2 4 2 4 3 2
(1)生成氢气的质量为________克。
(2)反应后所得溶液中溶质的质量分数。
2.课外活动小组的同学为测定某盐酸中溶质的质量分数,将50 g该盐酸滴入40 g质量分数为10%的氢氧化钠溶液
中,恰好完全反应。计算该盐酸中溶质的质量分数。(计算结果精确到0.1%)3.某碳酸钠样品含有少量的硫酸钠,取一定质量的该样品,完全溶解在水中配制成100 g溶液,将其全部加入到
100 g一定质量分数的硫酸溶液中,恰好完全反应,生成的气体全部逸出后,所得溶液质量是195.6 g,将溶液蒸干,得
到15.6 g硫酸钠。
计算:
(1)加入的硫酸溶液的溶质质量分数;
(2)原碳酸钠样品中碳酸钠的质量分数(计算结果精确到0.1%)。
4.为测定某AgNO 溶液的溶质质量分数,用溶质质量分数为7.3%的稀盐酸进行滴定。现取待测液50.0 g,滴定
3
过程如图所示。
(滴定反应为:AgNO+HCl===AgCl↓+HNO,Ag的相对原子质量为108,计算结果均保留1位小数)
3 3
(1)AgNO 的相对分子质量为:________;
3
(2)计算AgNO 溶液的溶质质量分数;
3(3)计算恰好完全反应时,所得溶液的溶质质量分数。
5.某课外活动小组为测定某不纯锌粒中含锌的质量分数,取来了一些锌粒样品,并取稀硫酸800 g,平均分成4
份,将四份不同质量的样品加入到四份稀硫酸中,进行实验(杂质不与稀硫酸反应),结果如下:
实验 1 2 3 4
加入样品的质量/g 6.5 13 19.5 26
生成H 的质量/g 0.16 0.32 0.40 m
2
(1)上表中m的数值是________;
(2)试计算这种锌粒样品中锌的质量分数(写出计算过程)。
6.欲测定某锌-铜合金中铜的质量分数,进行如下实验:取合金样品10 g放入烧杯中,将60 g稀硫酸分三次加
入,充分反应后,测得生成气体的质量如下:
实验次数 第一次 第二次 第三次
加入稀硫酸质量/g 20 20 20
生成气体质量/g 0.08 m 0.04
请回答下列问题并计算:
(1)第二次实验时生成气体质量m=________g;
(2)计算该合金样品中铜的质量分数。7.烧杯中装有一定量盐酸和硫酸铜的混合溶液,已知该溶液中含HCl的质量为3.65 g。某同学为测定该混合溶
液中硫酸铜的质量,向烧杯中逐渐加入10%的NaOH溶液,得到沉淀的质量如下表所示:
加入NaOH溶液的质量/g 20.0 40.0 60.0 80.0 100.0
生成沉淀的质量/g 0.0 0.00 2.45 4.90 4.90
请回答下列问题:
(1)最终得到沉淀的总质量为________g,该混合溶液中硫酸铜的质量为________g。
(2)参加反应的NaOH溶液的总质量是多少克?(要求写出计算过程,保留小数点后面一位)
8.小红同学在网店花了200元买了一个10克的手镯(银锌合金),她想探究此手镯中银的含量,于是请化学老师
和她一起探究,在实验室用足量的稀硫酸分多次与手镯充分反应,实验数据如下:
稀硫酸/g 10 10 10 10 10
剩余固体质量/g 8.7 7.4 6.1 4.8 4.8
根据上表中的数据分析,完成下列问题:
(1)如果小红用所得的银制作一枚戒指,其质量不超过多少克?(2)计算所用稀硫酸的溶质质量分数是多少?
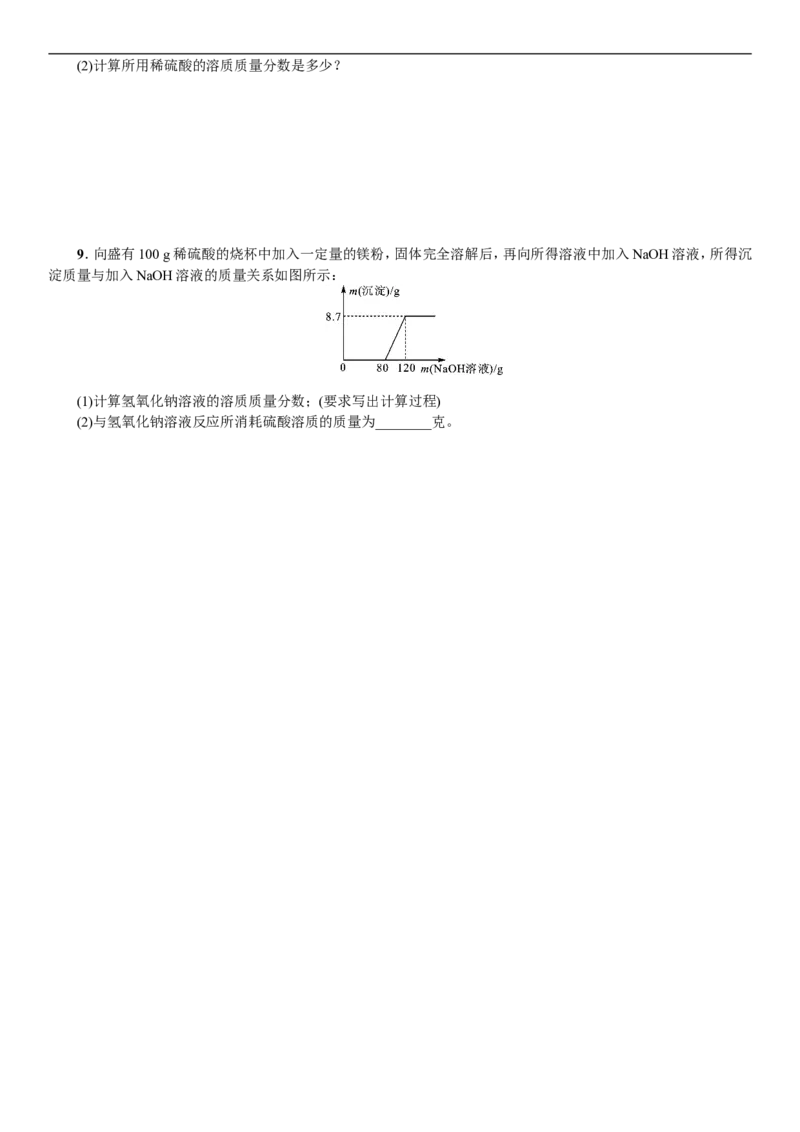
9.向盛有100 g稀硫酸的烧杯中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入NaOH溶液,所得沉
淀质量与加入NaOH溶液的质量关系如图所示:
(1)计算氢氧化钠溶液的溶质质量分数;(要求写出计算过程)
(2)与氢氧化钠溶液反应所消耗硫酸溶质的质量为________克。10.我市盛产石灰石,主要成分是CaCO 。某同学为了测定石灰石中碳酸钙的质量分数进行了如下实验。取一定
3
量的石灰石样品研碎和100 g溶质质量分数为10%的稀盐酸放入烧杯中。在化学反应过程中对烧杯及其中的剩余物
进行了五次称量,记录数据如下表:(假设反应匀速进行;杂质不溶于水,也不与稀盐酸反应,烧杯的质量为25 g)
反应时间/s 20 40 60 80 100
烧杯和药品质量/g 137.8 135.6 m 134.5 134.5
请计算:
(1)表中的“m”为________g;
(2)该石灰石样品中碳酸钙的质量分数。(计算结果精确至0.1%)
11.如图是某胃药标签的部分内容。小明同学测定该药品中NaHCO 含量的过程如下:取10粒该药剂研碎后放
3
入烧杯中,加入50克水后充分搅拌,再向其中滴加稀盐酸至溶液的pH=7时(已知药品中的其他成分既不溶于水,也
不与稀盐酸反应),形成NaCl的不饱和溶液,共消耗稀盐酸11.5克。称得反应后烧杯内物质的总质量为64.3克。请计
算:
(1)反应完成后生成气体的质量为________。
(2)反应后烧杯中溶液的质量和胃药中NaHCO 的质量分数。
312.如图是实验室所用盐酸试剂瓶上标签的部分内容,请仔细阅读后计算:
盐酸
体积:500 mL
化学式:HCl
相对分子质量:36.5
密度:1.18 g·cm-3
质量分数:37%
(1)欲配制溶质质量分数为5%的稀盐酸溶液200 g,需要溶质质量
分数为37%的浓盐酸多少毫升?(计算结果保留小数点后一位)
(2)化学综合实践活动小组的同学,对一造纸厂排放的污水进行检测,发现其主要的污染物为氢氧化钠。为了测
定污水中氢氧化钠的含量,他们量取80 g污水于烧杯中,逐滴加入溶质质量分数为5%的稀盐酸至73 g时恰好完全
反应(污水中的其他成分不与盐酸反应)。求污水中氢氧化钠的质量分数。
参考答案
题型之一 根据化学式的计算
例1 (1)3 (2)45 342 (3)1∶8
针对训练1.D 2.A 3.C 4.(1)4∶9 (2)114 5.(1)3 (2)6∶1 6.(1)C (2)152 (3)12 7.Al O 102 AlCl 133.5 8.
2 3 3
(1)4 (2)2 (3)96 9.(1)3 (2)①3 ②500 (3)酸 10.(1)7+10+5=22(个) (2)12×7∶1×10∶16×5=42∶5∶40
11.(1)KCl的相对分子质量为:39+35.5=74.5;
(2)设一个人每天摄入该品牌低钠盐不宜超过的质量为x。
x×70%×=2.3 g x=8.4 g
答:一个人每天摄入该品牌低钠盐的质量不宜超过8.4 g。
题型之二 有关化学方程式的计算
例2 (1)4.4 g
(2)设样品中碳酸钾的质量为x。
KCO+2HCl===2KCl+CO↑+HO
2 3 2 2
138 44
x 4.4 g
= x=13.8 g
样品中氯化钾的质量分数为×100%=86.2%
答:样品中氯化钾的质量分数为86.2%。
针对训练
1.A 2.C 3.C 4.D 5.B 6.B 7.C 8.D
9.设吸收二氧化碳的质量为x。
Ca(OH) +CO===CaCO ↓+HO
2 2 3 2
74 44
2.96 g x
= x=1.76 g
答:吸收二氧化碳的质量为1.76 g。
10.(1)减小 (2)设2.88 g CaO 完全反应生成O 的质量为x。
2 2
2CaO+2HO===2Ca(OH) +O↑
2 2 2 2
144 32
2.88 g x
= x=0.64 g
则鱼缸中水的溶氧量为0.64 g÷200 L=0.003 2 g/L
因为0.003 2 g/L>0.003 g/L
所以鱼缸中水的溶氧量符合最低要求。
11.由题意可知:HSO 完全反应后产生BaSO 沉淀的质量是4.66 g。
2 4 4
设20 g该品牌洁厕灵溶液中HSO 的质量为x。
2 4
Ba(OH) +HSO ===BaSO ↓+2HO
2 2 4 4 2
98 233
x 4.66 g
= x=1.96 g
由题意可知:与HCl完全反应的Ba(OH) 溶液的质量为:60 g-20 g=40 g。
2
设20 g该品牌洁厕灵溶液中HCl的质量为y。
Ba(OH) +2HCl===BaCl +2HO
2 2 2
171 73
40 g×17.1% y
= y=2.92 g
答:20 g该品牌洁厕灵溶液中HSO 的质量为1.96 g,HCl的质量为2.92 g。
2 4
题型之三 有关化学方程式与溶液的综合计算
例3 (1)由图知,完全反应后剩余固体的质量为3.5 g,即铜锌合金样品中铜的质量为3.5 g,则锌的质量为10 g
-3.5 g=6.5 g。
铜锌合金中,Zn的质量分数是×100%=65%。
(2)设反应中消耗稀硫酸溶液中溶质的质量为x。Zn+HSO ===ZnSO +H↑
2 4 4 2
65 98
6.5 g x
= x=9.8 g
所用稀硫酸溶液中溶质的质量分数为:×100%=19.6%。
答:所用稀硫酸溶液中溶质的质量分数是19.6%。
针对训练
1.(1)0.6 设氧化的铝片中铝的质量为x,生成硫酸铝的质量为y。
2Al+3HSO ===Al(SO )+3H↑
2 4 2 4 3 2
54 342 6
x y 0.6 g
= x=5.4 g
= y=34.2 g
氧化的铝片中氧化铝的质量为15.6 g-5.4 g=10.2 g
设氧化铝与硫酸反应生成硫酸铝的质量为z。
Al O+3HSO ===Al(SO )+3HO
2 3 2 4 2 4 3 2
102 342
10.2 g z
= z=34.2 g
反应后所得溶液的溶质质量分数为×100%=30%
答:略。
2.设盐酸中溶质的质量为x。
NaOH + HCl===NaCl+HO
2
40 36.5
40 g×10% x
= x=3.65 g
盐酸中溶质的质量分数为×100%=7.3%
答:略。
3.生成二氧化碳的质量:100 g+100 g-195.6 g=4.4 g
设样品中NaCO 的质量为x,反应的硫酸质量为y,生成NaSO 的质量为z。
2 3 2 4
NaCO+HSO ===Na SO +HO+CO↑
2 3 2 4 2 4 2 2
106 98 142 44
x y z 4.4 g
= = =
x=10.6 g y=9.8 g z=14.2 g
硫酸溶液中溶质的质量分数:×100%=9.8%
原样品的质量为:10.6 g+(15.6 g-14.2 g)=12 g
原样品中碳酸钠的质量分数为:×100%=88.3%
答:略。
4.(1)170 (1)AgNO 的相对分子质量=108+14+16×3=170;
3
(2)根据图像可知,当加入10克稀盐酸溶液时,沉淀的质量达到最大值(2.87克),
设AgNO 溶液的溶质质量是x,生成硝酸质量为y。
3
AgNO+HCl===AgCl↓+HNO
3 3
170 143.5 63
x 2.87 g y
= x=3.4 g
= y=1.26 g
AgNO 溶液的溶质质量分数:×100%=6.8%;
3
(3)恰好完全反应时,所得溶液的溶质质量分数为×100%=2.2%。答:略。
5.(1)0.40 设13 g不纯锌粒中Zn的质量为x。
Zn+HSO ===ZnSO +H↑
2 4 4 2
65 2
x 0.32 g
= x=10.4 g
锌粒样品中锌的质量分数为×100%=80%
答:锌粒样品中锌的质量分数为80%。(其他合理解法均可)
6.(1)0.08 (2)合金共产生氢气的质量为0.08 g+0.08 g+0.04 g=0.2 g
设该合金样品中锌的质量为x。
Zn+HSO ===ZnSO +H↑
2 4 4 2
65 2
x 0.2 g
= x=6.5 g
样品中铜的质量为10 g-6.5 g=3.5 g
铜的质量分数为×100%=35%
答:该合金样品中铜的质量分数为35%。
7.(1)4.90 8.0 设与盐酸和硫酸铜完全反应的氢氧化钠的质量分别为x和y。
HCl+NaOH===NaCl+HO
2
36.5 40
3.65 g x
= x=4.0 g
CuSO +2NaOH===Cu(OH) ↓+NaSO
4 2 2 4
80 98
y 4.90 g
= y=4.0 g
共用NaOH质量为8.0 g,氢氧化钠溶液总质量为=80.0 g
答:略。
8.(1)4.8克 (2)设10 g稀硫酸中溶质HSO 的质量为x。
2 4
Zn+HSO ===ZnSO +H↑
2 4 4 2
65 98
1.3 g x
= x=1.96 g
稀硫酸的溶质质量分数为×100%=19.6%
答:略。
9.(1)设与硫酸镁反应消耗NaOH的质量为x。
2NaOH+MgSO ===Mg(OH) ↓+NaSO
4 2 2 4
80 58
x 8.7 g
= x=12 g
NaOH溶液的溶质质量分数=×100%=30%
(2)设与氢氧化钠溶液反应所消耗硫酸溶质的质量为y。
2NaOH+HSO ===2H O+NaSO
2 4 2 2 4
80 98
80 g×30% y
= y=29.4 g
答:氢氧化钠溶液的溶质质量分数为30%,与氢氧化钠溶液反应所消耗硫酸溶质的质量为29.4 g。
10.(1)134.5 (2)137.8 g-135.6 g=2.2 g,135.6 g-134.5 g=1.1 g,共产生二氧化碳的质量为2.2 g+2.2 g+1.1 g
=5.5 g。设石灰石样品中碳酸钙的质量为x。
CaCO +2HC1===CaCl +HO+CO↑
3 2 2 2
100 44
x 5.5 g
= x=12.5 g
134.5 g+5.5 g-25 g-100 g=15 g
×100%=83.3%
答:该石灰石样品中碳酸钙的质量分数为83.3%。
11.(1)每粒0.5 g,10粒该药剂的质量为0.5 g×10=5 g。由质量守恒定律,生成二氧化碳气体的质量为5 g+50 g
+11.5 g-64.3 g=2.2 g。
(2)设参加反应的碳酸氢钠的质量为x。
NaHCO +HCl===NaCl+HO+CO↑
3 2 2
84 44
x 2.2 g
= x=4.2 g
反应后烧杯中溶液的质量为4.2 g+50 g+11.5 g-2.2 g=63.5 g。
胃药中NaHCO 的质量分数为×100%=84%。
3
答:反应后烧杯中溶液的质量为63.5 g;胃药中NaHCO 的质量分数为84%。
3
12.(1)200 g×5%=浓盐酸的体积×1.18 g·cm-3×37% 解得:浓盐酸的体积≈22.9 mL
(2)设污水中氢氧化钠的质量为x。
NaOH+HCl===NaCl+HO
2
40 36.5
x 5%×73 g
= x=4 g
污水中氢氧化钠的质量分数=×100%=5%
答:(1)需要溶质质量分数为37%的浓盐酸约22.9毫升。(2)污水中氢氧化钠的质量分数为5%。