文档内容
九年级(上)期末化学期末试卷附答案
一、本大题包括10小题,每小题2分,共20分.每小题的备选答案中只有一个答案符合题意,请将选出的选项序号填
入下面答题表内
1.(2分)某科学家在一次化学论坛会上提出“化学不是问题,化学解决问题”的观点,则下列叙述不合理的是
( )
A.利用化学合成药物,保障了人体健康
B.利用化学开发新材料,改善人类生存条件
C.利用化学保护环境,使人类生活得更美好
D.化石燃料的直接利用,促进了低碳经济的发展
2.(2分)为了鉴别二氧化碳、氧气、空气三种气体,可以选用的最佳方法是( )
A.将气体分别通入水中 B.将气体分别通入澄清石灰水中
C.分别将带火星的木条伸入气体中 D.将燃着的木条分别伸入气体中
3.(2分)(2008•上海)钒(V)被誉为金属中的“维生素”,其氧化物V O 中钒元素的化合价是( )
2 5
A.+1 B.+3 C.+5 D.+7
4.(2分)猪血中含有卟啉铁(C H C1FeN O )对缺铁性贫血有显著效果.以下说法不正确的是( )
34 32 4 4
A.卟啉铁中含有6种元素 B.干净的猪血是化合物
C.卟啉铁中碳元素的质量分数最大 D.人体补铁还有其他方法
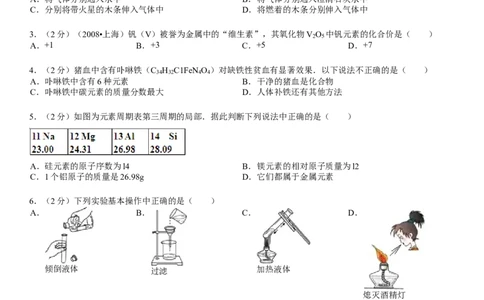
5.(2分)如图为元素周期表第三周期的局部.据此判断下列说法中正确的是( )
A.硅元素的原子序数为l4 B.镁元素的相对原子质量为l2
C.1个铝原子的质量是26.98g D.它们都属于金属元素
6.(2分)下列实验基本操作中正确的是( )
A. B. C. D.
倾倒液体 过滤 加热液体
熄灭酒精灯
7.(2分)在飞船的火箭推进器中常装有液态肼[N H 和过氧化氢[H O ,它们混合时的反应方程式为:
2 4 2 2
2H O +N H ═N +nH O,则下列说法正确的是( )
2 2 2 4 2 2
] ]
A.该反应为置换反应 B.反应前后原子总数发生变化
C.该化学方程式中n=4 D.氮是地壳中含量最高的元素
8.(2分)科学家已研制出新型的氧分子O ,对其说法正确的是( )
4
A.O 和O 都是由氧元素组成的单质 B.O 是一种新型的化合物
4 2 4
C.1个O 分子中含有2个O 分子 D.O 与O 的性质一定相同
4 2 2 4
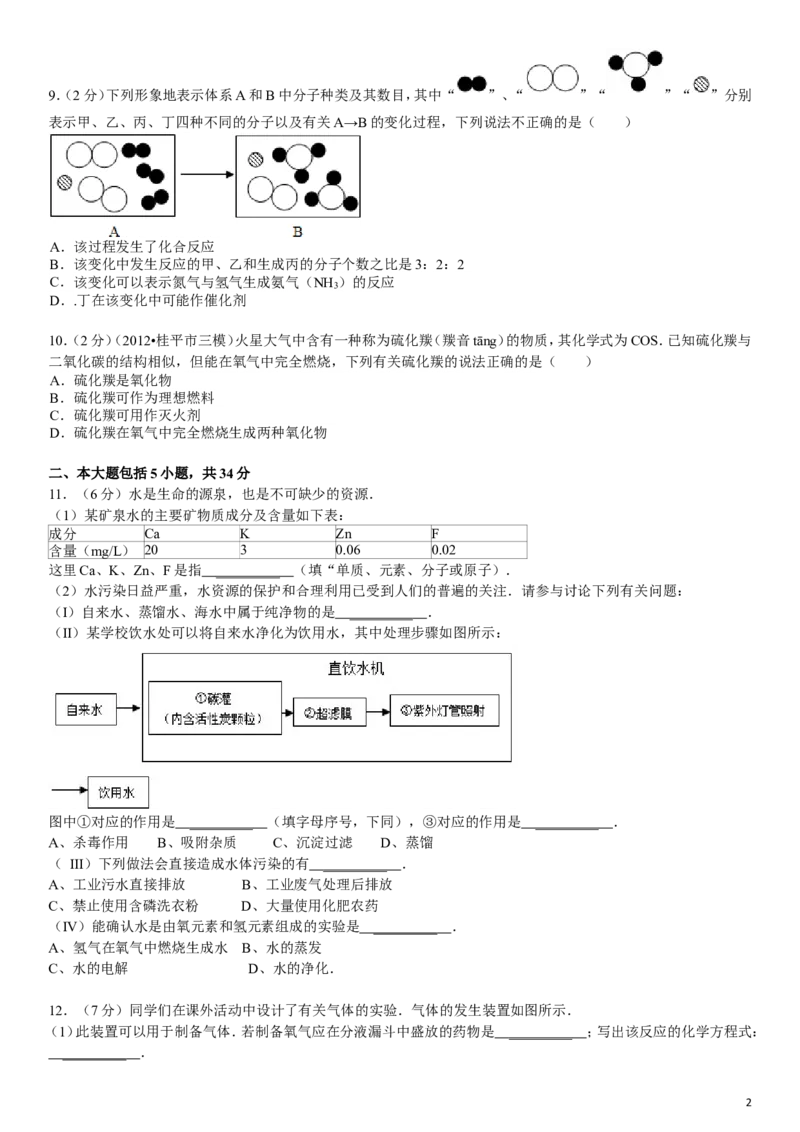
19.(2分)下列形象地表示体系A和B中分子种类及其数目,其中“ ”、“ ”“ ”“ ”分别
表示甲、乙、丙、丁四种不同的分子以及有关A→B的变化过程,下列说法不正确的是( )
A.该过程发生了化合反应
B.该变化中发生反应的甲、乙和生成丙的分子个数之比是3:2:2
C.该变化可以表示氮气与氢气生成氨气(NH )的反应
3
D..丁在该变化中可能作催化剂
10.(2分)(2012•桂平市三模)火星大气中含有一种称为硫化羰(羰音tāng)的物质,其化学式为COS.已知硫化羰与
二氧化碳的结构相似,但能在氧气中完全燃烧,下列有关硫化羰的说法正确的是( )
A.硫化羰是氧化物
B.硫化羰可作为理想燃料
C.硫化羰可用作灭火剂
D.硫化羰在氧气中完全燃烧生成两种氧化物
二、本大题包括5小题,共34分
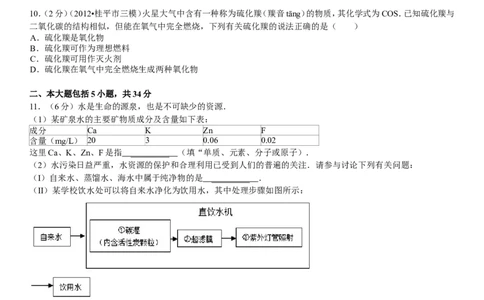
11.(6分)水是生命的源泉,也是不可缺少的资源.
(1)某矿泉水的主要矿物质成分及含量如下表:
成分 Ca K Zn F
含量(mg/L) 20 3 0.06 0.02
这里Ca、K、Zn、F是指 ________ _ (填“单质、元素、分子或原子).
(2)水污染日益严重,水资源的保护和合理利用已受到人们的普遍的关注.请参与讨论下列有关问题:
(I)自来水、蒸馏水、海水中属于纯净物的是 ________ _ .
(II)某学校饮水处可以将自来水净化为饮用水,其中处理步骤如图所示:
图中①对应的作用是 ________ _ (填字母序号,下同),③对应的作用是 ________ _ .
A、杀毒作用 B、吸附杂质 C、沉淀过滤 D、蒸馏
( III)下列做法会直接造成水体污染的有 ________ _ .
A、工业污水直接排放 B、工业废气处理后排放
C、禁止使用含磷洗衣粉 D、大量使用化肥农药
(IV)能确认水是由氧元素和氢元素组成的实验是 ________ _ .
A、氢气在氧气中燃烧生成水 B、水的蒸发
C、水的电解 D、水的净化.
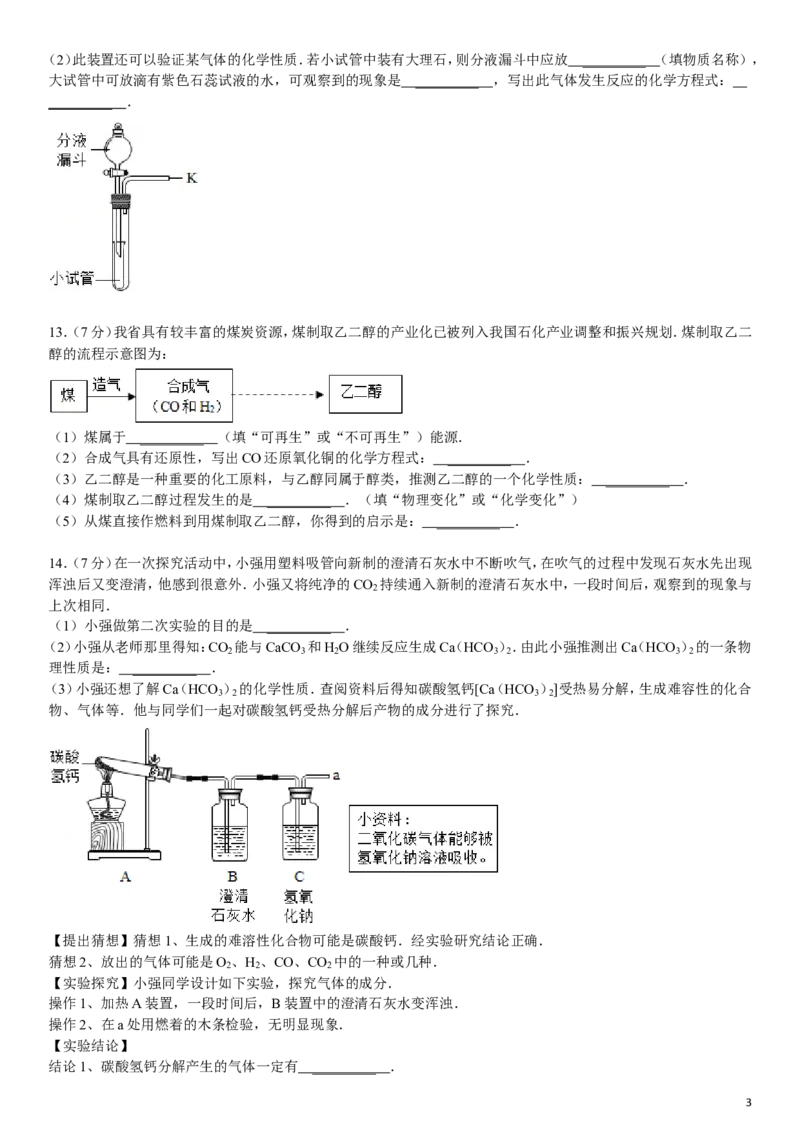
12.(7分)同学们在课外活动中设计了有关气体的实验.气体的发生装置如图所示.
(1)此装置可以用于制备气体.若制备氧气应在分液漏斗中盛放的药物是 ________ _ ;写出该反应的化学方程式:
________ _ .
2(2)此装置还可以验证某气体的化学性质.若小试管中装有大理石,则分液漏斗中应放 ________ _ (填物质名称),
大试管中可放滴有紫色石蕊试液的水,可观察到的现象是 ________ _ ,写出此气体发生反应的化学方程式:
_________ .
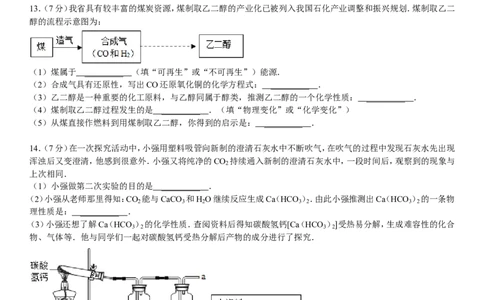
13.(7分)我省具有较丰富的煤炭资源,煤制取乙二醇的产业化已被列入我国石化产业调整和振兴规划.煤制取乙二
醇的流程示意图为:
(1)煤属于 ________ _ (填“可再生”或“不可再生”)能源.
(2)合成气具有还原性,写出CO还原氧化铜的化学方程式: ________ _ .
(3)乙二醇是一种重要的化工原料,与乙醇同属于醇类,推测乙二醇的一个化学性质: ________ _ .
(4)煤制取乙二醇过程发生的是 ________ _ .(填“物理变化”或“化学变化”)
(5)从煤直接作燃料到用煤制取乙二醇,你得到的启示是: ________ _ .
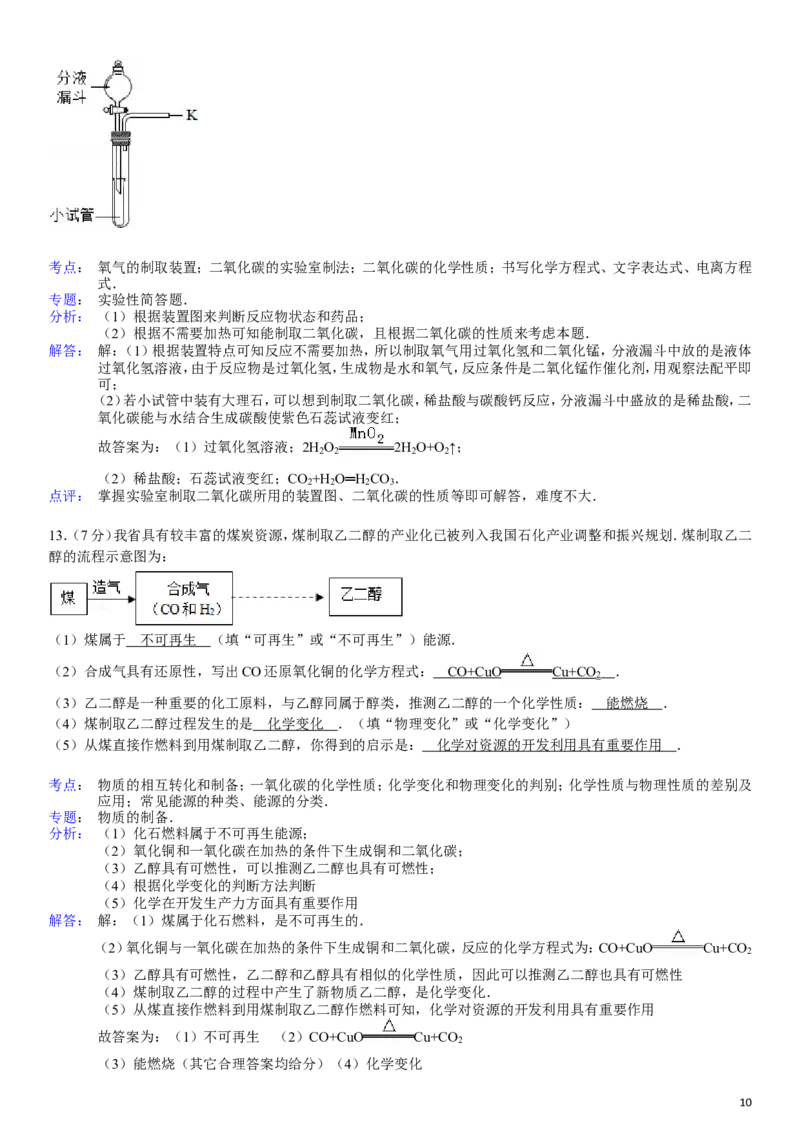
14.(7分)在一次探究活动中,小强用塑料吸管向新制的澄清石灰水中不断吹气,在吹气的过程中发现石灰水先出现
浑浊后又变澄清,他感到很意外.小强又将纯净的CO 持续通入新制的澄清石灰水中,一段时间后,观察到的现象与
2
上次相同.
(1)小强做第二次实验的目的是 ________ _ .
(2)小强从老师那里得知:CO 能与CaCO 和H O继续反应生成Ca(HCO ).由此小强推测出Ca(HCO )的一条物
2 3 2 3 2 3 2
理性质是: ________ _ .
(3)小强还想了解Ca(HCO )的化学性质.查阅资料后得知碳酸氢钙[Ca(HCO ) 受热易分解,生成难容性的化合
3 2 3 2
物、气体等.他与同学们一起对碳酸氢钙受热分解后产物的成分进行了探究.
]
【提出猜想】猜想1、生成的难溶性化合物可能是碳酸钙.经实验研究结论正确.
猜想2、放出的气体可能是O 、H 、CO、CO 中的一种或几种.
2 2 2
【实验探究】小强同学设计如下实验,探究气体的成分.
操作1、加热A装置,一段时间后,B装置中的澄清石灰水变浑浊.
操作2、在a处用燃着的木条检验,无明显现象.
【实验结论】
结论1、碳酸氢钙分解产生的气体一定有 ________ _ .
3结论2、碳酸氢钙受热分解的方程式为 ________ _ .
【表达交流】
交流1、从安全的角度考虑,操作2实验中存在的不足是 ________ _ .
交流2、小组内某同学对上述结论提出异议:
该同学的观点 请说出你的观点并阐述理由
该实验怎么没有对氧气进行验证 ________ _
15.(7分)学习了第六单元后,许多同学对璀璨夺目的金刚石是由碳元素组成的单质提出疑问,为研究金刚石的组成,
某研究小组进行了如下探究,请你帮助一起完成.
(1)小明设计的实验:将几颗细小颗粒的金刚石放入含有氧气的密闭容器内通过聚光法将其点燃,在产物中滴加澄清
的石灰水.
(2)分析、得出结论:小明通过聚光法使 ________ _ 从而金刚石燃烧起来,说明金刚石确有 ________ _ 性;澄
清的石灰水变浑浊,写出发生反应的化学方程式 ________ _ ,说明此反应生成了二氧化碳气体,从而小明得出金
刚石是由碳元素组成的单质.
(3)反思:用细小颗粒的金刚石进行实验的原因 ________ _ .
小明根据实验得出金刚石是由碳元素组成的单质的结论能否成立?请说明理由: ________ _
如果你能设计一个合理的实验,将奖励4分(化学试卷总分不超过60分)
________ _ .
三、本大题共6分
16.(6分)某大理石厂开采出来的大理石产品,为了检测大理石中碳酸钙的纯度,检测员称取了大理石样品20g,与
足量的稀盐酸反应,共收集到气体6.6g,则该大理石中碳酸钙的质量分数是多少?
4参考答案与试题解析
一、本大题包括10小题,每小题2分,共20分.每小题的备选答案中只有一个答案符合题意,请将选出的选项序号填
入下面答题表内
1.(2分)某科学家在一次化学论坛会上提出“化学不是问题,化学解决问题”的观点,则下列叙述不合理的是
( )
A.利用化学合成药物,保障了人体健康
B.利用化学开发新材料,改善人类生存条件
C.利用化学保护环境,使人类生活得更美好
D.化石燃料的直接利用,促进了低碳经济的发展
考点: 化学的用途.
2243409
专题: 化学与生活.
分析: 利用化学合成药物,保障人体健康;利用化学开发新材料,改善人类生存条件;利用化学保护环境,使人类生
活得更美好,可以据此解答该题.
解答: 解:A、利用化学合成药物,保障人体健康,如青霉素可以消炎杀菌,保障人体健康,故A正确;
B、利用化学开发新材料,改善人类生存条件,如飞机、汽车的各种制作材料,都是利用化学技术开发的新能
源,故B正确;
C、利用化学保护环境,使人类生活得更美好,如化学技术治理水污染,故C正确;
D、化石燃料中含有多种元素和物质,综合利用更能够体现它们的价值,故D错误.
故选D.
点评: 化学可以改变人类的生存条件,同时它的一些负面影响,给人类带来了灾难,我们人类应珍惜自己的生存环
境.
2.(2分)为了鉴别二氧化碳、氧气、空气三种气体,可以选用的最佳方法是( )
A.将气体分别通入水中 B.将气体分别通入澄清石灰水中
C.分别将带火星的木条伸入气体中 D.将燃着的木条分别伸入气体中
考点: 常见气体的检验与除杂方法.
2243409
专题: 物质的鉴别题.
分析: 一次性鉴别空气、氧气和二氧化碳三瓶无色气体,要求根据三种气体性质差别,所设计的方案能出现三种明
显不同的实验现象,达到鉴别气体的目的.
解答: 解:A、将气体分别通入水中,三种气体均不能产生明显现象,无法完成鉴别.
B、分别通入澄清石灰水只有二氧化碳能使澄清石灰水变浑浊,难以鉴别气体是空气和氧气.方案不可行;
C、将带火星的木条伸入瓶中,木条复燃的气体为氧气;木条在空气和二氧化碳中都有可能熄灭,现象不明
显,方案不可行;
D、将燃烧的木条伸入瓶中,木条燃烧无明显变化的气体为空气;木条燃烧更旺的气体为氧气;木条熄灭的气
体为二氧化碳气体.现象明显,方案可行;
故选D.
点评: 本题主要考查学生对氧气、空气、二氧化碳这三种气体的性质的了解,解题时需要认真分析题目给出的条件,
联系实际,逐一分析推断.
3.(2分)(2008•上海)钒(V)被誉为金属中的“维生素”,其氧化物V O 中钒元素的化合价是( )
2 5
A.+1 B.+3 C.+5 D.+7
考点: 有关元素化合价的计算.
2243409
专题: 化学式的计算.
分析: 根据氧化物中氧元素的化合价及化合物中各元素的正负化合价的代数和为0来解答.
解答: 解:V O 中氧元素的化合价为﹣2价,
2 5
设钒元素的化合价为+x价,
根据化合物中各元素的正负化合价的代数和为零,则
(+x)×2+(﹣2)×5=0
解得+x=+5.
故选C.
点评: 本题考查利用化学式计算元素的化合价,注意氧化物中氧元素的化合价为﹣2价是隐含信息,能正确应用化
5合物中元素的正负化合价的代数和为0.
4.(2分)猪血中含有卟啉铁(C H C1FeN O )对缺铁性贫血有显著效果.以下说法不正确的是( )
34 32 4 4
A.卟啉铁中含有6种元素 B.干净的猪血是化合物
C.卟啉铁中碳元素的质量分数最大 D.人体补铁还有其他方法
考点: 化学式的书写及意义;纯净物和混合物的判别;元素的质量分数计算.
2243409
专题: 化学用语和质量守恒定律.
分析: A、根据卟啉铁的化学式的含义进行分析判断.
B、干净的猪血中含有卟啉铁、水等物质.
C、根据化合物中元素的质量分数= ×100%,进行分析判断.
D、根据铁元素的摄入方法进行分析判断.
解答: 解:A、由卟啉铁的化学式可知,卟啉铁是由碳、氢、氯、铁、氮、氧六种元素组成的,故选项说法正确.
B、干净的猪血中含有卟啉铁、水等物质,属于混合物,故选项说法错误.
C、卟啉铁中碳原子的相对原子质量之和为12×34=408,氢原子的相对原子质量之和为1×32=32,氯原子的相
对原子质量之和为35.5,铁原子的相对原子质量之和为56,氮原子的相对原子质量之和为14×4=56,氧原子
的相对原子质量之和为16×4=64,碳元素的相对原子质量之和最大,则碳元素的质量分数最大,故选项说法
正确.
D、人体补铁还有其他方法,如使用铁锅等,故选项说法正确.
故选B.
点评: 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.
5.(2分)如图为元素周期表第三周期的局部.据此判断下列说法中正确的是( )
A.硅元素的原子序数为l4 B.镁元素的相对原子质量为l2
C.1个铝原子的质量是26.98g D.它们都属于金属元素
考点: 元素周期表的特点及其应用.
2243409
专题: 化学用语和质量守恒定律.
分析: 根据元素周期表中的信息,原子序数=核外电子数=质子数,元素符号、元素名称及相对原子质量进行解答.
解答: 解:根据元素周期表中的信息,可判断:
A.硅元素的原子序数为l4,故A说法正确;
B.镁元素的相对原子质量为24.31,故B说法错误;
C.相对原子质量是有单位的,其单位为“1”,铝元素的相对原子质量质量是26.98,故C说法错误;
D.硅元素属于非金属元素;故D说法错误;
故选A.
点评: 本题考查学生对元素周期表中的知识、特点的理解、掌握及其在解题中应用的能力.
6.(2分)下列实验基本操作中正确的是( )
A. B. C. D.
倾倒液体 过滤 加热液体
熄灭酒精灯
考点: 液体药品的取用;加热器皿-酒精灯;给试管里的液体加热;过滤的原理、方法及其应用.
2243409
专题: 常见仪器及化学实验基本操作.
分析: A、根据向试管中倾倒液体药品的方法进行分析判断.
B、过滤液体时,注意“一贴、二低、三靠”的原则.
C、根据给试管中的液体加热的方法进行分析判断.
6D、使用酒精灯时要注意“两查、两禁、一不可”.
解答: 解:A、向试管中倾倒液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨;图中瓶口没有紧挨、瓶塞没有倒
放、标签没有向着手心,所示操作错误.
B、过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流、漏斗下端没有紧靠在烧杯内壁
上,图中所示操作错误.
C、给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管容积的 ,图中所
示操作正确.
D、使用酒精灯时要注意“两查、两禁、一不可”,不能用嘴吹灭酒精灯,应用灯帽盖灭,图中所示操作错误.
故选C.
点评: 本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试
题的关键.
7.(2分)在飞船的火箭推进器中常装有液态肼[N H 和过氧化氢[H O ,它们混合时的反应方程式为:
2 4 2 2
2H O +N H ═N +nH O,则下列说法正确的是( )
2 2 2 4 2 2
] ]
A.该反应为置换反应 B.反应前后原子总数发生变化
C.该化学方程式中n=4 D.氮是地壳中含量最高的元素
考点: 置换反应及其应用;地壳中元素的分布与含量;质量守恒定律及其应用.
2243409
专题: 结合课本知识的信息.
分析: A、根据置换反应的特点考虑;
B、根据反应前后各原子个数相等来考虑;
C、根据质量守恒定律中的原子守恒考虑;
D、根据地壳中元素的含有情况考虑.
解答: 解:A、置换反应的特点是反应物与生成物均是一种单质与一种化合物,而该反应的反应物是两种化合物,故
不是置换反应;
B、根据质量守恒定律可知化学反应前后各原子个数必然相等,所以其原子总数一定相等,故错误;
C、根据质量守恒定律可知反应前后各原子个数相等,反应物中有8个氢原子,生成物中要想有8个氢原子,n
必须为4,故正确;
D、地壳中含量最多的元素是氧元素,不是氮元素,故错误;
故选C.
点评: 本题主要考查学生运用质量守恒定律进行推断的能力.结合质量守恒的应用及反应类型的判断对所列问题
分析探讨即可.
8.(2分)科学家已研制出新型的氧分子O ,对其说法正确的是( )
4
A.O 和O 都是由氧元素组成的单质 B.O 是一种新型的化合物
4 2 4
C.1个O 分子中含有2个O 分子 D.O 与O 的性质一定相同
4 2 2 4
考点: 氧元素组成的单质;单质和化合物的判别;分子、原子、离子、元素与物质之间的关系.
2243409
专题: 结合课本知识的信息.
分析: 根据物质的化学式进行分析,新型的氧分子O 是由氧元素组成的单质.
4
解答: 解:A、O 和O 都是由氧元素组成的单质,故A正确;
4 2
B、O 是一种由氧元素组成的单质,不是化合物,故B错误;
4
C、1个O 分子中含有4个氧原子,故C错误;
4
D、O 与O 的分子构成不同,故性质不同,故D错误;
2 4
故选A.
点评: 本题考查了氧元素组成的单质,完成此题,可以依据物质的化学式进行.
9.(2分)下列形象地表示体系A和B中分子种类及其数目,其中“ ”、“ ”“ ”“ ”分别
表示甲、乙、丙、丁四种不同的分子以及有关A→B的变化过程,下列说法不正确的是( )
7A.该过程发生了化合反应
B.该变化中发生反应的甲、乙和生成丙的分子个数之比是3:2:2
C.该变化可以表示氮气与氢气生成氨气(NH )的反应
3
D..丁在该变化中可能作催化剂
考点: 微粒观点及模型图的应用;催化剂的特点与催化作用;反应类型的判定.
2243409
专题: 化学反应模拟图型.
分析: A、根据该反应为甲、乙两种物质反应生成丙物质,反应符合“多变一”的特点分析;
B、根据该反应由3个甲分子与1个乙分子发生反应,生成2个丙分子分析;
C、根据氮气与氢气生成氨气(NH )的反应就是一分子氮气与三分子氢气反应生成两分子氨气分析;
3
D、根据丁在反应前后未发生变化,可推断丁可能做催化剂可能未参与反应.
解答: 解:A、根据微观示意图可知,该反应为甲、乙两种物质反应生成丙物质,反应符合“多变一”的化合反应的
特点,故正确;
B、该反应由3个甲分子与1个乙分子发生反应,其中的1个乙分子和丁分子没有参加反应,生成2个丙分
子,因此反应中甲、乙、丙前的化学计量数之比为3:1:2;故错误;
C、氮气与氢气生成氨气(NH )的反应就是一分子氮气与三分子氢气反应生成两分子氨气;故正确;
3
D、丁在反应前后未发生变化,可推断丁可能做催化剂;故正确;
故选项为:B.
点评: 解答本题的关键是要充分理解微观示意图提供的信息,准确判断参加反应的分子和生成物的分子及催化剂
的特点进行分析.
10.(2分)(2012•桂平市三模)火星大气中含有一种称为硫化羰(羰音tāng)的物质,其化学式为COS.已知硫化羰与
二氧化碳的结构相似,但能在氧气中完全燃烧,下列有关硫化羰的说法正确的是( )
A.硫化羰是氧化物
B.硫化羰可作为理想燃料
C.硫化羰可用作灭火剂
D.硫化羰在氧气中完全燃烧生成两种氧化物
考点: 二氧化碳的化学性质;从组成上识别氧化物;完全燃烧与不完全燃烧.
2243409
专题: 结合课本知识的信息.
分析: 根据硫化羰的化学式COS及性质描述,对有关的硫化羰的说法进行正误判断;COS是有C、S、O三种元素组
成的,能燃烧,燃烧后生成二氧化碳和二氧化硫.
解答: 解:A、硫化羰由三种元素组成,而氧化物是由两种元素组成的化合物,所以硫化羰不属于氧化物,故A错误;
B、由于燃烧后又二氧化硫这种有毒的气体,所以硫化羰不可作为理想燃料,故B错误;
C、据题中描述硫化羰“能在氧气中完全燃烧”可知,硫化羰具有可燃性,所以不能用作灭火剂.故C错误;
D、根据燃烧规律:含碳元素的物质燃烧生成二氧化碳,含硫元素物质燃烧生成二氧化硫;所以由C、O、S元
素组成的硫化羰完全燃烧的产生为二氧化硫和二氧化碳,故D正确.
故选D
点评: 此题主要考查了氧化物的概念以及燃烧的有关知识,并且联系环保知识,是一道不错的考题.
二、本大题包括5小题,共34分
11.(6分)水是生命的源泉,也是不可缺少的资源.
(1)某矿泉水的主要矿物质成分及含量如下表:
成分 Ca K Zn F
含量(mg/L) 20 3 0.06 0.02
这里Ca、K、Zn、F是指 元素 (填“单质、元素、分子或原子).
(2)水污染日益严重,水资源的保护和合理利用已受到人们的普遍的关注.请参与讨论下列有关问题:
(I)自来水、蒸馏水、海水中属于纯净物的是 蒸馏水 .
(II)某学校饮水处可以将自来水净化为饮用水,其中处理步骤如图所示:
8图中①对应的作用是 B (填字母序号,下同),③对应的作用是 A .
A、杀毒作用 B、吸附杂质 C、沉淀过滤 D、蒸馏
( III)下列做法会直接造成水体污染的有 AD .
A、工业污水直接排放 B、工业废气处理后排放
C、禁止使用含磷洗衣粉 D、大量使用化肥农药
(IV)能确认水是由氧元素和氢元素组成的实验是 AC .
A、氢气在氧气中燃烧生成水 B、水的蒸发
C、水的电解 D、水的净化.
考点: 自来水的生产过程与净化方法;电解水实验;水资源的污染与防治;纯净物和混合物的判别;元素的概念.
2243409
专题: 空气与水.
分析:(1)根据水的主要矿物质中的“Ca、K、Zn、F”等不是以单质、分子、原子等形式存在,而是指元素进行解答;
(2)Ⅰ根据自来水、蒸馏水、海水的成分进行解答;
Ⅱ根据活性炭具有吸附性、紫外灯管照射有杀菌消毒的作用进行解答;
Ⅲ根据造成水体污染的途径进行解答;
Ⅳ根据水通电分解生成氢气和氧气能确认水是由氧元素和氢元素组成进行解答.
解答: 解:(1)某矿泉水中的“Ca、K、F”等不是以单质、分子、原子等形式存在,这里的“Ca、K、Zn、F”所指是元素;
(2)(Ⅰ)自来水、蒸馏水、海水中属于纯净物的是蒸馏水;
(Ⅱ)活性炭具有吸附性,能吸附水中色素及有异味的杂质,因此在自来水的净化中活性炭的作用为吸附作
用;紫外线有消毒杀菌的作用;
ⅢA.工业废水直接排放,能造成水的污染;
B.工业废气处理后排放,可有效地降低大气污染,从而不会造成水体污染;
C.禁止使用含磷洗衣粉,能防止水源的污染 ;
D.大量使用化肥、农药,对水源污染较严重;
Ⅳ能确认水是由氧元素和氢元素组成的实验要根据质量守恒定律:反应前后元素种类不变;氢气在氧气中燃
烧生成水和水通电生成氧气和氢气,都能说明水中含有氢元素和氧元素;
故答案为:
(1)、元素;(2)、(Ⅰ)、蒸馏水;(Ⅱ)、B;A;(Ⅲ)、AD; (Ⅳ)AC.
点评: 本题难度不大,掌握元素与微观粒子及物质的区别、水的净化、水体污染、硬水和软水的区分方法及应用质量
守恒定律分析和解决问题是解答本题的关键.
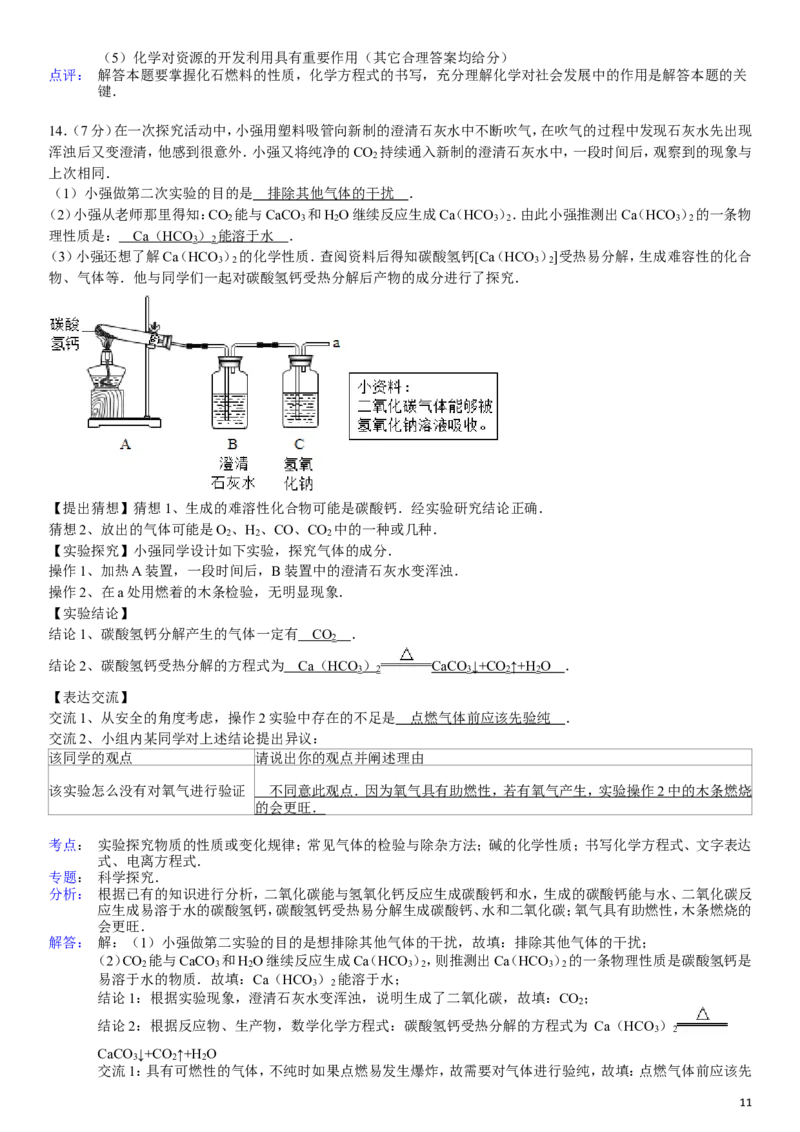
12.(7分)同学们在课外活动中设计了有关气体的实验.气体的发生装置如图所示.
(1)此装置可以用于制备气体.若制备氧气应在分液漏斗中盛放的药物是 过氧化氢溶液 ;写出该反应的化学方程
式: 2H O 2H O+O ↑ .
2 2 2 2
(2)此装置还可以验证某气体的化学性质.若小试管中装有大理石,则分液漏斗中应放 稀盐酸 (填物质名称),大
试管中可放滴有紫色石蕊试液的水,可观察到的现象是 石蕊试液变红 ,写出此气体发生反应的化学方程式:
CO +H O═H CO .
2 2 2 3
9考点: 氧气的制取装置;二氧化碳的实验室制法;二氧化碳的化学性质;书写化学方程式、文字表达式、电离方程
式.
2243409
专题: 实验性简答题.
分析: (1)根据装置图来判断反应物状态和药品;
(2)根据不需要加热可知能制取二氧化碳,且根据二氧化碳的性质来考虑本题.
解答: 解:(1)根据装置特点可知反应不需要加热,所以制取氧气用过氧化氢和二氧化锰,分液漏斗中放的是液体
过氧化氢溶液,由于反应物是过氧化氢,生成物是水和氧气,反应条件是二氧化锰作催化剂,用观察法配平即
可;
(2)若小试管中装有大理石,可以想到制取二氧化碳,稀盐酸与碳酸钙反应,分液漏斗中盛放的是稀盐酸,二
氧化碳能与水结合生成碳酸使紫色石蕊试液变红;
故答案为:(1)过氧化氢溶液;2H O 2H O+O ↑;
2 2 2 2
(2)稀盐酸;石蕊试液变红;CO +H O═H CO .
2 2 2 3
点评: 掌握实验室制取二氧化碳所用的装置图、二氧化碳的性质等即可解答,难度不大.
13.(7分)我省具有较丰富的煤炭资源,煤制取乙二醇的产业化已被列入我国石化产业调整和振兴规划.煤制取乙二
醇的流程示意图为:
(1)煤属于 不可再生 (填“可再生”或“不可再生”)能源.
(2)合成气具有还原性,写出CO还原氧化铜的化学方程式: CO+CuO Cu+CO .
2
(3)乙二醇是一种重要的化工原料,与乙醇同属于醇类,推测乙二醇的一个化学性质: 能燃烧 .
(4)煤制取乙二醇过程发生的是 化学变化 .(填“物理变化”或“化学变化”)
(5)从煤直接作燃料到用煤制取乙二醇,你得到的启示是: 化学对资源的开发利用具有重要作用 .
考点: 物质的相互转化和制备;一氧化碳的化学性质;化学变化和物理变化的判别;化学性质与物理性质的差别及
应用;常见能源的种类、能源的分类.
2243409
专题: 物质的制备.
分析: (1)化石燃料属于不可再生能源;
(2)氧化铜和一氧化碳在加热的条件下生成铜和二氧化碳;
(3)乙醇具有可燃性,可以推测乙二醇也具有可燃性;
(4)根据化学变化的判断方法判断
(5)化学在开发生产力方面具有重要作用
解答: 解:(1)煤属于化石燃料,是不可再生的.
(2)氧化铜与一氧化碳在加热的条件下生成铜和二氧化碳,反应的化学方程式为:CO+CuO Cu+CO
2
(3)乙醇具有可燃性,乙二醇和乙醇具有相似的化学性质,因此可以推测乙二醇也具有可燃性
(4)煤制取乙二醇的过程中产生了新物质乙二醇,是化学变化.
(5)从煤直接作燃料到用煤制取乙二醇作燃料可知,化学对资源的开发利用具有重要作用
故答案为:(1)不可再生 (2)CO+CuO Cu+CO
2
(3)能燃烧(其它合理答案均给分)(4)化学变化
10(5)化学对资源的开发利用具有重要作用(其它合理答案均给分)
点评: 解答本题要掌握化石燃料的性质,化学方程式的书写,充分理解化学对社会发展中的作用是解答本题的关
键.
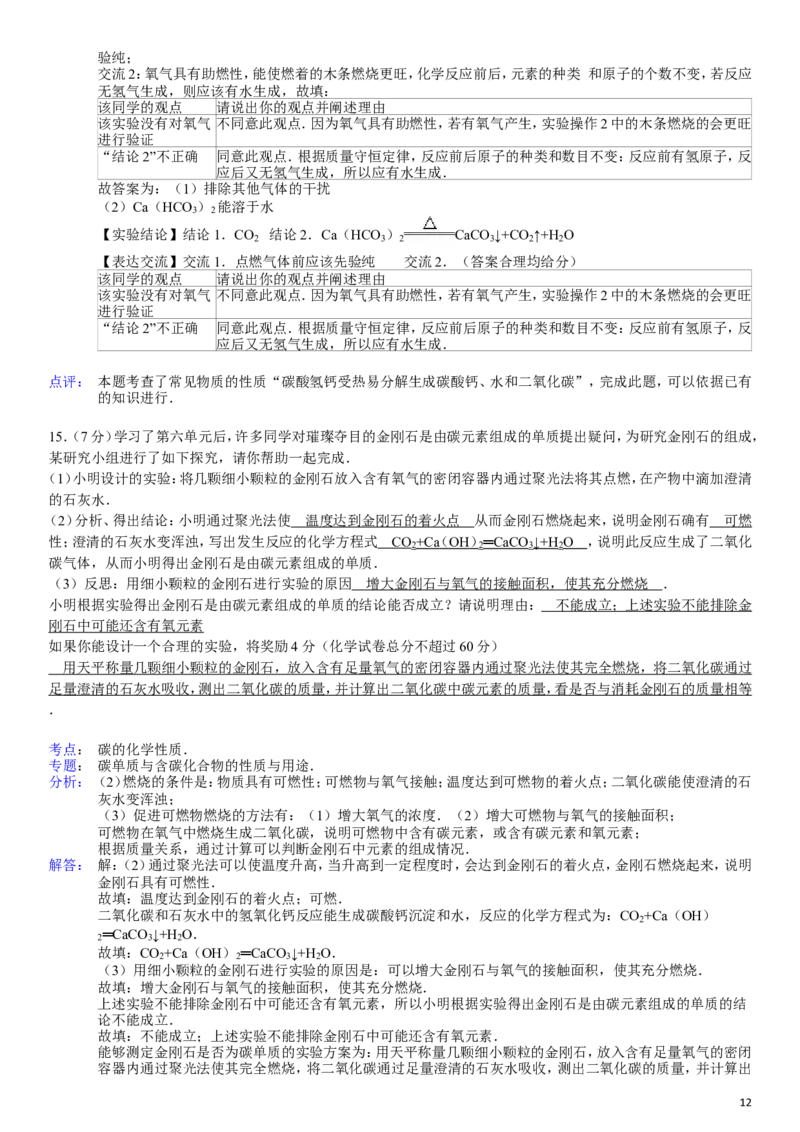
14.(7分)在一次探究活动中,小强用塑料吸管向新制的澄清石灰水中不断吹气,在吹气的过程中发现石灰水先出现
浑浊后又变澄清,他感到很意外.小强又将纯净的CO 持续通入新制的澄清石灰水中,一段时间后,观察到的现象与
2
上次相同.
(1)小强做第二次实验的目的是 排除其他气体的干扰 .
(2)小强从老师那里得知:CO 能与CaCO 和H O继续反应生成Ca(HCO ).由此小强推测出Ca(HCO )的一条物
2 3 2 3 2 3 2
理性质是: C a ( HCO ) 能溶于水 .
3 2
(3)小强还想了解Ca(HCO )的化学性质.查阅资料后得知碳酸氢钙[Ca(HCO ) 受热易分解,生成难容性的化合
3 2 3 2
物、气体等.他与同学们一起对碳酸氢钙受热分解后产物的成分进行了探究.
]
【提出猜想】猜想1、生成的难溶性化合物可能是碳酸钙.经实验研究结论正确.
猜想2、放出的气体可能是O 、H 、CO、CO 中的一种或几种.
2 2 2
【实验探究】小强同学设计如下实验,探究气体的成分.
操作1、加热A装置,一段时间后,B装置中的澄清石灰水变浑浊.
操作2、在a处用燃着的木条检验,无明显现象.
【实验结论】
结论1、碳酸氢钙分解产生的气体一定有 CO .
2
结论2、碳酸氢钙受热分解的方程式为 C a ( HCO ) CaCO ↓+CO ↑+H O .
3 2 3 2 2
【表达交流】
交流1、从安全的角度考虑,操作2实验中存在的不足是 点燃气体前应该先验纯 .
交流2、小组内某同学对上述结论提出异议:
该同学的观点 请说出你的观点并阐述理由
该实验怎么没有对氧气进行验证 不同意此观点.因为氧气具有助燃性,若有氧气产生,实验操作 2 中的木条燃烧
的会更旺.
考点: 实验探究物质的性质或变化规律;常见气体的检验与除杂方法;碱的化学性质;书写化学方程式、文字表达
式、电离方程式.
2243409
专题: 科学探究.
分析: 根据已有的知识进行分析,二氧化碳能与氢氧化钙反应生成碳酸钙和水,生成的碳酸钙能与水、二氧化碳反
应生成易溶于水的碳酸氢钙,碳酸氢钙受热易分解生成碳酸钙、水和二氧化碳;氧气具有助燃性,木条燃烧的
会更旺.
解答: 解:(1)小强做第二实验的目的是想排除其他气体的干扰,故填:排除其他气体的干扰;
(2)CO 能与CaCO 和H O继续反应生成Ca(HCO ),则推测出Ca(HCO )的一条物理性质是碳酸氢钙是
2 3 2 3 2 3 2
易溶于水的物质.故填:Ca(HCO ) 能溶于水;
3 2
结论1:根据实验现象,澄清石灰水变浑浊,说明生成了二氧化碳,故填:CO ;
2
结论2:根据反应物、生产物,数学化学方程式:碳酸氢钙受热分解的方程式为 Ca(HCO )
3 2
CaCO ↓+CO ↑+H O
3 2 2
交流1:具有可燃性的气体,不纯时如果点燃易发生爆炸,故需要对气体进行验纯,故填:点燃气体前应该先
11验纯;
交流2:氧气具有助燃性,能使燃着的木条燃烧更旺,化学反应前后,元素的种类 和原子的个数不变,若反应
无氢气生成,则应该有水生成,故填:
该同学的观点 请说出你的观点并阐述理由
该实验没有对氧气 不同意此观点.因为氧气具有助燃性,若有氧气产生,实验操作2中的木条燃烧的会更旺
进行验证
“结论2”不正确 同意此观点.根据质量守恒定律,反应前后原子的种类和数目不变:反应前有氢原子,反
应后又无氢气生成,所以应有水生成.
故答案为:(1)排除其他气体的干扰
(2)Ca(HCO ) 能溶于水
3 2
【实验结论】结论1.CO 结论2.Ca(HCO ) CaCO ↓+CO ↑+H O
2 3 2 3 2 2
【表达交流】交流1.点燃气体前应该先验纯 交流2.(答案合理均给分)
该同学的观点 请说出你的观点并阐述理由
该实验没有对氧气 不同意此观点.因为氧气具有助燃性,若有氧气产生,实验操作2中的木条燃烧的会更旺
进行验证
“结论2”不正确 同意此观点.根据质量守恒定律,反应前后原子的种类和数目不变:反应前有氢原子,反
应后又无氢气生成,所以应有水生成.
点评: 本题考查了常见物质的性质“碳酸氢钙受热易分解生成碳酸钙、水和二氧化碳”,完成此题,可以依据已有
的知识进行.
15.(7分)学习了第六单元后,许多同学对璀璨夺目的金刚石是由碳元素组成的单质提出疑问,为研究金刚石的组成,
某研究小组进行了如下探究,请你帮助一起完成.
(1)小明设计的实验:将几颗细小颗粒的金刚石放入含有氧气的密闭容器内通过聚光法将其点燃,在产物中滴加澄清
的石灰水.
(2)分析、得出结论:小明通过聚光法使 温度达到金刚石的着火点 从而金刚石燃烧起来,说明金刚石确有 可燃
性;澄清的石灰水变浑浊,写出发生反应的化学方程式 CO +Ca( OH ) ═CaCO ↓+H O ,说明此反应生成了二氧化
2 2 3 2
碳气体,从而小明得出金刚石是由碳元素组成的单质.
(3)反思:用细小颗粒的金刚石进行实验的原因 增大金刚石与氧气的接触面积,使其充分燃烧 .
小明根据实验得出金刚石是由碳元素组成的单质的结论能否成立?请说明理由: 不能成立;上述实验不能排除金
刚石中可能还含有氧元素
如果你能设计一个合理的实验,将奖励4分(化学试卷总分不超过60分)
用天平称量几颗细小颗粒的金刚石,放入含有足量氧气的密闭容器内通过聚光法使其完全燃烧,将二氧化碳通过
足量澄清的石灰水吸收,测出二氧化碳的质量,并计算出二氧化碳中碳元素的质量,看是否与消耗金刚石的质量相等
.
考点: 碳的化学性质.
2243409
专题: 碳单质与含碳化合物的性质与用途.
分析:(2)燃烧的条件是:物质具有可燃性;可燃物与氧气接触;温度达到可燃物的着火点;二氧化碳能使澄清的石
灰水变浑浊;
(3)促进可燃物燃烧的方法有:(1)增大氧气的浓度.(2)增大可燃物与氧气的接触面积;
可燃物在氧气中燃烧生成二氧化碳,说明可燃物中含有碳元素,或含有碳元素和氧元素;
根据质量关系,通过计算可以判断金刚石中元素的组成情况.
解答: 解:(2)通过聚光法可以使温度升高,当升高到一定程度时,会达到金刚石的着火点,金刚石燃烧起来,说明
金刚石具有可燃性.
故填:温度达到金刚石的着火点;可燃.
二氧化碳和石灰水中的氢氧化钙反应能生成碳酸钙沉淀和水,反应的化学方程式为:CO +Ca(OH)
2
═CaCO ↓+H O.
2 3 2
故填:CO +Ca(OH) ═CaCO ↓+H O.
2 2 3 2
(3)用细小颗粒的金刚石进行实验的原因是:可以增大金刚石与氧气的接触面积,使其充分燃烧.
故填:增大金刚石与氧气的接触面积,使其充分燃烧.
上述实验不能排除金刚石中可能还含有氧元素,所以小明根据实验得出金刚石是由碳元素组成的单质的结
论不能成立.
故填:不能成立;上述实验不能排除金刚石中可能还含有氧元素.
能够测定金刚石是否为碳单质的实验方案为:用天平称量几颗细小颗粒的金刚石,放入含有足量氧气的密闭
容器内通过聚光法使其完全燃烧,将二氧化碳通过足量澄清的石灰水吸收,测出二氧化碳的质量,并计算出
12二氧化碳中碳元素的质量,看是否与消耗金刚石的质量相等.
故填:用天平称量几颗细小颗粒的金刚石,放入含有足量氧气的密闭容器内通过聚光法使其完全燃烧,将二
氧化碳通过足量澄清的石灰水吸收,测出二氧化碳的质量,并计算出二氧化碳中碳元素的质量,看是否与消
耗金刚石的质量相等.
点评: 化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相
互之间的反应关系,有助于提高观察实验、进行实验的能力.所以,对化学实验不仅要认真观察,还应掌握设
计实验、观察实验现象的方法.
三、本大题共6分
16.(6分)某大理石厂开采出来的大理石产品,为了检测大理石中碳酸钙的纯度,检测员称取了大理石样品20g,与
足量的稀盐酸反应,共收集到气体6.6g,则该大理石中碳酸钙的质量分数是多少?
考点: 根据化学反应方程式的计算.
2243409
专题: 有关化学方程式的计算.
分析: 根据题意可知,生成的二氧化碳的质量为6.6g,根据二氧化碳的质量可以求出碳酸钙的质量,从而求出碳酸
钙的质量分数.
解答: 解:设生成6.6g二氧化碳需要碳酸钙的质量为x
CaCO +2HCl═CaCl +H O+CO ↑
3 2 2 2
100 44
x 6.6g
x=15g
该大理石中碳酸钙的质量分数为: =75%
答:该大理石中碳酸钙的质量分数为75%.
点评: 本题考查了根据化学方程式的计算,完成此题,可以依据已有的知识进行.
1314