文档内容
第三单元 自然界的水 课题1 水的组成
知识点1:水的物理性质和电解实验
1、水的物理性质
(1)纯净的水是无色无味的透明液体;
(2)在101kPa大气压下水的沸点100℃,凝固点(冰的熔点)0℃;
(3)4℃时水的最大密度是1g/mL(1g/cm3);
注:①水的密度随温度变化的规律: t>4℃和t<0℃时水是热胀冷缩,在0℃< t<4℃范围内,水是热缩冷胀。
②冰浮在水面上,说明相同温度下冰的密度小于水的密度。
(4)水可发生三态变化:气(水蒸气)液(水)固(冰);
(5)水不易导电。
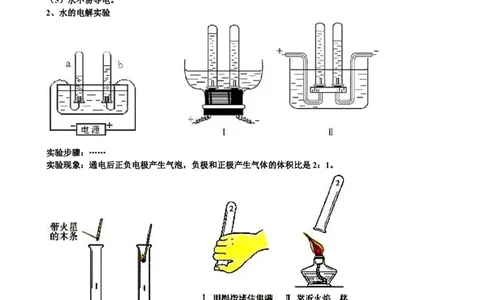
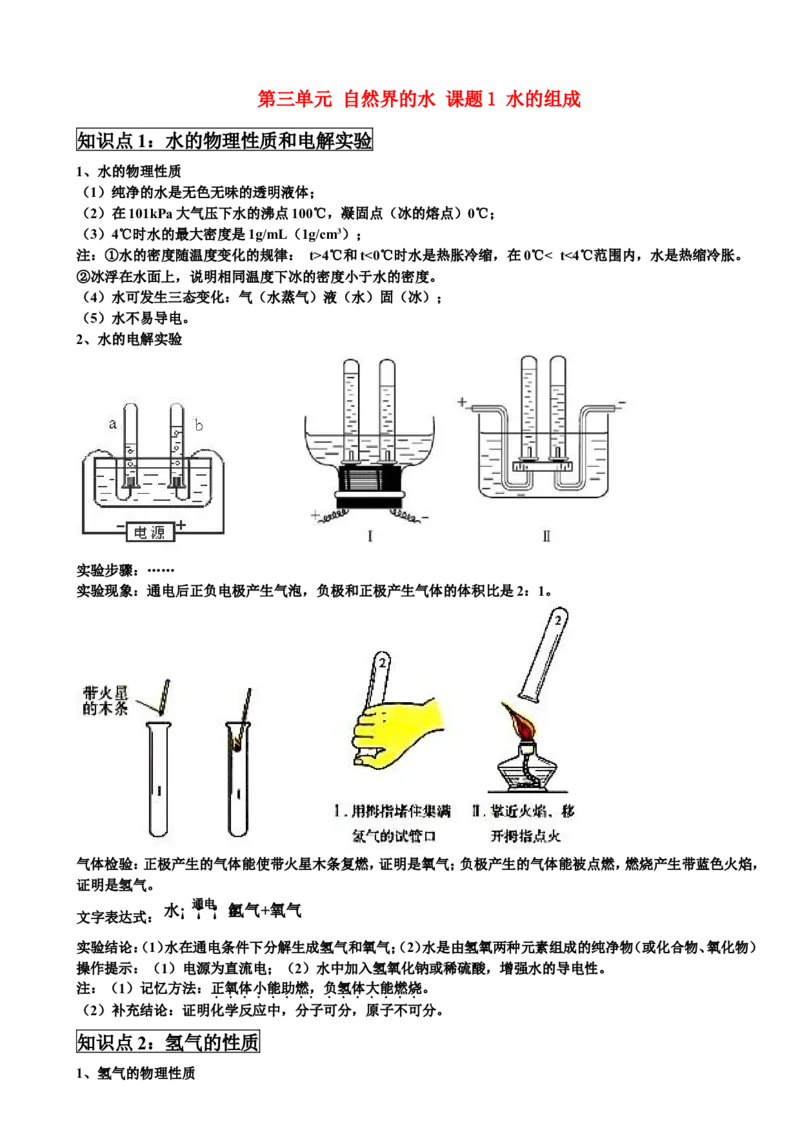
2、水的电解实验
实验步骤:……
实验现象:通电后正负电极产生气泡,负极和正极产生气体的体积比是2:1。
气体检验:正极产生的气体能使带火星木条复燃,证明是氧气;负极产生的气体能被点燃,燃烧产生带蓝色火焰,
证明是氢气。
通电
水¡ ª¡ ª¡ ú氢气+氧气
文字表达式:
实验结论:(1)水在通电条件下分解生成氢气和氧气;(2)水是由氢氧两种元素组成的纯净物(或化合物、氧化物)
操作提示:(1)电源为直流电;(2)水中加入氢氧化钠或稀硫酸,增强水的导电性。
注:(1)记忆方法:正氧体小能助燃,负氢体大能燃烧。
(2)补充结论:证明化学反应中,分子可分,原子不可分。
知识点2:氢气的性质
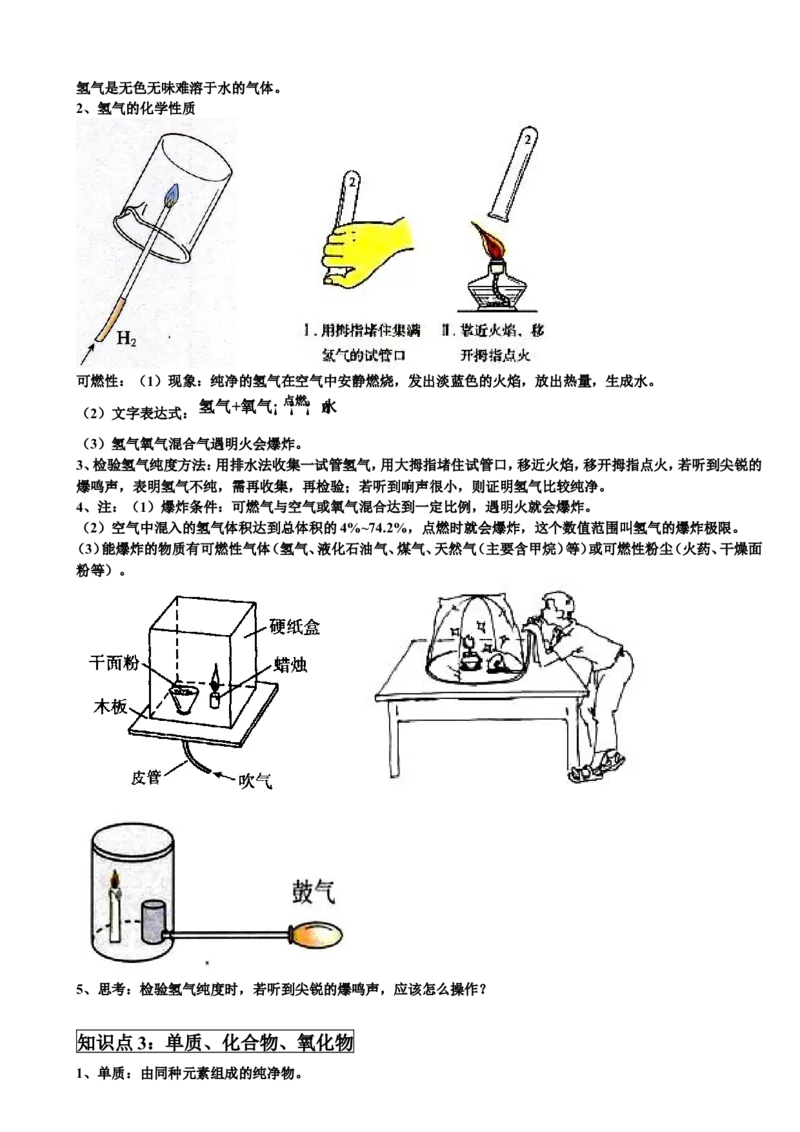
1、氢气的物理性质氢气是无色无味难溶于水的气体。
2、氢气的化学性质
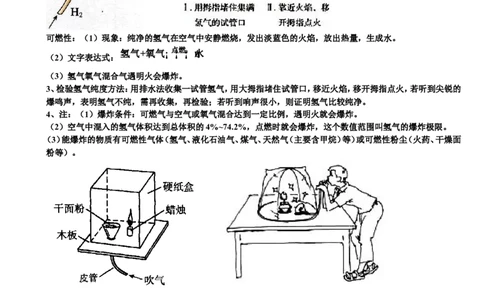
可燃性:(1)现象:纯净的氢气在空气中安静燃烧,发出淡蓝色的火焰,放出热量,生成水。
氢气+氧气¡ 点 ª¡ 燃 ª¡ ú水
(2)文字表达式:
(3)氢气氧气混合气遇明火会爆炸。
3、检验氢气纯度方法:用排水法收集一试管氢气,用大拇指堵住试管口,移近火焰,移开拇指点火,若听到尖锐的
爆鸣声,表明氢气不纯,需再收集,再检验;若听到响声很小,则证明氢气比较纯净。
4、注:(1)爆炸条件:可燃气与空气或氧气混合达到一定比例,遇明火就会爆炸。
(2)空气中混入的氢气体积达到总体积的4%~74.2%,点燃时就会爆炸,这个数值范围叫氢气的爆炸极限。
(3)能爆炸的物质有可燃性气体(氢气、液化石油气、煤气、天然气(主要含甲烷)等)或可燃性粉尘(火药、干燥面
粉等)。
5、思考:检验氢气纯度时,若听到尖锐的爆鸣声,应该怎么操作?
知识点3:单质、化合物、氧化物
1、单质:由同种元素组成的纯净物。2、化合物:由不同种元素组成的纯净物。
3、氧化物:由两种元素组成的化合物中,其中一种元素是氧元素。
注:
(1)分类标准:混合物和纯净物是按照所含物质种类的多少分类的;单质和化合物是按照纯净物中所含元素种类
的不同分类的。
混合物
物质 金属单质
( 按________分类 )
(宏观物质) 非金属单质
单质
稀有气体单质
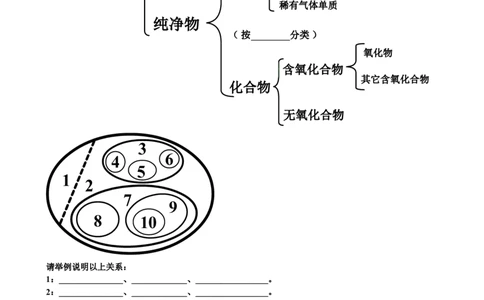
纯净物
( 按________分类 )
氧化物
含氧化合物
其它含氧化合物
化合物
无氧化合物
3
6
4
5
1
2
7
9
8 10
请举例说明以上关系:
1:_______________、_____________、_________________。
2:_______________、_____________、_________________。
3:_______________、_____________、_________________。
4:_______________、_____________、_________________。
5:_______________、_____________、_________________。
6:_______________、_____________、_________________。
7:_______________、_____________、_________________。
8:_______________、_____________、_________________。
9:_______________、_____________、_________________。
10:_______________、_____________、_________________。
(2)单质和化合物的关系:
定义 两者之间区别
单质化合物
规律方法探究
一、物质验纯
许多物质不纯时会发生事故,所以实验前应做好准备。易燃易爆气体,实验前必须检验纯度,防止与空气或氧气混
合后遇明火发生爆炸。常见的易燃易爆气体主要有氢气、甲烷、一氧化碳等。
遇明火爆炸的混合气必须同时有可燃性气体和助燃性气体,比如氢气和氧气。
二、理解物质宏观上是由元素组成的;微观上是由分子、原子等微粒构成的。
课后参考阅读“第四单元 物质构成的奥秘 P70~88”
三、单质和化合物的区别
两者都是纯净物。单质和化合物可以由其定义来区分,单质是由一种元素组成的纯净物,而化合物是由不同种元
素组成的。