文档内容
课题2金属的化学性质 教案
教学目标:
1.知道铁、铝、铜等常见金属与氧气的反应。
2.初步认识常见金属与盐酸、稀硫酸以及金属氧化物溶液间的置换反应。
3.熟悉常见金属的活动性顺序,学会利用金属与酸以及金属化合物溶液通过“置换”推断
常见金属活动性顺序。
4.发展学生敢于置疑、勤于动手的科学精神,发展求知欲和探究激情。
(注:“置换反应”概念的更深刻理解,于第二课时进行)
教学重点:
1.了解金属活动性顺序表,掌握置换反应的概念。
2. 认识部分金属重要化学性质(与氧气反应,与盐酸、稀硫酸反应及金属间的置
换)。
教学难点:
1. 活动性顺序强弱的探究及排序。
2. 金属活动性顺序表的应用。
教学方法:
对实验现象进行筛选、对比、归纳、分析、进行信息处理,获取科学结论的教学方法。
教会思路: 猜想与探究――→观察与检验――→分析与归纳――→解释与结论
教学准备:
镁、铝、锌、铁、铜等金属,硫酸铜溶液、硝酸银溶液、稀盐酸、稀硫酸等以及酒精灯,石棉
网、三角架、试管、镊子等。
教学过程:
教 学 教师活动 学生活动 设计意图
流程课 程 导读:提出思考问题。 读引言思考:铝为何具抗腐蚀性,其它金属如 明确课程目的,
引 何?化学性质有什么共性和差异性?规律怎 引导关注重点。
入 样?
情 景 演示:外观相似的四片 进行“猜金属”游戏,观察现象,猜测金属: 激发好奇心与求
创 金属片(Mg、Al、Zn、Fe, 知欲,激励探究激
设 编号)置于铁三角架上 情,并学习在真实
灼烧,由学生根据现象 据学生展示猜出的结果进行互动评价――学 的情景中发现规律
猜出金属名称。 生很难完全猜准,多数根据“燃烧”仅猜出 和问题。
“Mg”。
以 存 在 “ 问
题”为后续探究留
下悬念。
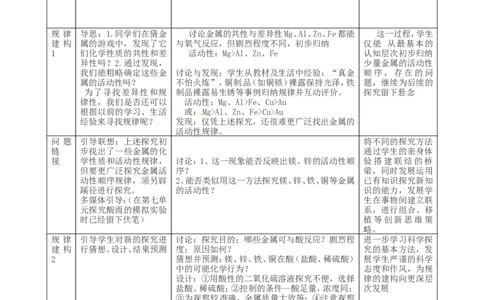
规 律 导思:1.同学们在猜金 讨论金属的共性与差异性Mg、Al、Zn、Fe都能 这一过程,学生
建 构 属的游戏中,发现了它 与氧气反应,但剧烈程度不同,初步归纳 仅能 从最基本的
1 们化学性质的共性和差 活动性:Mg>Al、Zn、Fe 认知层次初步归纳
异性吗?2.通过发现, 少量金属的活动性
我们能粗略确定这些金 讨论与发现:学生从教材及生活中经验:“真金 顺序,存在的问
属的活动性吗? 不怕火炼”,铜制品(如铜锁)裸露保持光泽,铁 题,继续为后续的
为了寻找差异性和规 制品裸露易生锈等事例归纳规律并互动评价。 探究留下悬念
律性,我们是否还可以 活动性:Mg、Al>Fe、Cu>Au
根据以前的学习、生活 或:Mg>Al、Zn、Fe>Cu>Au
经验来寻找规律呢? 发现:仅凭上述探究,还很难更广泛找出金属的
活动性规律。
问 题 引导联想:上述探究初 将不同的探究方法
链 步找出了一些金属的化 通过学生的亲身体
接 学性质和活动性规律, 讨论:1、这一现象能否反映出镁、锌的活动性顺 验搭建联结的桥
但要更广泛探究金属活 序? 梁,同时发展运用
动性顺序规律,须另辟 2、能否类似用这一方法探究镁、锌、铁、铜等金属 已有知识探究新知
蹊径进行探究。 的活动性? 识的能力,发展学
多媒体引导:(在第七单 生在事物间建立联
元探究酸雨的模拟实验 系,进行组合、移
时已经留下伏笔) 植等创新思维策
略。
规 律 引导学生对新的探究进 讨论:探究目的;哪些金属可与酸反应?剧烈程 进一步学习科学探
建 构 行猜想、设计、结果预测 度;原因如何? 究的基本方法,发
2 猜想并预测:镁、锌、铁、铜在酸(盐酸、稀硫酸) 展学生严谨的科学
中的可能化学行为? 态度和作风,为规
设计:①用酸性的二氧化硫溶液探究不便,选择 律的建构向更深层
盐酸、稀硫酸;②控制的条件—酸足量,浓度同; 次发展
③为观察较准确,金属质量大致等;④注意观察
反应剧烈程度,可对反应时间作记录或估计。
示范:操作的规范以及 组内合作探究并填写探究记录表(打印) 通过自己的实践,
如何检验产生的气体 表一:金属与稀盐酸反应: 检验自己的猜想,
金属 现象及反应时间 生 成 方程式 发展合作精神,体
物 验探究乐趣。
Mg
Zn
Fe
Cu
表二:金属与稀硫酸反应:(表略)
引导对信息进行处理, 各组交流获取的信息: 使学生享受自己获
并获取结论。 1.能与稀硫酸、盐酸反应的金属及不能反应的金 得成功的快乐,更属。 深层次对知识进行
2.反应的剧烈程度与速率(差异大的,进行讨论) 建构
分组:
活泼金属(可与盐酸、稀硫酸反应):Mg Zn
Fe
不活泼金属(不与盐酸、稀硫酸反应):Cu
活动性: Mg>Zn>Fe>Cu
展示结论并互动评价:
导思:同学们,你们的观 观看动画,对照自己的探究反思:(惊呀,笑): 创设轻松和谐的探
察真实可靠吗? 究氛围,发展学生
多媒体Flash动画: 想象力,将真实事
“金属与盐酸反应的比 物以“图景“形式
较” 与学生的认知特点
协调。
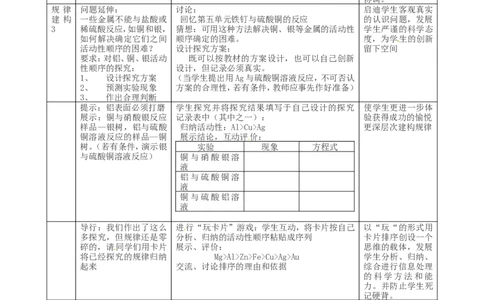
规 律 问题延伸: 讨论: 启迪学生客观真实
建 构 一些金属不能与盐酸或 回忆第五单元铁钉与硫酸铜的反应 的认识问题,发展
3 稀硫酸反应,如铜和银, 猜想:可用这种方法解决铜、银等金属的活动性 学生严谨的科学态
如何解决确定它们之间 顺序确定的困难。 度,为学生的创新
活动性顺序的困难? 设计探究方案: 留下空间
要求:对铝、铜、银活动 既可以按教材的方案设计,也可以自己创新
性顺序的探究: 设计,但记录必须真实。
1、 设计探究方案 (当学生提出用Ag与硫酸铜溶液反应,不可否认
2、 预测实验现象 方案的合理性,若有条件,教师应事先作好准备)
3、 作出合理判断
提示:铝表面必须打磨 学生探究并将探究结果填写于自己设计的探究 使学生更进一步体
展示:铜与硝酸银反应 记录表中(其中之一): 验获得成功的愉悦
样品—银树,铝与硫酸 归纳活动性:Al>Cu>Ag 更深层次建构规律
铜溶液反应的样品—铜 展示结论,互动评价:
树。(若有条件,演示银 实验 现象 方程式
与硫酸铜溶液反应) 铜与硝酸银溶
液
铝与硫酸铜溶
液
铜与硫酸铝溶
液
导行:我们作出了这么 进行“玩卡片”游戏:学生互动,将卡片按自己 以“玩“的形式用
多探究,但规律还是零 分析、归纳的活动性顺序粘贴成序列 卡片排序创设一个
碎的,请同学们用卡片 展示、评价: 思维的载体,发展
将已经探究的规律归纳 Mg>Al>Zn>Fe>Cu>Ag>Au 学生分析、归纳、
起来 交流、讨论排序的理由和依据 综合进行信息处理
的科学方法和能
力。并防止学生死
记硬背。
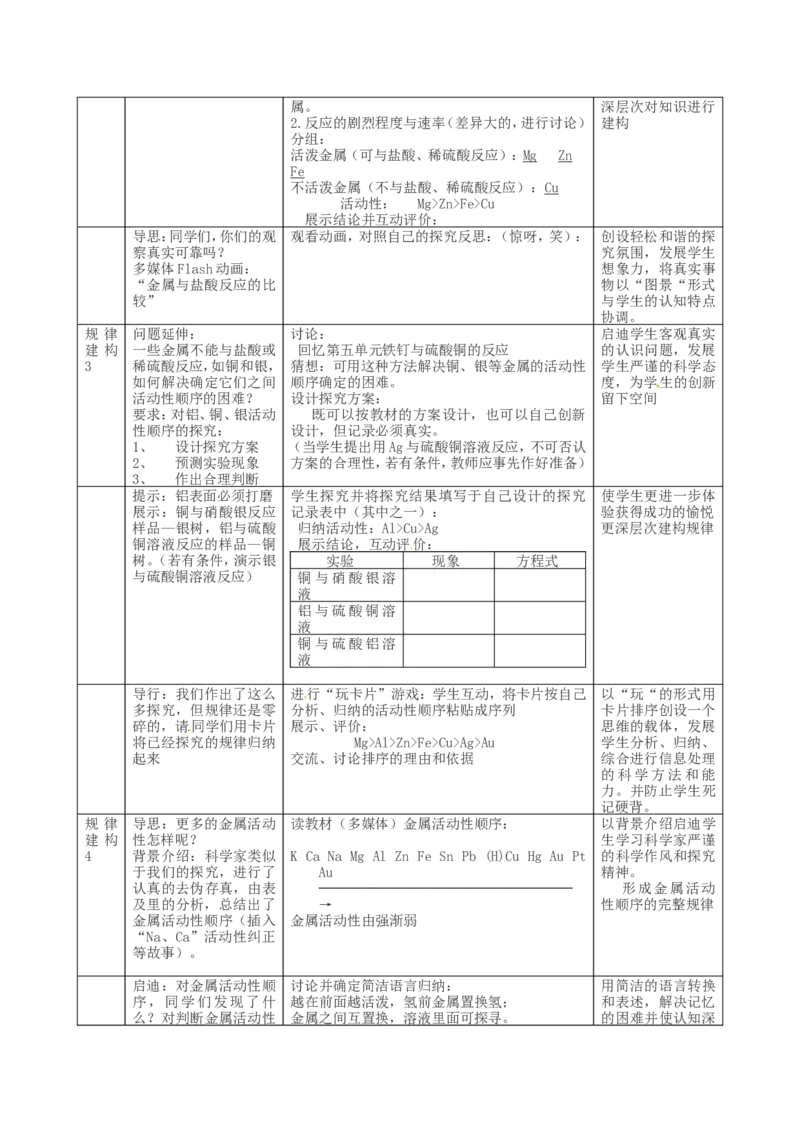
规 律 导思:更多的金属活动 读教材(多媒体)金属活动性顺序: 以背景介绍启迪学
建 构 性怎样呢? 生学习科学家严谨
4 背景介绍:科学家类似 K Ca Na Mg Al Zn Fe Sn Pb (H)Cu Hg Au Pt 的科学作风和探究
于我们的探究,进行了 Au 精神。
认真的去伪存真,由表 ────────────────── 形成金属活动
及里的分析,总结出了 → 性顺序的完整规律
金属活动性顺序(插入 金属活动性由强渐弱
“Na、Ca”活动性纠正
等故事)。
启迪:对金属活动性顺 讨论并确定简洁语言归纳: 用简洁的语言转换
序,同学们发现了什 越在前面越活泼,氢前金属置换氢; 和表述,解决记忆
么?对判断金属活动性 金属之间互置换,溶液里面可探寻。 的困难并使认知深提供了什么依据? 化。
运 用 问题:有X、Y、Z三种金 完成问题的解答,互动评价: 发展学生知识
与 深 属。1.X、Y、Z分别放入 答案:(1)X>Z>Y 的迁移,应用能
化 稀盐酸中,X溶解并放 (2)X>H>Z>Y 力,促使学生对认
出氢气,Y、Z无变化;2. 讨论: 知的自省与反思。
将Y放入Z的化合物溶 (1)氢的活动性排X之后,Y、Z之前的依据?
液中无变化;3.Z放入Y (2)假如只告之“将Y放入Z的化合物溶液
的化合物溶液中有Y析 中无变化”能否得出结论?你是如何思维
出:(1)则X、Y、Z的活 的?
动性顺序如何?
(2).科学家将氢的活
动性与金属活动性进行
比较并排序,当氢也排
在里边时,活动性顺序
如何?
课时 1.知道金属主要化学性质:活泼金属多共性,与氧与酸易反应。
小结 2.金属活动性顺序:以氢为界,五字断句。
3.活动性判断与应用(见归纳)。
作业设计:
1.课后习题3、6、8 2.设计一个实验证明活泼性 Zn > Fe > Cu
板书设计:
课题二 金属的化学性质
一. 金属和氧气的反应
镁铝常温下很容易反应,铜铁常温下反应很慢,金在高温下也不反应。
结论:不同的金属与氧气反应的难易程度不同。
活动性:Mg、Al>Fe、Cu>Au
二.金属与酸的反应
K Ca Na Mg Al Zn Fe Sn Pb (H)Cu Hg Au Pt Au
金属活动性由强渐弱
结论:不同的金属与酸反应的剧烈程度不同。
三.金属活动性顺序表的应用,置换反应的应用
越在前面越活泼 氢前金属置换氢 金属之间互置换 溶液里面可探寻
课后反思本课以多层次科学探究为主线,渗透建构主义思想,以“猜金属”、“玩卡片”创设情
景,互动评价激励探究热情,以“学生发展”为本,进行有意义的知识建构,符合学生心理特
点,学生兴趣盎然,参与主动,体验深刻。主要的缺陷是时间较为紧张,课堂上学生极为兴奋,
控制探究的进程较难。课堂各种活动亦应作好更充分的准备,多媒体应用尽可能贴切,实验
探究安排亦应更合理(如金属与稀硫酸、稀盐酸反应,将学生分为两部分分别进行以节约时
间),效果可能更好。