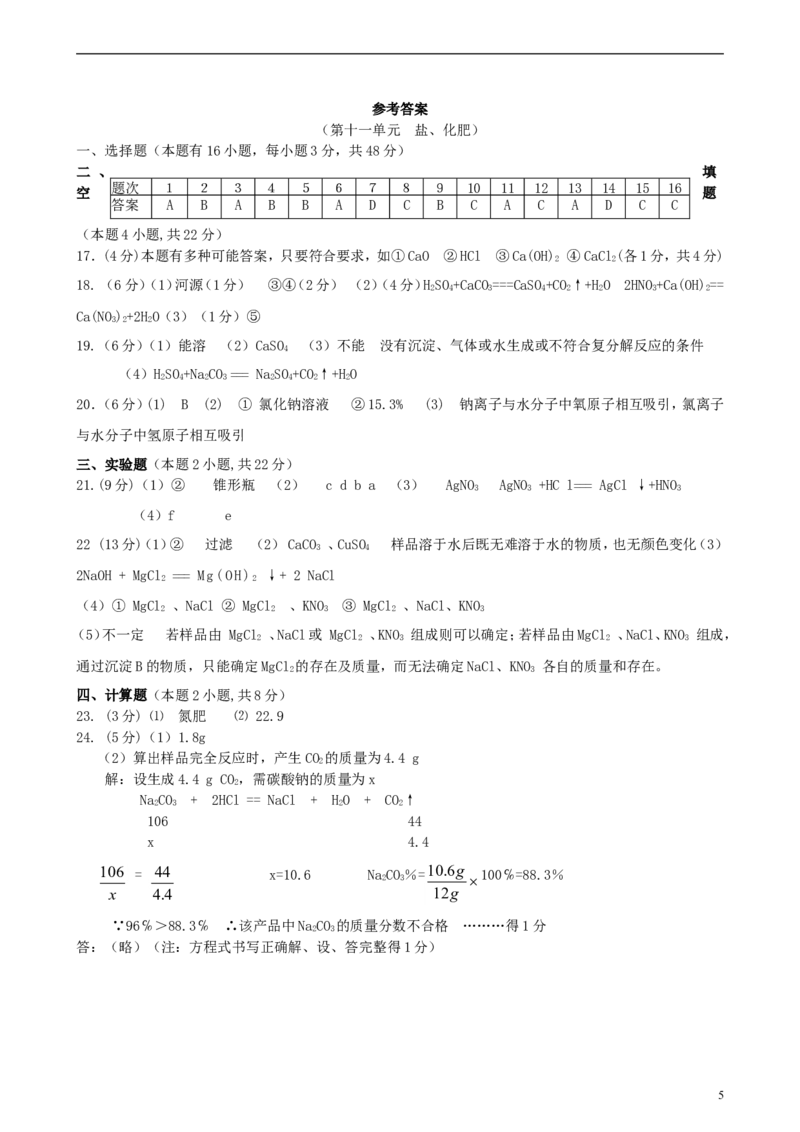文档内容
第十一单元 盐、化肥
可能用到的相对原子质量: H:1 C:12 N :14 O:16 S:32 Na:23 Cl:35.5 Ca:40
题次 一 二 三 四 总分
得分
一、选择题(本题有16小题,每小题3分,共48分)
1. 下
题次 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16
列 常
答案
见 的
物质中,不代表同一种物质的是
A.氯化钠、盐 B.氢氧化钠、苛性钠 C.碳酸钠、纯碱 D.碳酸氢钠、小苏打
2.在植物生长过程中,施用氮肥能使枝叶繁茂、磷肥能使果实饱满、钾肥能使茎秆健壮。种植吃叶的蔬菜
(如青菜),应施用较多的化肥是
A.磷肥 B.NHNO C.KSO D.微量元素肥料
4 3 2 4
3.下列关于物质的溶解性的叙述中,正确的是
A.硝酸盐都能溶于水 B.碳酸盐都不溶于水
C.硫酸盐都溶于水 D.碱多数易溶于水
4.某种物质是焙制糕点所用的发酵粉的主要成分之一,也是医疗上治疗胃酸过多症的一种药剂,这种物质
是
A.NaOH B.NaHCO C.CaO D.NaCl
3
5.下列化肥中,不属于盐的是
A.硝酸钠 B.氨水 C.碳酸氢铵 D.硫酸钾
6.在蔬菜生长过程中,常喷洒农药防治病虫害。据研究,用碱性溶液或清水浸泡,可使残留在蔬菜上的农药
的毒性降低。 因此,买来的蔬菜在食用前最好用稀碱水或清水浸泡一段时间, 浸泡蔬菜时应加入适量
A. 纯碱 B.白酒 C. 白糖 D. 食醋
7.下列各组物质中,不能发生复分解反应的是
A.HCl和Ca(OH) B.NaCO 和HSO C.Ca(OH) 和NaCO D.KCl和CuSO
2 2 3 2 4 2 2 3 4
8.下列说法中,错误的是
A.氮是植物体内蛋白质、核酸和叶绿素的组成元素
B.磷可以促进作物生长,还可以增强作物的抗寒、抗旱能力
C.钾也是植物体的组成元素,能促进植物的光合作用
D.不合理使用化肥会带来很多环境问题
9.在某溶液滴入稀盐酸,能产生使澄清石灰水浑浊的气体, 这说明某溶液中含有的离子是
A.Ca2+ B.CO2- C.SO2- D.OH-
3 4
10.某学习性学习小组的同学为家乡农业生产提出了下列建议, 其中不合理的是
A.要加大灌溉用水的管理力度,防止水资源的污染和浪费
B.禁止就地焚烧农作物秸秆, 应该将其回收用于制沼气
C.用熟石灰改良酸性土壤, 应同时施加碳铵(NHHCO)以提高土壤肥力
4 3
D.要综合利用农家肥和化肥, 重视在增施农家肥的基础上, 配合使用化肥
11.包裹松花蛋的泥灰的配料有纯碱、食盐、生石灰、草木灰。当用水将它们混合包在蛋壳外面后,发生复分
解反应的个数为
A.2个 B.4个 C.1个 D.3个
12.向含AgNO、Cu(NO) 、Mg(NO) 混合溶液中,加入一定量的锌粒,充分反应后过滤,向滤出的固体中滴加
3 3 2 3 2
稀盐酸,有气体生成,则滤出的固体中一定有
A.Ag、Cu、Mg B.Cu、Mg、Zn C.Ag、Cu、Zn D.Ag、Mg、Zn
13.只用一种试剂就能将NaOH、NaCO、Ba(OH) 三种溶液区分开来,这种试剂是
2 3 2
A.HSO B.HCl C.CaCl D.NHCl
2 4 2 4
114.下列各组物质,只用一种试剂(括号内物质)及相互之间的反应不能鉴别开来的是
A.固体:食盐、硝酸铵、烧碱 (水)
B.固体:硫酸铜、熟石灰、碳酸钙(稀盐酸)
C.溶液:纯碱、食盐、盐酸 (酚酞试液)
D.溶液:氯化钠、氯化钾、硫酸钾(硝酸银溶液)
15.(·江苏盐城)下表列出了除去物质中所含少量杂质的方法,其中错误的是
物质 所含杂质 除去杂质的方法
A CO CO 通过足量氢氧化钠溶液,干燥
2
B NaCl 泥沙 溶解、过滤、蒸发
C NaOH溶液 NaCO 加入足量稀盐酸至不再产生气泡
2 3
D Cu(NO) 溶液 AgNO 加入过量的铜粉,过滤
3 2 3
16.某无色溶液中能大量共存的离子组是
A.Na+、SO2-、Cl- 、Cu2+ B.OH- 、K+ 、SO2- 、Ba2+
4 4
C.NO- 、Mg2+、Cl- 、 K+ D.Na+、OH- 、NO- 、H+
3 3
二、填空题(本题4小题,共22分)
17.(4分)只用Ca、C、O、Cl、H五种元素的一种或几种,各写出一个化学式:
①氧化物__________ ②酸__________ ③碱__________ ④盐__________
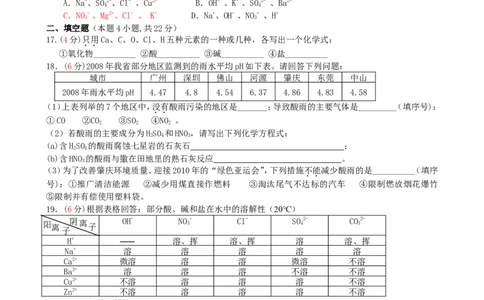
18.(6分)2008年我省部分地区监测到的雨水平均pH如下表。请回答下列问题:
城市 广州 深圳 佛山 河源 肇庆 东莞 中山
2008年雨水平均pH 4.47 4.8 4.54 6.37 4.86 4.83 4.58
(1)上表列举的7个地区中,没有酸雨污染的地区是_______;导致酸雨的主要气体是_________(填序号):
①CO ②CO ③SO ④NO 。
2 2 2
(2)若酸雨的主要成分为HSO 和HNO,请写出下列化学方程式:
2 4 3
(a)含HSO 的酸雨腐蚀七星岩的石灰石 ;
2 4
(b)含HNO 的酸雨与撒在田地里的熟石灰反应 。
3
(3)为了改善肇庆环境质量、迎接2010年的“绿色亚运会”,下列措施不能减少酸雨的是__________(填序
号):①推广清洁能源 ②减少用煤直接作燃料 ③淘汰尾气不达标的汽车 ④限制燃放烟花爆竹
⑤限制并有偿使用塑料袋。
19.(6分)根据表格回答:部分酸、碱和盐在水中的溶解性(20℃)
阳 离 阴 离 子 OH- NO 3 - Cl- SO 4 2- CO 3 2-
子
H+ 溶、挥 溶、挥 溶 溶、挥
Na+ 溶 溶 溶 溶 溶
Ca2+ 微溶 溶 溶 微溶 不溶
Ba2+ 溶 溶 溶 不溶 不溶
Cu2+ 不溶 溶 溶 溶 不溶
Zn2+ 不溶 溶 溶 溶 不溶
(1)Ba(OH) 的溶解性 。
2
(2)从上表中找出一种微溶性盐 (填化学式)。
(3)Zn(NO)、CuCl 两种溶液能不能发生反应 (填“能”或“不能”),理由是 。
3 2 2
(4)完成HSO 和表中的一种可溶性盐反应的化学方程式 。
2 4
20.(6分)(1)下列微粒模型示意图可能代表水分子的是 (选填字母序号)。
A B C D
(2)利用(1)的结论,通过观察左下图,试回答下列问题。
①框内代表的物质是 ;
2②框内NaCl质量分数为 ;
③请描述框内离子与分子结合时的特点
。
Na+ Cl-
三、实验题(本题3小题,共22分)
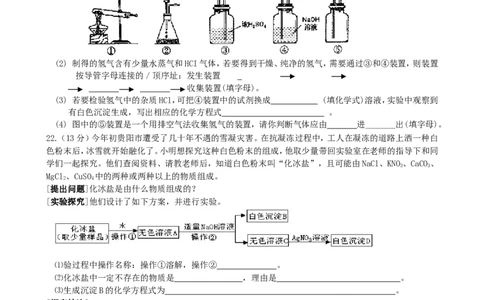
21.(9分)以下是小阳同学制取氢气的实验过程,根据题意回答以下问题。
(1) 如果他用锌粒和稀盐酸来制取氢气,可以选择 (填序号)做发生装置;装置②的主要仪器
有分液漏斗、带导管的双孔胶塞和 (填仪器名称)。
(2) 制得的氢气含有少量水蒸气和HCI气体,若要得到干燥、纯净的氢气,需要通过③和④装置,则装置
按导管字母连接的/顶序址:发生装置
收集装置(填字母)。
(3) 若要检验氢气中的杂质HCl,可把④装置中的试剂换成 (填化学式)溶液,实验中观察到
有白色沉淀生成,写出相应的化学方程式 。
(4) 图中的⑤装置是一个用排空气法收集氢气的装置,请你判断气体应由 进_______出(填字母)。
22.(13分)今年初贵阳市遭受了几十年不遇的雪凝灾害。在抗凝冻过程中,工人在凝冻的道路上洒一种白
色粉末后,冰雪就开始融化了。小明想探究这种白色粉末的组成,他取少量带回实验室在老师的指导下和同
学们一起探究。他们查阅资料、请教老师后,知道白色粉末叫“化冰盐”,且可能由NaCl、KNO、CaCO、
3 3
MgCl、CuSO 中的两种或两种以上的物质组成。
2 4
[提出问题]化冰盐是由什么物质组成的?
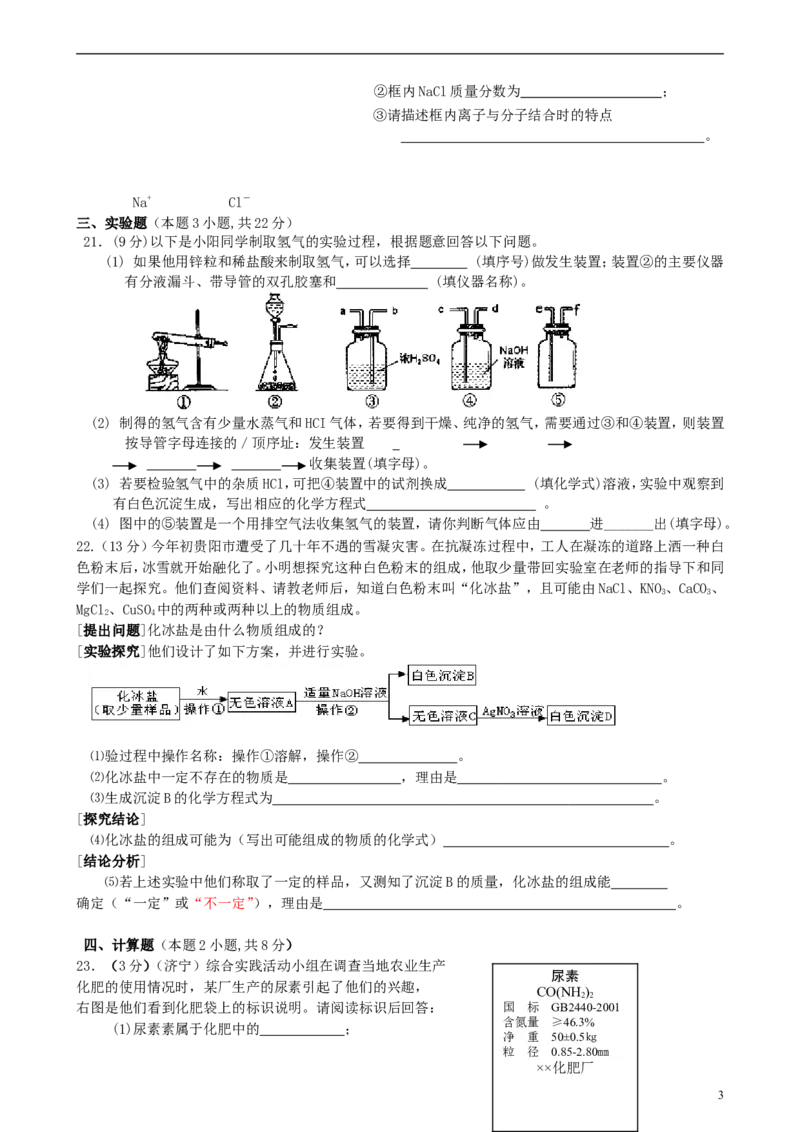
[实验探究]他们设计了如下方案,并进行实验。
⑴验过程中操作名称:操作①溶解,操作② 。
⑵化冰盐中一定不存在的物质是 ,理由是 。
⑶生成沉淀B的化学方程式为 。
[探究结论]
⑷化冰盐的组成可能为(写出可能组成的物质的化学式) 。
[结论分析]
⑸若上述实验中他们称取了一定的样品,又测知了沉淀B的质量,化冰盐的组成能
确定(“一定”或“不一定”),理由是 。
四、计算题(本题2小题,共8分)
23.(3分)(济宁)综合实践活动小组在调查当地农业生产
尿素
化肥的使用情况时,某厂生产的尿素引起了他们的兴趣,
CO(NH)
2 2
右图是他们看到化肥袋上的标识说明。请阅读标识后回答: 国 标 GB2440-2001
含氮量 ≥46.3%
(1)尿素素属于化肥中的 ;
净 重 50±0.5㎏
粒 径 0.85-2.80㎜
××化肥厂
3(2)每袋尿素中有效营养元素的含量不低
于 千克。(精确到0.1)
24.(5分)(兰州)某化工厂用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠
≥96%。为测定该产品中含碳酸钠的质量分数,进行了以下实验:取12.0g纯碱样品放入烧杯中,称得烧
杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反
应。实验数据记录如下:
所加盐酸的次数 第一次 第二次 第三次 第四次
盐酸的质量/g 25 25 25 25
烧杯及所盛物质总质量/g 181.2 204.4 228.6 253.6
请你据此分析计算:
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是 g。
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
4参考答案
(第十一单元 盐、化肥)
一、选择题(本题有16小题,每小题3分,共48分)
二 、 填
题次 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16
空 题
答案 A B A B B A D C B C A C A D C C
(本题4小题,共22分)
17.(4分)本题有多种可能答案,只要符合要求,如①CaO ②HCl ③Ca(OH) ④CaCl(各1分,共4分)
2 2
18. (6分)(1)河源(1分) ③④(2分) (2)(4分)HSO+CaCO===CaSO+CO↑+HO 2HNO+Ca(OH)==
2 4 3 4 2 2 3 2
Ca(NO)+2HO(3)(1分)⑤
3 2 2
19.(6分)(1)能溶 (2)CaSO (3)不能 没有沉淀、气体或水生成或不符合复分解反应的条件
4
(4)HSO+NaCO === NaSO+CO↑+HO
2 4 2 3 2 4 2 2
20.(6分)(1) B (2) ① 氯化钠溶液 ②15.3% (3) 钠离子与水分子中氧原子相互吸引,氯离子
与水分子中氢原子相互吸引
三、实验题(本题2小题,共22分)
21.(9分)(1)② 锥形瓶 (2) c d b a (3) AgNO AgNO +HC l=== AgCl ↓+HNO
3 3 3
(4)f e
22 (13分)(1)② 过滤 (2) CaCO 、CuSO 样品溶于水后既无难溶于水的物质,也无颜色变化(3)
3 4
2NaOH + MgCl === Mg(OH) ↓+ 2 NaCl
2 2
(4)① MgCl 、NaCl ② MgCl 、KNO ③ MgCl 、NaCl、KNO
2 2 3 2 3
(5)不一定 若样品由 MgCl 、NaCl或 MgCl 、KNO 组成则可以确定;若样品由MgCl 、NaCl、KNO 组成,
2 2 3 2 3
通过沉淀B的物质,只能确定MgCl 的存在及质量,而无法确定NaCl、KNO 各自的质量和存在。
2 3
四、计算题(本题2小题,共8分)
23. (3分) ⑴ 氮肥 ⑵ 22.9
24. (5分)(1)1.8g
(2)算出样品完全反应时,产生CO 的质量为4.4 g
2
解:设生成4.4 g CO,需碳酸钠的质量为x
2
NaCO + 2HCl == NaCl + HO + CO↑
2 3 2 2
106 44
x 4.4
106 = 44 x=10.6 NaCO%= 10.6g 100℅=88.3%
2 3
x 4.4 12g
∵96℅>88.3℅ ∴该产品中NaCO 的质量分数不合格 ………得1分
2 3
答:(略)(注:方程式书写正确解、设、答完整得1分)
5